19. Sténose valvulaire pulmonaire
V. Gournay
La SVP isolée est une cardiopathie congénitale relativement fréquente puisqu’elle représente environ 10 % des cardiopathies de l’enfant [1].
Description anatomoclinique
Dans la forme typique, la valve pulmonaire a une forme de dôme se projetant dans le tronc de l’AP [2]. Ce dôme, percé d’un orifice central, « le gicleur », est constitué par la fusion des commissures des feuillets valvulaires. La fusion des commissures est parfois incomplète, n’intéressant que leur partie périphérique en contact avec la paroi artérielle pulmonaire, alors que la partie centrale des valvules est libre. Le tissu des valvules pulmonaires est toujours plus ou moins épaissi, mais de façon modérée. L’anneau valvulaire pulmonaire lui-même est de taille normale.
En dehors de cette forme dite typique de SVP, il existe une forme atypique plus rare (5 à 15 % des cas). Celle-ci est caractérisée par une valve pulmonaire constituée de trois feuillets valvulaires très épais, avec peu ou pas de fusion commissurale. L’obstacle est constitué par des valvules dont la mobilité est réduite en raison de leur épaisseur, infiltrée de tissu myxoïde. Une hypoplasie de l’anneau valvulaire pulmonaire est fréquemment associée. La forme atypique de SVP est plus fréquemment observée dans le cadre de syndrome malformatif ou génétique, en particulier dans le syndrome de Noonan.
Des modifications secondaires à l’obstacle valvulaire pulmonaire sont asso ciées de façon quasi constante à la sténose valvulaire. Premièrement, on observe une augmentation de l’épaisseur de la paroi du VD, entraînant une diminution de la taille de sa cavité. L’hypertrophie pariétale du VD est parti culièrement marquée dans l’infundibulum pulmonaire, où elle peut entraîner un obstacle dynamique associé à la sténose valvulaire fixe. Dans certains cas extrêmes (SVP critique), la diminution de la taille de la cavité du VD peut aller jusqu’à une hypoplasie de la cavité et de l’anneau tricuspide, associée le plus souvent à une CIA de décharge (shunt droite-gauche). La deuxième modification secondaire à l’obstacle valvulaire pulmonaire est la dilatation poststénotique du tronc de l’AP, s’étendant sur toute sa longueur, de la valve jusqu’à la bifurcation, et parfois même englobant l’origine de l’AP gauche. Cette dilatation est créée par le jet à haute vélocité éjecté à travers le gicleur de l’orifice pulmonaire rétréci. Elle est en général moins marquée, voire absente, dans les formes atypiques de SVP.
La SVP critique se révèle dès la naissance par une cyanose (shunt droite-gauche auriculaire). En dehors de la forme critique néonatale, la SVP est asymptomatique et se dépiste lors d’un examen systématique (souffle systolique éjectionnel).
Échocardiographie Doppler
L’échographie cardiaque est l’examen clé du diagnostic et de l’évaluation de la sévérité de la SVP.
Échographie 2D
L’échocardiographie 2D permet de faire le diagnostic. Les incidences paraster nale petit axe et sous-costale sagittale permettent au mieux de visualiser la valve pulmonaire. L’ouverture valvulaire typique en dôme en systole est bien visible (figure 19.1). Ces incidences permettent également de mesurer le diamètre de l’anneau pulmonaire, le plus souvent normal dans les formes typi ques, afin d’aider à déterminer la taille du ballon à utiliser en cas de valvuloplastie. La dilatation post-sténotique du tronc de l’AP est aisément visible et mesurable (figure 19.2). L’échographie 2D permet également d’apprécier le degré d’hypertrophie du VD secondaire à la sténose, ainsi que sa cinétique. L’hypertrophie peut intéresser l’infundibulum, ajoutant une composante sous-valvulaire à l’obstacle. Dans les formes atypiques, l’échographie montre une valve pulmonaire très épaisse, quasiment immobile, insérée sur un anneau hypoplasique, avec une absence de dilatation post-sténotique, voire un rétrécissement supravalvulaire associé.
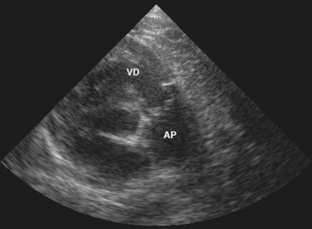 |
| Figure 19.1 Incidence parasternale petit axe d’une SVP typique. La valve pulmonaire épaissie forme un dôme avec une ouverture limitée. L’anneau valvulaire pulmonaire est de taille normale. |
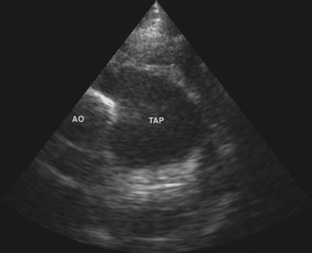 |
| Figure 19.2 Incidence parasternale petit axe. Le tronc de l’AP (TAP) est le siège d’une dilatation poststénotique notable.
Stay updated, free articles. Join our Telegram channel
Full access? Get Clinical Tree
 Get Clinical Tree app for offline access
Get Clinical Tree app for offline access

|




