Expositions aux radionucléides : médecine nucléaire, accidents et attentats
Doses délivrées au patient par examens diagnostiques en médecine nucléaire. Moyens de la réduction de la dose
Paramètres de la dose délivrée par un traceur radioactif
Nature du rayonnement émis
Rayonnement β et électrons
Rayonnements électromagnétiques
Période effective du traceur
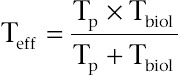
Quantité de radioactivité injectée
Estimation de la dose en médecine nucléaire
Paramètres biologiques de l’incorporation
Paramètres individuels
Âge
Fonction rénale
Fixation pathologique
Comment réduire la dose en médecine nucléaire ?
Justification
Optimisation
Activité injectée
Temps de comptage
Paramètres individuels
Type de rayonnements émis
Choix de l’isotope
![]()
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree


Expositions aux radionucléides : médecine nucléaire, accidents et attentats
9
En médecine nucléaire, l’exposition du patient résulte de l’administration d’un médicament radiopharmaceutique à l’origine d’une situation de contamination radioactive interne. Le marquage radioactif du traceur moléculaire est nécessaire pour sa détection par voie externe et pour la réalisation d’une image, en projection ou en coupes, de sa distribution dans l’organisme.
La distribution du traceur dépend des propriétés physiologiques de la molécule vectrice. Pour une application diagnostique donnée, un traceur est choisi en fonction de sa capacité d’incorporation dans une chaîne métabolique ou de fixation sur une cible moléculaire la plus spécifique de l’affection étudiée. Les caractéristiques biochimiques du traceur vont donc aboutir à son accumulation préférentielle au sein de certains organes, de certains tissus de ces organes ou au sein des lésions elles-mêmes. On notera par ailleurs des accumulations non spécifiques, le plus souvent liées à l’ élimination du traceur. Elles sont principalement vues dans les cavités excrétrices rénales et le tractus urinaire, voie majeure d’ épuration des traceurs et de leurs métabolites.
Les rayonnements émis par les traceurs utilisés en médecine nucléaire sont électromagnétiques, principalement gamma d’origine nucléaire, et corpusculaire sous la forme de radioactivité bêta, négative ou positive, d’ énergie variable selon les éléments ou d’ électrons Auger de faible énergie. Ces deux types de rayonnements aboutissent à deux formes d’exposition différentes.
Le rayonnement β-, émis par le noyau, ou les électrons Auger, émis par le nuage électronique, des atomes radioactifs sont arrêtés dans le milieu où ils ont été émis. Ils vont donc céder toute leur énergie à ce milieu et la distance qu’ils y parcourent est proportionnelle à leur énergie d’ émission. En moyenne, un électron de 2 MeV parcourt 1 cm dans un milieu liquide (cf. chapitre 2). Dans le cas d’un traceur radioactif qui s’est concentré dans un tissu, c’est celui-ci qui recevra toute l’ énergie cédée par les électrons émis et donc la dose correspondante. Le rayonnement β de l’iode 131 a un parcours moyen de 2 mm dans les tissus. Ceci explique que ces rayonnements β sont à l’origine d’une dose locale potentiellement importante et constituent le principe de base des applications de radiothérapie métabolique. En revanche, ces rayonnements sortent peu du tissu où le traceur s’est accumulé et il n’en résulte pas d’exposition significative à distance. Seule la composante γ éventuellement associée à l’ émission β sera source d’exposition à distance du patient. Le phosphore 32, émetteur β pur utilisé pour le traitement d’affections osseuses ou hématologiques, n’induit pas d’exposition dans l’environnement du patient.
Ils ne sont pas arrêtés mais seulement atténués par les tissus. De ce fait, l’accumulation d’un traceur émetteur de ce type de rayonnement au sein d’un organe transforme celui-ci en source de radiations ionisantes pour d’autres organes situés à distance. En corollaire, ils n’interagissent que peu dans l’organe de concentration du traceur et ne sont à l’origine que d’une faible exposition locale. Ces rayonnements sont à la base des applications diagnostiques des traceurs radioactifs puisqu’ils seront détectables à l’extérieur du patient et ne déposent qu’une part de leur énergie au sein des tissus, limitant ainsi l’exposition du patient.
Elle correspond au temps au bout duquel la moitié de la radioactivité a disparu du corps du patient à qui le traceur a été injecté. Elle comprend deux termes : la période physique, Tp, du radionucléide qui représente la durée au bout de laquelle son activité a décru de façon spontanée d’un facteur 2 et la période biologique, Tbiol, du traceur qui est le temps au bout duquel la moitié de la quantité de traceur injectée a été éliminée du corps.
La période effective Teff est égale au produit de ces deux périodes divisées par leur somme :
La forme de cette équation indique que la période effective est toujours plus proche de la période la plus courte. Plus la période effective est longue, plus la dose efficace délivrée au patient est élevée. La période effective de l’iode 131 est de 7,6 jours, il est donc totalement éliminé du patient après 2 mois environ.
Pour calculer la dose reçue par un organe et non plus à l’ensemble de l’organisme, on utilise le temps de résidence qui rend compte de la persistance d’un traceur au sein d’un organe ou d’un tissu.
La dose délivrée au patient est linéairement reliée à la quantité de radioactivité injectée. L’activité injectée conditionne le rapport signal/bruit des images, donc la qualité d’image, pour une durée d’acquisition donnée. Un rapport signal/bruit comparable pourra être obtenu en augmentant l’activité injectée ou en augmentant le temps d’acquisition des données. Le choix de l’activité injectée dépend donc de la qualité d’image voulue, du temps d’acquisition que l’on estime compatible avec la réalisation pratique des examens et, évidemment, de l’exposition acceptable du patient.
Un autre paramètre de choix de la quantité d’activité injectée est le type d’acquisition envisagée. Lorsque l’acquisition est divisée en images élémentaires afin de réaliser une étude séquentielle au cours du temps pour représenter de façon dynamique l’accumulation et l’ élimination du radiopharmaceutique, il faudra injecter une plus grande activité. C’est le cas également lorsque l’acquisition est faite en projections selon différents angles de vue afin de reconstruire des images tomographiques du volume étudié. L’accroissement de l’activité injectée est imposé par la nécessité de disposer d’un rapport signal/bruit suffisant pour ces images élémentaires, le temps d’acquisition de chacune d’elle étant nécessairement bref afin de maintenir l’acquisition totale dans un temps compatible avec la pratique clinique, 20 à 40 minutes en pratique.
Il s’agit d’un processus complexe en raison de l’hétérogénéité de la distribution des traceurs employés, de l’ évolution au cours du temps de cette distribution liée à l’ élimination et au métabolisme des molécules ainsi qu’au caractère dynamique des processus radioactifs.
Il est nécessaire de disposer pour chaque traceur employé de la cartographie type de sa distribution dans l’organisme identifiant les différents organes et tissus où il se concentre. Pour chaque organe, il est nécessaire de disposer de mesures de la concentration radioactive et de son évolution au cours du temps. De même, les voies de métabolisme et d’ élimination du traceur doivent être connues ainsi que l’ évolution au cours du temps de la radioactivité du corps entier.
En tenant compte des rayonnements émis par le marqueur radioactif, il est possible de calculer la dose délivrée aux organes concentrant le traceur. Lorsque le radioélément est émetteur bêta, la dose est délivrée in situ dans l’organe cible. À titre d’exemple, la dose délivrée à la thyroïde d’un adulte après absorption de 37 MBq d’iode 131 est de 13 Gy environ. Lorsque le radionucléide est émetteur gamma, il est nécessaire de calculer l’exposition des autres organes à partir des différents organes ayant accumulé le traceur. Des fantômes anthropomorphes sont utilisés pour calculer les paramètres de cette exposition à distance. Ainsi, à partir de l’ensemble de ces données, des procédures de calcul permettent de fournir une estimation de la dose aux principaux organes cibles, en mGy/MBq et de la dose efficace au corps entier en mSv/MBq.
La difficulté de ces calculs est accrue par différents paramètres qui influent sur la distribution du traceur au sein de l’organisme.
C’est un paramètre très important car la part anatomique et fonctionnelle des organes varie au cours de l’enfance jusqu’ à l’ âge adulte. Il a donc été nécessaire d’obtenir des données quantitatives spécifiques de tranches d’ âge au moyen de fantômes adaptés à ces différents âges. En pratique, l’enfance est divisée en 4 classes d’ âge.
D’autres paramètres tiennent à l’ élimination des traceurs. Ainsi, la dose délivrée par une même activité sera plus importante chez un insuffisant rénal en raison de l’allongement de la période biologique et donc effective d’un traceur à élimination rénale.
Enfin, il existe des variations de distribution entre les patients pour un même traceur. Si une tumeur accumule un traceur de façon importante, elle devient une source radioactive éventuellement intense pour les organes adjacents. Or il n’est pas possible de prévoir l’ensemble des configurations possibles pour les localisations tumorales et l’estimation dosimétrique devient donc particulièrement difficile.
Quoi qu’il en soit, il existe actuellement des valeurs dosimétriques tabulées, calculées sur la base de tels modèles de distribution et de fantômes. Elles sont proposées pour les principaux organes cibles et pour le corps entier avec des pondérations en fonction de l’ âge et, le cas échéant, de la fonction rénale. Le document 53 de la CIPR est entièrement consacré à ces données dosimétriques et, plus récemment, le document 80 fournit des valeurs complémentaires. Pour les raisons indiquées ci-dessus, ces documents ne peuvent tenir compte de l’accumulation tumorale éventuelle des traceurs et l’estimation accessible est nécessairement approximative pour un patient donné.
Comme pour toutes les applications d’imagerie médicale, le premier paramètre de réduction de la dose est la justification de l’investigation projetée. Son principe en est la discussion de l’indication entre le médecin référent et le spécialiste de médecine nucléaire dont le rôle est également de connaître les autres techniques d’imagerie afin d’orienter un patient vers une autre technique n’utilisant pas les RI si elle est d’efficacité égale ou supérieure.
Par ailleurs, le développement actuel de l’imagerie métabolique, très sensible au contexte de réalisation de l’examen, notamment du fait des traitements mis en œuvre, impose un contrôle strict des paramètres susceptibles d’altérer la qualité des informations produites et de déterminer le temps optimal de réalisation de l’exploration en sachant différer celle-ci, si nécessaire.
Nous avons vu que les principaux facteurs de l’exposition sont la quantité de traceur radioactif injecté et la nature des rayonnements émis.
Elle dépend du rapport signal/bruit nécessaire. L’augmentation de l’activité injectée accroît ce rapport. Cependant, il existe une limite technique à l’activité utilisable. C’est la saturation du détecteur. À ce seuil de saturation, toute augmentation supplémentaire d’activité représente une exposition inutile du patient puisque le détecteur ne peut enregistrer plus d’ événements par unité de temps. Toutefois, les évolutions techniques actuelles des gamma-caméras et plus encore des TEP ont repoussé ces limites et la responsabilité de l’utilisateur est accrue en matière de choix d’activité à injecter. Le rôle de la personne spécialisée en radiophysique médicale est renforcé pour la détermination de l’activité et du rapport signal sur bruit optimaux pour une application donnée. Par contre, malgré l’amélioration de la sensibilité de détection des appareils et l’allongement du temps d’acquisition, une réduction excessive de l’activité injectée conduira nécessairement à une dégradation de la statistique de comptage et donc de la qualité des images ainsi que de leur validité diagnostique.
La limitation de dose, pour un rapport signal/bruit donné, peut être obtenue par l’augmentation du temps de recueil des données. L’inconvénient est le risque de mouvements du patient au cours d’une acquisition très longue. Ces mouvements aboutissent à une dégradation de la qualité des images.
L’activité injectée doit également être fixée en fonction de paramètres tenant au patient lui-même et il est indispensable de disposer d’abaques d’activités tenant compte du poids, de l’ âge et, en fonction du métabolisme du traceur, de données physiologiques comme la fonction rénale par exemple.
C’est un paramètre fondamental de l’optimisation des explorations scintigraphiques. Le choix judicieux du radionucléide peut conduire à une réduction importante de l’exposition. Un exemple est fourni par le remplacement, en diagnostic, de l’iode 131 par l’iode 123 tant pour les explorations thyroïdiennes que pour le marquage de la meta-iodobenzylguanidine MIBG, (utilisée comme traceur des phéochromocytomes ou des tumeurs carcinoïdes), ou de ligands de la neurotransmission. L’iode 123 est un émetteur gamma pratiquement pur de moyenne énergie (170 keV) et de courte période physique (13 heures) alors que l’iode 131 est émetteur gamma à haute énergie (360 keV) et bêta (600 keV d’ énergie maximale), avec une période relativement longue (8 jours). En moyenne, l’iode 131 engendre une exposition 10 fois supérieure à celle due à l’iode 123. De plus, l’efficacité de détection des gamma-caméras est bien meilleure pour les rayonnements de basse énergie de l’iode 123 que pour ceux de l’iode 131, autre facteur d’accroissement du rapport signal/bruit lorsque l’isotope 123 est utilisé.
On peut également substituer à un traceur spécifique un traceur de comportement physiologique différent mais apportant des informations diagnostiques comparables avec des performances équivalentes. Le premier exemple est l’utilisation de traceurs marqués au technétium 99m pour l’imagerie de la perfusion myocardique et le diagnostic de la maladie coronaire en remplacement du thallium 201. Ce dernier est un analogue du potassium et il est distribué dans les mêmes secteurs biologiques que cet élément, alors que les substances technétiées ont une affinité pour les enzymes mitochondriales de la respiration cellulaire. Au plan dosimétrique, le thallium est très pénalisant, du fait d’une émission électromagnétique à faible énergie (80 keV) fortement atténuée par les tissus et d’une période physique de 3 jours. Au contraire, le technétium est un émetteur gamma pur de 140 keV avec une période courte de 6 heures qui permet l’obtention d’images de qualité supérieure tout en générant une exposition inférieure malgré une activité injectée supérieure à celle du thallium.
Le dernier exemple est celui, historique, de la scintigraphie au gallium 67 utilisée pour la mise en évidence de masses résiduelles de lymphomes. Émetteur de plusieurs rayonnements gamma de moyenne et haute énergie, de longue période physique et biologique, cet élément était responsable d’une des plus fortes expositions en médecine nucléaire. De plus, l’activité utilisable étant nécessairement limitée, la qualité des images était fréquemment médiocre. Malgré un métabolisme différent, le flurodéoxyglucose (FDG) utilisé en tomographie par émission de positons procure une efficacité diagnostique supérieure et une qualité d’image incomparable pour une exposition quatre fois moindre en raison de la très courte période physique et biologique du fluor 18, pourtant émetteur de rayonnements gamma à haute énergie après l’annihilation des positons.





