Chapitre 5 Myomes utérins
• Énumérer les principales complications des myomes en fonction de leur localisation. (B)
• Diagnostiquer une nécrobiose aseptique et mettre en route la thérapeutique la plus appropriée. (B)
• Mettre en œuvre les thérapeutiques nécessaires devant un myome entraînant des ménorragies. (A)
• Exposer les indications du traitement chirurgical des myomes et de ses alternatives. (A)
Fréquence
Elle est extrêmement importante puisque 20 % des femmes de 30 ans et 50 % des femmes de 50 ans sont porteuses de myomes Buttram et al., 1981 ; Verkauf, 1992 ; Rongières, 1999), l’obésité et la stérilité sont retrouvées chez 27,5 % des porteuses de fibromes (Verkauf, 1992). La fréquence diminue avec la parité et le tabagisme. Les femmes de race noire sont atteintes trois ou quatre fois plus souvent (Rongières, 1999).
Étiologie
On ne connaît rien de précis sur l’étiologie des myomes utérins.
 il n’y a pas de myome avant la puberté ;
il n’y a pas de myome avant la puberté ;
 les myomes se stabilisent ou peuvent régresser après la ménopause ou après castration, ou traitement par analogues du GnRH ;
les myomes se stabilisent ou peuvent régresser après la ménopause ou après castration, ou traitement par analogues du GnRH ;
 les myomes s’accroissent parfois rapidement pendant la grossesse pour régresser ensuite ;
les myomes s’accroissent parfois rapidement pendant la grossesse pour régresser ensuite ;
 les myomes augmentent parfois sous traitement estroprogestatif ;
les myomes augmentent parfois sous traitement estroprogestatif ;
 les myomes augmentent sous traitement estrogénique après la ménopause ;
les myomes augmentent sous traitement estrogénique après la ménopause ;
 l’endomètre des femmes porteuses de fibrome témoigne d’une hyperœstrogénie : il existe habituellement une hyperplasie de l’endomètre, source de saignements.
l’endomètre des femmes porteuses de fibrome témoigne d’une hyperœstrogénie : il existe habituellement une hyperplasie de l’endomètre, source de saignements.
Ces faits (en particulier la régression partielle après analogues du GnRH et la réaugmentation de taille à l’arrêt) conduisent à penser que les cellules des fibromes peuvent produire elles-mêmes de l’estrone et de l’estradiol puisque l’enzyme de conversion de l’estrone en estradiol, la 17-β-hydroxystéroïde oxydoréductase est présente dans le myomètre. Une activité aromatase a été mise en évidence dans les fibromes, en témoigne l’efficacité des anti-aromatases sur le volume des myomes. Les cellules des fibromes possèdent des récepteurs de l’estradiol et de la progestérone. La progestérone posséderait aussi un rôle de croissance tumorale soit direct, soit indirect par l’intermédiaire de l’EGF (Christin-Maitre, 1999) ; en témoigne l’efficacité des antiprogestatifs de type mifépristone (Mifégyne®) ou ulipristal (Ellaone®).
Pourquoi le gène CPY-19 s’active-t-il localement et permet-il le développement du myome ? Par un mécanisme paracrine ou autocrine ? La question est sans réponse. On sait simplement que l’AMP-C active son expression (Simpson, 1994).
Des facteurs de croissance tels que l’EGF, l’IGF-1, l’IGF-2 et le PDGF ont également été mis en évidence au niveau des cellules des myomes (Rein et al., 1992). Les myomes seraient donc des clones cytogénétiquement anormaux de cellules dérivées d’une cellule myométriale ayant subi une mutation somatique et dont les mécanismes, qui contrôlent sa croissance, sont perturbés (Barbieri et al., 1992).
Anatomie pathologique
Anatomie macroscopique
Le myome est une tumeur bénigne du muscle lisse d’où son nom plus adapté que celui de fibrome car il y a peu de tissu fibreux, elle est arrondie, dure, élastique, limitée par une pseudo-capsule qui permet le clivage entre le muscle utérin et le fibrome (c’est la myomectomie). Le myome est rarement seul, son volume varie de celui d’une tête d’enfant à un grain de mil. Ces minuscules myomes « graines de myome » sont souvent laissés en place dans une myomectomie qui ne permet que l’ablation des gros myomes, ce qui explique la fréquence des récidives après ces traitements conservateurs (50 % à 5 ans d’après Fédélé et al., 1995).
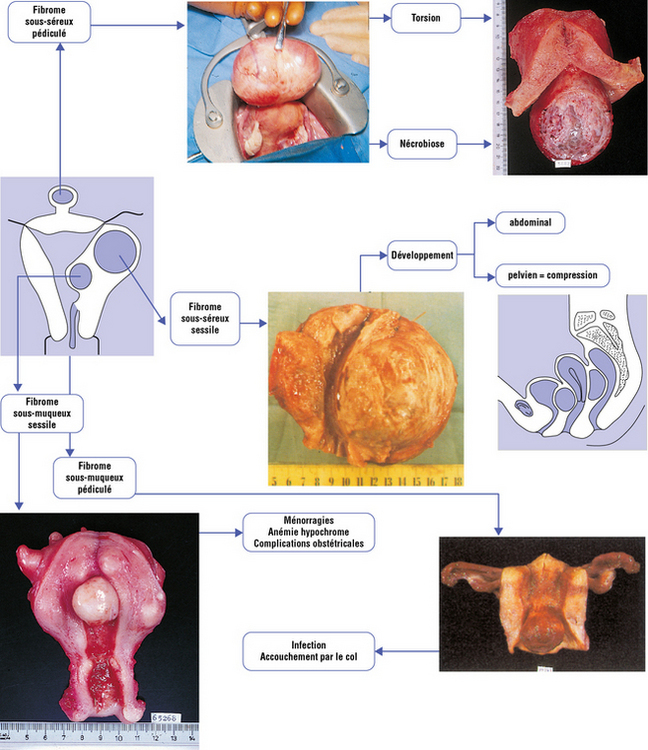
Le siège du myome varie en fonction des différentes parties de l’utérus (planche 5.1).
Si l’on envisage sa situation par rapport à la paroi utérine (cf. planche 5.1), le fibrome peut être sous-péritonéal (ou sous-séreux) et, dans ce cas, pédiculé ou sessile ; il peut aussi être interstitiel, ou intramural siégeant dans l’épaisseur du muscle qu’il refoule, ou sous-muqueux, faisant saillie dans la cavité utérine de type 2 (< 50 % intracavitaire) ou de type 1 (> 50 %). Le plus souvent, il a une base d’implantation large mais il peut être pédiculé, réalisant alors un myome sous-muqueux de type 0 de l’utérus qui peut éventuellement être accouché par le col.
Évolution et complications
Hémorragies
Nous le reverrons à la clinique, les ménorragies sont un signe et une complication fréquente des myomes, soit du fait de l’hyperplasie glandulaire créée par le déséquilibre estroprogestatif (et répondant bien au traitement progestatif) et associée à l’augmentation de taille du volume utérin, soit du fait d’une atrophie de l’endomètre, la pression mécanique exercée par les myomes sous-muqueux créant les conditions favorables au saignement : ulcération, infection, endométrite hémorragique (figure 5.1).
Transformation
Le myome peut se transformer, le mode de transformation le plus habituel étant la dégénérescence hyaline. Mais il peut également subir une nécrobiose aseptique par trouble de sa vascularisation ; il prend alors une teinte violet hortensia ; œdème et hémorragie dissocient les fibres musculaires. Il peut également se calcifier et apparaître sur un cliché de l’abdomen sans préparation. Il est parfois le siège d’une dégénérescence kystique, la dégénérescence hyaline évoluant vers la liquéfaction et la formation de cavités liquidiennes. La dégénérescence sarcomateuse est exceptionnelle et il est probable qu’il s’agisse plutôt d’un leiomyosarcome primitif.
Clinique
Signes fonctionnels
Le signe fonctionnel révélateur essentiel est la ménorragie : règles plus abondantes (hyperménorrhée) et surtout plus prolongées (de 10 à 25 jours). Souvent, elle s’associe à une polyménorrhée, les règles se répétant à intervalles rapprochés.
Les métrorragies isolées sont rares (10 % des cas).
Souvent, il s’agit de ménométrorragies pouvant donner un aspect presque continu aux hémorragies.
Les leucorrhées sont banales, surtout abondantes avant les règles ; rarement, il s’agit d’une hydrorrhée ou d’une pyorrhée (celle-ci doit faire soupçonner une complication septique ou une autre affection associée).
Les douleurs sont variables, soit à type de pesanteur pelvienne ou rectale, soit au contraire aiguës, à type de torsion ou de coliques expulsives.
Examen gynécologique
Examen du col au spéculum
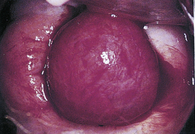
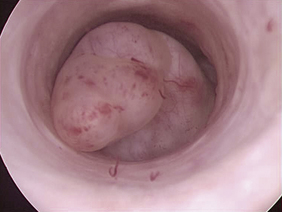
Parfois un myome sous-muqueux pédiculé peut apparaître à travers l’orifice cervical (figure 5.2). Le myome est parfois noirâtre, sphacélé et peut être pris à tort pour un polype ou un cancer.
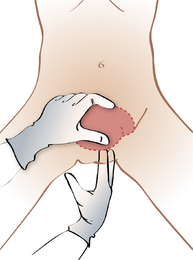
Toucher vaginal combiné au palper abdominal (figure 5.3)
 la situation du col : dévié ou non ;
la situation du col : dévié ou non ;
 la situation du corps utérin : antéversé ou rétroversé, déformé par une masse arrondie, lisse, de volume variable, ferme et élastique ou dure, surtout indolore, mobile et solidaire du corps utérin auquel sont transmis les mouvements imprimés à la tumeur et inversement, sans sillon de séparation entre la lésion et le corps utérin ;
la situation du corps utérin : antéversé ou rétroversé, déformé par une masse arrondie, lisse, de volume variable, ferme et élastique ou dure, surtout indolore, mobile et solidaire du corps utérin auquel sont transmis les mouvements imprimés à la tumeur et inversement, sans sillon de séparation entre la lésion et le corps utérin ;
 au niveau des annexes, le toucher vaginal étudiera l’état des ovaires, la souplesse et la sensibilité des culs-de-sac vaginaux ;
au niveau des annexes, le toucher vaginal étudiera l’état des ovaires, la souplesse et la sensibilité des culs-de-sac vaginaux ;
 enfin, on n’omettra pas d’examiner le périnée, l’âge habituel de survenue du myome étant également celui d’un prolapsus vaginal.
enfin, on n’omettra pas d’examiner le périnée, l’âge habituel de survenue du myome étant également celui d’un prolapsus vaginal.
Examens complémentaires
La pratique du frottis cervical est nécessaire, s’il n’y en a pas eu de récents (< 3 ans).
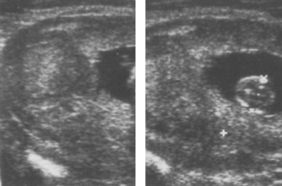
Échographie (figures 5.4a et b et 5.5)
C’est l’examen diagnostique de référence (Np3). Elle doit être réalisée par voie transabdominale et transvaginale (Np1).
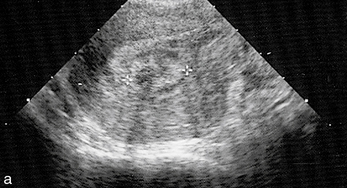
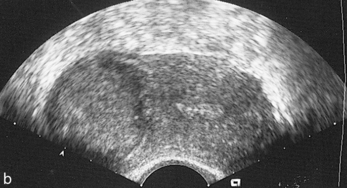
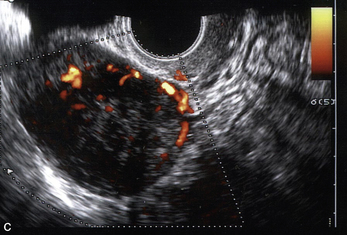
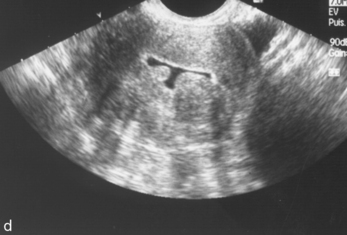
Figure 5.4 a. Coupe transversale de l’utérus : myome sous-muqueux.
c. Échographie doppler d’un myome.
Les myomes sous-séreux sont les plus faciles à reconnaître, déformant le contour externe de l’utérus. Cependant, un myome à pédicule étroit peut être confondu avec une tumeur de l’ovaire pleine comme un fibrothécome.
Les myomes sous-muqueux sont difficiles à voir en échographie abdominale mais sont bien vus en échographie vaginale ou en sonohystérographie. Ils dévient l’image linéaire de la cavité.
Le doppler couleur permet d’apprécier la topographie et l’importance des vaisseaux nourriciers qui entourent le myome (figure 5.4c) et permet de différencier un adénomyome d’un myome (Np4). L’étude hémodynamique ne permet pas de prévoir l’évolution du myome (Bernard et al., 1999).
L’hystérosonographie est un bon moyen d’exploration de la cavité utérine lorsqu’un myome sous-muqueux est suspecté (figure 5.4d).
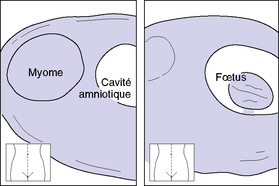
En cas de grossesse, l’œuf pourra être vu au milieu des myomes (cf. figure 5.5).
Il existe cependant des pièges qu’il faut connaître :
 lorsque l’utérus est rétroversé, on peut confondre sur une coupe longitudinale un fond utérin normal avec un myome du fond ;
lorsque l’utérus est rétroversé, on peut confondre sur une coupe longitudinale un fond utérin normal avec un myome du fond ;
 en position latérale, un myome sous-séreux à pédicule étroit peut en imposer pour une tumeur solide de l’ovaire ;
en position latérale, un myome sous-séreux à pédicule étroit peut en imposer pour une tumeur solide de l’ovaire ;
 une volumineuse masse ovarienne abdominopelvienne à prédominance solide peut prêter à confusion si on ne voit pas un utérus normal indépendant refoulé dans le Douglas.
une volumineuse masse ovarienne abdominopelvienne à prédominance solide peut prêter à confusion si on ne voit pas un utérus normal indépendant refoulé dans le Douglas.
Hystéroscopie
 affirmer le diagnostic de myomes sous-muqueux ;
affirmer le diagnostic de myomes sous-muqueux ;
 préciser les possibilités de résection endoscopique des myomes sous-muqueux de moins de 2 ou 3 cm (figure 5.6).
préciser les possibilités de résection endoscopique des myomes sous-muqueux de moins de 2 ou 3 cm (figure 5.6).
Radiographie sans préparation du pelvis
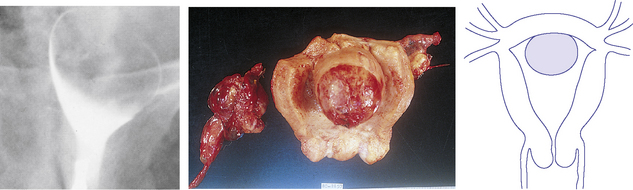
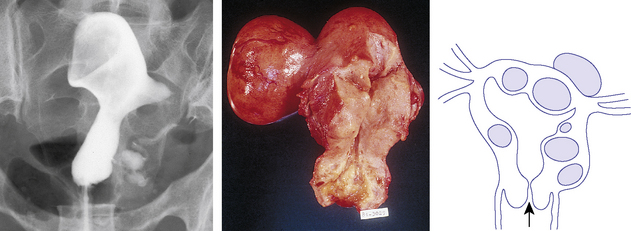
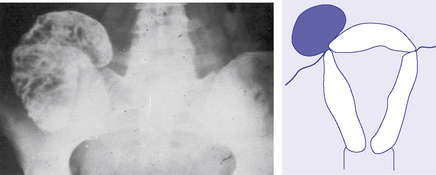
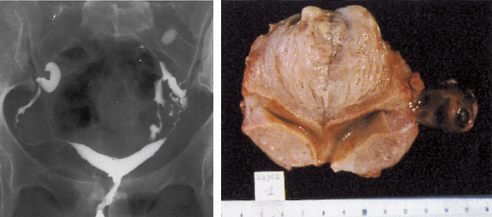
Elle peut repérer un myome calcifié (planche 5.2).
Hystérosalpingographie
Elle est peu prescrite du fait des progrès de l’échographie et de l’IRM. Elle peut être pratiquée (cf. planche 5.2) :
 en l’absence de contre-indications :
en l’absence de contre-indications :
 lorsqu’elle est utile : c’est-à-dire dans un contexte d’infertilité (Np4) de façon à voir aussi la qualité des trompes.
lorsqu’elle est utile : c’est-à-dire dans un contexte d’infertilité (Np4) de façon à voir aussi la qualité des trompes.
Les résultats de l’hystérographie sont les suivants :
 un myome sous-muqueux intracavitaire se traduit par :
un myome sous-muqueux intracavitaire se traduit par :
 une image lacunaire intracavitaire, permanente, régulière à bords nets, bien visible sur le profil qui montre sa base d’implantation. Celle-ci est utile à connaître pour diriger la voie d’abord en cas de myomectomie ;
une image lacunaire intracavitaire, permanente, régulière à bords nets, bien visible sur le profil qui montre sa base d’implantation. Celle-ci est utile à connaître pour diriger la voie d’abord en cas de myomectomie ; un myome interstitiel se traduit par une déformation des bords de la cavité : empreinte régulière réalisant une image de soustraction. Plusieurs myomes donneront une image à contours polycycliques ;
un myome interstitiel se traduit par une déformation des bords de la cavité : empreinte régulière réalisant une image de soustraction. Plusieurs myomes donneront une image à contours polycycliques ;
 les myomes sous-séreux ne donnent souvent aucune image radiologique. La cavité est de forme normale, parfois des signes indirects sont seuls visibles, latérodéviation de la cavité, image étirée d’une trompe. Ces différents types d’images peuvent s’associer pour déformer la cavité utérine.
les myomes sous-séreux ne donnent souvent aucune image radiologique. La cavité est de forme normale, parfois des signes indirects sont seuls visibles, latérodéviation de la cavité, image étirée d’une trompe. Ces différents types d’images peuvent s’associer pour déformer la cavité utérine.
IRM
Elle est plus souvent prescrite du fait des alternatives au traitement chirurgical qui en sont la principale indication en plus des échecs de l’échographie. Son caractère reproductible et peu opérateur dépendant en fait un examen de référence pour le pelvis ; elle nécessite des coupes en T1, T2 et gadolinium avec coupes en sagittal, coronal et transversal. Le myome est souvent en hypo-T2 comparé au myomètre avec une vascularisation variable lors de l’injection du gadolinium, l’injection du produit de contraste faisant apparaître le myome souvent avant le reste du myomètre, l’intensité de la prise de contraste permet de prévoir sa vascularisation.
Bilan général
Un bilan général complétera toujours l’étude clinique.
 le degré d’obésité, celle-ci pouvant poser des problèmes au chirurgien et à l’anesthésiste ;
le degré d’obésité, celle-ci pouvant poser des problèmes au chirurgien et à l’anesthésiste ;
 l’état cardio-artériel : prise de la tension artérielle, radiographie pulmonaire, électrocardiogramme ; le retentissement de l’anémie ;
l’état cardio-artériel : prise de la tension artérielle, radiographie pulmonaire, électrocardiogramme ; le retentissement de l’anémie ;
 l’état de la circulation veineuse, en particulier recherche d’antécédents de phlébite.
l’état de la circulation veineuse, en particulier recherche d’antécédents de phlébite.
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree