Chapitre 33 Échographie gynécologique pelvienne
Introduction
• La grossesse extra-utérine est peu fréquente (0,5 à 2 % des grossesses) mais doit être évoquée systématiquement chez toute femme en période d’activité génitale symptomatique (métrorragies, douleurs) en raison de sa gravité potentielle (mortalité et conséquences fonctionnelles).
• Le kyste hémorragique fonctionnel ou lutéal, lui, est une pathologie fréquente, dont la présentation échographique donne lieu à de nombreux faux positifs de grossesse extra-utérine ou de kystes organiques avec des prises en charge excessives ou inadaptées.
Généralités
Conditions de l’examen
Description échographique des organes
Utérus
Version, flexion, latérodéviation
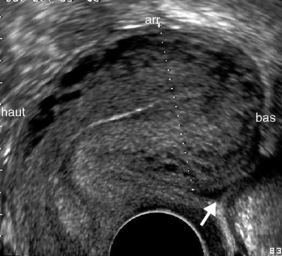
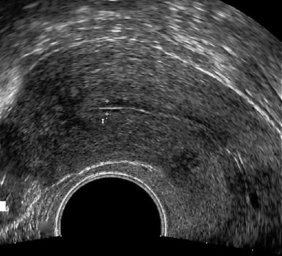
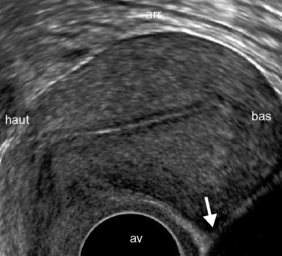
L’utérus est formé de deux structures fonctionnellement distinctes, le corps et le col. L’angle relatif entre le grand axe du corps et le grand axe du col définit la flexion. L’antéflexion est la configuration anatomique la plus fréquente mais la rétroflexion-rétroversion est physiologique mais peut parfois être induite par un processus rétractile pathologique (endométriose). Cette configuration est peu favorable à l’exploration par voie sus-pubienne et peut induire des diagnostics erronés notamment de myomes postérieurs. C’est pourquoi la voie endovaginale avec positionnement de la sonde dans le cul-de-sac vaginal postérieur devra lui être préférée (figures 33.1 et 33.2).
Différents segments utérins
L’utérus doit systématiquement être mesuré lors de l’échographie :
• en coupe sagittale la hauteur utérine (incluant le col), le diamètre antéropostérieur à hauteur du corps ;
• en coupe axiale le diamètre transverse évalué à hauteur de la naissance des ostiums tubaires (corporéo-fundiques).
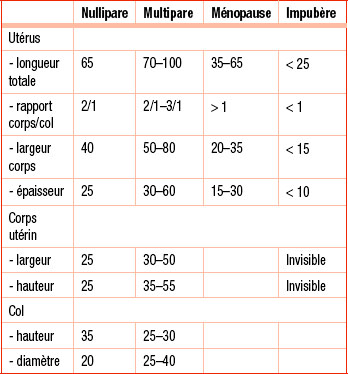
Les mensurations utérines varient en fonction de la parité et de l’imprégnation hormonale (involution ménopausique). Les ordres de grandeur sont résumés dans le tableau 33.1.
Structure utérine
Transversalement, l’utérus est constitué de plusieurs structures de dedans en dehors.
En phase ovulatoire, l’endomètre prend en coupe axiale, un aspect en cible (ligne cavitaire hyperéchogène-endomètre hypoéchogène-ligne basale hyperéchogène). Enfin, en phase sécrétoire ou lutéale, l’endomètre devient hyperéchogène de façon centripète à partir de la zone basale (développement des replis glandulaires endométriaux tortueux réfléchissant les ultrasons) pour devenir totalement hyperéchogène à J21, augmenter concomitamment de taille et atteindre 12 à 14 mm (tableau 33.4).
Tableau 33.4 Variations de l’aspect endométrial au cours du cycle.
| Phase menstruelle | Ligne cavitaire dédoublée Débris-caillots Endomètre non visible |
| Phase sécrétoire (J5-J14) | 1–12 mm Hypoéchogène |
| Phase ovulatoire | Environ 12 mm Hypoéchogène – Liseré basal Aspect en cocarde |
| Phase sécrétoire | 12–14 mm Hyperéchogénicité centripète Hyperéchogénicité complète J21 |
| Ménopause | 2 à 5 mm sans THM toujours < 8 mm hyperéchogène – parfois glandulokystique |
Ainsi, l’exploration des pathologies endométriales (en général hyperéchogène) devra s’effectuer en première partie de cycle afin de ne pas être masquée au sein d’un endomètre épais et hyperéchogène. À la ménopause l’endomètre régresse, il ne doit pas excéder 8 mm. Une taille entre 5 et 8 mm doit inciter à la prudence en l’absence de tout THM. La présence de multiples petites formations kystiques sont possibles ; elles sont cryptiques endométriales et correspondent à un endomètre glandulo-kystique classique dans le cadre de traitements hormonaux type Nolvadex®. Une épaisseur inférieure à 2 mm signe l’atrophie endométriale quel que soit le statut hormonal (figures 33.3 à 33.5).
Figure 33.3 Utérus antéversé par voie vaginale : l’endomètre est atrophique en raison d’une contraception progestative.
Ovaires
Les ovaires, de forme ovalaire, sont de localisation variable. Ils sont le plus généralement situés de part et d’autre de l’utérus dans la fossette ovarienne en arrière et en dessous des vaisseaux iliaques externes. C’est la localisation préférentielle chez les femmes nulligestes. Leur mise en évidence ne pose alors pas de problème particulier. L’ovaire peut être parfois localisé dans le cul-de-sac de Douglas ou être très haut. Pour les ovaires hauts situés, la main gauche peut abaisser les annexes par un palper abdominal ; mais parfois ils ne sont visualisables que par voie sus-pubienne (figures 33.6 et 33.7).
La taille de l’ovaire (tableau 33.2) varie en fonction de l’âge et du cycle. Il est préférable de mesurer la surface ovarienne plutôt que le grand axe seul. L’ovaire contient plusieurs follicules (en général entre 5 et 11) répartis régulièrement dans le parenchyme. Ils sont de petite taille. En phase menstruelle ou folliculaire précoce, 5 à 7 follicules de moins de 10 mm sont présents. En phase préovulatoire, au 8–10e jour, 1 ou 2 follicules deviennent prédominants et dépassent 14 mm de diamètre. Ils grandissent de 2 à 3 mm par jour pour atteindre un diamètre d’environ 20 mm (de 16 à 28 mm) avec une paroi discrètement épaissie et crénelée et parfois présence d’un cumulus oophorus (petit kyste dans le follicule) juste avant l’ovulation ; au moment de l’ovulation, l’ovocyte est expulsé et le follicule régresse en corps jaune (tableau 33.3). L’ovulation s’accompagne d’un petit épanchement physiologique parfois hémorragique dans le cul-de-sac de Douglas. Le corps jaune peut être d’aspect variable : en général sous forme d’une anfractuosité à centre liquidien hypoéchogène et paroi épaisse contournées, il peut être échogène en raison d’un saignement intrafolliculaire ou anéchogène s’il se transforme en un kyste lutéal pouvant atteindre la taille de 3 cm. En l’absence de grossesse, le corps jaune régresse et s’atrophie. Il n’est plus identifiable en fin de cycle.
Tableau 33.3 Follicule au cours du cycle.
| Phase folliculaire (J1-14) | 5 à 7 follicules antraux (2–9 mm) J8-10 : 1 follicule dominant 14 mm J10-14 : + 2 mm/j |
| Phase ovulatoire | Follicule dominant : 20–25 mm (→ 30 mm) Présence d’un cumulus oophorus Aspect épaissi et crénelé de la paroi folliculaire |
| Phase lutéale (J16-28) | Présence d’un corps jaune épaississement de la paroi folliculaire, parfois caillot Aspect parfois hétérogène, remanié kystique et hémorragique |
Pathologies utérines
Malformations utérines
Un défaut de fusion des canaux de Müller peut ensuite survenir, constituant l’ensemble des hémimatrices : utérus bicorne-bicervical (ou didelphe), utérus bicorne unicervical et utérus à fond arqué (fusion subcomplète) (figure 33.8), (vidéo 33.1![]() ).
).
Lorsque l’échographie est prise en défaut, l’IRM pelvienne permet de poser le diagnostic.
Pathologies myométriales
Adénomyose
Par voie endocavitaire, le diagnostic est évoqué devant :
• un utérus souvent asymétrique (dans les formes diffuses) ;
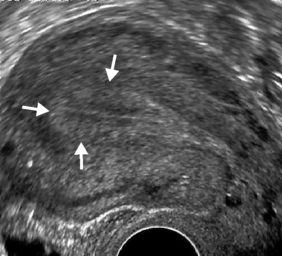
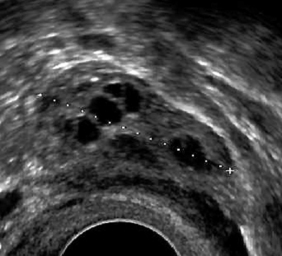
• la présence de lacunes myométriales anéchogènes, juxta-endométriale ou plus profondes – critère le plus sensible et le plus spécifique (Sp : 99 %, VPP : 99 %) –, correspondant aux foyers endométriaux hétérotopiques ;
• une jonction endomètre-myomètre mal définie, floue (figure 33.9) ;
• dans les formes localisée, des plages d’hétérogénéité myométriale localisée sans effet de masse, parfois un pseudo-nodule hyperéchogène (à ne pas confondre avec un myome) ;
• il peut également exister un aspect peigné, finement strié de la zone sous-endométriale (figure 33.10).
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree