Chapitre 3 Dosages biologiques en gynécologie
• Expliquer le rôle de l’hypothalamus dans la sécrétion des hormones gonadotropes hypophysaires. (C)
• Expliquer le rôle de l’hypothalamus dans la sécrétion de la prolactine. (C)
• Expliquer le rôle de FSH et de LH sur l’ovaire. (B)
• Expliquer les effets de la prolactine sur l’axe hypothalamo-hypophyso-ovarien. (B)
• Prescrire et interpréter un dosage qualitatif ou quantitatif d’HCG conformément aux références médicales opposables. (A)
• Comprendre le rôle important de la TSH dans le fonctionnement gonadique. (B)
• Prescrire les dosages suivants – (B) : progestérone plasmatique chez la femme normale ; prolactine plasmatique chez la femme normale ; testostérone plasmatique chez la femme normale ; FSH-LH chez la femme ménopausée.
• Prescrire et interpréter les dosages des principaux marqueurs tumoraux en gynécologie. (A)
Nous étudierons les dosages hormonaux puis les marqueurs tumoraux.
Rappel physiologique
Hypothalamus et fonction gonadotrope (figure 3.1)
Plusieurs groupes de neurones sécrètent la gonadolibérine ou GnRH au sein du noyau arqué ventromédian de l’hypothalamus antérieur (éminence médiane) et du noyau supra-optique.
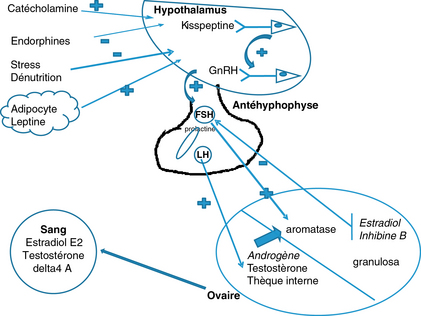
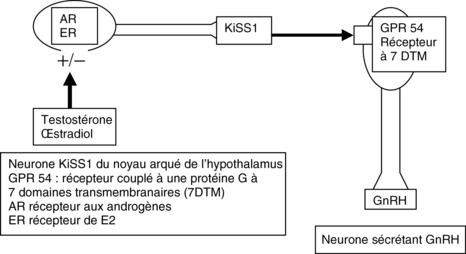
Figure 3.1 Régulation neuroendocrinienne de l’ovaire.
a. Régulation hypothalamo-hypophysaire.
b. Le système KiSS1–KiSS1R active les neurones sécrétant GnRH.
La sécrétion pulsatile de GnRH drainée par le système porte hypothalamo-hypophysaire entraîne la sécrétion pulsatile par l’hypophyse antérieure de FSH et LH destinées au développement folliculaire terminal.
La fréquence et l’amplitude de la pulsatilité de GnRH varient au cours du cycle. L’accélération de l’activité électrique du centre d’automatisme du noyau arqué ventromédian est suivie d’un pic de GnRH toutes les 120 minutes en début de phase folliculaire et toutes les 70 minutes environ en période ovulatoire.
Il existe une sensibilité particulière de l’éminence médiane à l’estradiol circulant capable, à partir d’un certain seuil, d’augmenter brutalement la sécrétion de GnRH entraînant le pic ovulatoire. C’est le feedback positif (non spécifique du système nerveux féminin) qui est mieux compris depuis la découverte de neurones contrôlant ceux qui sécrètent GnRH, en particulier le système KiSSpeptin-KiSSR (anciennement GPR 54). Les récepteurs KiSS sont situés sur les corps cellulaires des neurones GnRH (Roa, 2011).
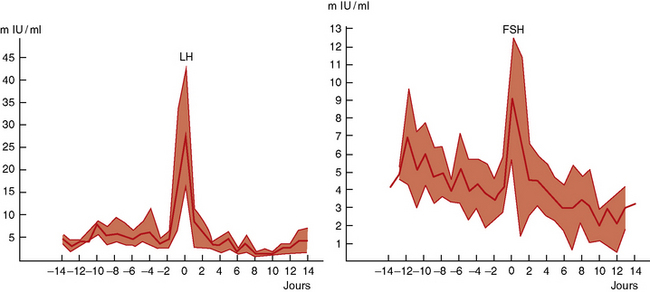
Parallèlement, lors du pic ovulatoire, la sensibilité des cellules gonadotropes est accrue par des taux croissant d’estradiol et, pour une même stimulation par GnRH, une réponse plus importante des gonadotrophines FSH et surtout LH est observée (figure 3.2).
Des éléments nouveaux complètent ces données physiologiques et c’est un domaine en pleine expansion. Le système KiSS1–Kiss1R active les neurones sécrétant GnRH. KiSS1R est un récepteur à sept domaines transmembranaires exprimé dans l’hypothalamus et l’antéhypophyse. Un ligand naturel de ce récepteur est un peptide de 54 acides aminés, Kisspeptine ou Kp (la métastine, produit de clivage de la protéine codée par le gène suppresseur de métastases KiSS1). Kp est un activateur de la sécrétion de GnRH et joue un rôle important dans l’initiation de la puberté. L’expression hypothalamique de KiSS1 est régulée par les stéroïdes sexuels chez les primates suggérant un rôle de ce système dans le feedback négatif. Par exemple, chez la souris, les neurones sécrétant KiSS sont situés dans les noyaux arqué et périventriculaire antéroventral (AVPV) de l’hypothalamus. La testostérone (par un récepteur des androgènes) ou l’estradiol (par un récepteur ERα) diminuent l’expression de KiSS1 au niveau du noyau arqué (rétrocontrôle négatif) mais ont des effets opposés dans l’AVPV (rétrocontrôle positif). L’absence de récepteurs ERα sur les neurones sécrétant GnRH (y compris chez les primates) rend le rôle stimulant de Kp tout à fait essentiel pour comprendre le rétrocontrôle positif qui s’exerce donc par cet intermédiaire. Toutefois, on sait que l’hypothalamus des rongeurs est différent de celui des primates et de l’humain et beaucoup reste à découvrir pour comprendre définitivement les mécanismes de feedback dans notre espèce (Roa, 2011).
D’autres neurones interfèrent, ceux sécrétant la neurokinine B (NKB), produit du gène TAC3 et la dynorphine (Dyn) dans le noyau arqué, y compris chez les primates et l’Homme. Certains neurones Kiss co-expriment NKB et Dyn donnant des neurones KNDy, augmentant la complexité (figure 3.1b). Des mutations inactivatrices de ces différents systèmes (Kp/KISSR, TAC3/TACR3) expliquent des cas d’hypogonadismes hypogonadotropes congénitaux.
La leptine sécrétée par les adipocytes exerce un rôle facilitant sur la pulsatilité de GnRH et des récepteurs de la leptine ont été localisés sur les neurones KiSS. Il s’agit donc d’une action en cascade.
Les stéroïdes ovariens sont synthétisés par les cellules des follicules en croissance : cellules de la granulosa qui aromatisent les androgènes produits par la thèque interne stimulée par LH, l’enzyme aromatase étant stimulée par FSH (cf. figure 3.8).
Par ailleurs, des peptides sont sécrétés par les cellules de la granulosa pour moduler au niveau de l’ovaire l’action des gonadotrophines. Les plus connus sont les inhibines qui freinent préférentiellement FSH : l’inhibine B est sécrétée par les cellules de la granulosa du follicule dominant et son taux circulant évolue parallèlement à celui de l’estradiol en phase folliculaire et en période ovulatoire ; l’inhibine A est sécrétée par les cellules de la granulosa lutéinisées du corps jaune et le taux circulant évolue parallèlement à celui de la progestérone en phase lutéale. Les inhibines spécifiques (A et B), comme les stéroïdes, peuvent maintenant être dosées dans le sang veineux périphérique.
L’encéphale, relais d’une infinité de stimuli et intégrateur de multiples neuropeptides tient les noyaux hypothalamiques sous sa dépendance par l’intermédiaire de substances excitatrices (noradrénaline, sérotonine) ou inhibitrices (dopamine, opiacés) ce qui rend compte de la fréquence des perturbations du cycle d’origine psychologique.
 la nécessité d’une stimulation discontinue (pulsatile) pour induire l’ovulation avec la GnRH ;
la nécessité d’une stimulation discontinue (pulsatile) pour induire l’ovulation avec la GnRH ;
 la possibilité d’empêcher la sécrétion des gonadotrophines et donc la maturation folliculaire par l’administration continue de ce peptide, l’emploi d’agonistes à demi-vie plus longue ou d’antagonistes qui saturent le récepteur et empêchent immédiatement l’action de la GnRH.
la possibilité d’empêcher la sécrétion des gonadotrophines et donc la maturation folliculaire par l’administration continue de ce peptide, l’emploi d’agonistes à demi-vie plus longue ou d’antagonistes qui saturent le récepteur et empêchent immédiatement l’action de la GnRH.
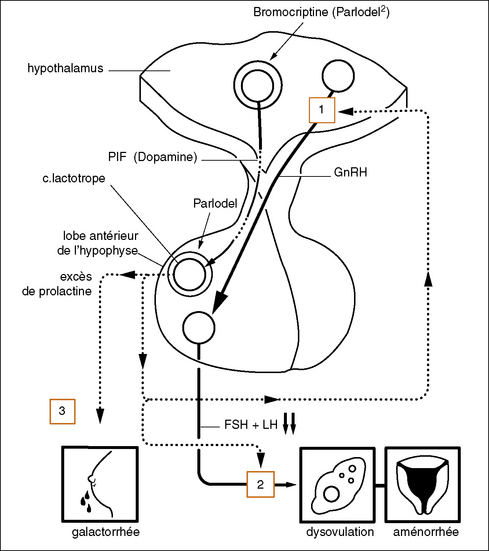
Hypothalamus et sécrétion de prolactine (figure 3.3)
L’hypothalamus intervient dans le contrôle de la sécrétion de prolactine (PRL) par un double mécanisme :
 un mécanisme d’inhibition par des prolactin inhibiting factor (PIF), le principal étant la dopamine sécrétée par l’hypothalamus. Elle atteint l’hypophyse antérieure par le système porte hypothalamo-hypophysaire et inhibe la sécrétion de prolactine ;
un mécanisme d’inhibition par des prolactin inhibiting factor (PIF), le principal étant la dopamine sécrétée par l’hypothalamus. Elle atteint l’hypophyse antérieure par le système porte hypothalamo-hypophysaire et inhibe la sécrétion de prolactine ;
 la sécrétion de prolactine stimule la sécrétion de dopamine par l’hypothalamus (utilisation du système porte hypothalamo-hypophysaire à contre-courant).
la sécrétion de prolactine stimule la sécrétion de dopamine par l’hypothalamus (utilisation du système porte hypothalamo-hypophysaire à contre-courant).
L’hyperprolactinémie interagit avec les hormones gonadotropes :
 en diminuant la fréquence et l’amplitude de la pulsatilité du GnRH (récepteurs de la PRL sur les neurones sécrétant GnRH) ou plus récemment sur les neurones KiSS1;
en diminuant la fréquence et l’amplitude de la pulsatilité du GnRH (récepteurs de la PRL sur les neurones sécrétant GnRH) ou plus récemment sur les neurones KiSS1;
 en abaissant les taux circulants de FSH et LH libérés par les cellules gonadotropes ;
en abaissant les taux circulants de FSH et LH libérés par les cellules gonadotropes ;
 en empêchant la maturation folliculaire et en abaissant le taux d’estradiol circulant. Correctement stimulés de façon pulsatile, la cellule gonadotrope et l’ovaire peuvent fonctionner normalement malgré l’hyperprolactinémie.
en empêchant la maturation folliculaire et en abaissant le taux d’estradiol circulant. Correctement stimulés de façon pulsatile, la cellule gonadotrope et l’ovaire peuvent fonctionner normalement malgré l’hyperprolactinémie.
Ainsi une prolactine élevée va entraîner le plus souvent une galactorrhée et une aménorrhée. La bromocriptine (Parlodel®) active les récepteurs à dopamine, ce qui freine la sécrétion de prolactine de la même manière que le fait la dopamine endogène ou d’autres PIF et bloque la libération hypophysaire de la prolactine en réserve.
La TRH a une activité de stimulation de la sécrétion de prolactine, en plus de celle de TSH.
Cycle ovarien
Cinq cents follicules primordiaux débutent une activité de croissance à chaque cycle, dont 15 à 20 vont évoluer. Il s’écoule 3 à 4 mois entre le moment où un follicule quitte le stade quiescent (follicule primordial) et celui de l’ovulation (figure 3.4).
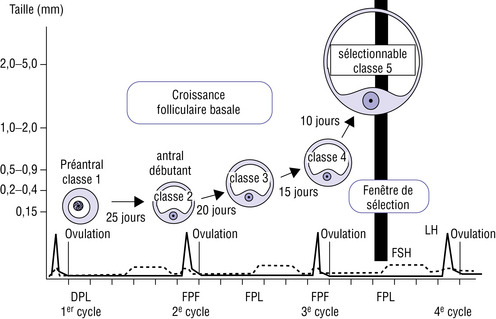
DPL : début de la phase lutéale. FPF : fin de la phase folliculaire. FPL : fin de la phase lutéale.
(d’après Gougeon, 2010)
La théorie des deux cellules, coopérant pour la synthèse des stéroïdes et la croissance folliculaire et des deux gonadotrophines, est fondamentale (cf. figure 3.1a). Les cellules de la granulosa sécrètent l’AMH apparenté à TGF-β (anti-Mullerian hormone) ; les cellules de Sertoli sécrètent aussi l’AMH qui inhibe in utero le développement des canaux de Müller chez l’homme. Des souris femelles qui sont dépourvues d’AMH ont des ovaires contenant moins de follicules primordiaux mais plus de follicules en croissance. L’AMH joue donc un rôle de blocage (protection) du stock de follicules primordiaux. Les taux circulants diminuent avec l’âge et un taux bas est le témoin d’un capital folliculaire (follicules antraux de 5 mm) faible. À l’opposé, le taux d’AMH circulant est élevé dans le syndrome des ovaires micropolykystiques où le nombre de petits follicules est augmenté, ce qui pourrait contribuer à expliquer l’anovulation de ces patientes par inefficacité relative de FSH.
FSH augmente la population de cellules de la granulosa et la production d’estrogènes et d’inhibine, ce qui va freiner la sécrétion de FSH et arrêter le développement des follicules les moins développés n’en épargnant qu’un ou deux : le follicule dominant. Ce phénomène se produit au 5e–7e jour du cycle. On peut distinguer le follicule dominant sur des critères morphologiques. La granulosa de ce follicule est le siège d’une multiplication cellulaire intense avec synthèse de l’estradiol par aromatisation des androgènes (Young, 1999).
On a insisté récemment sur le rôle de modulation des facteurs de croissance, mais beaucoup d’inconnues demeurent. Parmi les facteurs de prolifération stimulant les mitoses, citons l’EGF (epidermal growth factor) qui favorise aussi la vascularisation ; l’IGF-1 (insulin like growth factor de type I) synthétisé par les cellules de la thèque interne, qui agit en synergie avec FSH pour augmenter les mitoses. Une protéine du groupe des inhibines, l’activine, synthétisée par les cellules de la granulosa augmente l’expression du récepteur de FSH sur ces mêmes cellules.
La maturation du follicule s’accompagne d’un arrêt de la prolifération (le nombre des mitoses s’annule). L’IGF-2 (insulin like growth factor de type II) synthétisé par les cellules de la granulosa et prédominant dans notre espèce inhibe les fonctions FSH induite et principalement l’aromatase. L’IGF-2 induit l’apparition de récepteurs de LH sur les cellules de la granulosa en préovulatoire. Le TGF-β (transforming growth factor) synthétisé par les cellules de la granulosa s’oppose à l’action proliférante de l’EGF.
Ce schéma sans cesse plus complexe sera sans doute précisé dans un avenir proche.
La thèque s’épaissit et se différencie en deux couches externe et interne, elle seule fabrique les stéroïdes androgènes (androstènedione et testostérone) sous l’influence de LH. C’est l’aromatisation par les cellules de la granulosa des androgènes sécrétés par la thèque interne (androstènedione → estrone, testostérone → estradiol) qui permet la production des estrogènes (cf. figure 3.8). Une application clinique en est la classe thérapeutique des inhibiteurs de l’aromatase dans le traitement hormonal du cancer du sein opéré.
La lutéinisation des cellules de la granulosa se poursuit sous l’influence de la LH dont les récepteurs ont été mis en place par IGF-2. Ces cellules lutéinisées sécrètent la 17-OH-progestérone, la progestérone, l’estradiol. En l’absence de nidation, le corps jaune involue après 14 jours d’existence par apoptose. Il se produit une lutéolyse avec atrésie et envahissement par du tissu conjonctif. Les courbes de l’estradiol et de la progestérone plasmatique au cours du cycle sont rapportées à la figure 3.5.
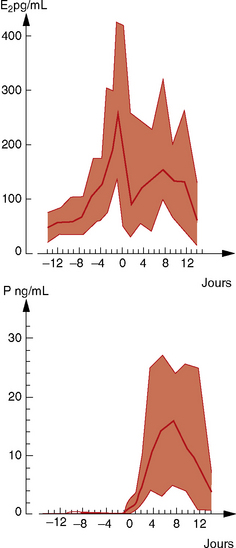
Figure 3.5 Variations du taux d’estradiol et de progestérone au cours du cycle.
Le jour 0 représente le jour de l’ovulation.
(d’après Scholler)
Après la ménopause, la disparition des follicules explique l’absence de sécrétion de l’œstradiol et de la progestérone mais aussi la chute de l’inhibine B et de l’AMH. Il a été montré récemment que le secteur androgénique de l’ovaire devenait fibreux et que la sécrétion des androgènes s’effondrait malgré l’élévation de la LH et de la FSH (secondaire à un taux d’inhibine B nul) (Young, 1999).
Un certain nombre de gènes intervenant dans la folliculogenèse ont été découverts récemment :
 le gène FOXL2 qui joue un rôle très précoce dans la folliculogenèse. Des mutations de ce gène expliquent les insuffisances ovariennes prématurées avec blépharophimosis, aspect particulier des paupières ;
le gène FOXL2 qui joue un rôle très précoce dans la folliculogenèse. Des mutations de ce gène expliquent les insuffisances ovariennes prématurées avec blépharophimosis, aspect particulier des paupières ;
 le gène BMP15 (bone morphogenic protein) qui, lorsqu’il est muté, donne aussi un tableau d’insuffisance ovarienne prématurée ;
le gène BMP15 (bone morphogenic protein) qui, lorsqu’il est muté, donne aussi un tableau d’insuffisance ovarienne prématurée ;
 enfin, le gène WnT4 qui joue un rôle dans la différenciation de la gonade féminine. Une mutation de ce gène a été trouvée chez une femme de 18 ans avec aménorrhée primaire, hyperandrogénie et absence d’utérus. Il s’agit d’un gène qui peut expliquer certains syndromes de Rokitansky-Küster-Hauser.
enfin, le gène WnT4 qui joue un rôle dans la différenciation de la gonade féminine. Une mutation de ce gène a été trouvée chez une femme de 18 ans avec aménorrhée primaire, hyperandrogénie et absence d’utérus. Il s’agit d’un gène qui peut expliquer certains syndromes de Rokitansky-Küster-Hauser.
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree