Chapitre 28 Contraception hormonale1
OBJECTIFS DES CHAPITRES 28 ET 29
• Expliquer aux couples les modalités, les avantages et les inconvénients de l’utilisation des – (B) : contraceptifs oraux ; stérilets ; préservatifs et diaphragmes ; spermicides ; méthode des températures.
• Énumérer les indications et contre-indications des – (A) : estroprogestatifs ; stérilets.
• Expliquer les différents types de contraceptifs oraux en vente en France. (B)
• Prescrire et surveiller une contraception orale. (A)
• Prescrire, poser et surveiller un stérilet. (B)
• Prescrire une contraception orale. (A)
• Prescrire une contraception du lendemain. (A)
• Mettre en route la conduite la plus appropriée chez une femme qui saigne – (B) : sous contraception orale ; avec un stérilet.
• Mettre en route la conduite la plus appropriée chez une femme qui a oublié de prendre un ou plusieurs comprimés de sa plaquette de pilules. (B)
• Prescrire un traitement médicamenteux chez une femme qui prend une contraception estroprogestative. (B)
• Mettre en route la conduite la plus appropriée chez une femme qui n’a plus ses règles – (B) : sous contraception orale ; avec un stérilet.
• Expliquer les indications et les méthodes de la stérilisation masculine et féminine. (B)
Situation paradoxale en France
Pourtant de nombreuses mesures ont été prises pour informer les couples, favoriser l’accessibilité aux consultations de contraception, faciliter la délivrance des produits contraceptifs. Citons l’éducation sexuelle obligatoire en milieu scolaire, l’autorisation de la stérilisation, la suppression de l’autorisation parentale pour les mineures, la délivrance gratuite de la contraception d’urgence (2001), la délivrance de la contraception hormonale par les sages-femmes dans les suites de couches ou d’IVG (2004), le renouvellement des ordonnances par les pharmaciens, l’examen gynécologique et la pose de stérilets par les sages-femmes (2009) (Aubin, 2009).
Malgré ces modifications législatives et une couverture contraceptive particulièrement étendue (plus de 95 % de femmes ayant une activité sexuelle et ne souhaitant pas avoir d’enfants déclarent utiliser un moyen de contraception), le taux d’IVG reste stable et à un niveau relativement élevé : 200 000 IVG par an, soit 14,7 IVG pour 1000 femmes en 2007 à comparer au 8/1000 des Pays-Bas (Vilain, 2009).
Les professionnels de santé doivent donc :
 éviter de suivre une « norme contraceptive » avec prescription : du préservatif, seul ou associé à la pilule, en début de vie sexuelle ; de la pilule seule pour les femmes jeunes ayant une vie sexuelle stable ; du DIU pour les femmes déjà mères et qui ne désirent plus d’enfant ;
éviter de suivre une « norme contraceptive » avec prescription : du préservatif, seul ou associé à la pilule, en début de vie sexuelle ; de la pilule seule pour les femmes jeunes ayant une vie sexuelle stable ; du DIU pour les femmes déjà mères et qui ne désirent plus d’enfant ;
 lutter contre les idées fausses comme la pilule rend stérile (34 % des jeunes de 15 à 20 ans le pensent) la pilule fait grossir (24 % des femmes le pensent) le stérilet est contre-indiqué chez les femmes sans enfants (50 % le pensent) ;
lutter contre les idées fausses comme la pilule rend stérile (34 % des jeunes de 15 à 20 ans le pensent) la pilule fait grossir (24 % des femmes le pensent) le stérilet est contre-indiqué chez les femmes sans enfants (50 % le pensent) ;
 organiser des consultations de contraception selon le mode BERCER (bienvenue–entretien–renseignements–choix–explication–retour) recommandé par l’OMS (HAS, 2004) ;
organiser des consultations de contraception selon le mode BERCER (bienvenue–entretien–renseignements–choix–explication–retour) recommandé par l’OMS (HAS, 2004) ;
 prescrire une contraception choisie par la femme ou le couple et non par le médecin ou la sage-femme en réévaluant à chaque consultation si la contraception est toujours la plus adaptée à la vie sexuelle, sentimentale, professionnelle ;
prescrire une contraception choisie par la femme ou le couple et non par le médecin ou la sage-femme en réévaluant à chaque consultation si la contraception est toujours la plus adaptée à la vie sexuelle, sentimentale, professionnelle ;
 prescrire en tenant compte des moyens financiers de la femme (les pilules remboursées ne sont pas obsolètes). Il y a des possibilités de prise en charge dans les centres de planification familiale pour les mineures mais aussi dans certaines conditions pour les majeures ;
prescrire en tenant compte des moyens financiers de la femme (les pilules remboursées ne sont pas obsolètes). Il y a des possibilités de prise en charge dans les centres de planification familiale pour les mineures mais aussi dans certaines conditions pour les majeures ;
 profiter des consultations de contraception pour :
profiter des consultations de contraception pour :
 vérifier les vaccinations (rubéole, hépatite B et bientôt le vaccin anti-HPV contre le cancer du col),
vérifier les vaccinations (rubéole, hépatite B et bientôt le vaccin anti-HPV contre le cancer du col),Contraception hormonale
Enfin, nous insisterons sur la contraception d’urgence ou « la pilule du lendemain ».
Différents types de contraceptions hormonales
Estroprogestatifs
Les estroprogestatifs associent un estrogène et un progestatif de synthèse.
Estrogène
Il s’agit le plus souvent d’un estrogène de synthèse, l’éthinylestradiol (EE), dérivé artificiel de l’estradiol, principal estrogène sécrété par l’ovaire auquel un radical éthinyl a été ajouté.
L’éthinylestradiol confère au produit un effet estrogénique puissant permettant au stéroïde d’échapper à la dégradation digestive au prix d’une surcharge hépatique, le foie scindant le radical éthinyl de l’estradiol proprement dit qui est ensuite dégradé par cet organe par hydroxylation, comme l’hormone naturelle. Le point essentiel est l’induction enzymatique importante créée par cette transformation biochimique source d’effets secondaires doses dépendants : synthèse de triglycérides, de facteurs de coagulation, d’angiotensinogène, de protéines de liaison des stéroïdes hépatiques (SHBG : sex-hormone binding globulin, TBG : thyroxine binding globulin, CBG : cortisol binding globulin). Ce dernier point permet de comprendre certaines modifications de dosages hormonaux plasmatiques de femmes sous estroprogestatifs avec augmentation des hormones totales : thyroxine, cortisol, testostérone pouvant conduire à des interprétations erronées. Les doses d’éthinylestradiol utilisées vont de 50 à 15 μg/jour avec des effets secondaires diminués mais non abolis par les doses plus faibles. De nouveaux contraceptifs utilisant des estrogènes naturels, le valérate d’estradiol (EV – Qlaira®), le 17-β-estradiol (Zoely®) ou l’estétrol (E4) sont commercialisés. Le valérate d’estradiol est une forme estérifiée de l’estradiol naturel. L’estétrol (E4) est un estrogène naturel synthétisé par le foie du fœtus pendant la grossesse. Il faut maintenant étudier les effets de ces différentes molécules sur le métabolisme mais aussi sur le risque thromboembolique.
Progestatifs de synthèse
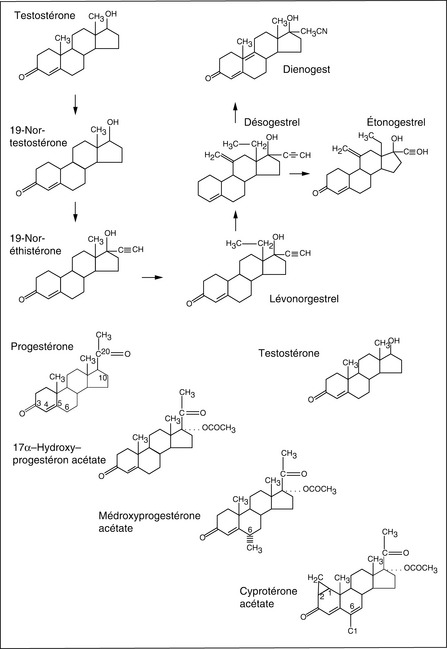
Ils appartiennent à deux grandes familles : les dérivés de la testostérone, norgonane à 19 atomes de carbone (par ex. le lévonorgestrel) et norestrane 18 atomes de carbone (par ex. la noréthistérone), ou les dérivés de la progestérone et de la 17-alpha-hydroxyprogestérone, prégnane (par ex. acétate de chlormadinone). Il s’agit plus récemment de dérivés du norgestrel : désogestrel, norgestimate ou gestodène. Ces derniers stéroïdes sont plus fortement antigonadotropes, pouvant être utilisés à doses plus faibles, ce qui contribue à la diminution de la dose totale de stéroïde et accroît la tolérance métabolique. Enfin, un nouveau progestatif, apparenté à la spironolactone (anti-aldostérone), la drospirénone, est proposé dans trois spécialités non remboursées. La drospirénone est dérivée de la 17-alpha-spironolactone. Elle garde une activité de type progestérone (anti-androgène faible) et a donc un effet anti-aldostérone avec augmentation de l’excrétion urinaire de Na+ entraînant une perte de poids significative avec la première association et un effet anti-acnéique notable (Foidart, 2000).
Il y a de nouveaux progestatifs qui n’en sont pas : la norelgestromine comprise dans le patch contraceptif est un précurseur (comme le norgestimate) du norgestrel et est donc androgénique ; l’étonorgestrel (implant ou anneau contraceptif) est un métabolite dérivé du désogestrel très peu androgénique obtenu à partir du norgestrel (qui, lui, est androgénique). Il est encore moins androgénique que le désogestrel et par là même potentiellement intéressant (Gaspard, 2004).
 les progestatifs norstéroïdes de première génération (noréthistérone), de seconde génération (lévonorgestrel), de troisième génération (norgestimate, désogestrel, gestodène) et de quatrième génération dérivés de la spironolactone, la drospirénone ;
les progestatifs norstéroïdes de première génération (noréthistérone), de seconde génération (lévonorgestrel), de troisième génération (norgestimate, désogestrel, gestodène) et de quatrième génération dérivés de la spironolactone, la drospirénone ;
 les dérivés non norstéroïdes pregnanes : acétate de chlormadinone, acétate de cyprotérone (figure 28.1).
les dérivés non norstéroïdes pregnanes : acétate de chlormadinone, acétate de cyprotérone (figure 28.1).
Estroprogestatifs par voie orale (tableau 28.1)
Les estroprogestatifs oraux comportent un estrogène et un progestatif.
Tableau 28.1 Estroprogestatifs utilisés en contraception (2011).
| Spécialité | Dénomination commune internationale Progestatifs dose mg/dose d’estrogènes μg EE | Particularités de l’association |
|---|---|---|
| Progestatifs de première génération, androgéniques | ||
| Stédiril® Triella® | Norgestrel : 0,5 mg/50 μg Noréthistérone : 0,5–0,75–1 mg/35 μg | Normodosée monophasique R Minidosée triphasique R |
| Progestatifs de deuxième génération, androgéniques | ||
| Adépal® Pacilia® Gé Minidril® Ludéal® Gé Zikiale® Gé Leeloo® Gé Lovavulo® Gé Trinordiol® Daily® Gé Amarance® Gé Evanécia® Gé | Lévonorgestrel : 0,15–0,2 mg/30/40 μg Lévonorgestrel : 0,15–0,2 mg/30/40 μg Lévonorgestrel : 0,15 mg/30 μg Lévonorgestrel : 0,15 mg/30 μg Lévonorgestrel : 0,15 mg/30 μg Lévonorgestrel : 0,100 mg/20 μg Lévonorgestrel : 0,100 mg/20 μg Lévonorgestrel : 0,05–0,075–0,125 mg/30/40/30 μg Lévonorgestrel : 0,05–0,075–0,125 mg/30/40/30 μg Lévonorgestrel : 0,05–0,075–0,125 mg/30/40/30 μg Lévonorgestrel : 0,05–0,075–0,125 mg/30/40/30 μg | Minidosée biphasique R/G Minidosée biphasique R/G Minidosée monophasique R/G Minidosée monophasique R/G Minidosée monophasique R/G Minidosée monophasique R Minidosée monophasique R Minidosée triphasique R/G Minidosée triphasique R/G Minidosée triphasique R/G Minidosée triphasique R/G |
| Progestatifs de troisième génération, parfois androgéniques | ||
| Cycléane 30® Cycléane 20® Mercilon® Désobel® Gé 20 Désobel® Gé 30 Varnoline® Varnoline continue® Harmonet® Carlin® Gé 20 Carlin® Gé 30 Méliane® Effezial® Gé 20 Effezial® Gé 30 Felixita® Gé 20 Mélodia® Minesse® Moneva® Minulet® Phaeva® Tri-Minulet® Perleane® Gé Cilest® Effiprev® Tricilest® Triafemi® Jasmine® Jaminelle® Jasminelle continu® Yaz® Belara® Qlaira® Zoely® | Désogestrel : 0,15 mg/30 μg Désogestrel : 0,15 mg/20 μg Désogestrel : 0,15 mg/30 μg Désogestrel : 0,15 mg/20 μg Désogestrel : 0,15 mg/30 μg Désogestrel : 0,15 mg/30 μg Désogestrel : 0,15 mg/30 μg Gestodène : 0,020 mg/20 μg Gestodène : 0,075 mg/20 μg Gestodène : 0,075 mg/30 μg Gestodène : 0,020–0,075 mg/20 μg Gestodène : 0,075 mg/20 μg Gestodène : 0,075 mg/30 μg Gestodène : 0,075 mg/20 μg Gestodène : 0,060 mg/15 μg Gestodène : 0,060 mg/15 μg Gestodène : 0,075 mg/30 μg Gestodène : 0,075 mg/30 μg Gestodène : 0,05–0,07–0,1 mg/30-40-30 μg Gestodène : 0,05–0,07–0,1 mg/30-40-30 μg Norgestimate : 0,250 mg/35 μg Norgestimate : 0,250 mg/35 μg Norgestimate : 0,180–0,215–0,250 mg/35 μg Norgestimate : 0,180–0,215–0,250 mg/35 μg Drospirénone* : 3 mg/30 μg Drospirénone : 3 mg/20 μg Drospirénone : 3 mg/20 μg + 7 cp placebo Drospirénone : 3 mg/20 μg + 4 cp placebo Drospirénone : 3 mg/15 μg Acétate de chlormadinone : 2 mg/30 μg Diénogest 2 à 3 mg/valérate d’estradiol 1 à 3 mg Nomégestrol 2,5 mg/17-β-estradiol 1,5 mg | Minidosée monophasique Minidosée monophasique G Minidosée monophasique G Minidosée monophasique R Minidosée monophasique R Minidosée monophasique Minidosée monophasique R Minidosée monophasique Minidosée monophasique R Minidosée monophasique R Minidosée monophasique Minidosée monophasique R Minidosée monophasique R Minidosée monophasique Microdosée monophasique Microdosée monophasique Minidosée monophasique Minidosée monophasique Minidosée triphasique Minidosée triphasique Minidosée triphasique Minidosée monophasique Minidosée monophasique Minidosée triphasique** Minidosée triphasique** Minidosée monophasique Minidosée monophasique Minidosée monophasique Minidosée monophasique Minidosée monophasique Minidosés quadriphasique Monophasique |
| Patch contraceptif | ||
| Evra® | Norelgestromine : 0,150 mg/20 μg | |
| Anneau contraceptif vaginal | ||
| NuvaRing® | Étonogestrel : 0,120 mg/15 μg | |
EE : éthinylestradiol ; R = remboursement à 65 % ; G = générique.
* Progestatif anti-androgénique et anti-aldostérone.
** Triphasique pour le progestatif seulement ; existe aussi en prise continue (7Pla) pour diminuer le risque d’oubli.
Le progestatif a varié au cours des années :
 les pilules dites de première génération comportent de la noréthistérone et de la norgestriénone. Seule Triella® (triphasique) et Miniphase® (biphasique) sont encore commercialisées ;
les pilules dites de première génération comportent de la noréthistérone et de la norgestriénone. Seule Triella® (triphasique) et Miniphase® (biphasique) sont encore commercialisées ;
 les pilules de deuxième génération contiennent du lévonorgestrel ou du D-norgestrel comme Stédiril®, Minidril® (monophasique), Adépal® (biphasique), Trinordiol® (ou Daily® Gé) triphasique ;
les pilules de deuxième génération contiennent du lévonorgestrel ou du D-norgestrel comme Stédiril®, Minidril® (monophasique), Adépal® (biphasique), Trinordiol® (ou Daily® Gé) triphasique ;
 les pilules de troisième génération contiennent le gestodène, le désogestrel, le norgestimate : Cilest®, Effiprev®, Cycléane 30®, Varnoline®, Leeloo Gé®, Minulet®, Moneva®, Phaeva®, Triminulet®. On retrouve aussi les pilules les plus faiblement dosés, Cycléane 20®, Mercilon®, Harmonet®, Méliane®, Minesse®, Mélodia® ;
les pilules de troisième génération contiennent le gestodène, le désogestrel, le norgestimate : Cilest®, Effiprev®, Cycléane 30®, Varnoline®, Leeloo Gé®, Minulet®, Moneva®, Phaeva®, Triminulet®. On retrouve aussi les pilules les plus faiblement dosés, Cycléane 20®, Mercilon®, Harmonet®, Méliane®, Minesse®, Mélodia® ;
 les pilules de quatrième génération contiennent la drospirénone, dérivée de la spironolactone (Jasmine®, Jasminelle® et Yaz®).
les pilules de quatrième génération contiennent la drospirénone, dérivée de la spironolactone (Jasmine®, Jasminelle® et Yaz®).
Par ailleurs, deux associations estroprogestatives contenant des dérivés prégnanes existent en France : éthinylestradiol–acétate de chlormadinone (Belara®) et éthinylestradiol–acétate de cyprotérone (Diane 35® et ses nombreux génériques). Cette dernière ne dispose pas de l’autorisation de mise sur le marché en AMM pour la contraception.
Le taux d’estrogènes est variable :
 les estroprogestatifs classiques à 50 μg associent l’éthinyl estradiol à un progestatif qui diffère selon les produits. Il s’agit toujours d’un progestatif norgonane dérivé de la testostérone. Ce progestatif est à dose identique dans tous les comprimés (pilule dite monophasique). Elles sont actuellement peu utilisées ;
les estroprogestatifs classiques à 50 μg associent l’éthinyl estradiol à un progestatif qui diffère selon les produits. Il s’agit toujours d’un progestatif norgonane dérivé de la testostérone. Ce progestatif est à dose identique dans tous les comprimés (pilule dite monophasique). Elles sont actuellement peu utilisées ;
 les pilules estroprogestatives combinées minidosées. Elles comportent de 15 à 35 μg d’éthinylestradiol :
les pilules estroprogestatives combinées minidosées. Elles comportent de 15 à 35 μg d’éthinylestradiol :
 elles sont monophasiques lorsque l’éthinylestradiol et le progestatif sont à un taux constant dans chaque comprimé,
elles sont monophasiques lorsque l’éthinylestradiol et le progestatif sont à un taux constant dans chaque comprimé, elles sont biphasiques lorsque l’éthinylestradiol et les progestatifs varient une fois dans le cycle,
elles sont biphasiques lorsque l’éthinylestradiol et les progestatifs varient une fois dans le cycle, elles sont triphasiques lorsqu’il y a variation du progestatif et/ou de l’estrogène et du progestatif trois (deux) fois dans le cycle. En fait, il n’est pas apparu de différences tangibles entre les pilules mono-, bi- ou triphasiques (Van Vliet, 2005),
elles sont triphasiques lorsqu’il y a variation du progestatif et/ou de l’estrogène et du progestatif trois (deux) fois dans le cycle. En fait, il n’est pas apparu de différences tangibles entre les pilules mono-, bi- ou triphasiques (Van Vliet, 2005),L’association d’éthinylestradiol et d’acétate de cyprotérone (Diane 35®, Evépar®, Holgyème®, Minerva®) doit être mise à part car ce produit contient un anti-androgène puissant : l’acétate de cyprotérone qui peut être utilisé comme anti-acnéique. Cependant cette spécialité (pourtant utilisée depuis très longtemps) n’a pas l’AMM pour la contraception. L’HAS recommande d’utiliser pour la contraception et le traitement des acnés légères et modérées l’association norgestimate–éthinylestradiol 35 μg : Tricilest® et Triafemi® qui ont l’AMM pour les deux indications (tableau 28.2). Toutefois, la revue Prescrire (2005) pense que ces deux produits n’apportent pas de progrès démontrés.
Tableau 28.2 Traitement de l’acné/association estro-anti-androgénique.
| Spécialité | Dénomination commune internationale Progestatifs dose mg/dose d’estrogènes μg | Type |
|---|---|---|
| Diane 35® Evépar®, Holgyème® Lumalia®, Minerva® | Acétate de cyprotérone : 2 mg/35 μg EE | Minidosée monophasique Pas d’AMM contraception |
| Tricilest® Triafemi® | Norgestimate : 0,180–0,215–0,250 mg/35 μg EE Norgestimate : 0,180–0,215–0,250 mg/35 μg EE | Minidosée triphasique AMM acné + contraception |
En 2011, a été introduite une pilule comportant 1,5 mg de 17-β-estradiol et 2,5 mg de nomégestrol (Zoely®) ou estradiol valérate 1 à 3 mg et diénogest 2 à 3 mg (Qlaira®). L’idée est d’apporter une contraception avec un estrogène naturel à la place de l’éthinylestradiol.
Estroprogestatifs par voie percutanée
Il s’agit d’un patch (Evra®) qui délivre 20 μg/jour d’éthinylestradiol (600 μg/dispositif) et 0,150 mg de norelgestromine (6 mg/dispositif). Le patch est collé sur l’avant-bras, l’abdomen, la fesse. Il est mis le premier jour des règles ou le jour du saignement après un arrêt de pilule, ou le jour de retrait de l’implant. Il peut aussi être mis au 20e jour après une fausse couche ou une IVG, et 28 jours après un accouchement si la femme n’allaite pas. Il est changé toutes les semaines et après trois patchs consécutifs la patiente a 1 semaine sans traitement, période pendant laquelle elle a une hémorragie de privation. Elle remet un patch de la boîte suivante 7 jours après le retrait de celui de la boîte précédente. L’absorption du produit se fait par voie percutanée évitant le premier passage hépatique mais les indications, contre-indications, effets secondaires sont les mêmes que pour la voie orale. C’est l’observance qui serait meilleure évitant la prise quotidienne et les problèmes de prise défectueuse en raison de vomissements ou de diarrhées (Burkman, 2004). Si l’efficacité contraceptive est bonne, la femme reste tributaire du taux de décollement du patch (2 % environ), ce qui risque d’être cause d’échec si elle ne s’en aperçoit pas. Si la femme s’en rend compte, elle peut le recoller si le décollement date de moins de 24 heures, sinon il faut en mettre un autre et utiliser des préservatifs pendant 8 jours. L’indice de Pearl est de 0,6 à 1 dans les études. L’efficacité serait moindre si la femme pèse plus de 90 kg (Prescrire, 2004). Le prix est d’environ 15 €/mois, non remboursé. Les patchs usagés doivent être remis dans leur boîte et rapportés au pharmacien pour une élimination correcte de ce déchet. Ils ne doivent pas être jetés à la poubelle.
Estroprogestatifs par voie vaginale
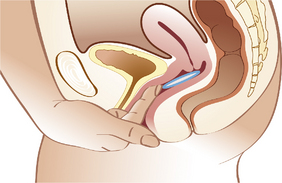
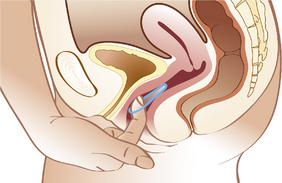
NuvaRing® est un anneau souple de diamètre extérieur de 54 mm, dont la section mesure 4 mm qui comprend un copolymère avec en inclusion les stéroïdes (2,7 mg d’éthinylestradiol et 11,7 mg d’étonogestrel) qui vont pouvoir diffuser passivement de façon continue (figures 28.2 à 28.4). Il délivre 30 μg d’éthinylestradiol/jour et 0,120 mg d’étonogestrel, progestatif très peu androgénique. La voie vaginale permet aussi d’éviter le premier passage hépatique de la voie orale, mais les indications, contre-indications, effets secondaires sont les mêmes que pour la voie orale (Johansson, 2004 ; Magnusdottir, 2004 ; Rad, 2006). Il y a en plus des troubles gynécologiques : vaginites, leucorrhées, gêne locale chez environ 20 % des femmes (Prescrire, 2005). L’anneau est placé entre J1 et J5 même si les règles ne sont pas finies ou à l’arrêt d’une contraception orale ou lors du retrait de l’implant. Il peut aussi être mis en place juste après une fausse couche, une IVG ou 4 semaines après un accouchement. Il sera laissé en place pendant 3 semaines. Un autre anneau sera placé après 1 semaine sans traitement, période pendant laquelle surviendra une hémorragie de privation. On peut proposer pour faciliter l’observance de mettre l’anneau le 1er jour du mois et le retirer le 24e jour en remettant celui de la boîte suivante le premier du mois suivant. Il faudra alors conseiller une deuxième contraception par préservatif le premier mois puisque le premier jour du mois du calendrier n’est pas forcément celui du cycle. En cas d’expulsion accidentelle, on peut le rincer à l’eau tiède et le remettre en place s’il a été hors du vagin moins de 3 heures. Passé ce délai, il vaut mieux en mettre un neuf et utiliser les préservatifs les huit premiers jours. Les anneaux usagés sont remis dans leur boîte d’origine et rapportés au pharmacien pour élimination des déchets. Il ne faut pas les jeter dans les toilettes. L’indice de Pearl est de 0,6 à 1,7 (Novak, 2003 ; Oddsson, 2005). Le prix est d’environ 15 €/mois, non remboursé.
Progestatifs purs
Microprogestatifs
Les microprogestatifs (minipills des Anglo-Saxons) ne comportent que des progestatifs donnés à faible dose et en continu tout au long du cycle (prise quotidienne ininterrompue même pendant les règles à heure fixe). Le retard de prise ne doit pas être supérieur à 3 heures.
Le lévonorgestrel (Microval®) et le noréthistérone (Milligynon®) ont une faible action antigonadotrope et n’agissent que sur la glaire et l’endomètre (ces deux spécialités sont remboursées et peu onéreuses).
Désogestrel
Le désogestrel (Cérazette®), plaquette de 28 comprimés dosés à 0,075 mg, a une action antigonadotrope et bloque l’ovulation dans plus de 90 % des cycles, ce qui augmente son efficacité. On observe parfois un moins bon contrôle du cycle avec possibilité d’une aménorrhée ou spotting, il faudra en informer les patientes. Contrairement au lévonorgestrel, le décalage de prise maximum toléré est de 12 heures comme pour les contraceptions estroprogestatives. L’indice de Pearl est de 0,5; le prix est de 10 à 15 €/mois, non remboursé (tableau 28.3).
Tableau 28.3 Contraceptifs microprogestatifs.
| Spécialité | Dénomination commune internationale | Type |
|---|---|---|
| Microval® Milligynon® Cérazette® | Lévonorgestrel : 0,03 mg Acétate de noréthistérone : 0,6 mg Désogestrel : 0,75 mg | Microdosé en continue orale R Microdosé en continue orale R Microdosé en continue orale |
| Dépo-Provéra® | Médroxyprogestérone acétate : 150 mg | Suspension injectable IM |
| Nexplanon® | Étonorgestrel : 68 mg | Implant R |
R = remboursement à 65 %.
Implant progestatif à l’étonogestrel (Nexplanon®)
Le Nexplanon® (figure 28.5) est autorisé en France. Il s’agit d’un bâtonnet radio-opaque de 40 mm de long et 2 mm de diamètre qui contient 68 mg d’étonogestrel, métabolite du désogestrel donc peu androgénique. Il remplace depuis 2011 l’Implanon® auquel on a ajouté un fil de barium – ce qui le rend radio-repérable – facilitant ainsi sa localisation en cas de retrait difficile. Introduit sous la peau du bras non dominant après une anesthésie locale, il inhibe l’ovulation et modifie la glaire cervicale pendant 3 ans. Cependant son l’efficacité contraceptive peut être diminuée dans la troisième année pour les femmes présentant un surpoids (IMC > 25). Il devra donc chez ces femmes être remplacé plus tôt, au bout de 30 mois. Il doit être posé entre le 1er et le 5e jour du cycle, le lendemain de la dernière prise d’un estroprogestatif, immédiatement après une IVG ou 4 semaines après un accouchement ou un avortement tardif. L’étonogestrel passe en dose très faible dans le lait maternel. La pose de cet implant pendant l’allaitement ne se justifie que si une autre contraception est impossible. Le retour de l’ovulation après ablation est de 3 semaines. L’indice de Pearl est de 0,1. Il est remboursé à 65 % et son prix est de 106,76 €.
Progestatifs macrodosés
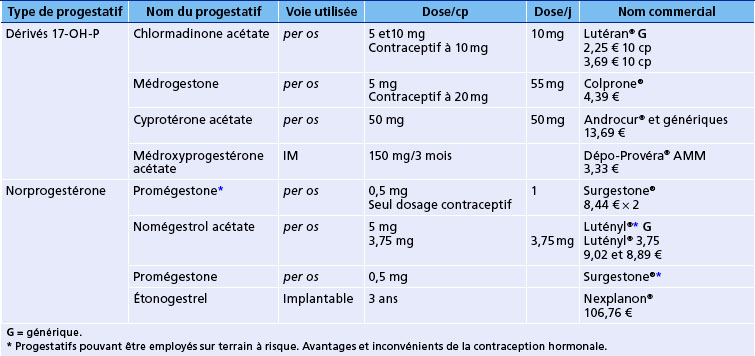
Les progestatifs macrodosés ne sont pas à proprement parler des contraceptifs. Les dérivés 19-nor-prégnane (structure de base de la progestérone), l’acétate de chlormadinone (Lutéran®), la promégestone (Surgestone®), le nomégestrol (Lutényl®) sont dépourvus d’effets virilisants. La prise de deux comprimés d’acétate de chlormadinone 5 mg ou de 1 comprimé de nomégestrol 5 mg ou de 0,500 mg de promégestone du 6e au 25e jour du cycle permet une sécurité contraceptive équivalente aux estroprogestatifs. Ils sont utiles en cas de contre-indications aux œstrogènes de synthèse pris per os (Madelemat, 2008).
Un progestatif retard injecté trimestriellement en intramusculaire à la dose de 150 mg de médroxyprogestérone acétate (Dépo-Provéra®) ou toutes les 8 semaines à la dose de 200 mg (Noristérat®) permet une contraception efficace au prix de troubles du cycle (aménorrhée, spotting) et de (possible) prise de poids.
Cette méthode est utilisée largement dans les pays en voie de développement, car il demande moins de participation. Une association avec un œstrogène (valérianate d’œstradiol commercialisé sous le nom de Mesigyna® ou Norgynon® de Schering) ou avec du cypionate d’estradiol (Lulelle® de Pharmacia-Upjohn) a une demande d’AMM européenne en cours.
Pilule d’urgence (tableau 28.4)
Il s’agit d’un comprimé de lévonorgestrel 1,5 mg (soit l’équivalent de 50 comprimés de Microval®) à prendre en une seule prise dans les 72 heures qui suit le rapport non protégé (commercialisé sous le nom de Norlevo®) Il ne s’agit pas d’une contraception régulière mais d’une contraception d’urgence (cf. p. 434). L’efficacité est maintenue avec une prise dans les 3 à 5 jours suivant le rapport mais avec une baisse d’efficacité au fil des heures. Remboursé à 65 % sur prescription médicale, il est à disposition dans les infirmeries des collèges et des lycées et en pharmacie sans ordonnance et gratuitement pour les mineures. L’efficacité est excellente et il n’existe pas de contre-indications.
Tableau 28.4 Contraception orale d’urgence.
| Spécialité | Dénomination commune internationale | Type |
|---|---|---|
| Norlevo® Ellaone® | Lévonorgestrel : 1,5 mg Ulipristal : 30 mg | Progestatif seul R SPRM : agoniste-antagoniste du récepteur de la progestérone (sur prescription) R |
R = remboursement à 65 %.
Mode d’action des estroprogestatifs
Estroprogestatifs combinés
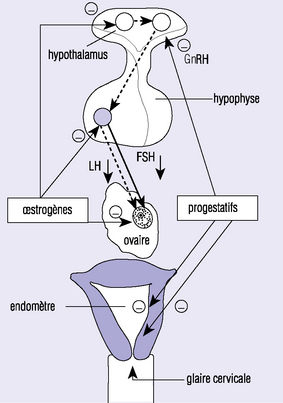
Les estroprogestatifs, qu’ils soient pris par voie orale, percutanée ou vaginale, agissent à trois niveaux (figure 28.6) :
 sur l’axe hypothalamo-hypophysaire en bloquant la libération des gonadotrophines hypophysaires. Ils suppriment le pic de LH d’où l’absence d’ovulation. C’est le rôle essentiel du progestatif et on admet que 50 μg d’EE bloque également le pic ovulatoire de LH. En dessous, c’est le rôle de l’association (et principalement du progestatif) qui assure l’efficacité ;
sur l’axe hypothalamo-hypophysaire en bloquant la libération des gonadotrophines hypophysaires. Ils suppriment le pic de LH d’où l’absence d’ovulation. C’est le rôle essentiel du progestatif et on admet que 50 μg d’EE bloque également le pic ovulatoire de LH. En dessous, c’est le rôle de l’association (et principalement du progestatif) qui assure l’efficacité ;
 action locale : les estrogènes associés aux progestatifs entraînent une atrophie de l’endomètre, le rendant impropre à la nidation et modifient la glaire cervicale qui devient épaisse empêchant l’ascension des spermatozoïdes.
action locale : les estrogènes associés aux progestatifs entraînent une atrophie de l’endomètre, le rendant impropre à la nidation et modifient la glaire cervicale qui devient épaisse empêchant l’ascension des spermatozoïdes.
L’efficacité des pilules classiques à 50 μg est excellente (indice de Pearl* = 0,15 à 0,45 % année/femmes) mais expose aux effets secondaires des fortes doses d’estrogènes de synthèse.
Progestatifs seuls (tableau 28.5)
En traitement continu (micropilule), ils ont surtout une action sur la glaire cervicale qui est épaisse et constitue un obstacle à l’ascension des spermatozoïdes. Le col est fermé, l’endomètre atrophique. Ils ne bloquent pas l’ovulation et ils laissent persister une sécrétion estrogénique endogène (hyperestrogénie relative) responsable de mastopathie. En fait, avec le lévonorgestrel (Microval®) ou la noréthistérone (Milligynon®), 28 % seulement des femmes ont une ovulation. Le désogestrel (Cérazette®) a une action antigonadotrope plus puissante qui bloque l’ovulation dans plus de 98 % des cycles augmentant l’efficacité : indice de Pearl à 0,52. Il peut aussi y avoir un décalage de la prise jusqu’à 12 h, ce qui rend l’observance moins contraignante, contrairement aux microprogestatifs (3 h).
Avantages des estroprogestatifs
Ils sont souvent passés sous silence pourtant ils sont réels. Il s’agit de :
 la correction des anomalies menstruelles (dysménorrhée) ;
la correction des anomalies menstruelles (dysménorrhée) ;
 la diminution de l’incidence des ménorragies et des infections utéro-annexielles (2 fois moins) ;
la diminution de l’incidence des ménorragies et des infections utéro-annexielles (2 fois moins) ;
 la diminution des interventions pour kyste de l’ovaire, bien que des kystes fonctionnels puissent se voir sous estroprogestatifs faiblement dosés en estrogènes ;
la diminution des interventions pour kyste de l’ovaire, bien que des kystes fonctionnels puissent se voir sous estroprogestatifs faiblement dosés en estrogènes ;
 la baisse des interventions pour pathologie bénigne du sein (4 fois moins) ;
la baisse des interventions pour pathologie bénigne du sein (4 fois moins) ;
 la protection contre le risque des cancers de l’ovaire, de l’endomètre, colorectal (2 fois moins ; Np2) ; mais par contre au prix d’une majoration du risque de cancer du col de l’utérus ;
la protection contre le risque des cancers de l’ovaire, de l’endomètre, colorectal (2 fois moins ; Np2) ; mais par contre au prix d’une majoration du risque de cancer du col de l’utérus ;
Il y a peut-être une diminution du risque de fibrome et d’ostéoporose. Il n’y a pas de risque d’augmentation du cancer du foie, ni des maladies cardiovasculaires à condition de ne pas fumer, sans compter l’avantage incontestable d’une médecine préventive liée aux examens gynécologiques fréquents auxquels se soumettent les femmes sous contraceptifs. Au total, les femmes qui utilisent les estroprogestatifs auraient même sur le long terme une baisse de la mortalité par rapport aux non-utilisatrices (Vessey, 2010 ; Hannaford, 2010).
Inconvénients des estroprogestatifs
Les effets secondaires sont fonction du type d’estroprogestatifs et de leur composition.
Troubles métaboliques
Les troubles métaboliques comportent :
 les troubles de la glucorégulation avec hyperinsulinisme et mauvaise tolérance aux hydrates de carbone responsables d’une tendance à l’hyperglycémie : les estrogènes mais aussi les progestatifs peuvent être en cause ;
les troubles de la glucorégulation avec hyperinsulinisme et mauvaise tolérance aux hydrates de carbone responsables d’une tendance à l’hyperglycémie : les estrogènes mais aussi les progestatifs peuvent être en cause ;
 l’augmentation des triglycérides et du cholestérol est liée à l’effet hépatique de l’éthinylestradiol. Il est dose-dépendant et patiente-dépendant. Il entraîne une augmentation modérée du cholestérol et de ses sous-fractions HDL (le « bon » cholestérol) et une baisse discrète du LDL cholestérol athérogène. En l’absence de tabagisme, le rôle athérogène des estroprogestatifs avec les dosages actuels semble minime s’il existe et semble être l’exclusivité de sujets génétiquement à risque (familles d’hypercholestérolémiques ou d’hyperlipidémies mixtes, diabétiques) (Basdevant, 1989) ;
l’augmentation des triglycérides et du cholestérol est liée à l’effet hépatique de l’éthinylestradiol. Il est dose-dépendant et patiente-dépendant. Il entraîne une augmentation modérée du cholestérol et de ses sous-fractions HDL (le « bon » cholestérol) et une baisse discrète du LDL cholestérol athérogène. En l’absence de tabagisme, le rôle athérogène des estroprogestatifs avec les dosages actuels semble minime s’il existe et semble être l’exclusivité de sujets génétiquement à risque (familles d’hypercholestérolémiques ou d’hyperlipidémies mixtes, diabétiques) (Basdevant, 1989) ;
 une hypercoagulabilité : augmentation de l’adhésivité et de l’agrégabilité des plaquettes, augmentation de la synthèse hépatique de certains facteurs de la coagulation (facteurs II, VII, IX, X) et diminution de l’antithrombine III, entraînant un risque accru (RR × 3) d’accidents thromboemboliques. Le risque absolu de maladie thromboembolique veineuse est cependant faible et estimé à 15/100 000 avec les progestatifs de 2e génération et 30 avec les progestatifs de 3e génération, alors qu’il est de 5 à 11/100 000 sans contraception orale. Cette notion est toutefois remise en cause (Heinemann, 2010).
une hypercoagulabilité : augmentation de l’adhésivité et de l’agrégabilité des plaquettes, augmentation de la synthèse hépatique de certains facteurs de la coagulation (facteurs II, VII, IX, X) et diminution de l’antithrombine III, entraînant un risque accru (RR × 3) d’accidents thromboemboliques. Le risque absolu de maladie thromboembolique veineuse est cependant faible et estimé à 15/100 000 avec les progestatifs de 2e génération et 30 avec les progestatifs de 3e génération, alors qu’il est de 5 à 11/100 000 sans contraception orale. Cette notion est toutefois remise en cause (Heinemann, 2010).
 le plan métabolique : diminution du HDL cholestérol pour les norgonanes, peu ou pas de modifications pour les dérivés de la 17-alpha-hydroxyprogestérone ou les nor-prégnanes, intolérance au glucose accrue par les dérivés norgonanes et à un moindre degré les dérivés de la 17-alpha-hydroxyprogestérone, rappelant la moindre tolérance au glucose en deuxième partie de cycle ;
le plan métabolique : diminution du HDL cholestérol pour les norgonanes, peu ou pas de modifications pour les dérivés de la 17-alpha-hydroxyprogestérone ou les nor-prégnanes, intolérance au glucose accrue par les dérivés norgonanes et à un moindre degré les dérivés de la 17-alpha-hydroxyprogestérone, rappelant la moindre tolérance au glucose en deuxième partie de cycle ;
 les effets sur la coagulation (diminution de la fibrinolyse avec les composés norgonanes) ; baisse de la SHBG avec les composés norgonanes.
les effets sur la coagulation (diminution de la fibrinolyse avec les composés norgonanes) ; baisse de la SHBG avec les composés norgonanes.
Le risque absolu de maladie thromboembolique veineuse est faible chez les femmes à l’âge de la reproduction et est estimé entre 5 et 10 pour 100 000 années-femmes (AF). Aucune étude ne démontre une baisse du risque thromboembolique veineux par l’utilisation des pilules estroprogestatives minidosées les plus récentes. Les progestatifs de troisième génération doublent le risque de thrombose veineuse profonde (Lidegaard, 2011) et ceux de quatrième génération (drospirénone) le multiplient par 1,5 à 2 (Prescrire, 2010). Il faut donc en première prescription proposer les estroprogestatifs minidosés comportant un progestatif de deuxième génération : éthinylestradiol 30 ou 40 mcg + lévonorgestrel ou norethistérone (Hannaford, 2011 ; Prescrire, 2011).
La rétention hydrosodée avec augmentation de l’angiotensinogène (impact hépatique) et de la rénine (d’où l’hyperaldostéronisme) induit un risque d’hypertension artérielle chez des sujets prédisposés et contribue à la prise de poids. C’est l’intérêt du nouveau progestatif, la drospirénone apparentée à un anti-aldostérone, de limiter ces deux effets et de diminuer la prise de poids mais aussi le développement intempestif mais rare de la pilosité. Cependant la drospirénone apparentée à un diurétique expose à un risque d’hyperkaliémie et des interactions médicamenteuses supplémentaires (Prescrire, 2009).
L’augmentation des acides biliaires multiplie le risque de lithiase par deux. La prudence s’impose donc chez les femmes qui ont une lithiase biliaire ou ont eu une cholestase ou un prurit pendant la grossesse.
Incidents mineurs
Les incidents mineurs sont possibles en cas de :
 surcharge en estrogènes : nausées, vomissements, instabilité, énervement, céphalées, tension mammaire, sécrétion cervicale abondante, candidose ;
surcharge en estrogènes : nausées, vomissements, instabilité, énervement, céphalées, tension mammaire, sécrétion cervicale abondante, candidose ;
 surcharge en progestatifs : état dépressif, céphalées à l’arrêt du traitement, chloasma, sécheresse vaginale, lourdeur des jambes, métrorragies par atrophie de l’endomètre.
surcharge en progestatifs : état dépressif, céphalées à l’arrêt du traitement, chloasma, sécheresse vaginale, lourdeur des jambes, métrorragies par atrophie de l’endomètre.
Accidents graves mais rares
Les accidents graves mais rares doivent être connus :
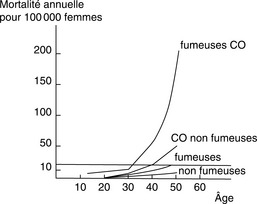
 les accidents vasculaires cérébraux. RR = 2,75 soit un accident vasculaire cérébral pour 24 000 utilisatrices pendant un an. Ce risque est diminué par l’utilisation des pilules à faible taux d’œstrogènes et augmenté par l’existence d’une HTA. Il est inférieur à celui qu’entraînent les grossesses en l’absence de contraception (Gillum, 2000). Le tabagisme et l’âge se potentialisent pour faire augmenter les accidents vasculaires tout à fait exceptionnels avant 35 ou 40 ans (figure 28.7). La prise de pilule associée à une consommation de 15 cigarettes/jour multiplie le risque par 21. La consommation de tabac sera évaluée avant de prescrire un estroprogestatif. La patiente sera ensuite orientée vers une consultation anti-tabac ;
les accidents vasculaires cérébraux. RR = 2,75 soit un accident vasculaire cérébral pour 24 000 utilisatrices pendant un an. Ce risque est diminué par l’utilisation des pilules à faible taux d’œstrogènes et augmenté par l’existence d’une HTA. Il est inférieur à celui qu’entraînent les grossesses en l’absence de contraception (Gillum, 2000). Le tabagisme et l’âge se potentialisent pour faire augmenter les accidents vasculaires tout à fait exceptionnels avant 35 ou 40 ans (figure 28.7). La prise de pilule associée à une consommation de 15 cigarettes/jour multiplie le risque par 21. La consommation de tabac sera évaluée avant de prescrire un estroprogestatif. La patiente sera ensuite orientée vers une consultation anti-tabac ;
 le risque d’infarctus du myocarde n’est également augmenté que chez les fumeuses (> 15 cigarettes/jour). Le risque relatif est alors de 4,2 soit un cas sur mille fumeuses (Mant, 1998). C’est ce risque cardiaque et vasculaire qui fait contre-indiquer la prescription ou la poursuite des estroprogestatifs au-delà de 35 ans chez la patiente fumeuse ;
le risque d’infarctus du myocarde n’est également augmenté que chez les fumeuses (> 15 cigarettes/jour). Le risque relatif est alors de 4,2 soit un cas sur mille fumeuses (Mant, 1998). C’est ce risque cardiaque et vasculaire qui fait contre-indiquer la prescription ou la poursuite des estroprogestatifs au-delà de 35 ans chez la patiente fumeuse ;
 l’apparition de tumeurs hépatiques (hépatomes, hamartomes, hémangiomes) a été décrite pour les femmes prenant un estroprogestatif notamment séquentiel (retiré du marché). Il ne faut donc pas négliger une douleur hépatique chez une femme sous estroprogestatifs. Il faut rappeler la grande fréquence des hémangiomes rendant l’imputabilité difficile (Hannaford, 2010).
l’apparition de tumeurs hépatiques (hépatomes, hamartomes, hémangiomes) a été décrite pour les femmes prenant un estroprogestatif notamment séquentiel (retiré du marché). Il ne faut donc pas négliger une douleur hépatique chez une femme sous estroprogestatifs. Il faut rappeler la grande fréquence des hémangiomes rendant l’imputabilité difficile (Hannaford, 2010).
Problèmes carcinologiques
Le cancer du col n’est pas hormono-dépendant et le renouvellement de la contraception a fait progresser son dépistage et baisser sa fréquence. Cependant des études récentes (Moreno, 2002) font état d’une augmentation du risque (RR = 1,5) pour des femmes qui ont bénéficié d’une utilisation prolongée de la contraception orale et porteuse d’un HPV oncogène. Dans l’étude prospective anglaise de 17 000 femmes suivies de 1968 à 2004, il existe un risque relatif à 4 mais lié aux rapports sexuels plus fréquents et au rôle de l’HPV (Vessey, 2006).
Pour le cancer du sein, il y a controverse. L’analyse des données de la méta-analyse d’Oxford montre une légère augmentation du risque (RR = 1,24) d’autant plus que la pilule a été débutée avant 20 ans (RR = 1,59). Ce risque augmente en fonction de la durée d’utilisation. Aucune modification du risque n’a été observée en fonction du type de pilules ni en fonction de la parité ou des antécédents familiaux. Une autre méta-analyse a trouvé un RR de 1,52 en cas d’utilisation de la pilule au moins 4 ans avant la première grossesse (Kahlenborn, 2008). Ce résultat n’a pas été confirmé par l’étude prospective anglaise déjà citée (Vessey, 2010). Aucune élévation de la mortalité par cancer du sein n’a été mise en évidence pour de longues durées d’utilisation (Colditz, 1994). Cependant, il faut rester prudent car les résultats concernant les pilules les plus récentes ne sont pas connus, faute de recul (Clemons, 2001).
Globalement, l’utilisation de la contraception orale diminue légèrement la mortalités toutes causes confendues (Vessey, 2010).
Effets secondaires des minipilules
Les effets secondaires des minipilules moins dosées en estrogènes sont identiques.
Effets secondaires des estroprogestatifs percutanés
Le dispositif transdermique Evra® contient de la norelgestromine et de l’éthinylestradiol : sa composition suffit à comprendre que les atouts de la voie cutanée avec perte de l’effet de premier passage hépatique sont annihilés par l’emploi de l’EE qui augmente les facteurs de coagulation et les protéines vectrices SHBG, TBG. Le progestatif de troisième génération norelgestromine est androgénique avec prise de poids, acné, troubles du cycle et augmentation de volume des seins et au plan biologique, baisse du HDL et élévation du cholestérol et du LDL cholestérol. Il est donc logique de voir s’installer une controverse entre les tenants de ce nouveau mode contraceptif qui écrivent que la compliance est meilleure avec le patch comparé à une pilule triphasique, et les opposants qui indiquent qu’il n’y a là aucun progrès avec un moyen moins pratique et moins sûr.
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree