Chapitre 19 Cancer du sein
• Expliquer les modalités du dépistage du cancer du sein, les avantages et inconvénients. (B)
• Diagnostiquer un cancer in situ du sein et mettre en route les thérapeutiques les plus appropriées. (A)
• Diagnostiquer un cancer invasif du sein et mettre en route les thérapeutiques les plus appropriées. (A)
• Expliquer à la patiente les modalités de traitement d’un cancer in situ du sein et donner le pronostic à 5 ans. (B)
• Expliquer à la patiente les modalités de traitement d’un cancer invasif du sein aux stades I et II et donner le pronostic à 5 ans. (B)
Épidémiologie
L’incidence est en France de 101/100 000 soit plus de 53 000 nouveaux cas par an. Cette incidence augmente de 2 % par an environ dans tous les pays occidentaux (Guizard, 2008). Elle augmente aussi avec l’âge passant de 30/100 000 avant 35 ans à 400/100 000 après 65 ans (figure 19.1).
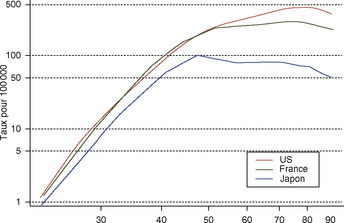
Figure 19.1 Taux d’incidence du cancer du sein en fonction de l’âge aux États-Unis, en France et au Japon (OMS).
Mortalité
En France, la mortalité par cancer du sein est en légère décroissance depuis 2000 (– 1,3 % de 2000 à 2005). Elle est de 35 pour 100 000 femmes, soit environ 12 000 décès par an (Guizard, 2008) (figure 19.2).
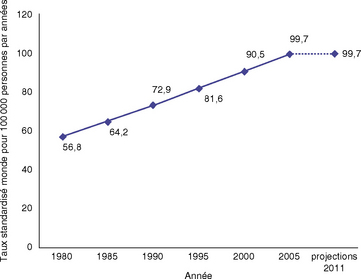
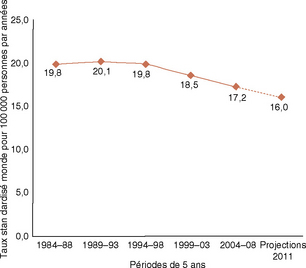
Figure 19.2 Incidence estimée et mortalité pour le cancer du sein chez la femme dans le monde.
Sources : période 1980 à 1985 Belot A, 2008; période1990 à 2011 HCL/InVS/INCa/Francim/Inserm, 2011, Traitement : INCa 2011, Sources : InVS/Inserm 20111, HCL/InVS/INCa/Francim/Inserm 20112, Traitement : INCa 2011
Facteurs de risque
Ils sont souvent à tort considérés comme des facteurs devant jouer un rôle dans le processus carcinogénétique. En réalité, leur seule caractéristique est de présenter une liaison statistique significative avec la maladie. Leur identification a un double intérêt : servir de base à l’élaboration d’hypothèses explicatives à vérifier par des études expérimentales, repérer un sujet qui peut faire l’objet d’une surveillance accrue. Certains ne sont pas modifiables : l’âge, les antécédents familiaux, d’autres le sont : l’obésité, les traitements hormonaux, l’alcool. Ces principaux facteurs sont rapportés dans le tableau 19.1.
Tableau 19.1 Détermination des facteurs de risque du cancer du sein par rapport à une population témoin.
| Facteur de risque | Risque multiplié par |
|---|---|
| Premier cancer du sein et deuxième sein | 5 à 6 |
| Prédisposition familiale | 3 |
| Mère ou sœur avec cancer du sein | 5 |
| Parité : | 3 |
| Absence d’allaitement | 2 |
| Mastopathie avec hyperplasie atypique | 3 à 5 |
| Haut niveau socio-économique : | 2 |
| Premières règles précoces Ménopause tardive Traitements hormonaux de la ménopause | 1,5 ? |
| Ethnie blanche | ? |
| Autres cancers : endomètre, côlon | 3 |
Facteurs liés à la reproduction
Ils sont les plus anciennement connus.
Les femmes stériles par anovulation ont un taux de cancer du sein 5 fois plus élevé que les femmes ayant une stérilité tubaire, par contre les femmes castrées ont un taux plus faible. Les traitements inducteurs de l’ovulation (inductions simples ou FIV) n’augmentent pas le risque (Modan, 1998).
Les nullipares et les femmes, qui ont eu leur premier enfant après 35 ans, ont un risque de cancer du sein 4 fois supérieur aux multipares. Le célibat et l’absence d’allaitement sont des facteurs de risque de cancer du sein mais ils sont liés en fait à la nulliparité ou à la grossesse tardive. Les fausses couches spontanées ou les IVG ne sont pas des facteurs de risque (Palmer, 1997).
Les effets de la contraception estroprogestative sont débattus
Près de 20 enquêtes ont été conduites dans le monde. La grande majorité d’entre elles ne met pas en évidence une liaison significative entre la prise d’estroprogestatifs, sa durée et l’apparition d’un cancer du sein (Clavel, 1991). Une étude américaine (Colditz, 1994) sur les infirmières suivies 12 ans a montré que les causes de décès n’étaient pas différentes chez les femmes utilisant les OP.
Plusieurs études sont inquiétantes dont celles de Pike et de MacPherson. Une étude hollandaise (Rookus, 1994) montre l’existence d’un risque plus élevé chez les femmes âgées de plus de 45 ans, qui ont pris la pilule avant 20 ans (RR = 40) et ceci d’autant plus que la durée de la prise est longue et que la pilule est plus faiblement dosée en estrogènes (RR = 1 pour les OP à 50 μg contre 1,6 pour celles à moins de 50 μg). Une méta-analyse parue en 1996 portant sur 50 études montre que si ce risque existe, il est très faible (RR = 1,07) et disparaît 10 ans après la fin de la prise (Collaborative Group on hormonal factors in breast cancer, 1996) et qu’il ne faut pas non plus exclure de la contraception les femmes à risques familiaux (Grabrick, 2000 ; Burke, 2000).
Traitements substitutifs de la ménopause
Dès 1992, une méta-analyse indiquait que le risque relatif était de 1,63 chez les femmes prenant un traitement substitutif après une ménopause naturelle contre 1,13 en l’absence de traitement (Sillero-Arenas, 1992). Ce risque augmentait avec la durée du traitement et a été confirmé par la méta-analyse du Collaborative Group of hormonal factors in breast cancer (Lancet, 1996). D’autres études ont été publiées (Colditz, 1994 ; Gapstur, 1999 ; Schairer, 2000) qui concluent aussi à une augmentation faible du risque sans que l’on sache les conséquences en termes de mortalité ou de pronostic. L’étude randomiséeWHI (2002) et l’étude anglaise Million Women Study (Beral, 2002) ont bien confirmé cette augmentation du risque qui passe de 1 à 1,2 au-delà de 5 ans de prise. Ces études rapportent aussi le fait que la progestérone ou la tibolone (Livial®) ne protègent pas contre le risque de cancer du sein mais l’augmente. L’étude française E3N montre que la prise d’œstrogènes par voie percutanée, avec ou sans progestérone naturelle, n’augmente pas ce risque (Fournier, 2005).
Ces informations doivent être données à la patiente qui doit prendre part à la décision de prendre ou non un THS. Elles ne remettent pas en cause la légitimité des traitements substitutifs pour les troubles du climatère mais les prescripteurs doivent prendre en compte cette augmentation du risque. Lors de la prescription d’œstrogènes l’association de progestérone est nécessaire pour protéger du risque de cancer de l’endomètre. En revanche, si la femme a été hystérectomisée, la progestérone ne doit pas être prescrite. Dans tous les cas, le traitement doit être prescrit à la dose la plus faible et doit être de courte durée, inférieure à 5 ans. Le risque disparaît dans les 5 ans qui suivent l’arrêt du traitement. La baisse de la prescription de traitement hormonal de la ménopause après la publication du WHI a fait baisser l’incidence du cancer du sein de 9 à 22 % surtout dans les pays ou 40 à 50 % des femmes ménopausées étaient traitées (Lopes, 2010 ; cf. chap. 27).
Facteurs familiaux
On considère le risque familial élevé s’il y a :
 quatre cas au moins de cancer du sein ou de l’ovaire chez des apparentés du premier ou du deuxième degré dans la même branche parentale quel que soit l’âge de survenue ;
quatre cas au moins de cancer du sein ou de l’ovaire chez des apparentés du premier ou du deuxième degré dans la même branche parentale quel que soit l’âge de survenue ;
 trois cas de cancer du sein unis entre eux par un lien de premier degré : un cas avant 41 ans ou trois cas avant 50 ans ;
trois cas de cancer du sein unis entre eux par un lien de premier degré : un cas avant 41 ans ou trois cas avant 50 ans ;
 deux cancers du sein invasifs survenus avant 40 ans chez des apparentés proches ;
deux cancers du sein invasifs survenus avant 40 ans chez des apparentés proches ;
 un cancer du sein chez un homme associé chez un des apparentés proche à un cancer du sein invasif avant 50 ans ou deux cancers du sein invasifs quel que soit l’âge ;
un cancer du sein chez un homme associé chez un des apparentés proche à un cancer du sein invasif avant 50 ans ou deux cancers du sein invasifs quel que soit l’âge ;
 un cas de cancer de l’ovaire (quel que soit l’âge au moment du diagnostic) et un cas de cancer du sein chez des apparentés au premier degré ;
un cas de cancer de l’ovaire (quel que soit l’âge au moment du diagnostic) et un cas de cancer du sein chez des apparentés au premier degré ;
 un cas associant un cancer du sein et un cancer de l’ovaire.
un cas associant un cancer du sein et un cancer de l’ovaire.
Eisenger (2004) a établi un score pour proposer une consultation d’oncogénétique (tableau 19.2).
Tableau 19.2 Échelle de facteurs de risques de cancer du sein en fonction des antécédents familiaux.
| Facteur de risque | Points |
|---|---|
| BCRA 1 ou 2 identifié dans la famille | 5 |
| Cancer du sein chez une femme de moins de 30 ans | 3 |
| Cancer du sein chez une femme de 30 à 40 ans | 3 |
| Cancer du sein chez une femme de 40 à 50 ans | 2 |
| Cancer du sein chez une femme de 50 à 70 ans | 1 |
| Cancer du sein chez un homme | 4 |
| Cancer de l’ovaire | 3 |
En effet, des gènes prédisposants ont été identifiés : c’est le locus BCRA 1 localisé sur le bras long du chromosome 17. Sa fréquence est de 1/150 femmes (0,33 %), il est à pénétrance variable, on le retrouve dans 45 % des cancers familiaux du sein, des cancers survenant avant 40 ans ou bilatéraux mais aussi des ovaires, du côlon (RR 4) et de la prostate (RR 3). Le gène BCRA2 est porté dans le chromosome 13. Les mutations des gènes BCRA1 et 2 rendent compte de la moitié des cancers du sein familiaux, alors que les mutations de BCRA1 sont associées à la quasi-totalité des cancers familiaux. L’incidence des mutations est de 1/400 pour BCRA-1 et 1/200 pour BCRA2.
Chez les porteurs de mutation des gènes, le taux de cancers du sein est de 60 % à 50 ans contre 5 % dans la population générale et de 90 % à 80 ans contre 10 % dans la population générale. Le risque relatif est donc de 10 à 11 par rapport à la population normale. Ce risque est néanmoins encore important entre 20 et 50 ans : 13 % entre 30 et 39 ans, 23 % entre 40 et 49 ans (tableau 19.3). Quatre autres gènes ont été identifiés FGFR2 et TNRC9 qui augmentent le risque de 20 % et MAP3K1 et LSP1 qui l’augmente de 10 % dès lors qu’il n’existe qu’une seule mutation.
Tableau 19.3 Risque de cancer du sein chez les femmes prédisposées ou non.
| Absence de mutation BRCA-1 | Présence d’une mutation BRCA-1 | |
|---|---|---|
| Incidence cumulée (0 à 75 ans) de cancers (tous sites confondus) | 25 à 30 % | 90 à 93 % |
| Incidence cumulée (0 à 75 ans) de cancer du sein | 7 à 10 % | 80 à 90 % |
| Âge moyen d’apparition d’un cancer du sein | 59 ans | 43 ans |
| Risque cumulé (0 à 74 ans) pour : | 1,5 % 3 % 1,1 % 0,6 % | 40 à 60 % 3 à 12 % 1,1 % 0,6 % |
| Même porteuses du gène, 10 à 20 % des femmes ne feront pas un cancer du sein. | ||
(d’après Stoppa-Lyonnet et al., 1997)
La négativité du test n’élimine pas l’existence d’un gène de prédisposition mais seule l’identification d’une mutation chez la femme porteuse du cancer permet de retenir le caractère génétique.
 proposer à la patiente une surveillance rapprochée (mammographie ou IRM dès 30 ans ?) et proposer une castration après 40 ans, voire une mastectomie bilatérale avec reconstruction ;
proposer à la patiente une surveillance rapprochée (mammographie ou IRM dès 30 ans ?) et proposer une castration après 40 ans, voire une mastectomie bilatérale avec reconstruction ;
 rechercher chez les apparentés indemnes de cancer la mutation identifiée dans le but de les surveiller étroitement (mammographie ou IRM dès 30 ans ?) et aussi proposer une castration après 40 ans, voire une mastectomie bilatérale avec reconstruction.
rechercher chez les apparentés indemnes de cancer la mutation identifiée dans le but de les surveiller étroitement (mammographie ou IRM dès 30 ans ?) et aussi proposer une castration après 40 ans, voire une mastectomie bilatérale avec reconstruction.
L’existence d’un autre cancer du sein, du côlon, de l’endomètre constitue également un facteur de risque
Anatomie pathologique
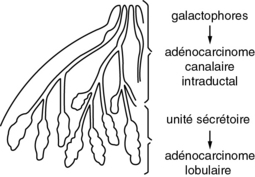
Le sein normal comporte un arbre galactophorique et du tissu conjonctif. Le cancer se développe le plus souvent à partir de l’arbre galactophorique (figure 19.3).
Les carcinomes mammaires sont de loin les plus fréquents
Adénocarcinomes intragalactophoriques ou canalaires « intraductal-carcinoma »
Une classification histopronostique peut être proposée. On utilise celle de Scarff-Bloom-Richardson (SBR). Ce score tient compte de la différenciation et de l’activité mitotique.
Adénocarcinomes lobulaires in situ (ou ductulaires)
Ils sont développés au niveau de l’unité sécrétoire hormonosensible que représente le lobule mammaire et sont constitués par le canal intralobulaire, ses dix ou douze terminaisons ductulaires et le tissu conjonctif qui le circonscrit.
Ils représentent 15 % des carcinomes in situ et sont en général découverts de manière fortuite. Ils sont divisés en trois catégories lobular intra-epitheleial neoplasia (LIN 1 à 3 selon l’importance des lésions). Ils constituent un facteur de risque pour les deux seins de développer un carcinome lobulaire infiltrant de l’ordre de 1 % par an (Prescrire, 2003). Lorsqu’ils deviennent invasifs, ils donnent des cancers anaplasiques, infiltrants, évolutifs, ayant une fréquence élevée de ganglions envahis, de pronostic sombre.
Histoire naturelle du cancer du sein
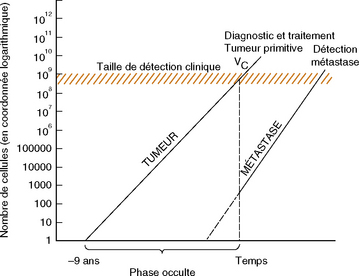
Il naît à partir d’une cellule d’un canal galactophore dans 85 % des cas et d’un lobule sécrétoire dans 1 % des cas (figure 19.4).
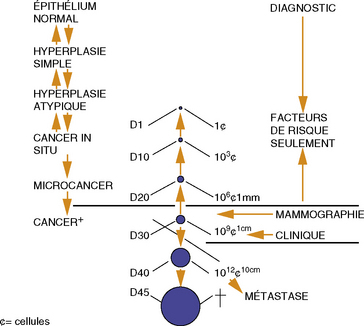
Figure 19.4 Histoire naturelle du cancer du sein.
Ce schéma montre bien la longue histoire du cancer avant le diagnostic clinique.
On considère qu’il faudra en moyenne 10 ans avec des extrêmes de 1,5 à 20 ans avant que la tumeur devienne cliniquement palpable soit 1 cm environ. On est alors au 30e doublement. La tumeur fait 1 milliard de cellules et 3 millions de cellules cancéreuses sont déversées dans le sang ou la lymphe toutes les 24 heures. Ce fait explique que les métastases soient en place au moment du diagnostic clinique (figure 19.5) mais trop petites pour être détectables.
Extension du cancer
L’extension lymphatique régionale se fait par :
Elle est d’autant plus fréquente que la tumeur est plus grosse :
 un tiers des patientes dont la tumeur est inférieure à 3 cm ont des ganglions envahis (N +) ;
un tiers des patientes dont la tumeur est inférieure à 3 cm ont des ganglions envahis (N +) ;
 la moitié des patientes dont la tumeur est supérieure à 3 cm ont des ganglions envahis.
la moitié des patientes dont la tumeur est supérieure à 3 cm ont des ganglions envahis.
Le cancer du sein est une maladie générale
 sur cent femmes qui récidivent, quatre-vingt-douze ont des métastases à distance et seulement huit ont des récidives locorégionales ;
sur cent femmes qui récidivent, quatre-vingt-douze ont des métastases à distance et seulement huit ont des récidives locorégionales ;
 chez les femmes qui meurent dans les 5 ans après le traitement initial (50 % des N + et 25 % des N –), toutes meurent de métastases qui existaient à l’état microscopique lors du traitement initial ;
chez les femmes qui meurent dans les 5 ans après le traitement initial (50 % des N + et 25 % des N –), toutes meurent de métastases qui existaient à l’état microscopique lors du traitement initial ;
 chez les malades qui survivent au-delà de 10 ans (50 % des N – et 25 % des N +), existaient des métastases microscopiques qui ont dû régresser après le traitement de la tumeur initiale ou sous l’influence de l’amélioration immunitaire.
chez les malades qui survivent au-delà de 10 ans (50 % des N – et 25 % des N +), existaient des métastases microscopiques qui ont dû régresser après le traitement de la tumeur initiale ou sous l’influence de l’amélioration immunitaire.
 le dépistage, puisque plus le diagnostic est précoce, meilleur devrait être le résultat car l’on peut espérer intervenir avant l’installation des micrométastases ;
le dépistage, puisque plus le diagnostic est précoce, meilleur devrait être le résultat car l’on peut espérer intervenir avant l’installation des micrométastases ;
 l’utilisation de la chimiothérapie ou de l’hormonothérapie adjuvante puisque les micrométastases sont en place lors du traitement locorégional et qu’elles sont particulièrement chimio- et/ou hormonosensibles.
l’utilisation de la chimiothérapie ou de l’hormonothérapie adjuvante puisque les micrométastases sont en place lors du traitement locorégional et qu’elles sont particulièrement chimio- et/ou hormonosensibles.
Le cancer du sein : un cancer hormono-dépendant
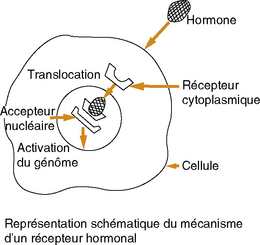
La glande mammaire normale est un tissu cible pour l’action d’hormones variées, et en particulier les estrogènes et la progestérone. Ces cellules contiennent des protéines particulières appelées récepteurs hormonaux (figure 19.6). Dans le cas des hormones stéroïdes (estrogène et progestérone), ces récepteurs sont cytoplasmiques. Pour la prolactine par contre, ils sont membranaires. Les récepteurs ayant capté l’hormone spécifique, le complexe hormone–récepteur va dans le noyau où il va induire l’action spécifique de l’hormone. Par ailleurs, les estrogènes (estradiol) vont stimuler la resynthèse de leur propre récepteur et augmenter la synthèse des récepteurs de progestérone (PgR). À l’opposé, la synthèse du récepteur à estrogènes est bloquée par la présence de progestérone. Ainsi peut-on définir à l’étage cellulaire l’hormono-dépendance d’une tumeur.
Génomique
L’étude des gènes d’expression tumoraux permet aussi de classer les tumeurs à bon ou mauvais pronostic (Van’t Veer, 2002). Dans cette étude, le taux de survie globale à 10 ans était de 94,5 % dans le groupe génétiquement à bon pronostic et de 54,6 % dans celui à mauvais pronostic. Le taux de survie sans métastases à 10 ans était respectivement de 85 % pour les bons pronostics et 50,6 % pour les mauvais et ceci quel que soit l’envahissement ganglionnaire.
 l’envahissement ganglionnaire et le développement de métastases à distance sont des propriétés de la tumeur indépendantes et déterminées génétiquement ;
l’envahissement ganglionnaire et le développement de métastases à distance sont des propriétés de la tumeur indépendantes et déterminées génétiquement ;
 la capacité de métastase étant une propriété génétique de la tumeur, le bénéfice du dépistage et du traitement est limité. Cela expliquerait peut-être l’absence de baisse de la mortalité dans presque tous les pays.
la capacité de métastase étant une propriété génétique de la tumeur, le bénéfice du dépistage et du traitement est limité. Cela expliquerait peut-être l’absence de baisse de la mortalité dans presque tous les pays.
Diagnostic précoce du cancer du sein
Dépistage
Pourquoi le dépistage du cancer du sein ?
La nécessité du dépistage du cancer du sein repose sur plusieurs données :
 le taux de mortalité du cancer du sein, malgré les progrès thérapeutiques survenus, est stable depuis 30 ans (cf. figure 19.2) ;
le taux de mortalité du cancer du sein, malgré les progrès thérapeutiques survenus, est stable depuis 30 ans (cf. figure 19.2) ;
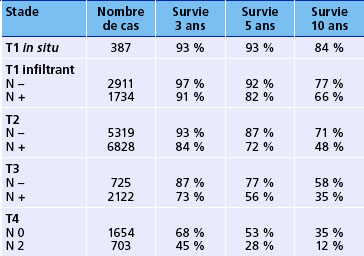
 le pronostic d’une tumeur du sein dépend du stade auquel le diagnostic, et donc le traitement, est effectué (tableau 19.4). Le but du dépistage est donc de confier au thérapeute une tumeur de taille inférieure à 2 cm sans envahissement ganglionnaire, autorisant un traitement conservateur et ayant un bon pronostic. Faute d’un traitement plus efficace, on espère ainsi infléchir la courbe de mortalité.
le pronostic d’une tumeur du sein dépend du stade auquel le diagnostic, et donc le traitement, est effectué (tableau 19.4). Le but du dépistage est donc de confier au thérapeute une tumeur de taille inférieure à 2 cm sans envahissement ganglionnaire, autorisant un traitement conservateur et ayant un bon pronostic. Faute d’un traitement plus efficace, on espère ainsi infléchir la courbe de mortalité.
Auto-examen des seins
Ici, dans l’auto-examen, le succès signifie la découverte de la maladie et il est évident que la femme n’acceptera jamais facilement cette pratique ou, si elle l’accepte, inconsciemment elle le fera mal pour ne rien trouver… On est donc forcé de reconnaître que si l’auto-examen est bien connu, il est peu pratiqué, souvent mal fait pour des raisons psychologiques. Enfin et malheureusement, il n’améliore pas la survie des femmes qui le pratiquent (Thomas, 2002).
Examen clinique par le médecin
L’examen clinique médicalisé est donc un bon moyen de dépistage, peut-être pas supérieur à l’auto-examen en qualité, mais ayant une meilleure pénétration dans la population. Il est cependant insuffisant pour la découverte des petits cancers infracliniques. Il ne permet pas la baisse de la mortalité (Bobo, 2000). Cette méthode est recommandée 2 fois par an pour les personnes ayant une mutation de BCRA en commençant après 20–25 ans (HAS, 2012).
Examens complémentaires
Mammographie
Elle a été introduite par Egan pour le dépistage en 1960. Depuis, la technique a beaucoup évolué et avec les nouveaux mammographes on obtient d’excellents clichés pour des doses à la peau de 0,2 à 0,3 rad. On fait en général deux clichés par sein, l’un craniocaudal, l’autre de profil qui peut être remplacé par une incidence médiolatérale. Lundgren a proposé de ne faire qu’un seul cliché en oblique externe, plus simple pour le triage. C’est la solution de deux clichés par seins qui a été retenue en France pour les campagnes de dépistage de masse qui ont été initiées dans tout le pays en 2004.
Risques du dépistage par mammographie
Depuis les études de MacKenzie en 1965 constatant un risque plus grand de cancers du sein chez les femmes tuberculeuses ayant reçu de fortes doses d’irradiation en radioscopie, la crainte d’induire des cancers par dépistage radiologique hante les esprits. En fait, avec les techniques actuelles, le risque est voisin de zéro et comparable à une cigarette par jour, 15 km à vélo, 150 km en voiture. En revanche, le dépistage radiologique comporte 15 à 20 % de faux négatifs et engendre des examens en excès avec des biopsies inutiles, le diagnostic de lésions in situ voire invasives qui n’auraient jamais évolué expliquant l’incidence, qui est passée en 20 ans de 25000 nouveaux cas par an à 53000 sans baisse de la mortalité. Enfin, le dépistage radiologique n’a pas entraîné une baisse des traitements agressifs mais au contraire une augmentation des mastectomies de 20 % (Prescrire, 2006).
Autres examens complémentaires
Ils n’ont pas fait la preuve de leur utilité :
 la xérographie donne de moins bonnes images avec une irradiation supérieure et a été abandonnée dans les différents programmes ;
la xérographie donne de moins bonnes images avec une irradiation supérieure et a été abandonnée dans les différents programmes ;
 l’échographie n’est dans l’état actuel de la technique pas assez performante pour le dépistage des petites lésions, même si elle est d’un apport important pour le diagnostic des lésions ;
l’échographie n’est dans l’état actuel de la technique pas assez performante pour le dépistage des petites lésions, même si elle est d’un apport important pour le diagnostic des lésions ;
 l’IRM peut être utilisée chez les femmes jeunes à haut risque génétique.
l’IRM peut être utilisée chez les femmes jeunes à haut risque génétique.
Résultat des campagnes de dépistage organisées
L’effet bénéfique des campagnes de dépistage sur la mortalité des femmes de plus de 50 ans a été confirmé par une méta-analyse de treize programmes. La baisse de la mortalité est d’environ 26 % (Kerlikowske, 1995). Pour les femmes de moins de 50 ans, une méta-analyse de huit programmes fait apparaître une réduction de la mortalité de 18 %, mais apparaissant tardivement après 10 ans (Hendrick, 1997).
Ces résultats sont cependant contestés par plusieurs groupes (Fletcher, 1993 ; Wright et Mueller, 1995 ; Götzsche, 2000) en raison du taux de faux négatifs, du taux de faux positifs entraînant des interventions inutiles, du surtraitement de femmes dont la maladie infraclinique n’aurait jamais évolué et qui seraient mortes d’une autre cause (3 %). Dans l’état actuel des techniques, le bénéfice/risque du dépistage n’est acceptable que dans la tranche d’âge 50–70 ans. Il est incertain sur la mortalité car dans les pays d’Europe où il n’est pas organisé et où l’accès au soin est identique, la mortalité a baissé du fait de traitements plus adaptés (Autier, 2011). Il faut en informer les femmes (Prescrire, 2006).
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree