Chapitre 18 Pathologie bénigne des seins1
Cependant le cancer est toujours présent à cette consultation :
 dans la pensée de la femme qui consulte ;
dans la pensée de la femme qui consulte ;
 dans l’esprit du médecin qui a peur de ne pas en faire le diagnostic assez tôt.
dans l’esprit du médecin qui a peur de ne pas en faire le diagnostic assez tôt.
Il y aura donc dans cette pathologie trois risques :
 pécher par optimisme et ne pas faire le diagnostic d’un cancer qui peut être associé ou ressembler à une lésion bénigne ;
pécher par optimisme et ne pas faire le diagnostic d’un cancer qui peut être associé ou ressembler à une lésion bénigne ;
 multiplier les examens complémentaires coûteux et inutiles ;
multiplier les examens complémentaires coûteux et inutiles ;
 faire monter fréquemment la patiente sur la table d’opération.
faire monter fréquemment la patiente sur la table d’opération.
Rappel physiologique (figures 18.1 à 18.4)
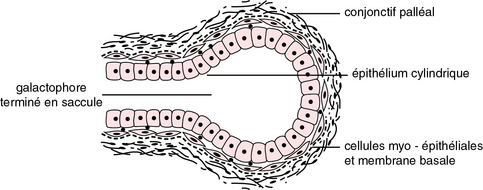
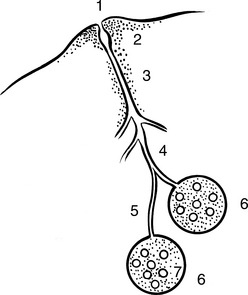
Figure 18.2 Structure histologique d’une terminaison galactophorique.
Source : Abrégé de sénologie de J.Y. Pons. Paris : Masson ; 1985.
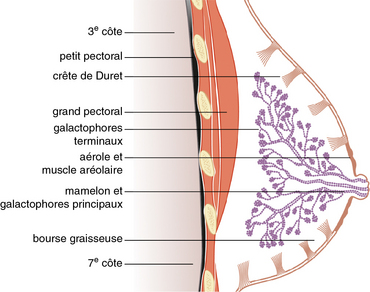
Figure 18.3 Coupe sagittale du sein.
Source : Abrégé de sénologie de J.Y. Pons. Paris : Masson ; 1985.
Histologie
Tissu hétérogène, le sein est fait de 15 à 20 galactophores entourés de cellules myoépithéliales, d’unités sécrétoires situées à leurs extrémités qui proliféreront en acini lors de la lactation mais surtout de tissus conjonctifs, en particulier le tissu palléal, richement vascularisé, et de tissus adipeux. Les travées conjonctives sont responsables de l’aspect lobulé de la glande mammaire formée d’une vingtaine de lobules, chacun de ces lobules étant drainé par un galactophore qui aboutit à un pore s’ouvrant à l’extrémité du mamelon. Celui-ci est doté de fibres érectiles et de corpuscules sensoriels.
Hormono-dépendance
Estradiol
Il fait proliférer les galactophores en longueur en augmentant l’activité mitotique de l’extrémité. De plus, il élève la perméabilité des capillaires et donc l’œdème du stroma conjonctif.
Progestérone
 anti-estrogène : action antimitotique (très précise dans le cycle cellulaire entre G1 et S, ce qui explique qu’il faut une imprégnation progestative durable pour que toutes les cellules bénéficient de cet effet antimitotique) ;
anti-estrogène : action antimitotique (très précise dans le cycle cellulaire entre G1 et S, ce qui explique qu’il faut une imprégnation progestative durable pour que toutes les cellules bénéficient de cet effet antimitotique) ;
Prolactine
Elle a un rôle physiologique limité à la lactation,2 cependant sa présence semble indispensable à la différenciation acineuse. Elle stimule l’activité sécrétoire de l’épithélium glandulaire aussi bien que la croissance des cellules épithéliales des acini en présence d’estradiol. Elle agit sur les récepteurs cellulaires spécifiques de membrane dont elle régule la synthèse en relation avec la présence d’estradiol. Elle pourrait stimuler la synthèse des récepteurs cytoplasmiques d’estradiol.
Autres hormones
Glucocorticoïdes
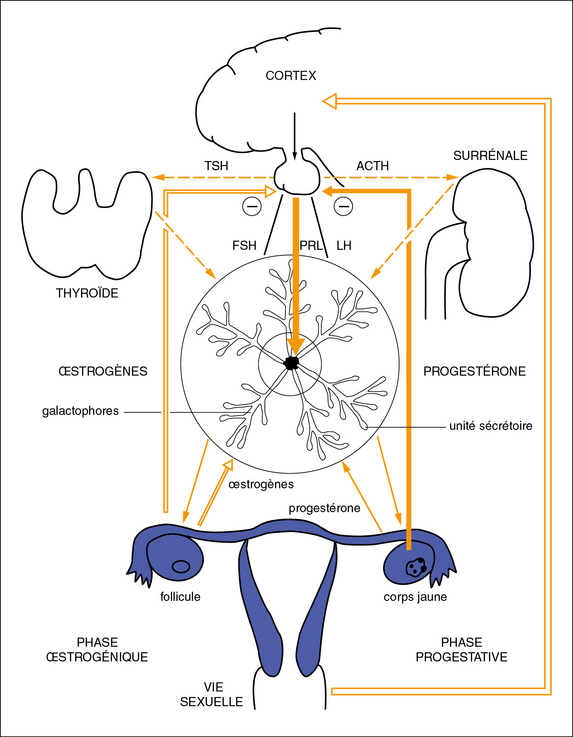
Ils interviennent dans la lactogenèse, l’hormone de croissance et les hormones thyroïdiennes stimulent la croissance des galactophores. L’aldostérone et l’insuline auraient un rôle facilitant sur la différenciation lobulaire en association avec la prolactine. Les gonadostimulines hypophysaires agiraient par contrôle du métabolisme des stéroïdes (figure 18.5).
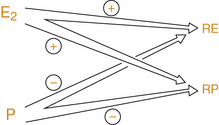
Figure 18.5 Régulation des récepteurs.
E2 : estradiol. P : progestérone. RE : récepteur d’estradiol. RP : récepteur de progestérone.
Récepteurs hormonaux
Les récepteurs hormonaux de E2 et de P ont été mis en évidence dans le tissu mammaire humain normal et pathologique. La détection des récepteurs est plus aisée dans des tissus à forte densité cellulaire comme les adénomes. Les relations entre récepteurs de E2 et de P sont sans doute plus complexes dans le sein que dans l’endomètre et le schéma de la figure 18.5, bien que didactique, s’applique davantage à l’endomètre qu’au tissu mammaire. Par exemple, la progestérone agit de façon synergique avec l’œstradiol pour transformer la partie distale des galactophores en acini, mais elle antagonise les effets de l’œstradiol sur la croissance des galactophores et du tissu palléal.
La progestérone ne diminue pas le nombre de récepteurs de l’estradiol dans le tissu mammaire. La découverte récente de deux types (A et B) de récepteurs de la progestérone d’action opposée et de deux types de récepteurs de l’œstradiol (α et β) va sans doute permettre une meilleure compréhension de ces phénomènes dans l’avenir. Enfin, comme au niveau de l’endomètre, la progestérone active la 17-β-hydroxystéroïde déshydrogénase transformant l’œstradiol en œstrone, ce qui diminue son activité biologique (Mauvais-Jarvis, 1997).
In vivo, une étude utilisant de façon randomisée des traitements en gel – placebo, œstradiol, progestérone, œstradiol plus progestérone – a révélé que l’œstradiol augmente significativement l’index mitotique par rapport au placebo ; l’addition de la progestérone annule cet effet et ramène l’indice mitotique à celui observé après placebo (Chang, 1995).
Le sein évolue avec l’âge
 l’achèvement de la première grossesse à terme marque la fin de la croissance mammaire et la différenciation cellulaire complète du tissu mammaire. La survenue à un âge précoce d’une première grossesse est un facteur de protection vis-à-vis du risque de cancer ;
l’achèvement de la première grossesse à terme marque la fin de la croissance mammaire et la différenciation cellulaire complète du tissu mammaire. La survenue à un âge précoce d’une première grossesse est un facteur de protection vis-à-vis du risque de cancer ;
 à l’âge adulte, on assiste à un envahissement du sein par le tissu adipeux et à une disparition progressive des unités sécrétoires et du tissu conjonctif ;
à l’âge adulte, on assiste à un envahissement du sein par le tissu adipeux et à une disparition progressive des unités sécrétoires et du tissu conjonctif ;
 la préménopause voit réapparaître un déséquilibre estroprogestatif plus marqué. On observe un aplatissement des cellules cylindriques galactophoriques, associé à une diminution du nombre des cellules myoépithéliales, à un amincissement irrégulier de la membrane basale et surtout à des remaniements fibreux du conjonctif palléal. Certains canaux enserrés dans la fibrose subissent une distension kystique ;
la préménopause voit réapparaître un déséquilibre estroprogestatif plus marqué. On observe un aplatissement des cellules cylindriques galactophoriques, associé à une diminution du nombre des cellules myoépithéliales, à un amincissement irrégulier de la membrane basale et surtout à des remaniements fibreux du conjonctif palléal. Certains canaux enserrés dans la fibrose subissent une distension kystique ;
 à la ménopause, le sein n’est plus qu’un tissu adipeux, plus rarement il est fait de tissu conjonctif scléreux (10 % des cas).
à la ménopause, le sein n’est plus qu’un tissu adipeux, plus rarement il est fait de tissu conjonctif scléreux (10 % des cas).
Pathologie bénigne du mamelon
Anomalies congénitales (planche 18.1.a et b)
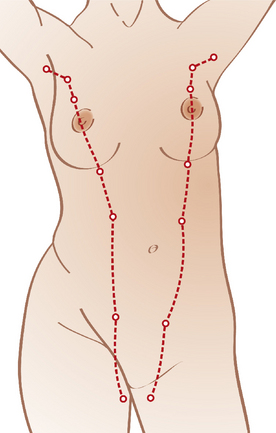
Les mamelons surnuméraires sont fréquents (0,4 à 0,6 % des sujets), il peut s’agir d’un sein complet ou simplement de l’aréole d’un sein, avec ou sans mamelon. Ces structures siègent sur la crête mammaire (figure 18.6) quand elles contiennent du tissu glandulaire. Ces structures subissent les mêmes influences hormonales avec possibilité de sécrétion mais aussi la même pathologie : adénome, maladie de Paget.
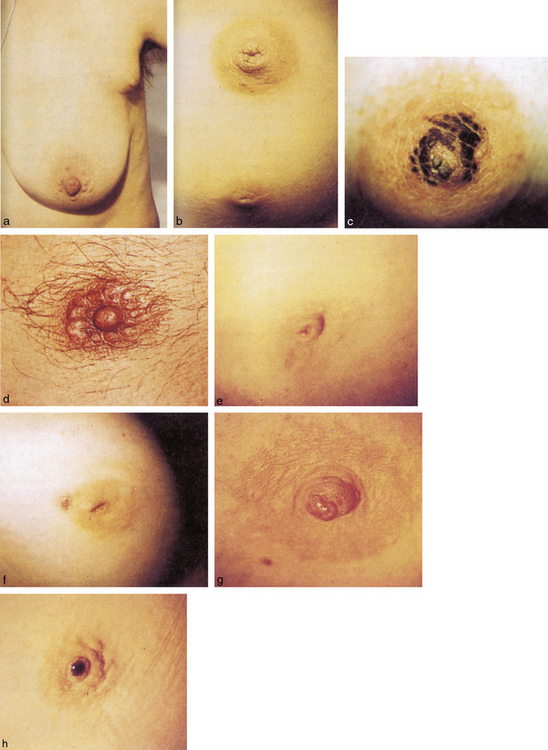
Planche 18.1 Pathologie bénigne du mamelon
L’exérèse chirurgicale est habituellement proposée ou demandée pour motif esthétique.
Pathologie non tumorale
Hyperkératose du mamelon (planche 18.1.c)
L’hyperkératose confère à l’aréole et au mamelon un aspect rugueux et encrassé, unilatéral. Il s’agit en général de l’extension d’un nævus.
Eczéma du mamelon
Il donne au mamelon un aspect suintant et croûteux. La lésion est en général bilatérale et empiète sur l’aréole ou la peau. Il faut en rechercher la cause : gale, mycose, produit de lavage ou de toilette.
Une fois la cause reconnue et supprimée, il faut traiter par :
Maladie de Fox-Fordyce (planche 18.1.d)
Elle correspond à une dilatation parfois kystique des glandes sudoripares apocrines. On trouve donc cette maladie dans toutes les régions où ces glandes existent, c’est-à-dire aux aisselles, au pubis, aux grandes lèvres, au périnée et aux mamelons.
Ectasie ductale (planche 18.1.e)
Il s’agit d’une dilatation avec rétention dans les canaux de la région péri-aréolaire associée à une fibrose et souvent à une inflammation. L’aspect clinique est souvent voisin de celui d’un comédocarcinome.
L’âge moyen des cas traités est de 55 ans.
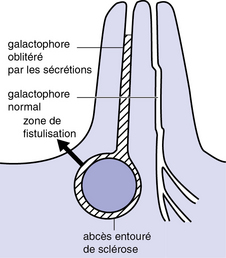
Abcès péri-aréolaires récidivants (planche 18.1.f)
Ils se voient chez les femmes qui ont une ectasie ductale avec rétraction du mamelon. Cliniquement, on observe un abcès de la région péri-aréolaire résistant aux antibiotiques. Lorsqu’il y a simplement incision et drainage, il y a récidive régulière, et parfois même l’installation d’une fistule entre le canal lactifère et l’épiderme aréolaire. Le trajet fistuleux est tapissé par un granulome inflammatoire. Le schéma de la figure 18.7 permet de comprendre la pathogénie de l’affection. Le traitement est essentiellement chirurgical, après un drainage correct par une incision péri-aréolaire. Dans un second temps, on fera l’excision de tout le granulome inflammatoire car sinon il se reproduit des épisodes inflammatoires.
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree