Chapitre 15 Endométriose
• Expliquer à la patiente ce qu’est une endométriose, les conséquences de cette affection, les principes thérapeutiques. (B)
• Diagnostiquer une endométriose externe et mettre en route les thérapeutiques les plus appropriées. (B)
• Diagnostiquer une adénomyose et mettre en route les thérapeutiques les plus appropriées. (B)
• Décrire les signes échographiques et hystérographiques d’une endométriose. (C)
L’endométriose se définit comme la présence de tissu endométrial comportant à la fois des glandes et du stroma en dehors de la cavité utérine. La présence de lésions histologiques n’est pas synonyme de l’existence de la maladie clinique (CNGOF, 2006).
Fréquence
L’adénomyose ou endométriose interne est présente sur 10 à 40 % des pièces d’hystérectomie, quelle qu’en soit la raison (Siegler et al., 1994).
Étiologie
Adénomyose
L’endomètre pénètre le myomètre par des diverticules qui s’enfoncent petit à petit dans l’épaisseur du muscle au-delà de 2,5 mm. Ces diverticules restent le plus souvent localisés à la partie interne du myomètre, mais ils peuvent atteindre, en profondeur, la couche sous-séreuse. Les diverticules ainsi constitués restent parfois en communication avec la cavité utérine mais souvent ils s’isolent, formant des îlots de muqueuse utérine en pleine épaisseur du muscle.
La physiopathologie de l’adénomyose est mal connue. Les traumatismes que constituent les grossesses, les révisions utérines, les curetages, les résections endométriales, semblent favoriser la formation de tels diverticules. Une adénomyose expérimentale est réalisée lorsqu’on invagine l’endomètre dans une cicatrice de césarienne. L’epidermal growth factor (EGF) pourrait jouer un rôle en stimulant la synthèse de la tenascine produite par les fibroblastes du stroma endométrial. Cette protéine, inhibiteur de la fibronectine, favoriserait la prolifération et la migration des cellules glandulaires endométriales dans le myomètre (Deffieux, 2004).
Endométriose externe
Elle désigne toutes les autres localisations (planche 15.1) :
 soit à l’intérieur du pelvis, les îlots hétérotopiques colonisant les ovaires, les ligaments utéro-sacrés, le Douglas, voire le grêle terminal ou le rectosigmoïde. Les îlots d’endométriose peuvent être sous-péritonéaux, enserrer l’uretère et être responsables d’une hydronéphrose. De même dans le cul-de-sac de Douglas, ils peuvent s’infiltrer entre le rectum et le vagin et réapparaître dans le cul-de-sac postérieur du vagin ; c’est l’endométriose profonde ;
soit à l’intérieur du pelvis, les îlots hétérotopiques colonisant les ovaires, les ligaments utéro-sacrés, le Douglas, voire le grêle terminal ou le rectosigmoïde. Les îlots d’endométriose peuvent être sous-péritonéaux, enserrer l’uretère et être responsables d’une hydronéphrose. De même dans le cul-de-sac de Douglas, ils peuvent s’infiltrer entre le rectum et le vagin et réapparaître dans le cul-de-sac postérieur du vagin ; c’est l’endométriose profonde ;
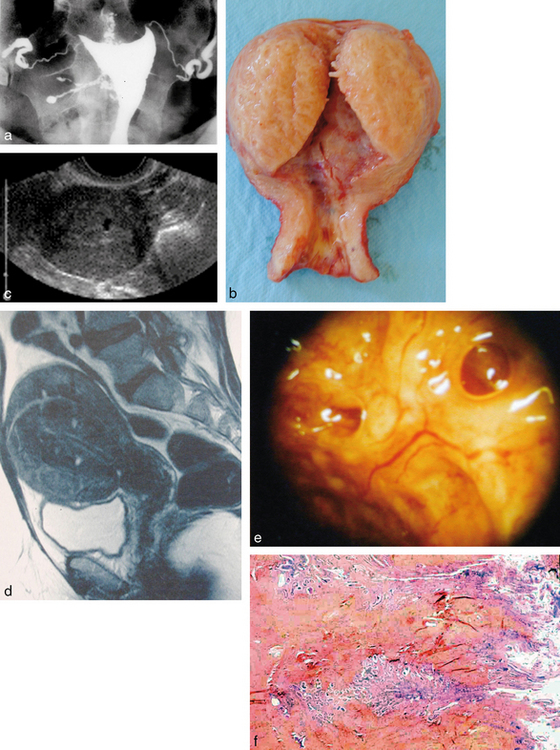
Planche 15.1 Imagerie dans l’adénomyose
Plusieurs hypothèses peuvent expliquer ces localisations :
 la théorie de la transplantation de fragment d’endomètre du fait d’un reflux menstruel par les trompes, de métastases lymphatiques ou vasculaires (Halme, 1984) ;
la théorie de la transplantation de fragment d’endomètre du fait d’un reflux menstruel par les trompes, de métastases lymphatiques ou vasculaires (Halme, 1984) ;
 la théorie métaplasique : différents stimuli pourraient entraîner le développement en position métaplasique de tissu de type endométrial à partir de cellules d’origine cœlomique. Ces stimuli pourraient être des substances libérées par l’endomètre, des stimuli hormonaux ou infectieux ;
la théorie métaplasique : différents stimuli pourraient entraîner le développement en position métaplasique de tissu de type endométrial à partir de cellules d’origine cœlomique. Ces stimuli pourraient être des substances libérées par l’endomètre, des stimuli hormonaux ou infectieux ;
 la théorie immunitaire, étant donné la fréquence du reflux tubaire pendant les règles retrouvée chez 90 % des femmes ; l’acceptabilité et le développement de la greffe endométriale seraient dus à un déficit immunitaire : pathologie auto-immune ? (Dmowski, 1981) ;
la théorie immunitaire, étant donné la fréquence du reflux tubaire pendant les règles retrouvée chez 90 % des femmes ; l’acceptabilité et le développement de la greffe endométriale seraient dus à un déficit immunitaire : pathologie auto-immune ? (Dmowski, 1981) ;
 des recherches sur les gènes susceptibles de favoriser l’adhésion et le développement de l’endomètre ectopique sont en cours.
des recherches sur les gènes susceptibles de favoriser l’adhésion et le développement de l’endomètre ectopique sont en cours.
Devenir de l’endomètre ectopique
Quoi qu’il en soit, l’endométriose se rencontre pendant la période d’activité génitale ou après la ménopause en cas de sécrétion hormonale pathologique (tumeur hormono-sécrétante) ou au cours d’un traitement hormonal. Normalement, elle guérit avec la ménopause (Belaich, 2003).
Clinique et investigations paracliniques
Adénomyose
À l’examen, l’utérus apparaît globalement augmenté de volume, régulier le plus souvent, dur et fibreux, le reste de l’examen est négatif ; des fibromes peuvent être associés (50 % des cas) ou une endométriose externe (15 %) rendant le diagnostic difficile (GEE, 1994).
Aucune étude contrôlée n’a montré que l’adénomyose était à elle seule responsable de fausses couches ou de mauvais taux d’implantation en FIV (Deffieux et al., 2004).
L’échographie doit être faite en 2e partie de cycle et par voie vaginale (planche 15.1.c). Elle permet d’observer un utérus volumineux, globuleux avec des lacunes anéchogènes, des zones hétérogènes ou mal définies au sein du myomètre. La sensibilité serait de l’ordre de 70 % avec une spécificité de 70 à 90 % (Taourel, 2004).
En IRM (planche 15.1.d), les foyers d’adénomyose apparaissent sous la forme de foyers sous-endométriaux, d’hypersignal en T2. L’hyperplasie musculaire entourant les foyers ectopiques d’endomètre se traduit par un hyposignal hétérogène en T2. La mesure de l’épaisseur moyenne de la zone jonctionnelle semble être le meilleur signe. Elle est de 15 mm chez les patientes ayant une adénomyose contre 7,7 mm chez les patientes indemnes. La sensibilité et la spécificité de l’IRM sont comparables à celles de l’échographie vaginale mais sont moins opérateurs dépendants (Deffieux et al., 2004).
L’hystéroscopie (planche 15.1.e) peut dans certains cas permettre de voir de petits orifices punctiformes correspondant aux canaux diverticulaires.
L’hystérographie a été longtemps l’examen de référence. Elle n’est plus pratiquée que dans les infertilités. Elle montre alors des signes directs pathognomoniques (planche 15.1.a) : les diverticules rectilignes et courts, terminés en massue.
Quand les diverticules sont exclus, des signes indirects attirent parfois l’attention :
 ectasie d’une seule corne utérine : la corne est élargie dans tous ses diamètres ;
ectasie d’une seule corne utérine : la corne est élargie dans tous ses diamètres ;
 ectasie généralisée, il y a une hypertrophie globale de la cavité utérine – qui, fait essentiel, est exempte de lacune – et rigide ;
ectasie généralisée, il y a une hypertrophie globale de la cavité utérine – qui, fait essentiel, est exempte de lacune – et rigide ;
 une segmentation rigide en ligne brisée des bords et du fond utérin ;
une segmentation rigide en ligne brisée des bords et du fond utérin ;
 des trompes dont la partie initiale est verticale (tuba erecta) donnant au fond utérin un aspect en « lampe d’Aladin ».
des trompes dont la partie initiale est verticale (tuba erecta) donnant au fond utérin un aspect en « lampe d’Aladin ».
Endométriose externe intrapéritonéale
En l’absence d’antécédents infectieux, le diagnostic le plus probable est celui d’endométriose.
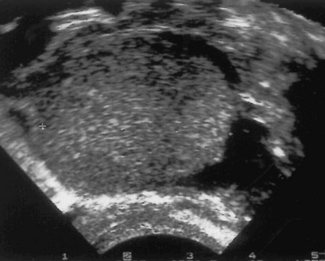
L’échographie, en particulier vaginale, peut orienter le diagnostic en cas de masses annexielles. Les kystes ovariens endométriaux, s’ils ont plus de 2 cm de diamètre, seront évoqués sur des images arrondies, avec des contours internes lisses et réguliers. On observe, dans les kystes, des échos de faible brillance, qui sont répartis de façon uniforme dans l’ensemble du kyste. Il y a un renforcement postérieur, il n’y a pas de cloisons intrakystiques (figure 15.1). Après mobilisation du kyste par la sonde vaginale par exemple, on peut observer la mise en mouvement des échos intrakystiques.
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree