Syndromes occlusifs
C. Lacombe, M. Lewin, L. Azizi and L. Arrivé
L’occlusion intestinale aiguë est définie par un arrêt brutal et complet du transit des matières et des gaz, se manifestant radiologiquement par la présence de niveaux hydroaériques (NHA). Cependant, la séméiologie est très variable, car de multiples pathologies peuvent être responsables d’un syndrome occlusif. L’imagerie, notamment le scanner, joue un rôle majeur dans la prise en charge précoce d’un syndrome occlusif en permettant d’affirmer le diagnostic, puis de localiser et d’identifier l’obstacle, 60 à 80 % des occlusions affectant l’intestin grêle [1]. L’intérêt d’un diagnostic rapide réside en la possibilité par la suite d’instaurer un traitement spécifique, le plus souvent chirurgical lorsqu’il s’agit d’un obstacle organique, avant l’apparition de complications, dominées par l’ischémie du segment lésé.
Séméiologie
Examens d’imagerie
Clichés d’abdomen sans préparation
Classiquement, le diagnostic d’occlusion digestive, grêle ou colique, se fait sur le cliché d’abdomen sans préparation (ASP) debout, par la mise en évidence de NHA« plus larges que hauts », nombreux et de petite taille dans le grêle, et « plus hauts que larges », comportant des haustrations, dans le côlon (figures 1 et 2).
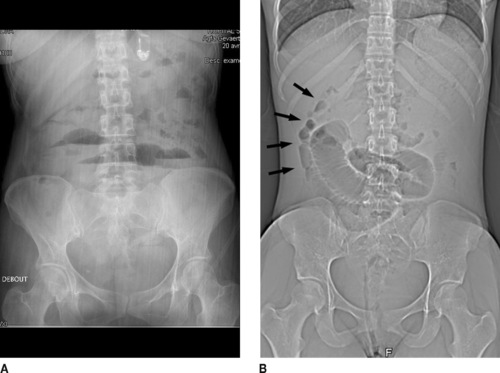 |
| Figure 1 A : Occlusion du grêle. Abdomen sans préparation (ASP) debout de face montrant des niveaux hydroaériques plus larges que hauts. B : Occlusion du grêle (patient différent). Topogramme de face réalisant un ASP couché. Noter la distension des anses grêles, reconnaissables à leur plissement. En aval, le côlon droit n’est pas distendu (flèches), confirmant le niveau grêlique de l’obstruction. |
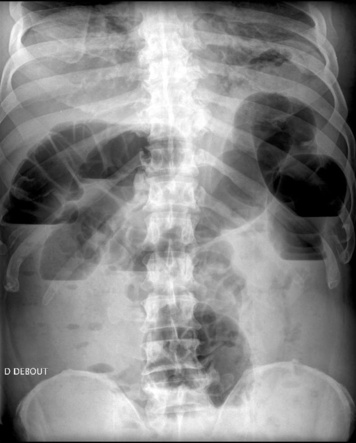 |
| Figure 2 Occlusion du côlon. ASP debout montrant des niveaux hydroaériques plus hauts que larges. |
Dans le cas du patient de réanimation, l’ASP ne pouvant généralement se faire que couché, il est souvent impossible de mettre en évidence des niveaux de face. Le plus souvent, on ne visualisera que la distension grêle et/ou colique selon les cas. Il n’est donc que très peu contributif. Néanmoins, il peut parfois montrer un segment plat, témoin indirect de la localisation de l’obstacle (figure 1B). Il peut également trouver son intérêt dans le suivi évolutif d’une occlusion fonctionnelle.
Le cliché en décubitus pris en latéral gauche (DLG) permet de visualiser d’éventuels NHA de profil chez un patient couché ; mais chez un patient corpulent, l’épaisseur à traverser par le faisceau de rayons X étant très importante, ce cliché est le plus souvent ininterprétable.
Ainsi, les clichés d’ASP peuvent confirmer un diagnostic clinique d’occlusion intestinale mais ne permettent pas d’identifier la cause de l’obstruction ni d’en rechercher les critères de gravité.
Scanner
Le scanner abdominal est l’examen de référence à réaliser devant un tableau clinique d’occlusion abdominale. En effet, il permet de faire la distinction fondamentale entre occlusion fonctionnelle et occlusion organique, d’identifier précisément le niveau et la cause de l’obstacle si l’obstruction est organique, et de montrer d’éventuels signes de sévérité. Réalisé le plus souvent dans un contexte d’urgence, et sur des patients peu compliants, le scanner du patient de réanimation est susceptible d’être de mauvaise qualité, voire ininterprétable, ce qui peut nuire à la fiabilité diagnostique. Il importe donc, malgré les difficultés de mobilisation, les sondes, les drains, les cathéters, etc., de respecter certaines règles techniques afin que le patient et le personnel de réanimation ne soient pas descendus en radiologie « pour rien ».
Pour limiter les artéfacts de durcissement, le patient doit être installé, dans la mesure du possible les bras relevés au-dessus de la tête (figure 3). De même, on préfèrera maintenir le matériel médical comme les seringues électriques à distance de la peau du patient. Les artéfacts respiratoires peuvent être gênants dans l’interprétation d’un abdomen occlus. Si le patient est conscient, une bonne explication préalable des instructions « données par la machine » permet au patient de tenir une apnée suffisante pour le balayage abdominal (à l’étage pelvien, les mouvements respiratoires n’ont que très peu d’influence). Si le patient est intubé et qu’une interruption de la ventilation d’une quinzaine de secondes est supportable par le patient, le réanimateur peut proposer au radiologue d’arrêter le respirateur pendant l’acquisition.
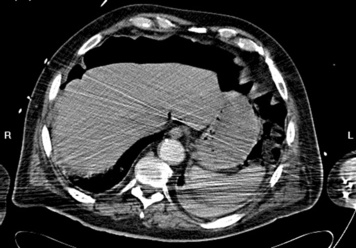 |
| Figure 3 Artéfacts de durcissement. Scanner abdominal chez un patient de réanimation en position « bras le long du corps » produisant des artéfacts de durcissement : images linéaires hyperdenses de disposition radiaire à partir des humérus. Noter par ailleurs le volumineux pneumopéritoine préhépatique. |
Les techniques d’acquisition ont énormément évolué ces dix dernières années. Les techniques incrémentales (ou « séquentielles », coupe par coupe) sont devenues obsolètes. En 2006, la plupart des centres disposent au moins d’un scanner « hélicoïdal » simple détecteur, et au mieux d’un scanner « multibarettes », dont le nombre de détecteurs (ou « barrettes ») augmente avec la génération de la machine (de 4 à 128 actuellement). Le principe de ces scanners hélicoïdaux ou multibarettes est le même, quel que soit le nombre de barrettes : l’acquisition correspond à l’acquisition d’un volume, avec possibilité par la suite de reconstruire les images dans les trois plans de l’espace, en coupes d’épaisseur variable. L’intérêt d’un scanner multibarettes réside en la diminution du temps d’acquisition proportionnelle au nombre de détecteurs, et donc en la diminution du temps d’apnée (de l’ordre de quelques secondes pour un scanner abdominopelvien sur un 128 barrettes).
Devant une occlusion intestinale, on réalisera un scanner abdominopelvien, dont la technique est la suivante. La première acquisition se fait sans injection en coupes jointives de 5 à 7 mm afin de rechercher des éléments apparaissant spontanément hyperdenses pouvant orienter le diagnostic, notamment dans les iléus réflexes : lithiases biliaires ou urinaires, calcifications pancréatiques ou vasculaires, hématomes, etc. Ensuite, est réalisée une acquisition avec injection de produit de contraste iodé, en l’absence de contre-indication. La reconstruction dans le plan axial se fait en coupes fines (3 mm), jointives ou chevauchantes. En cas de suspicion clinique d’infarctus mésentérique, il est recommandé de réaliser une acquisition au temps « artériel » et au temps « veineux », mais dans la plupart des autres cas, le temps « veineux » est suffisant. À noter que, chez les patients de réanimation, l’hémodynamique est souvent altérée et les temps « artériel » (35 s) et « veineux » (70 s) classiques peuvent être retardés, avec une opacification artérielle au temps « veineux » (et pire, pas d’opacification au temps « artériel » !). Pour éviter cet écueil, on peut utiliser un logiciel détectant le bolus de produit de contraste, placé dans l’aorte. On peut également faire démarrer l’acquisition volontairement plus tardivement, vers 45 s pour le temps « artériel » et 80 s pour le temps « veineux ».
Une opacification digestive par voie basse peut être discutée. Largement répandue chez les patients valides, elle présente de multiples inconvénients chez le patient de réanimation, en ralentissant l’examen, en étant mal supportée et rarement contributive (évacuation prématurée du lavement). De plus, elle est contre-indiquée dans certains diagnostics comme le mégacôlon toxique en raison du risque perforatif. Une opacification digestive par voie haute peut également être envisagée. Elle est aisée chez le patient porteur d’une sonde nasogastrique, par le remplissage de la sonde, mais dans un contexte d’urgence, avec l’éventualité d’une sanction chirurgicale, elle peut être contre-indiquée.
Ainsi, de façon générale, on préférera ne pas utiliser de balisage digestif. Il existe néanmoins quelques circonstances cliniques justifiant une opacification digestive, comme une suspicion de fistule. L’opacification devra être réalisée prudemment à l’eau ou aux hydrosolubles dilués. Selon le niveau digestif incriminé, on procèdera à une opacification haute ou basse.
Malgré l’avènement des scanners multidétecteurs et leur rapidité d’acquisition, le temps d’interprétation reste toujours aussi long, notamment en ce qui concerne le diagnostic étiologique d’une occlusion intestinale, car il est nécessaire d’analyser le tube digestif sur toute sa longueur pour localiser et identifier l’obstacle.
L’interprétation des images d’un scanner réalisé pour occlusion intestinale se fait à la console, idéalement en mode « cineview » qui permet de faire défiler les coupes axiales à grande vitesse et, ainsi, de suivre les organes dans leur continuité. Cet outil est particulièrement utile dans l’analyse du tube digestif, qui peut être rapidement suivi de haut en bas, sachant que le suivi de l’intestin grêle est souvent long et difficile. Des reconstructions multiplanaires peuvent être réalisées si nécessaire. Elles n’ont d’intérêt que centrées sur une zone dont l’interprétation pose problème, pour une meilleure analyse de l’obstacle par exemple (figure 4).
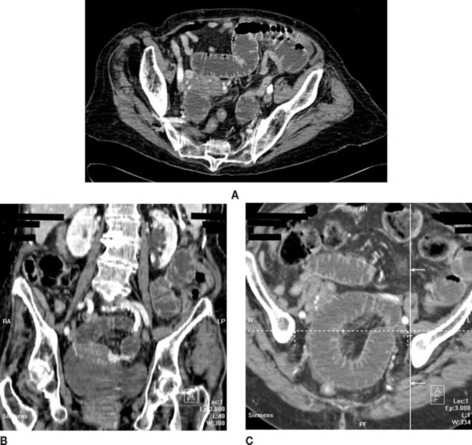 |
| Figure 4 Occlusion du grêle sur hernie interne dans le ligament large. Les reconstructions axiales standard (A) ne permettent pas de visualiser avec certitude la zone jonctionnelle. Les reconstructions coronale (B) et oblique (C) permettent une meilleure visualisation du mécanisme herniaire et de l’anse intestinale étranglée en forme de U fermé. |
Autres examens
L’échographie abdominale n’a pas de place dans l’exploration d’une occlusion intestinale, notamment en raison du barrage gazeux digestif masquant les organes sous-jacents. On peut à la rigueur détecter un syndrome occlusif lors d’une échographie abdominale réalisée en première intention au lit du malade dans le cadre d’un abdomen aigu, en visualisant directement des anses digestives distendues, mais le bilan étiologique ne pourra être réalisé qu’au scanner.
L’imagerie par résonance magnétique (IRM) n’a pas encore réellement d’indication dans l’occlusion intestinale à l’heure actuelle. Elle peut être intéressante dans les pathologies pelviennes responsables d’un syndrome occlusif (notamment dans le bilan lésionnel des cancers du rectum ou dans les pathologies fistuleuses périanales ou périrectales par exemple), mais étant donné la lourdeur d’un examen IRM chez un patient de réanimation, on préférera attendre la sortie de réanimation pour réaliser l’examen.
L’index ou transit baryté est parfois discuté dans le cadre d’un syndrome occlusif. Il consiste en l’ingestion (ou en l’injection par la sonde nasogastrique) d’un verre de baryte pure, dont on suit le cheminement sur des ASP réguliers (toutes les 2 h), l’idée étant de visualiser le niveau de l’arrêt de produit de contraste en vue d’un traitement spécifique. Si l’examen est théoriquement très séduisant, il est peu contributif en pratique, et d’autant moins chez un patient alité, chez qui les ASP sont en général de mauvaise qualité. En effet, le produit avance très lentement en raison de la baisse de la motricité gastrique réactionnelle à l’occlusion, avec, parfois, un bol de baryte encore au niveau du duodénum au bout de 12 h. De plus, en raison de la distension liquidienne, la baryte se dilue dans le liquide de stase, et n’est plus visible au bout de quelques heures, souvent avant même d’arriver à l’obstacle. Le transit baryté, qui est donc un examen très long, n’est pas recommandé car sa faible rentabilité tend plus à retarder le diagnostic qu’à y contribuer.
Séméiologie tomodensitométrique de l’occlusion et démarche diagnostique
Devant une suspicion d’occlusion digestive, le rôle du scanner est d’abord d’affirmer le diagnostic d’occlusion organique, en éliminant le diagnostic d’occlusion fonctionnelle, puis de localiser et d’identifier l’obstacle, et enfin de rechercher des signes de gravité.
Affirmer le diagnostic
Différencier l’occlusion organique de l’occlusion fonctionnelle : mise en évidence de la zone jonctionnelle
C’est l’étape clé du diagnostic étiologique d’une occlusion digestive. L’occlusion organique, qu’elle soit grêle ou colique, est définie par la présence d’un obstacle endoou exoluminal, s’accompagnant d’une disparité de calibre entre les anses d’amont, dilatées, et les anses d’aval, « plates ». Ce niveau transitionnel est également appelé « zone jonctionnelle » ou « zone de transition ».
La mise en évidence de la zone de transition permet le diagnostic différentiel entre occlusion fonctionnelle et occlusion organique. Cependant, cette zone peut être difficile à identifier au sein du grêle en raison de la compression de l’intestin plat par l’intestin dilaté, et dans ce cas, il existe des astuces pouvant aider à l’interprétation.
Tout d’abord, devant une occlusion, on peut aller directement au rectum, grâce au mode « cineview », afin de suivre le côlon de bas en haut, jusqu’au cæcum, pour voir s’il est dilaté ou non. En effet, le côlon, plus court et plus large que le grêle, est plus facilement explorable par un suivi coupe à coupe dynamique à la console. Ainsi, si l’obstacle est colique, il sera facilement identifié.
Si le côlon est dilaté sur toute sa longueur, sans obstacle décelable, on s’orientera vers une occlusion fonctionnelle (il faut néanmoins se méfier des obstacles très bas situés, comme les tumeurs anales).
Si le côlon est plat, le siège de l’occlusion est en amont. On s’attachera donc à rechercher la dernière anse iléale. Si elle est plate, cela témoigne de la présence de grêle plat et de grêle dilaté et, indirectement, de la présence d’une zone de transition grêlique, donc d’une occlusion organique du grêle.
La deuxième astuce pour trouver la zone de transition entre grêle plat et grêle dilaté consiste en la recherche du signe du granité fécal ou feces sign en anglais (figure 5). Ce signe est défini par la présence au sein de l’intestin grêle d’un contenu dont l’aspect tomodensitométrique est celui des matières fécales [2]. Il témoigne de la digestion incomplète qui s’exerce à ce niveau, et localise donc indirectement l’arrêt du transit. La prévalence de ce signe dans la littérature est assez faible (7 à 8 %), car il se développe progressivement après l’arrêt du transit ; ainsi, il est rarement visible dans les occlusions explorées à un stade aigu, alors qu’on le retrouve fréquemment dans les occlusions subaiguës ou chroniques. Dans les occlusions explorées tardivement, il peut mesurer plusieurs centimètres, voire plus dans les occlusions chroniques, où on peut le voir sur 1 ou 2 m [3]. À noter que chez des patients ayant une stase stercorale importante intéressant l’ensemble du cadre colique, cet aspect de granité fécal peut être retrouvé dans la dernière anse iléale ; il ne traduit dans ce cas que l’extension du fécalome à l’iléon terminal.
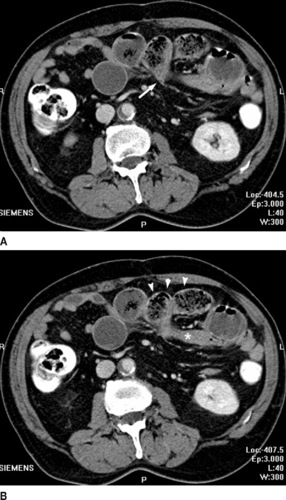 |
| Figure 5 Occlusion sur bride subaiguë sur deux coupes contiguës de scanner abdominal avec injection montrant le signe du bec (flèche blanche, figure 5A) au niveau de la zone jonctionnelle, en aval de laquelle le grêle est plat (*, figure 5B) et le signe du granité fécal (têtes de flèches, figure 5B) dans le grêle dilaté d’amont. |
En pratique, devant une occlusion grêle avec présence d’un signe du granité fécal de plusieurs centimètres, on procédera comme pour le reste du tube, en le suivant de manière dynamique coupe après coupe à la console. On recherchera les deux extrémités du feces sign, l’extrémité distale, où le granité est le plus marqué, correspondant à la jonction grêle plat–grêle dilaté (où l’on visualisera le classique « signe du bec » s’il s’agit d’une occlusion sur bride), et l’extrémité proximale, en général mal limitée, traduisant sa formation progressive ascendante.
Malheureusement, il peut arriver qu’en raison d’une distension intestinale majeure refoulant les anses saines, et en l’absence de granité fécal, on individualise la présence d’anses plates au contact d’anses dilatées, mais que l’on ne puisse pas identifier la zone jonctionnelle et l’obstacle. Dans ce cas, les reconstructions multiplanaires peuvent être très utiles. Mais parfois, elles sont également prises en défaut, et l’on ne pourra donner qu’une localisation approximative de l’obstacle en fonction du type d’anses plates, sans qu’il soit identifié.
Si un examen attentif ne retrouve pas de zone jonctionnelle, et que l’absence de grêle ou de côlon plat confirme cette absence, on conclura au diagnostic d’occlusion fonctionnelle, qui est donc un diagnostic d’élimination.
En cas d’occlusion fonctionnelle, on recherchera systématiquement une cause, notamment à l’aide d’un fenêtrage adapté à la recherche d’un pneumopéritoine, d’un rétropneumopéritoine, d’une pneumatose plus ou moins associée à une aéroportie et/ou une aéromésentérie (ischémie mésentérique) ou bien une aérobilie, que l’on peut retrouver dans l’iléus biliaire (fenêtres « pulmonaires » ou « osseuses »).
Identifier l’obstacle
Une fois la zone jonctionnelle mise en évidence, l’identification de l’obstacle à son niveau est beaucoup plus aisée. Les causes sont variées et détaillées plus bas, mais on retiendra que la cause la plus fréquente d’occlusion du côlon est l’affection tumorale, facilement visible, alors que l’occlusion du grêle la plus fréquente est l’occlusion sur bride ou sur adhérence péritonéale, de diagnostic plus difficile. En effet, les signes d’occlusion sur bride, ou adhérence, classiquement décrits dans la littérature sont inconstants, surtout en ce qui concerne les adhérences qui peuvent ne pas être visibles au scanner. On est parfois ainsi amené à poser le diagnostic d’occlusion sur bride par élimination, devant une occlusion du grêle avec présence de grêle plat et de grêle dilaté, sans autre obstacle visible.
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree








