Chapitre 9 Techniques et indications des lambeaux de reconstruction intrathoracique
PRINCIPES GÉNÉRAUX
Volume
Au regard de ce point, il faut considérer que l’épiploon s’insinue parfaitement dans les espaces anfractueux du médiastin, se glissant sans les comprimer ni les contraindre dans les différents culs-de-sac du péricarde ou les sinus étroits séparant les gros vaisseaux (figure 9.1). Son volume toutefois reste imprévisible avant l’instant de la laparotomie qui l’expose définitivement au regard. En pratique, aucun examen préopératoire ne permet, outre une laparoscopie, de contourner cette incertitude. Dans la plupart des cas, cependant, même lorsque l’abdomen avait été précédemment violé chirurgicalement, notre expérience nous a enseigné que l’exploration soigneuse de la cavité péritonéale permettait toujours d’y lever un lambeau épiploïque dont la masse suffisait à traiter tous les problèmes médiastinaux.
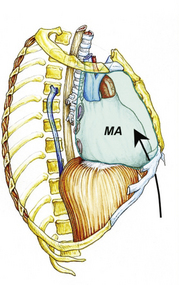
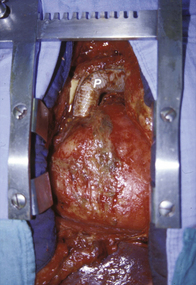
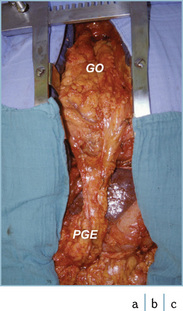
9.1 Exemple de comblement du médiastin antérieur (MA) (a).
INDICATIONS TOPOGRAPHIQUES SÉLECTIVES
Médiastin antérieur
Contenant le coeur et les gros vaisseaux, le médiastin antérieur est toujours abordé par voie de sternotomie médiane. Sa couverture ou son comblement doivent être envisagés de façon primaire après les exérèses étendues du plastron sternocostal qui, associées à un évidement de la graisse médiastinale, exposent les gros troncs artériels, les veines brachiocéphaliques et d’éventuelles tranches de résection pulmonaires. Il en va de même dans les médiastinites purulentes qui compliquent secondairement une chirurgie de revascularisation myocardique, une transplantation cardiaque, ou un remplacement prothétique de l’aorte (figure 9.1).
Médiastin postérieur
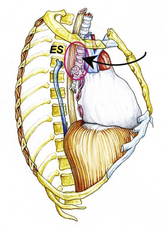
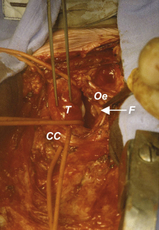
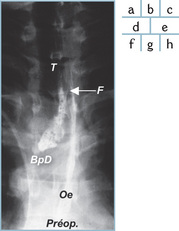
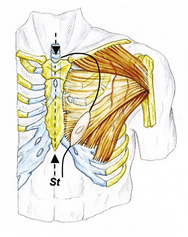
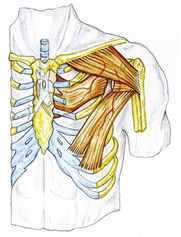
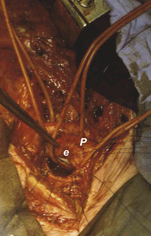
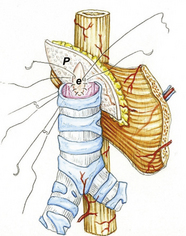
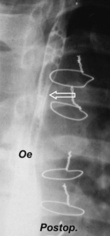
9.2 Exemple de transfert intrathoracique dans l’étage supérieur (ES) du médiastin postérieur (a).
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree








