Ischémies digestives
B. Scotto, D. Alison and D. Perrotin
L’ischémie intestinale qui regroupe des pathologies distinctes nécessitant des traitements très différents est de diagnostic difficile, encore trop tardif en raison d’une sémiologie peu spécifique. Le pronostic global est directement lié à la rapidité de la prise en charge.
Le développement de l’imagerie en coupes et plus particulièrement des scanners multibarrettes qui sont réalisés en urgence devant tout syndrome abdominal aigu a amélioré la gestion de cette pathologie. L’intervention chirurgicale diagnostique et thérapeutique devient exceptionnelle.
Le diagnostic d’ischémie intestinale artérielle aiguë, subaiguë, chronique et celui d’ischémie intestinale veineuse reposent sur un faisceau d’arguments cliniques et scanographiques.
Évoquer la possibilité d’une ischémie intestinale devant un syndrome abdominal, notamment chez le sujet âgé polyvasculaire, impose la réalisation d’un examen scanographique multiphasique qui permet non seulement de poser le diagnostic, mais également d’en rechercher l’étiologie et de guider le traitement dont la caractéristique est d’être multidisciplinaire, associant chirurgiens, anesthésistes, réanimateurs, urgentistes et radiologues.
Généralités
Rappels physiopathologiques élémentaires
L’ischémie intestinale se définit comme une inadéquation entre les besoins et les apports en oxygène des organes vascularisés par la circulation mésentérique. Cette mise au point sera limitée au territoire entérocolique. Elle est le plus souvent la conséquence d’une réduction du flux sanguin dans les vaisseaux mésentériques. Ce déficit circulatoire entraîne des anomalies directement liées à l’anoxie tissulaire et des anomalies secondaires à la reperfusion des organes caractérisée par la libération de métabolites, notamment de radicaux libres.
L’ischémie intestinale rassemble un large spectre de tableaux variés de souffrance intestinale allant d’une simple altération réversible de la fonction intestinale à l’infarctus mésentérique. Les anomalies fonctionnelles apparaissent en premier, d’abord sous la forme d’un hyperpéristaltisme intestinal, de diarrhée, puis d’un iléus par réponse sympathique. Les anomalies morphologiques intéressent d’abord la muqueuse, avec augmentation de la perméation cellulaire, puis dégénérescence muqueuse et nécrose superficielle. À ce stade, les lésions sont réversibles, décrites sous le terme d’infarctus muqueux. Si l’ischémie perdure, l’atteinte progresse en profondeur, atteignant la sous-muqueuse puis la musculeuse. L’atteinte sous-muqueuse comprend une extravasation plasmatique puis une hémorragie. On parle alors d’infarctus mural. Quand l’atteinte intéresse la musculeuse, on parle d’infarctus transmural. L’atteinte muqueuse survient dans les 30 min qui suivent l’ischémie, l’atteinte sous-muqueuse ensuite. Quant à l’atteinte musculaire, elle survient dans les 4 h.
La connaissance des modifications macroscopiques permet de différencier les formes graves d’ischémie artérielle avec atteinte transmurale qui nécessitent une résection chirurgicale des formes moins sévères d’infarctus superficiel ou mural dont l’évolution peut être favorable sous traitement médical.
Incidence
L’incidence de l’ischémie intestinale est difficile à préciser en raison de la variabilité clinique.
Les ischémies artérielles aiguës correspondraient à 0,9 % des hospitalisations pour douleur abdominale et à 0,4 % des laparotomies faites en urgence. Le taux de mortalité élevé, qui était de 60 à 90 % selon les séries, semble diminuer ces dernières années pour approcher les 48 % [1, 2].
L’imagerie en coupes, notamment le scanner, objective que cette fréquence est plus importante notamment chez le sujet âgé. De même, l’ischémie veineuse a été sousestimée. Elle représenterait de 20 à 30 % des tableaux abdominaux aigus d’origine vasculaire. Le scanner en permet plus facilement le diagnostic, limitant ainsi les résections intestinales étendues inutiles.
De nombreux éléments sont responsables de la diversité des tableaux cliniques :
– le mécanisme de l’ischémie : artérielle ou veineuse, obstructive ou non obstructive ;
– la rapidité d’installation de l’ischémie ;
– l’état général du patient ;
– le traitement en cours ;
– les circonstances d’apparition de l’ischémie.
L’important est donc d’évoquer le diagnostic pour faire réaliser en urgence un examen tomodensitométrique abdominopelvien à la recherche systématique des différents éléments sémiologiques d’ischémie intestinale.
Examen scanographique
C’est l’examen d’imagerie de référence pour le diagnostic d’ischémie digestive.
L’apparition des scanners multibarrettes (16 barrettes et, aujourd’hui, 64 barrettes) a révolutionné l’exploration de ces patients. L’obtention d’une véritable angiographie artérielle et veineuse a rendu inutile la réalisation d’artériographie à visée diagnostique [3].
Le scanner permet d’une part d’étudier les anomalies pariétales digestives, mésentériques, mésocoliques, et d’autre part de distinguer une étiologie obstructive artérielle ou veineuse, ou bien une étiologie non obstructive.
La réalisation de cet examen en urgence se fait :
– sans opacification digestive ;
– avec une voie veineuse de bon calibre permettant une injection à haut débit ;
– avec d’abord une hélice sans injection intravasculaire de produit de contraste iodé ;
– puis une hélice précoce d’angiographie artérielle ;
– enfin une hélice parenchymateuse pariétale digestive 55 à 60 s après l’injection du produit de contraste ;
– sur toute la hauteur de l’abdomen et du pelvis.
Les hélices sont analysées dans différents fenêtrages – classique abdominal, vasculaire, pulmonaire (recherche d’air extradigestif) – et dans différents plans – axial, coronal, sagittal et oblique.
Sur l’hélice sans injection sont recherchés :
– des calcifications notamment vasculaires ;
– des signes d’hémorragie : hyperdensité spontanée ;
– des signes d’obstruction vasculaire : hyperdensité spontanée intravasculaire ;
– un pneumopéritoine ;
– une aéroportie, une aéromésentérie ;
– une pneumatose digestive.
L’hélice angiographique donne une cartographie vasculaire artérielle de l’aorte abdominale, notamment des artères à destinée digestive, et met éventuellement en évidence des voies de suppléance. Un travail de reconstruction 3D peut révéler une sténose, une obstruction (hypodensité intraluminale) ou une compression vasculaire.
L’hélice parenchymateuse réalisée autour de 60 s après le début de l’injection permet l’étude :
– de la paroi digestive : épaisseur, prise de contraste [4] ;
– des différents mésos ;
– des veines de drainage du tube digestif (perméables ou non) ;
– de l’ensemble de la cavité abdominopelvienne.
Les différents éléments scanographiques recueillis aux phases successives de l’acquisition associés aux éléments cliniques et biologiques permettent le diagnostic :
– d’ischémie artérielle aiguë dans lesquelles les lésions intéressent toute la paroi intestinale et le mésentère voisin (infarctus intestino-mésentérique ou colique transmural) ;
– d’ischémie artérielle subaiguë qui correspond à une atteinte muqueuse et sousmuqueuse respectant la musculeuse propre et la séreuse ;
– d’ischémie chronique secondaire à une lésion sténosante ou tronculaire obstructive intéressant deux des trois troncs digestifs ; tronc coeliaque (TC), artère mésentérique supérieure (AMS), artère mésentérique inférieure (AMI) selon la règle de Mikkelsen [5] ; cette règle est à nuancer car l’obstruction doit porter majoritairement sur l’AMS, dont l’atteinte module la gravité de la symptomatologie ;
– d’ischémie veineuse, conséquence d’une thrombose de l’axe veineux mésentérique à l’origine d’une congestion hémorragique passive ou d’un infarcissement de la paroi et du méso voisin.
Ischémie artérielle aiguë intestino-mésentérique et colique
Bases physiopathologiques
Les vaisseaux mésentériques contiennent environ le tiers du volume sanguin total de l’organisme au repos. Ils reçoivent 20 à 25 % du débit cardiaque au repos et jusqu’à 35 % en postprandial. Environ 70 % du débit mésentérique sont destinés à la muqueuse intestinale.
Expérimentalement, une réduction de 75 % du flux de l’AMS pendant 12 h n’entraîne aucune lésion.
Malgré la très grande richesse vasculaire de la paroi intestinale, les accidents ischémiques sont fréquents en raison de la réduction du débit splanchnique au cours de toute hypovolémie systémique. Lorsque le mécanisme de compensation est dépassé, les lésions tissulaires apparaissent dans les différentes couches pariétales. C’est l’infarctus transmural.
Les anomalies fonctionnelles apparaissent très rapidement sous forme d’un apéristaltisme du segment ischémié (figures 1 et 2). On observe une stagnation du bolus puis une distension liquidienne progressive par accumulation des sécrétions digestives au niveau de la zone atteinte et en amont. Cela favorise la pullulation microbienne qui, associée à la distension intestinale, est responsable de la présence d’une quantité importante de gaz endoluminal.
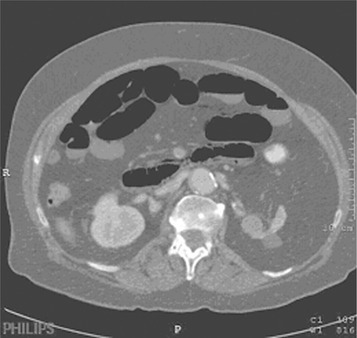 |
| Figure 1 Anses grêles ischémiques dilatées. |
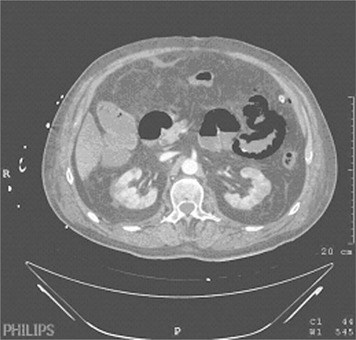 |
| Figure 2 Anses jéjunales nécrosées distendues. |
La nécrose muqueuse permet ainsi l’apparition de la pneumatose intestinale puis de l’aéromésentérie et de l’aéroportie (figure 3). La paroi intestinale ischémiée est amincie et le mésentère adjacent est le siège d’une infiltration hémorragique par hyperperméabilité capillaire autorisant l’extravasation des éléments figurés du sang (figures 4 et 5). Macroscopiquement, l’intestin est noir mais, à la coupe, ses parois sont fines avec des zones de raccordement brutal avec le tube digestif sain d’amont et d’aval. La lumière du segment ischémié est distendue, remplie de liquide hématique. La perforation digestive est plus tardive, la musculeuse résistant plus à l’anoxie que la muqueuse et la sous-muqueuse, et survient en 1 à 4 jours avec péritonite.
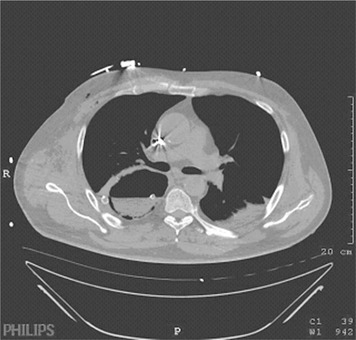 |
| Figure 3 Nécrose d’un transplant gastrique intrathoracique avec pneumatose pariétale. |
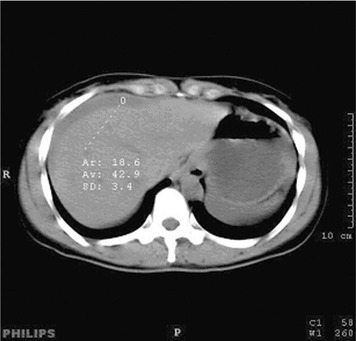 |
| Figure 4 Hémopéritoine périhépatique (d = 42 UH). |
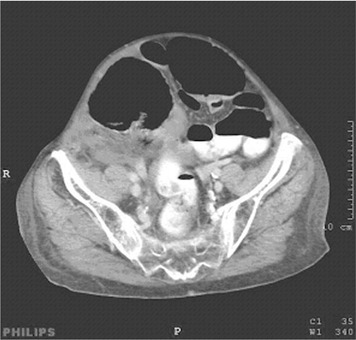 |
| Figure 5 Infiltration hématique péritonéale au contact du côlon nécrosé. |
Les atteintes tissulaires intestinales peuvent également survenir au cours de la période de reperfusion dont les effets peuvent être encore plus néfastes que ceux de l’ischémie, conduisant à une défaillance multiviscérale.
Terrain
L’ischémie intestinale artérielle aiguë regroupe essentiellement des formes occlusives thrombotiques et emboliques. Les formes non occlusives à vaisseaux perméables concernent 20 à 30 % des cas.
Les différentes étiologies concernent des patients à risque élevé :
– les sujets athéromateux (sujets tabagiques, antécédents d’ischémie des membres inférieurs, d’infarctus du myocarde, accident vasculaire cérébral, etc.) ; l’ischémie est due à une thrombose sur athéromatose, le plus souvent tronculaire proximale ;
– les sujets ayant un trouble du rythme cardiaque ; l’embolie peut être d’origine aortique (anévrisme, plaque d’athérome, iatrogène après aortographie, etc.), l’embolie cruorique massive est moins proximale que la thrombose, et souvent multiple et plurifocale ;
– les sujets ayant présenté un bas débit circulatoire à l’origine d’une hypoxie prolongée : choc cardiogénique, choc septique, choc hypovolémique, notamment au décours d’une chirurgie cardiaque ou viscérale chez un sujet âgé et/ou athéromateux ;
– les patients hémodialysés (9 à 20 % des décès en hémodialyse ont été rapportés à une ischémie intestinale aiguë non occlusive [6].
Clinique
Le tableau clinique est extrêmement variable :
– douleur abdominale sévère et continue en discordance avec un examen clinique pauvre ;
– parfois de début très brutal (en rapport avec une origine embolique) ;
– météorisme abdominal, vomissements ;
– diarrhée parfois sanglante suivie d’un état de choc ;
– défense ou contracture abdominale avec matité des flancs (ascite hémorragique) ;
– silence auscultatoire.
Le tableau clinique se constitue en moins de 24 h, mais il existe des formes se complétant en quelques jours.
Apport de l’imagerie
L’abdomen sans préparation (ASP) est le plus souvent trompeur, ne montrant qu’une distension gazeuse non systématisée ; exceptionnellement, on peut observer une pneumatose intestinale ou aéroportie, reflet d’un diagnostic trop tardif (figures 6 et 7).
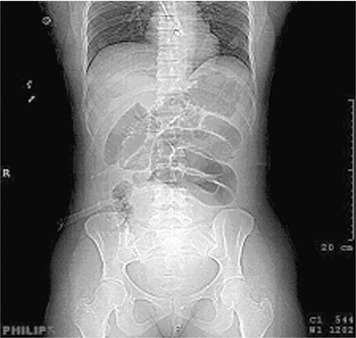 |
| Figure 6 Topogramme du scanner, dilatation des anses grêles nécrosées. |
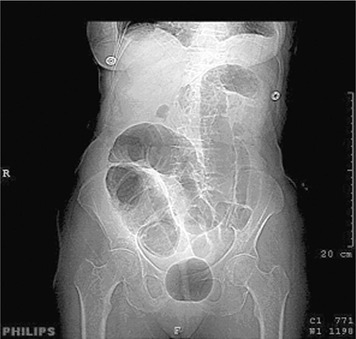 |
| Figure 7 Topogramme du scanner montrant une distension colique avec pneumatose cæcale chez un patient ayant une nécrose colique droite. |
L’échographie abdominopelvienne couplée au doppler peut visualiser une thrombose tronculaire proximale de l’AMS, mais sera très insuffisante pour apprécier l’état des parois intestinales. Elle nécessiterait une étude avec sonde à basse fréquence pour l’analyse vasculaire artérielle et veineuse, puis une étude avec sonde à haute fréquence à la recherche d’anomalies pariétales digestives : paroi épaissie, disparition de la stratification et de la vascularisation pariétale. C’est un examen relativement long et de rentabilité très variable qui ne doit pas retarder la réalisation du scanner.
Seul le scanner réalisé en urgence permet le diagnostic et la prise en charge thérapeutique dans les meilleurs délais.
Le diagnostic repose sur des éléments sémiologiques peu nombreux mais précis. L’étude des anomalies des parois intestinales et du mésentère adjacent est plus importante que celle des signes directs d’atteinte vasculaire [6, 7 and 8].
Sur la série sans injection, on recherche :
– des anses grêles distendues par du liquide à différencier de l’infiltration hématique des structures péritonéales adjacentes ;
– une infiltration hématique de la musculeuse donnant un anneau hyperdense « noyé » dans un environnement liquidien (figure 8) ;