16 Système Nerveux Autonome, Hypothalamique et Limbique
Hypothalamus et glande pituitaire (hypophyse)
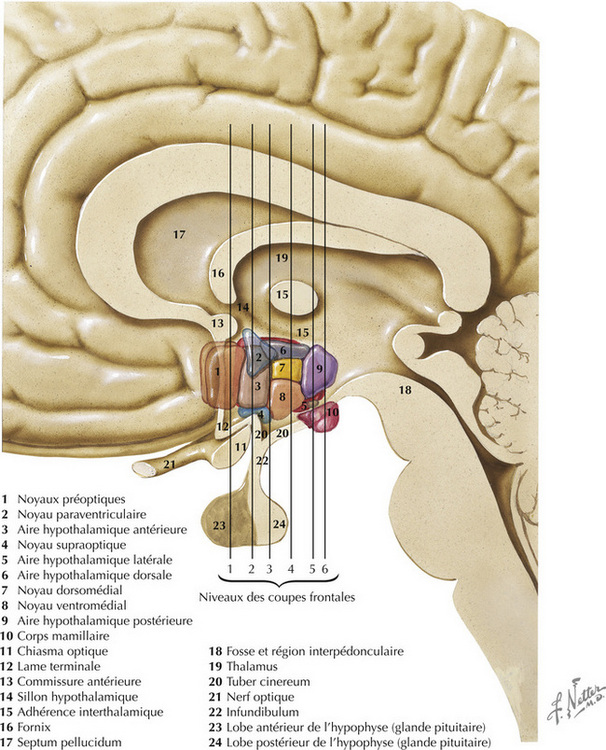
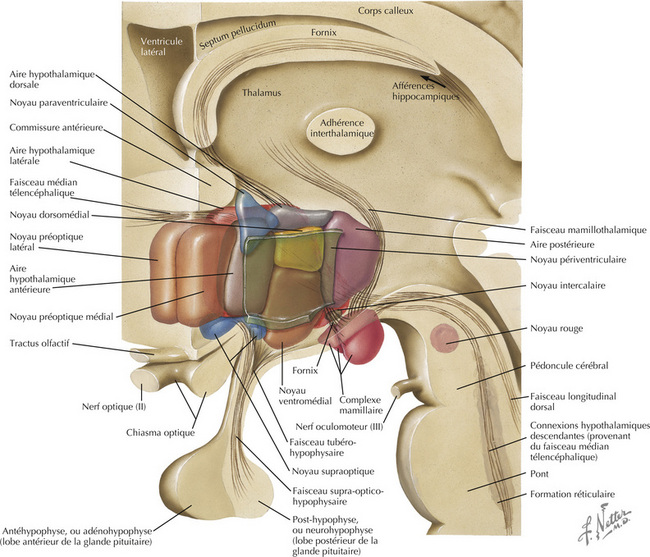
16.2 Anatomie générale de l’hypothalamus
16.3 Coupes frontales passant par l’hypothalamus – 1 et 2 : aires préoptiques et supraoptiques
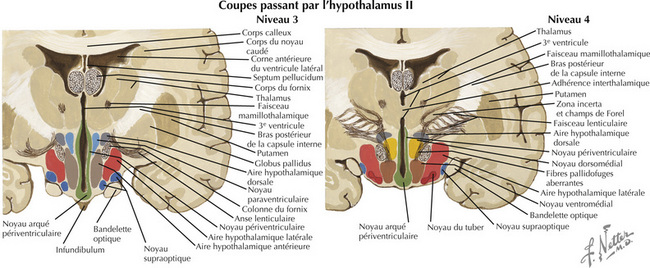
16.4 Coupes frontales passant par l’hypothalamus – 3 et 4 : zone tubérale
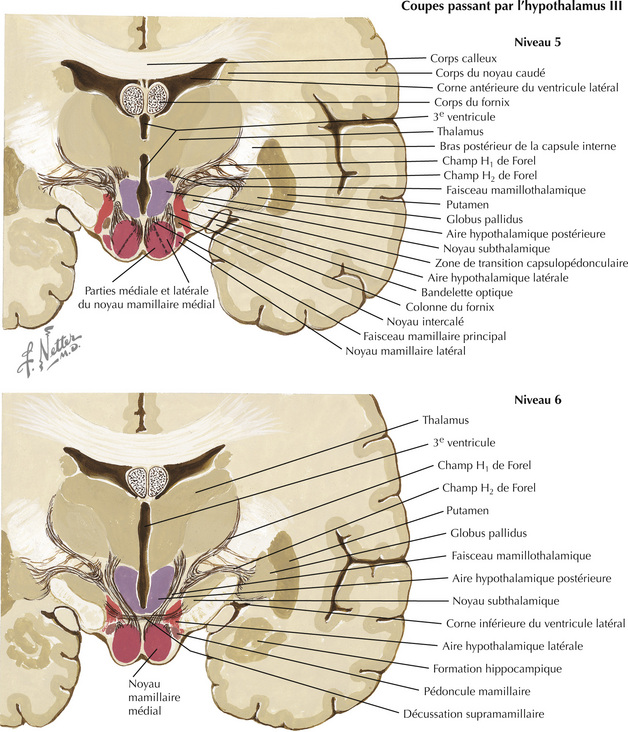
16.5 Coupes frontales passant par l’hypothalamus – 5 et 6 : aire mamillaire
16.6 Reconstruction schématique de l’hypothalamus
16.7 Régions du prosencéphale associées à l’hypothalamus
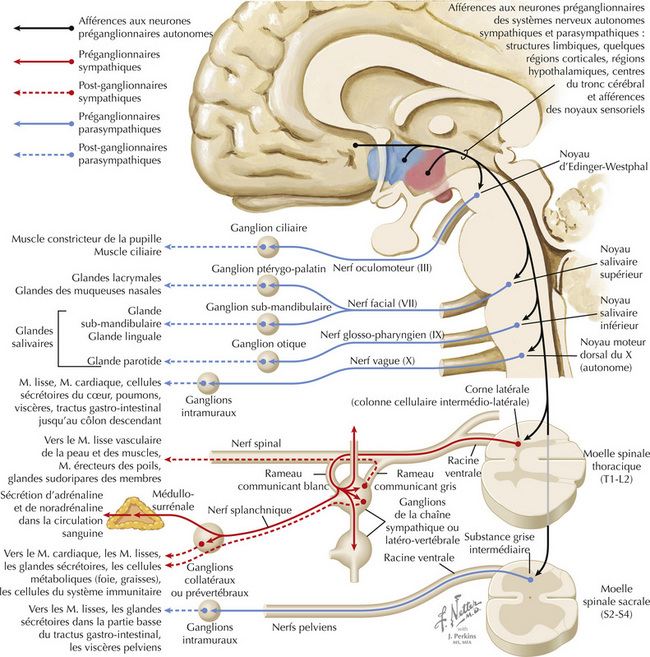
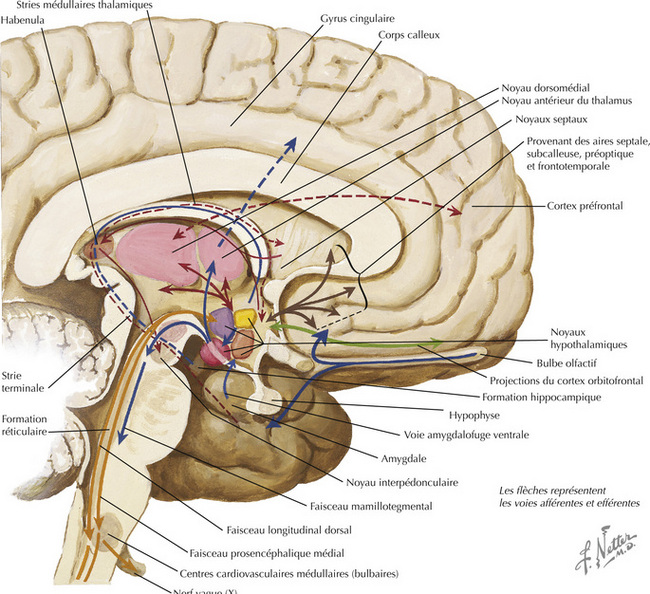
16.8 Voies afférentes et efférentes associées à l’hypothalamus
16.9 Schéma des principales voies afférentes hypothalamiques
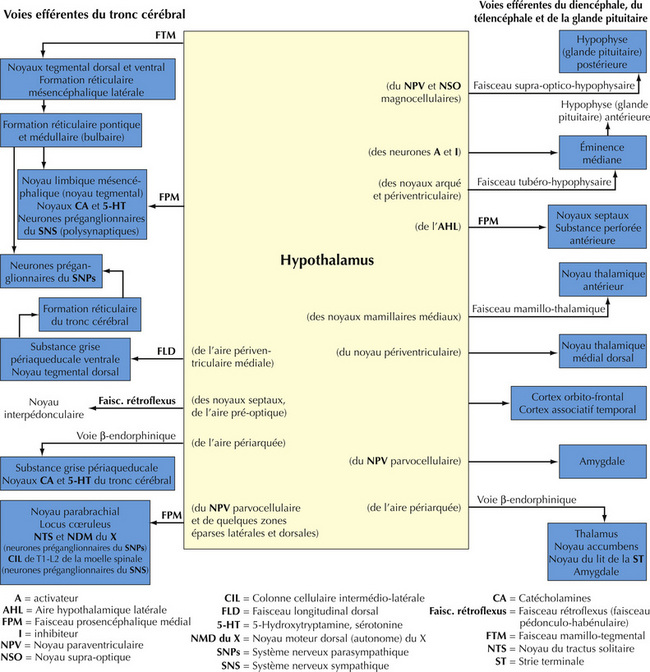
16.10 Schéma des principales voies efférentes hypothalamiques
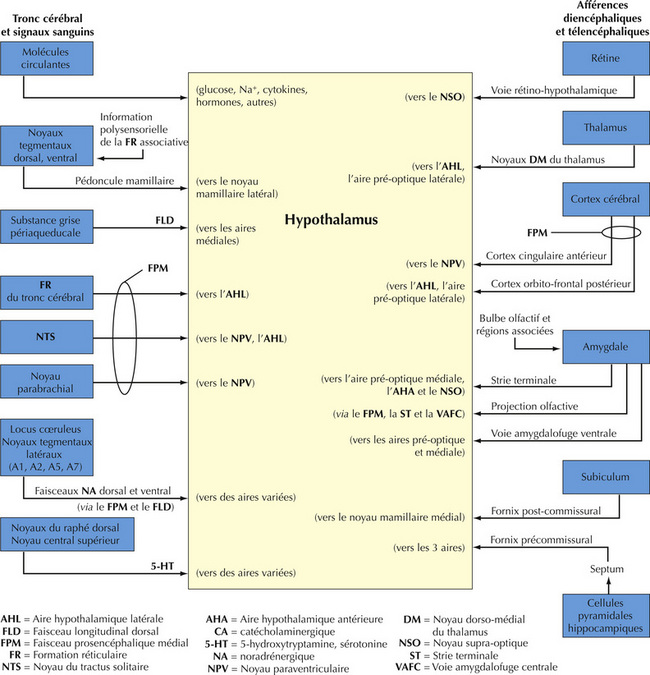
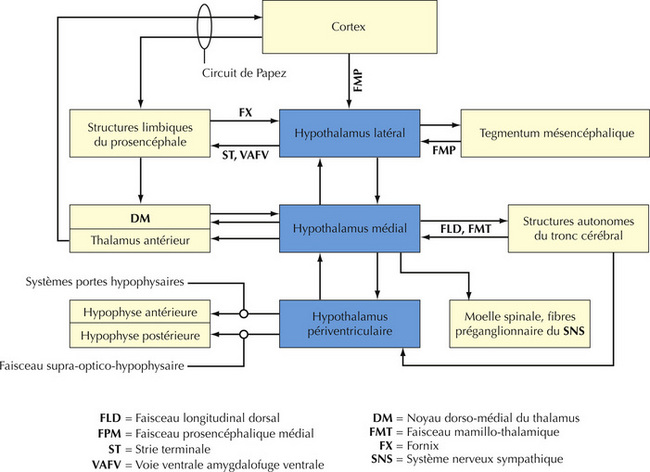
16.11 Résumé des connexions générales hypothalamiques
16.12 Noyau paraventriculaire de l’hypothalamus : régulation de l’activité neurohormonale, autonome préganglionnaire et limbique
16.13 Mécanismes d’action des cytokines sur l’hypothalamus et d’autres régions et sur le comportement
16.14 Organes circumventriculaires
16.15 Circulation portale hypophysaire
16.16 Régulation de la sécrétion hormonale du lobe antérieur de l’hypophyse
16.17 Hormones de la glande hypophysaire (ou pituitaire) postérieure : ocytocine et vasopressine
16.18 Régulation par la vasopressine (hormone antidiurétique, HAD) de l’équilibre hydrique et de l’osmolalité
16.19 Hypothalamus et thermorégulation
16.20 Régulation de la pression sanguine à court terme
16.21 Régulation de la pression sanguine à long terme
16.22 Contrôle nerveux de l’appétit et de la faim
16.23 Rôles neuronal et neuroendocrinien dans les réponses de type « fuite-combat »
Système limbique
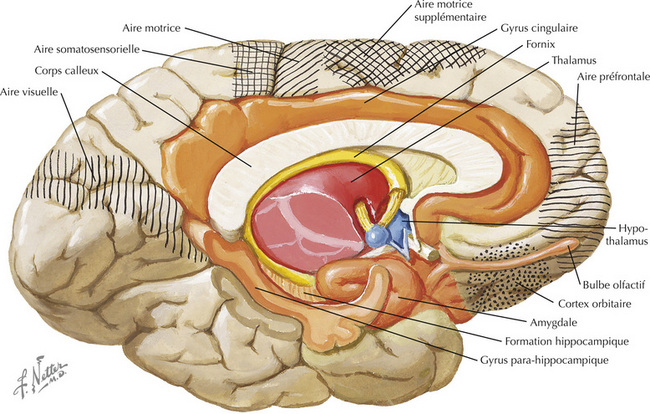
16.25 Anatomie du système limbique
16.26 Formation hippocampique : anatomie générale
16.27 Connexions neuronales à la formation hippocampique
16.28 Principales voies afférentes et efférentes de la formation hippocampique
16.29 Connexions afférentes principales à l’amygdale
16.30 Connexions efférentes principales à l’amygdale
16.31 Résumé des principales voies afférentes et efférentes à l’amygdale
16.32 Principales connexions afférentes et efférentes aux noyaux septaux
Système olfactif
L’hypothalamus, constitué d’un ensemble de noyaux et de faisceaux situés dans le diencéphale ventral, régule les fonctions viscérales autonomes et neuroendocriniennes, en particulier des loges antérieure et postérieure de l’hypophyse. La plupart des noyaux se trouvent à la frontière postérieure (corps mamillaires) et antérieure (lame terminale, commissure antérieure) de l’hypothalamus. Ces noyaux sont divisés en quatre régions principales : préoptique, antérieure (ou supraoptique), tubérale, mamillaire (ou postérieure). Dans le sens médiolatéral (en partant du 3e ventricule), les noyaux sont subdivisés en trois régions : périventriculaire, médiale, latérale. L’hypophyse (ou glande pituitaire) est reliée à la base de l’hypothalamus par I ’éminence médiane et I ’infundibulum (ou tige pituitaire). L’éminence médiane est une zone importante de transduction neuroendocrinienne.
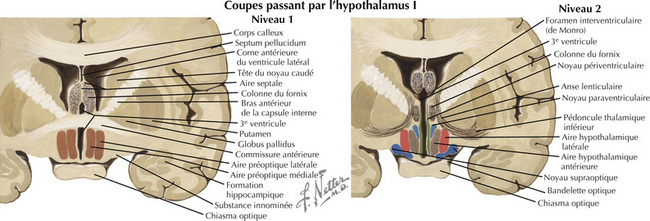
Figure 16.3 Coupes frontales passant par l’hypothalamus –1 et 2 : aires preoptiques et supraoptiques
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree