CHAPITRE 15 VASCULARITES, ANÉVRISMES ET FAUX ANÉVRISMES ARTÉRIELS PULMONAIRES M. El Hajjam, J. Sellier, A. Machet, M. Bensalah, S. Binsse, C. Lagrange, A. Demir, J.-P. Pelage and P. Lacombe En dehors la maladie veineuse thrombo-embolique, les pathologies acquises des vaisseaux pulmonaires sont rares. Les anomalies artérielles élémentaires sont nombreuses et parfois associées : sténoses, occlusions, thromboses, embolies, ané-vrismes et faux anévrismes, s’inscrivant dans des cadres radiocliniques souvent trompeurs. Si les quatre premiers types de lésions artérielles ne posent pas de problème de définition, la distinction entre anévrisme et faux anévrisme est souvent débattue. Un vrai anévrisme pulmonaire correspond à une dilatation de la lumière du vaisseau concerné de 50 % ou plus par rapport au diamètre de référence, calculé à la limite périphérique de la paroi. Ana-tomiquement, les trois tuniques de la paroi vasculaire sont présentes, étirées mais non rompues. Une ectasie répond à la même définition, mais la dilatation de la lumière est inférieure à 50 % par rapport au calibre normal. Un faux ané-vrisme se caractérise par la rupture des trois tuniques, quel que soit le diamètre du vaisseau dans la zone pathologique. Entre ces deux extrêmes, les définitions sont floues, et Marx et al. [47] proposent que lorsqu’une tunique est préservée, généralement l’adventice, le terme d’anévrisme mixte soit retenu. Nous utiliserons ici le terme de faux anévrisme quand une ou plusieurs tuniques artérielles sont rompues – définition communément admise par les chirurgiens – tout en sachant qu’en imagerie, la frontière entre rupture d’une, deux ou trois tuniques vasculaires est imprécise. Les anévrismes des artères pulmonaires sont rares. Dans une revue de la littérature, Navarro et al. [51] signalent 8 cas sur 109 571 autopsies, et 6 cas sur 4 126 anévrismes thoraciques, tous vaisseaux confondus. Parmi tous les anévrismes mycotiques, la localisation pulmonaire a une fréquence de 5,3 %. Une vascularite se définit comme un processus inflammatoire des vaisseaux sanguins qui peut conduire à la destruction des parois vasculaires et à des lésions ischémiques des organes irrigués par ces vaisseaux [69]. En raison de la richesse de son réseau vasculaire, du grand nombre de cellules vasoactives et de sa sensibilité aux agents antigéniques d’origine hématogène ou aérienne, le poumon est fréquemment affecté dans ce groupe hétérogène de vascularites. Même s’il n’existe pas de consensus quant à la classification de ces maladies, on peut schématiquement en distinguer trois groupes : – le groupe des angéites granulomateuses incluant la maladie de Wegener, l’angéite allergique et granulomateuse de Churg et Strauss, la granulomatose sarcoïdosique nécrosante, la granulomatose lymphomatoïde et la granulomatose bronchocentrique ; – le groupe des capillarites avec hémorragie pulmonaire diffuse comme la périartérite noueuse microscopique, le lupus érythémateux systémique et le syndrome de Goodpasture ; – le groupe des vascularites se compliquant d’anévrismes, de sténoses et de faux anévrismes, dominé par la maladie de Takayasu et la maladie de Behçet. Seul ce dernier groupe sera détaillé dans ce chapitre. Décrite à la fin du XIXe siècle, la maladie de Takayasu est une vascularite non spécifique idiopathique touchant principalement les gros vaisseaux, l’aorte, l’artère pulmonaire et leurs branches. Sa distribution est mondiale, mais elle touche de façon préférentielle les pays d’Extrême-Orient, d’Amérique latine puis du Bassin méditerranéen. Sa fréquence est moindre dans les pays occidentaux, estimée à 2,6 cas par million d’habitants dans le Minnesota. Les femmes sont neuf fois plus souvent affectées que les hommes et l’âge moyen de découverte est de 30 ans [37]. L’étiologie de la maladie de Takayasu est inconnue. Son association à certaines affections a fait envisager une origine postinfectieuse (tuberculose, maladies virales) ou auto-immune à médiation cellulaire. Les publications initiales se sont focalisées sur l’atteinte de l’aorte et de ses branches, principalement les troncs supra-aortiques, conduisant à l’appellation de « maladie des femmes sans pouls ». La première description de l’atteinte des artères pulmonaires date de 1940. Cette localisation n’a pas été prise en compte dans la classification artériographique de la maladie établie selon la topographie des lésions. Ce n’est qu’en 1975 que Lupi et al. [45] ont isolé le type IV, caractérisé par l’atteinte artérielle pulmonaire, quelle que soit la topographie des lésions systémiques (fig. 15-1). Fig. 15-1 Maladie de Takayasu avec atteinte synchrone pulmonaire et aortique (type IV). – type I : il correspond à l’atteinte de l’aorte thoracique et de ses branches (subclavières, carotides communes, tronc artériel brachiocéphalique et coronaires) ; – type II : il correspond à l’atteinte de l’aorte abdominale et de ses branches ; – type III : il regroupe les deux premiers types ; – type IV : il définit l’atteinte pulmonaire pour certains auteurs, alors que pour d’autres, il correspond soit à l’atteinte totale de l’aorte et de ses branches, soit à la forme anévrismale systémique de la maladie, c’est-à-dire à la phase athéromateuse tardive [49]. – faire un diagnostic précoce sur des critères cliniques, biologiques et surtout d’imagerie de la paroi des vaisseaux ; tâche difficile car cette affection est considérée comme une des plus trompeuses et son pronostic dépend du délai thérapeutique [37, 83] ; – établir un diagnostic d’évolutivité ou d’activité pour adapter le traitement médical et surtout préciser le moment des thérapeutiques non médicales sur des lésions fixées ; – choisir le mode d’imagerie le moins invasif, c’est-à-dire éviter la ponction vasculaire, pour évaluer l’étendue des lésions systémiques et pulmonaires et choisir la meilleure modalité thérapeutique, chirurgie ou angiographie inter-ventionnelle ; – prendre en charge les complications, dominées par les hémoptysies dans les atteintes pulmonaires. La fréquence des atteintes artérielles pulmonaires est très diversement appréciée : sur des critères cliniques ou d’épreuves fonctionnelles respiratoires, on ne la retrouve que dans 4 à 16 % des cas. Si l’on se réfère à des critères anatomiques ou si l’atteinte pulmonaire est recherchée systématiquement par angiographie numérisée ou par des méthodes isotopiques, cette fréquence s’échelonne entre 14,3 et 86 %, le plus souvent supérieure à 50 % [45, 54, 82]. À la phase active, un épaississement irrégulier de la paroi artérielle affecte principalement la média et l’adventice. Il existe un épaississement réactionnel de l’intima qui a un aspect plissé mais sans modification de la lumière vasculaire. Les secteurs artériels pulmonaires touchés correspondent aux artères élastiques comprenant les troncs proximaux et s’étendant jusqu’aux branches lobulaires. Sur le plan histolo-gique ou immunohistochimique, on constate une infiltration de cellules inflammatoires dans la zone jonctionnelle média-adventitielle constituée de lymphocytes T, de lymphocytes B et de granulocytes. Celle-ci est faite de cellules lymphoplasmocytaires mononucléées ou géantes multinucléées, groupées en granulomes ou réparties de façon diffuse. Il s’y associe une rupture des limitantes élastiques. Une augmentation de calibre des vasa vasorum est souvent constatée, de même qu’une infiltration inflammatoire autour de ces derniers. L’infiltration inflammatoire se prolonge dans l’atmosphère péri-vasculaire cellulograisseuse, et la présence de petites zones de nécrose avec micro-abcès et débris du tissu élastique de la média vient compléter les constatations histologiques. En résumé, les anomalies touchent toutes les tuniques artérielles, détruisent les composantes élastiques et s’accompagnent de lésions de nécrose de la média et de l’adventice. Cependant, il existe une grande variabilité de la composante inflammatoire d’un patient à l’autre [37]. La phase tardive ou occlusive survient des mois, voire des années, après la phase initiale. Le délai moyen séparant les deux phases est inconnu, mais estimé de 1 à 8 ans [49]. Anatomiquement il existe un important amincissement de la média, une rupture constante des limitantes élastiques, un épaissis-sement fibreux marqué de l’adventice et un épaississement intimal régulier, différents de ceux de la maladie veineuse thrombo-embolique. Ces remaniements transmuraux touchent toutes les branches ayant des vasa vasorum, épargnant les artères musculaires. Ils occasionnent des modifications de la lumière circulante : sténoses, occlusions, irrégularités par thrombose et anévrismes. La distinction entre les deux phases repose sur de nombreux critères cliniques, biologiques ou d’imagerie, essentiels pour la prise en charge thérapeutique. Cependant, autant il apparaît possible d’affirmer la notion d’activité de la maladie, autant la non-activité ne peut être que suspectée. Cette constatation est d’ailleurs confirmée dans les faits puisque 45 % des patients présentent des signes d’évolution malgré un traitement bien conduit [82], et 44 % des biopsies chirurgicales vasculaires présentent une juxtaposition de zones actives et inactives même dans des zones fibreuses [32, 54]. Cela renforce l’importance d’une imagerie fonctionnelle illustrant l’activité inflammatoire comme l’imagerie par résonance magnétique (IRM), en particulier les séquences de diffusion, et la tomographie par émission de positons couplée au scanner (TEP-scan). – l’atteinte valvulaire pulmonaire est exceptionnelle, contrastant avec la fréquence de l’atteinte valvulaire aortique ; – l’absence de calcifications artérielles pulmonaires même au stade tardif ; – les sténoses distales sont possibles, souvent associées à des lésions proximales, sources d’hypertension artérielle pulmonaire et d’hémoptysies ; le diagnostic différentiel avec les sténoses congénitales ou les sténoses acquises non inflammatoires s’avère particulièrement difficile (fig. 15-2) [6, 38, 73] ; Fig. 15-2 Maladie de Takayasu avec atteinte artérielle pulmonaire périphérique. – un aspect de « vaisseau dans le vaisseau » a souvent été décrit ; il correspond à une thrombose complète organisée, au sein de laquelle cheminent des néovaisseaux ayant des caractéristiques particulières ; ce sont des artères musculaires avec des couches bien différenciées et dotées de fibres élastiques qui circulent depuis la zone périvasculaire, à travers la paroi artérielle d’origine et la zone thrombosée, jusqu’à la lumière artérielle pulmonaire au-delà de la zone d’occlusion ; il s’agit donc des vasa vasorum pulmonaires alimentés par les artères systémiques thoraciques [37, 52,82] ; – la notion d’artériolite pulmonaire ou d’artérite cellulaire est souvent citée ; certaines observations iraient dans le sens d’une atteinte périphérique spécifique, surtout quand une atteinte proximale concomitante a été constatée [37, 45] ; pour d’autres auteurs, ces anomalies ne seraient que la conséquence de l’hypertension artérielle pulmonaire ; – la dilatation « angiomatoïde » des petits vaisseaux pulmonaires a été rapportée [28, 37, 52]. Son origine est mal connue ; on incrimine l’hypervascularisation systémique de suppléance des lésions obstructives proximales ; une hypertension artérielle pulmonaire pourrait en découler, par maladie veino-occlusive secondaire au développement des capillaires dans toutes les structures parenchymateuses et, en particulier, les septa interlobulaires [36]. Si le diagnostic d’artérite inflammatoire est évoqué, la recherche d’une atteinte pulmonaire est essentielle : sa présence permet d’affirmer le diagnostic de maladie de Takayasu [37]. De même, si les signes thoraciques sont au premier plan (douleurs, hémoptysies, cœur pulmonaire aigu, infarctus pulmonaire), la recherche d’une atteinte systémique facilitera la démarche diagnostique et, surtout, la distinction souvent difficile avec une maladie veineuse thromboembolique (voir fig. 15-1) [27, 30]. Quant aux atteintes artérielles pulmonaires révélatrices de la maladie, Neidhart et al. [52] en ont colligé 33 cas dans la littérature, dont 11 étaient isolées. Il ressort de l’étude de ces observations d’atteinte artérielle pulmonaire que la phase active est mal connue et très peu documentée. La symptomatologie pulmonaire paraît découler plus d’une évolutivité des lésions sténosantes fibreuses d’une phase occlusive jusqu’alors bien compensée, que d’une mauvaise tolérance d’une phase active. La fréquence des hémo-ptysies par développement de la circulation systémique serait un argument en faveur de cette hypothèse. De plus, il ne semble pas exister de facteur géographique ou racial dans l’atteinte pulmonaire, ni de corrélation entre la fréquence des atteintes pulmonaires et celle des artères systé-miques [71]. En revanche, plus une atteinte systémique est sévère, plus elle a de risque d’être associée à une atteinte pulmonaire [82]. La radiographie standard du thorax est considérée comme peu contributive au diagnostic, surtout s’il n’existe pas de signe direct ou indirect d’atteinte systémique : mamelonnement du contour de l’aorte thoracique descendante, calcifications linéaires ou, plus rarement, en motte (plug) de l’aorte et de ses branches, saillie du bouton aortique ou du bord droit de l’aorte ascendante, encoches costales liées à la circulation collatérale intercostale de compensation des obstructions des artères subclavières [49]. Les chiffres très dispersés de sensibilité et de spécificité de la radiographie du thorax dans l’atteinte pulmonaire de la maladie de Takayasu s’accordent mal avec certaines publications où les anomalies paraissent presque constantes [6, 37, 71]. Cependant, un cliché du thorax normal ne permet pas d’exclure le diagnostic. L’aspect des hiles pulmonaires est variable (fig. 15-3 et 15-4). Chaque hile peut être petit ou gros de façon symétrique ou asymétrique. La corrélation avec l’angiographie paraît bonne. Un hile petit ou absent se rencontre dans les sténoses proximales. Un gros hile peut correspondre soit à des anévrismes proximaux ou post-sténotiques, soit à un épaississement de la paroi artérielley pulmonaire sans anévrisme, soit aux deux à la fois. De plus, un gros hile peut être lié à une redistribution du flux au profit du côté le moins atteint ou à une hypertension artérielle pulmonaire. Dans ce dernier cas, on s’attachera à rechercher des signes d’hypertrophie du ventricule droit de face ou de profil. Fig. 15-3 Maladie de Takayasu de type IV. Fig. 15-4 Maladie de Takayasu de type IV. Sur la radiographie standard, le hile droit était petit et une redistribution vasculaire vers la gauche était constatée. Le parenchyme pulmonaire peut être le siège d’anomalies traduisant une ischémie : réduction de volume avec ascension d’une coupole diaphragmatique, opacité mal limitée d’un infarctus, excavation prédominant aux lobes supérieurs, parfois surinfectée (fig. 15-5). L’épaississement des scissures est très fréquent et les épanchements pleuraux plus rares. La silhouette cardiaque peut avoir l’aspect d’une cardiopathie valvulaire aortique ou hypertensive. L’ensemble de ces anomalies contribue à orienter vers une maladie veineuse thrombo-embolique. Fig. 15-5 Maladie de Takayasu révélée par l’atteinte pulmonaire. L’échographie-Doppler superficielle, endovasculaire ou transœsophagienne a été utilisée dans la maladie de Takayasu [41, 71]. Cet examen permet d’éliminer une thrombose veineuse profonde, d’attirer l’attention sur les artères systémiques dont les tuniques sont épaissies (troncs supra-aortiques) ou sur l’orifice aortique siège possible d’une régurgitation diastolique, et ainsi d’attribuer une obstruction artérielle pulmonaire à une artérite inflammatoire. – faire un diagnostic non invasif de lésion artérielle pulmonaire aussi bien à la phase aiguë qu’à la phase occlusive, avec peu de faux négatifs ; – détecter les signes d’activité et d’évolutivité, éléments déterminants pour la mise en route du traitement corticoïde et immunosuppresseur et critère essentiel pour fixer le moment du traitement non médical [28, 54]. Plusieurs travaux illustrent l’efficacité de ces méthodes isotopiques dans le diagnostic d’activité, la réponse au traitement et la récidive [54, 74]. Ces progrès sont similaires à ceux de l’angio-tomodensitométrie (angio-TDM) et de l’IRM. La TDM hélicoïdale multicoupes joue actuellement un rôle déterminant dans l’appréciation des anomalies murales systé-miques et pulmonaires pour le diagnostic à la phase initiale de la maladie et un rôle potentiel pour le diagnostic d’activité [11, 57]. Avant injection, les parois vasculaires sont identifiables car épaissies, d’une densité spontanée égale ou supérieure à celle du muscle (47 à 82 UH – unités Hounsfield), voire calcifiées pour les artères systémiques, contrastant avec une lumière vasculaire hypodense en raison de l’anémie. En angio-TDM apparaît à la phase vasculaire précoce un rehaussement pariétal inhomogène donnant une image en « double anneau », bien connue pour l’aorte, à notre connaissance non rapportée pour l’artère pulmonaire : l’anneau interne hypodense contraste avec le rehaussement intense de la lumière vasculaire. Il correspondrait à l’épaississement de l’intima ; l’anneau externe hyperdense serait lié à une prise de contraste des zones média-adventicielles et des vasa vasorum dilatés. La limite périphérique de l’anneau externe est imprécise en raison de la prise de contraste de l’atmosphère cellulograisseuse périvasculaire. L’épaississement est supérieur ou égal à 3 mm, pouvant atteindre 7 à 8 mm au maximum. Il se détecte plus facilement dans la zone de contact entre la face postéro-gauche de l’aorte ascendante et antéro-droite du tronc de l’artère pulmonaire. Il peut être annulaire ou semi-lunaire. La prise de contraste pariétale est plutôt tardive et persiste de longues minutes. Elle peut passer facilement inaperçue sur une phase artérielle pulmonaire précoce, d’où la nécessité de réaliser une acquisition tardive car l’image du « double anneau » se renforce dans le temps. Ces anomalies étaient présentes six fois sur huit dans la série de Park et al. [57]. Les anomalies pulmonaires ne se limitent pas à un épaississe-ment pariétal artériel avec retentissement sur les lumières : sténoses, occlusions et plus rarement anévrismes (voir fig. 15-1 et fig. 15-6). En effet, on retrouve également les signes en faveur d’une ischémie parenchymateuse (infarctus parfois excavé ou réaction pleurale), d’une hypertension artérielle pulmonaire (diamètre du tronc de l’artère pulmonaire supérieur à 29 mm, hypertrophie ou dilatation des cavités cardiaques droites) ou du développement de la circulation systémique bronchique et non bronchique, conséquences des sténoses artérielles pulmonaires. Les anomalies vasculaires seront détaillées dans le paragraphe consacré à l’angiographie. Rappelons la possibilité d’adénomégalies médiastinales et l’absence d’argument en faveur d’une fibrose médiastinale ou d’une tumeur. Fig. 15-6 Maladie de Takayasu avec hémoptysie massive. Angiographie interventionnelle pulmonaire et systémique. Au niveau parenchymateux ont été décrites des « images en mosaïque » avec un contraste entre des zones hypodenses correspondant aux territoires atteints où les artères sont sté-nosées, contrastant avec un parenchyme normal hyperdense à cause de la redistribution vasculaire. De plus, une observation originale de micronodules centrolobulaires diffus, secondaires à une distension des vaisseaux périphériques par l’hypervascularisation systémique de compensation a été publiée par Hara et al. [28]. Si la place du scanner est essentielle dans le diagnostic positif et le bilan d’extension de la maladie, elle reste à confirmer dans le diagnostic d’activité [68]. L’examen comporte des séquences rapides en FSE T1 avec ou sans saturation de la graisse, avant et après injection de chélate de gadolinium. Des acquisitions sont pratiquées aux temps artériel, veineux, puis à 5, 10 et 15 minutes après l’injection du produit de contraste [32, 84]. Les séquences de diffusion deviennent systématiques et permettent d’évaluer avant et après traitement l’activité de l’atteinte pariétale par l’intensité du signal et la valeur du coefficient apparent de diffusion. Six types d’épaississement de la paroi des vaisseaux ont été décrits par Hoe et al. [32] selon sa topographie au sein de la paroi vasculaire (intima, média ou adventice) et la prise de contraste dans ou autour de l’artère. Un épaississement de 3 à 7 mm concentrique ou en croissant est détectable ; il est en moyenne plus important dans la phase active (de 5 à 7 mm). Dans 30,8 % des cas, l’intima est seule concernée, dans 53,8 % l’intima et la média sont clairement distinctes, et dans 38,5 % l’intima et la média ne sont pas dissociables. La détection d’un épaississement dans la zone de contact entre l’aorte et l’artère pulmonaire revêt une grande importance pour le diagnostic étiologique de vascularite. Si le signal de la paroi vasculaire ou son rehaussement précoce est supérieur ou égal à celui du myocarde, la maladie est considérée comme active ; la corrélation est meilleure avec la vitesse de sédimentation, qu’avec les données cliniques et la protéine C réactive. Pour le diagnostic positif, les chiffres de sensibilité et de spécificité de l’IRM sont bons : ils sont de 100 % par rapport à l’angiographie dans la série de 20 malades rapportée par Yamada et al. [84]. Ces chiffres doivent cependant être relativisés puisque la méconnaissance des lésions murales par l’angiographie est connue. L’utilisation récente d’un produit de contraste strictement intravasculaire comme le gadofosveset trisodium augmente les performances de l’IRM pour différencier une maladie active d’une forme inactive. Ce produit est capté par les vasa vasorum, ce qui rehausse de façon significative le signal de la paroi vasculaire en cas d’activité [56]. L’angiographie numérisée couplée à l’hémodynamique permet la description des lésions spécifiques artérielles pulmonaires (fig. 15-7) [43, 48, 82]. Cependant, ces descriptions se réfèrent presque exclusivement à la phase inactive et rares sont les corrélations angiographie-phase active puisque à cette phase le bilan est réalisé de façon non invasive. Fig. 15-7 Maladie de Takayasu avec atteinte pulmonaire (type IV). Signes directs: Les signes angiographiques directs sont les sténoses, les occlusions, les anévrismes, l’épaississement des parois et les irrégularités des bords. Les sténoses sont longues, proximales classiquement régulières, prédominant à l’étage segmentaire, puis lobaire, tronculaire et, plus rarement, sous-segmentaire. En cas de sténose courte proximale tronculaire, le diagnostic avec les sténoses ou coarctations congénitales est difficile [73]. Si les lésions sont distales, on peut rencontrer un aspect en « arbre mort » et une hypoperfusion parenchymateuse (voir fig. 15-2). L’atteinte bilatérale est plus fréquente, le côté droit plus souvent touché, les lobes supérieurs plus que les lobes inférieurs. À ce titre, la distribution des lésions est différente de celle de la maladie veineuse thrombo-embolique. Dans les sténoses serrées, des thromboses endoluminales surajoutées contribuent à donner un aspect irrégulier des bords artériels. Les occlusions sont souvent proximales abruptes ou en « flamme de bougie ». Les anévrismes sont rares. Souvent post-sténotiques, ils peuvent être isolés, semblables aux faux anévrismes de la maladie de Behçet, comme dans la troisième observation rapportée par Kerr et al. [37]. La distance entre la lumière circulante de l’artère pulmonaire et le bord du hile souligné par l’air intrapulmonaire permet d’évaluer indirectement l’épaisseur de la paroi. Il n’est pas rare d’avoir un gros hile sur la radiographie standard et une sténose artérielle à l’angiographie. Signes indirects: Lupi et al. [45] ont insisté sur les signes indirects comprenant des flux asymétriques ou des retards d’opacification aux bases. Ils soulignent également que l’angiographie est précise pour la détection des lésions distales, alors que les mesures de pressions à la recherche de gradients sont plus sensibles que l’angiographie pour les lésions proximales. Comme nous l’avons déjà souligné, la coexistence d’une atteinte aortique et pulmonaire est d’une grande importance diagnostique. Nous insisterons sur les conséquences broncho-systémiques des lésions pulmonaires. La gravité de certaines formes pulmonaires de maladie de Takayasu découle soit de l’ischémie pulmonaire, soit du cœur pulmonaire aigu consécutif aux sténoses ou occlusions, soit des hémoptysies [6]. Les formes ischémiques pourraient être la conséquence d’une phase active aiguë, avant que la circulation de suppléance sys-témique ait pu s’installer. Plus tardivement dans le cours de la maladie, les hémoptysies sont la conséquence de la reprise en charge progressive de la circulation fonctionnelle par les artères à haute pression provenant de l’aorte. Tous les pédicules systémiques peuvent participer à cette suppléance, surtout s’il existe des adhérences pleurales secondaires à un infarctus. Une des particularités de la maladie de Takayasu est d’impliquer des rameaux provenant des artères coronaires. Cette participation coronarienne serait favorisée par une atteinte extensive de l’aorte thoracique avec obstruction des artères bronchiques. Sur 2 922 coronarographies, Matsunaga et al. [50] ont retrouvé 16 cas de shunts coronaropulmonaires chez des patients présentant presque tous (15/16) des anomalies scintigraphiques pulmonaires, et dont la moitié concernait des patients atteints de maladie de Takayasu. Les shunts étaient alimentés par les branches atriales gauches de l’artère circonflexe ou sino-auriculaires de la coronaire droite. Ces anastomoses existent anatomiquement dans les zones non couvertes par le péricarde ; elles cheminent autour de la zone d’abouchement des veines pulmonaires dans l’atrium gauche. Vers le poumon, elles débouchent dans les vasa vaso-rum et au niveau précapillaire. Nous avons rapporté une observation originale d’hémoptysie massive liée à une hypervascularisation systémique alimentée par une branche de l’artère coronaire droite. Un double traitement par angioplastie de l’artère pulmonaire droite et embolisation sélective du rameau coronarien alimentant le shunt systémopulmonaire a permis un bon résultat à long terme sans récidive de l’hémoptysie (voir fig. 15-6). La rareté de la maladie dans les pays occidentaux ajoute aux difficultés diagnostiques des atteintes artérielles de la maladie de Takayasu : celles-ci s’illustrent, en effet, par le fait que la grande majorité des patients ayant une symptomatologie thoracique au premier plan sont traités comme des maladies veineuses thrombo-emboliques, malgré la normalité de l’écho-Doppler veineux des membres inférieurs. La scintigraphie pulmonaire ne fait que renforcer cette conviction. Il s’agit, de fait, d’une présentation clinique inversée par rapport à la forme systémique classique. La présence de l’anémie et le syndrome inflammatoire biologique dans un tableau de maladie de système doivent inciter à la recherche de signes artériels. Le diagnostic n’est parfois rectifié que des années plus tard quand les signes systémiques s’installent et que la phase occlusive est patente. Les autres diagnostics sont les fibroses médiastinales, les compressions extrinsèques, les tumeurs primitives sarcomateuses de l’artère pulmonaire et les sténoses congénitales ou acquises idiopathiques (fig. 15-8). Fig. 15-8 Maladie veineuse thrombo-embolique avec occlusion ostiale de l’artère pulmonaire droite. Insuffisance cardiaque droite sévère. À la phase active, le traitement est médical, reposant sur la corticothérapie. Une rémission est obtenue dans 40 à 60 % des cas. En cas d’échec, on peut avoir recours au cyclophos-phamide, à l’azathioprine ou au méthotrexate [52]. Vingt pour cent des patients résistent au traitement. Dans ces formes réfractaires ou récidivantes, les biothérapies semblent donner de bons résultats cliniques et sérologiques, notamment le traitement par le tocilizumab qui est un anticorps monoclonal humanisé qui bloque l’action des récepteurs de l’interleukine-6 [77]. Dans les atteintes pulmonaires, il est fréquent de constater l’inefficacité du traitement sur les signes droits. Contrairement aux sténoses non inflammatoires où l’efficacité des techniques d’angioplastie a été démontrée, l’expérience est presque inexistante dans les atteintes pulmonaires de la maladie de Takayasu [6, 38]. En revanche, la chirurgie est efficace avec de bons résultats à long terme [73]. La présence d’une rétinopathie, d’une hypertension artérielle, d’une insuffisance aortique ou d’anévrismes assombrit le pronostic [4]. Sur les 33 cas d’atteinte pulmonaire répertoriés par Neidhart et al. [52], 3 décès ont été rapportés. La maladie de Behçet est une affection inflammatoire systé-mique chronique d’étiologie inconnue évoluant par poussées [16]. Initialement décrite comme une triade comprenant des ulcérations aphtoïdes buccales et génitales associées à une uvéite, cette affection se manifeste également par des lésions cutanées, articulaires, vasculaires, pulmonaires, cérébrales, digestives et urogénitales ayant une vascularite comme substratum anatomopathologique commun. Sa distribution est mondiale, mais sa prévalence est plus marquée le long de l’ancienne route de la soie depuis le Bassin méditerranéen et le Moyen-Orient jusqu’à l’est de l’Asie. Les chiffres de prévalence pour 100 000 habitants s’échelonnent de 80 à 370 cas en Turquie, à 30 cas dans les autres pays d’Asie et moins encore dans les pays occidentaux et les États-Unis. La prépondérance masculine est nette dans les formes d’apparition précoce (avant 25 ans) ou en cas d’atteinte cardiovasculaire ; elle a une incidence pronostique péjorative. La répartition par sexe est équilibrée. La pathogénie est mal connue, mais plusieurs constatations de laboratoire sont en faveur de mécanismes immunologiques induits par des agents microbiens (virus de l’Herpès simplex, streptocoques) chez des individus ayant une susceptibilité génétique particulière. L’importante influence génétique est confortée par la positivité au HLA-B51 et le risque majoré au sein d’une même famille. L’hypersécrétion de cytokines (interleukine-2 et interféron), l’accroissement du chimiotactisme des neutrophiles et le rôle central de la réponse immunitaire à cellules T sont d’autres éléments pathogéniques essentiels [16]. Un épaississement intimal des artères élastiques proxi-males est souvent constaté. La formation de thrombus endo-luminal vasculaire, pulmonaire ou cardiaque est possible au contact de zones d’inflammation lymphocytaire de l’intima ou de l’endocarde (fig. 15-9) [75]. En raison de l’évolution par poussées, la juxtaposition de lésions d’âges différents est fréquente : infiltrat inflammatoire, fibrose des parois vasculaires ou de l’endocarde ou thrombus reperméabilisé. Fig. 15-9 Maladie de Behçet avec anévrismes artériels pulmonaires et hémoptysie.
VASCULARITES PULMONAIRES
Maladie de Takayasu
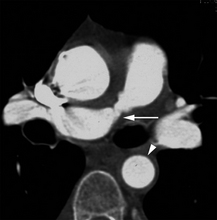
Angio-TDM montrant une sténose tronculaire de l’artère pulmonaire droite (flèche). L’épaississement de la paroi aortique (tête de flèche) permet de rattacher la sténose artérielle pulmonaire à la maladie de Takayasu.
Anatomie pathologique
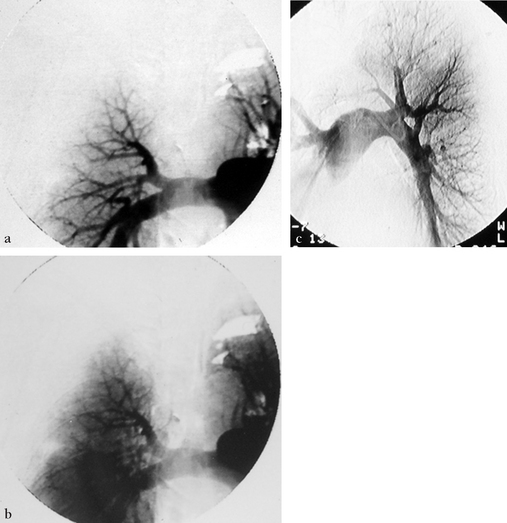
(a) Angiographie numérisée de face centrée sur le champ pulmonaire droit : temps précoce. Réduction de calibre des branches segmentates du lobe supérieur droit. (b) Temps tardif : hypovascularisation pulmonaire dans les territoires correspondants. (c) Angiographie pulmonaire sélective gauche (autre patient) : sténoses irrégulières des artères segmentaires du culmen.
Clinique et biologie
Imagerie
Radiographie du thorax
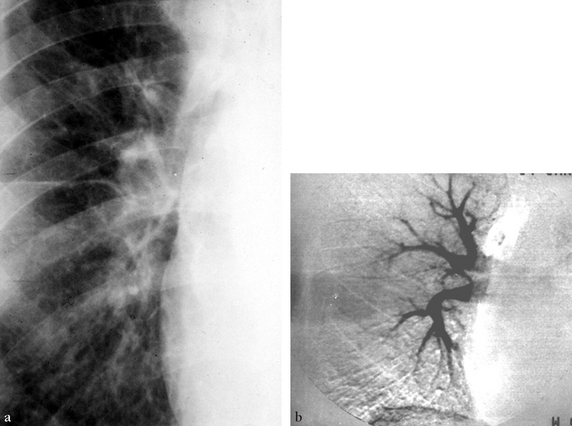
(a) Radiographie standard centrée sur le hile droit. Les limites du hile sont imprécises et les arborisations vasculaires grêles. (b) Correspondance angiographique. Les sténoses pulmonaires intéressent toutes les artères proximales.
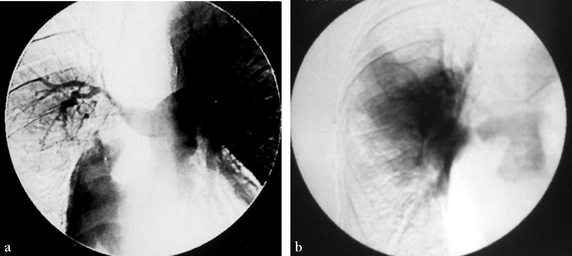
(a) Angiographie pulmonaire numérisée. Occlusion subtotale de l’artère pulmonaire droite et de ses branches. (b) Temps tardif où la parenchymographie se limite à la portion périhilaire.
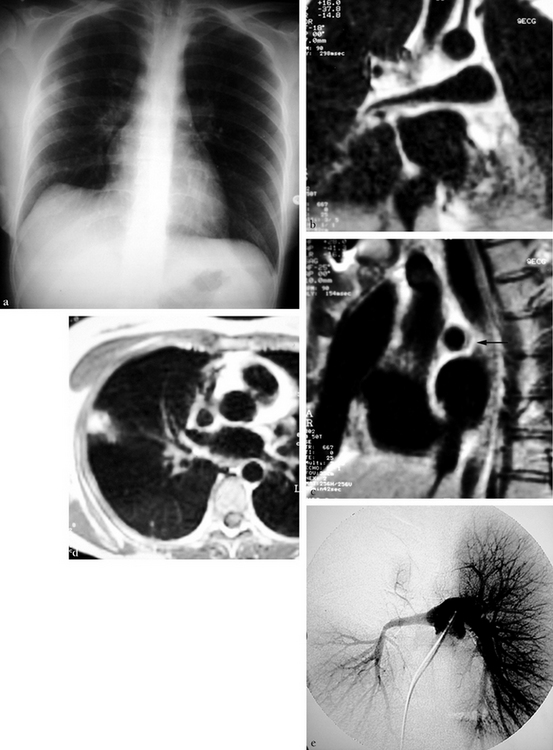
(a) Radiographie thoracique de face montrant une opacité axillaire droite et une surélévation de la coupole diaphragmatique homolatérale. (b) IRM frontale en SE T1 montrant un épaississement de la paroi de l’artère pulmonaire droite et une réduction progressive de son calibre. (c) IRM sagittale en SE T1 : l’épaississement de la paroi de l’artère pulmonaire droite est asymétrique, en hyposignal semi-lunaire (flèche). (d) IRM axiale en SE T1 : hypersignal périphérique sous-pleural compatible avec un infarctus pulmonaire. (e) Angiographie pulmonaire numérisée : sténose régulière longue et significative de l’artère pulmonaire droite avec hypovascularisation périphérique.
Échographie-Doppler
Examens isotopiques
Angio-tomodensitométrie
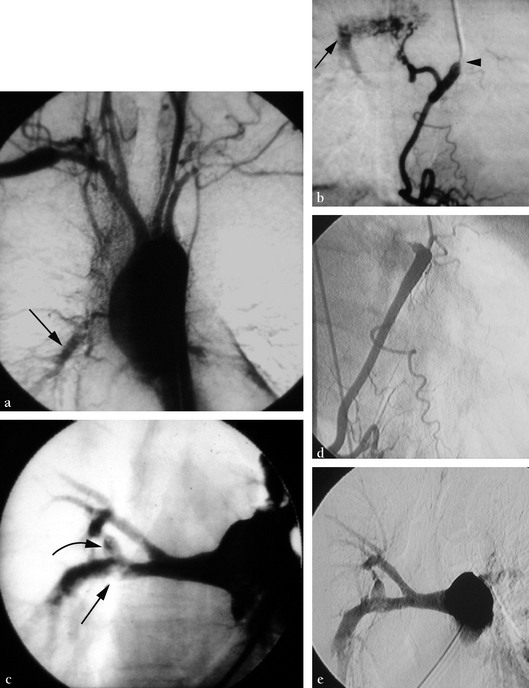
(a) Aortographie de face numérisée. Les sténoses des troncs supra-aortiques sont visibles. On constate l’opacification précoce de l’artère pulmonaire droite, témoignant d’un shunt systémopulmonaire sur une vraisemblable lésion de type IV (flèche). (b) L’opacification de l’artère coronaire droite en oblique antérieure droite permet de découvrir la présence d’un rameau atrial hypertrophié alimentant le shunt systémopulmonaire. L’artère pulmonaire droite apparaît dans sa portion terminale (flèche). À noter une sténose spécifique ostiale de la coronaire droite (tête de flèche). (c) L’angiographie pulmonaire droite confirme les sténoses tronculaires et lobaires dont une est serrée (flèche) et un anévrisme sur une de ses branches (flèche courbe). Une angioplastie de l’artère pulmonaire droite est pratiquée, complétée par une embolisation du rameau atrial, permettant la disparition des hémoptysies. (d,e) Contrôles à 14 ans montrant la disparition du rameau atrial de la coronaire droite (d) et le bon résultat sur l’artère pulmonaire droite où l’anévrisme est inchangé (e).
IRM
Angiographie pulmonaire
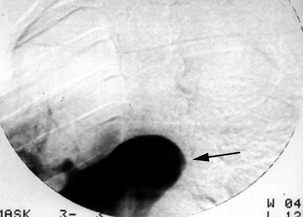
Angiographie numérisée par injection périphérique en oblique antérieure gauche montrant une occlusion complète de l’artère pulmonaire gauche (flèche) et de l’artère médiastinale du lobe supérieur droit.
Diagnostic différentiel
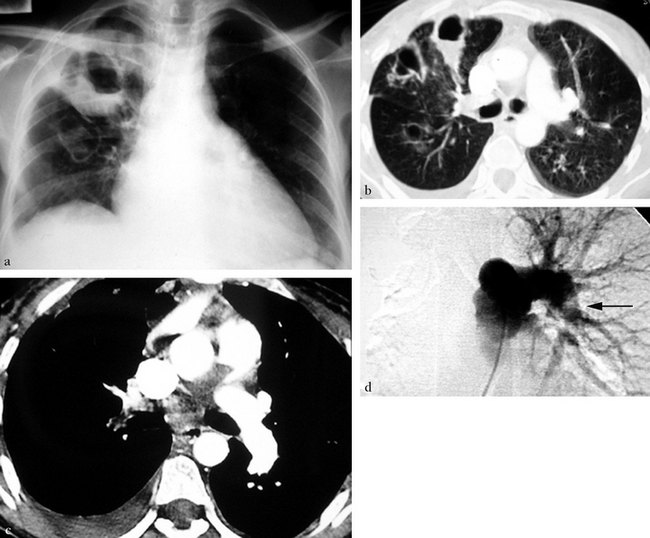
(a) Pneumopathie excavée du lobe supérieur droit, séquelle d’un infarctus pulmonaire. (b) Image TDM de la suppuration pulmonaire. (c) Angio- TDM montrant l’obstruction de l’artère pulmonaire droite. (d) Angiographie pulmonaire globale confirmant l’occlusion de l’artère pulmonaire droite à son origine. Le diagnostic d’embolie pulmonaire cruorique a été confirmé par une biopsie intra-artérielle pulmonaire d’une lésion lacunaire endoluminale (flèche).
Traitement
Maladie de Behçet
Anatomie pathologique
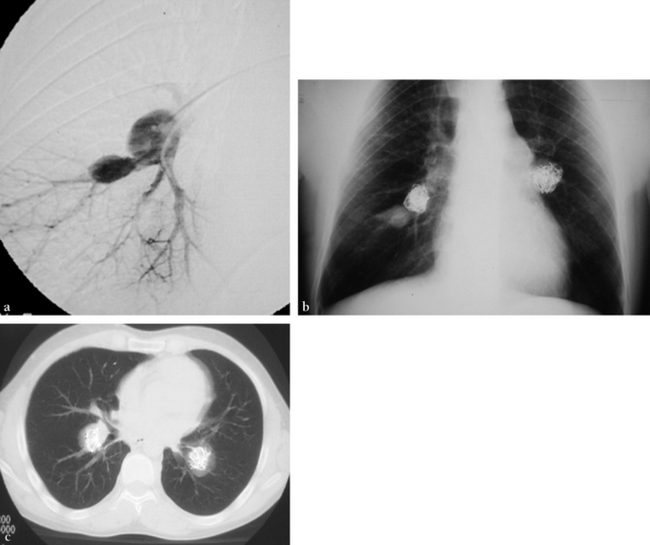
(a) Angiographie pulmonaire droite hypersélective lobaire moyenne montrant deux anévrismes distincts et des images de thrombose périphérique témoignant de la vascularite pulmonaire. Embolisation des anévrismes par spirales métalliques. (b) Radiographie standard de contrôle. (c) Contrôle TDM après embolisation.![]()
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree


15: VASCULARITES, ANÉVRISMES ET FAUX ANÉVRISMES ARTÉRIELS PULMONAIRES






