Chapitre 8 Scanner des artères coronaires
Comme il analyse à la fois le luminogramme artériel mais aussi le remodelage pariétal et la densité de la plaque, le coroscanner présente un intérêt grandissant dans l’évaluation préthérapeutique des coronaropathies. En effet, le dépistage des lésions coronariennes à risque repose sur la détection des rétrécissements significatifs du luminogramme, mais aussi sur la nature lipidique de la plaque, sa localisation sur l’arbre coronarien et l’importance des dégâts engendrés en amont par une rupture de plaque. Moins invasif que la coronarographie, le coroscanner permet également de suivre les patients stentés ou pontés. Ainsi, les équipes cardiologiques substituent de plus en plus fréquemment un coroscanner à la classique coronarographie de contrôle réalisée 6 mois après un stenting du tronc commun. Les pontages sont également parfaitement visibles quelle que soit la technique chirurgicale utilisée, et le coroscanner est un outil très performant pour affirmer leur perméabilité et étudier leur développement.
Lésions non athéromateuses
Anomalie d’implantation
Exceptionnellement, l’artère coronaire gauche (ou l’IVA) peut naître directement du tronc de l’artère pulmonaire (fig. 8.3, ![]()
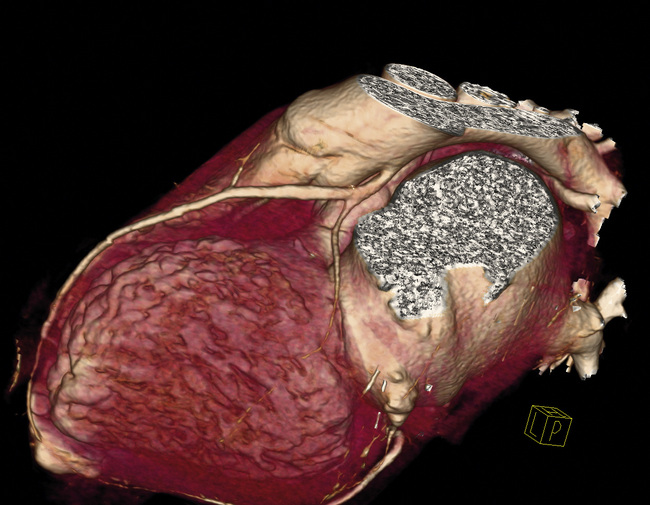
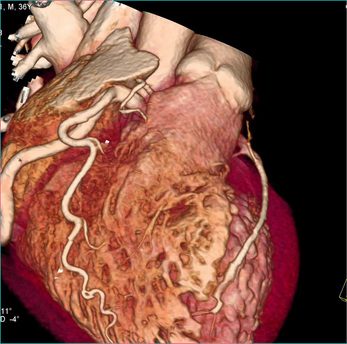
Les reconstructions VRT montrent une naissance aberrante d’une IVA de large calibre depuis la face postérieure de l’artère pulmonaire, alors que la CX et la droite naissent en position anatomique. Ce patient a bénéficié d’une réimplantation de l’IVA (![]() vidéo 8.1).
vidéo 8.1).
Reproduit avec l’autorisation de Daniel Colombier, clinique Pasteur, Toulouse.
). Dans la littérature anglo-saxonne, cette anomalie est décrite sous l’acronyme ALCAPA (anomalous left coronary artery from the pulmonary artery). Cette variante, habituellement isolée, est rare, avec une incidence estimée à 1/300 000 nouveau-nés. Elle se révèle dans la période néonatale par un tableau d’ischémie myocardique. En effet, la diminution des pressions artérielles pulmonaires après la fermeture du canal artériel va entraîner un hypodébit, voire un vol coronarien. Néanmoins, certaines formes paucisymptomatiques ne sont découvertes qu’à l’âge adulte.
Fistule
La communication entre une artère coronaire et une autre structure vasculaire est la variante coronarienne la plus fréquente. Fréquemment, ces anomalies sont totalement asymptomatiques et leur incidence croît donc avec les possibilités de découverte fortuite par coroscanner. L’artère nourricière est dans 50 % des cas la coronaire droite, dans 30 % l’IVA et dans 20 % la CX. La fistule entraîne une dilatation et un aspect tortueux du vaisseau. Plus l’orifice de naissance est proximal sur le réseau coronarien, plus la dilatation de la fistule sera importante. Dans certains cas, il existe même des portions anévrismales (fig. 8.4). Dans 90 % des cas, cette fistule se draine dans les cavités droites, avec par ordre de fréquence le ventricule droit, l’oreillette droite, le sinus coronarien et enfin l’artère pulmonaire. Elles peuvent être alimentées par un ou plusieurs vaisseaux coronaires (fig. 8.5, ![]()
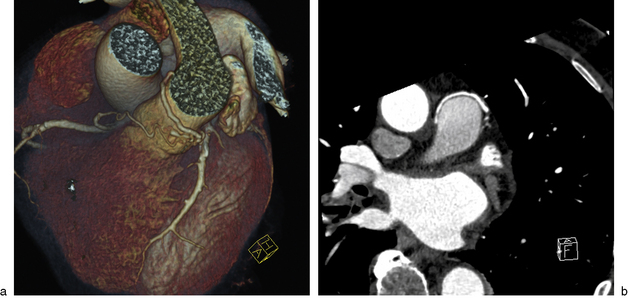
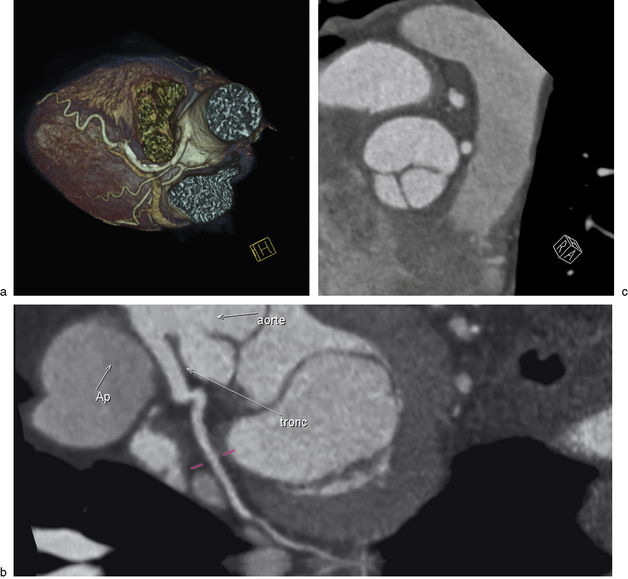
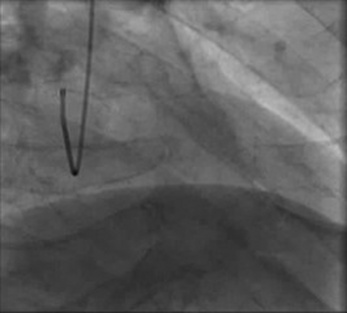
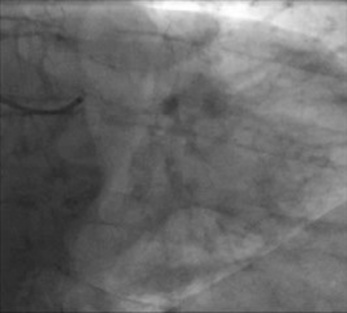
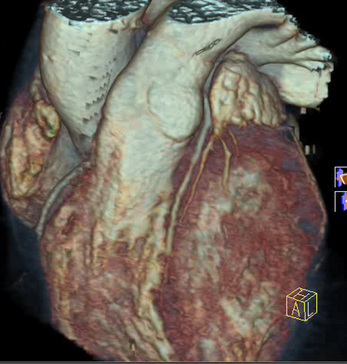
Fig. 8-5 Homme de 64 ans présentant une dyspnée à l’effort.
a. La vue tridimensionnelle du coroscanner découvre une fistule alimentée à la fois par la coronaire droite, mais aussi par des branches de L’IVA. b. Cette fistule précroise le tronc de l’artère pulmonaire. Elle s’abouche dans le tronc de l’artère pulmonaire (![]() vidéo 8.2).
vidéo 8.2).
Reproduit avec l’autorisation de Nicolas Combes, clinique Pasteur, Toulouse.
).
Les fistules coronariennes/artérielles systémiques sont un cas particulier. Elles font communiquer une artère coronaire avec une artère systémique médiastinale : bronchique, péricardique ou diaphragmatique. À la différence des autres fistules, elles sont acquises ou développées par des conditions pathologiques où un recrutement artériel local est provoqué par une inflammation chronique. Ainsi, l’évolution de bronchectasies (séquellaires de tuberculose, par exemple) entraîne une hyperartérialisation systémique pulmonaire et le recrutement d’anastomoses coronariennes/systémiques. Dans de rares cas, ces fistules peuvent être responsables d’un vol coronarien, notamment à l’effort (fig. 8.6, ![]()
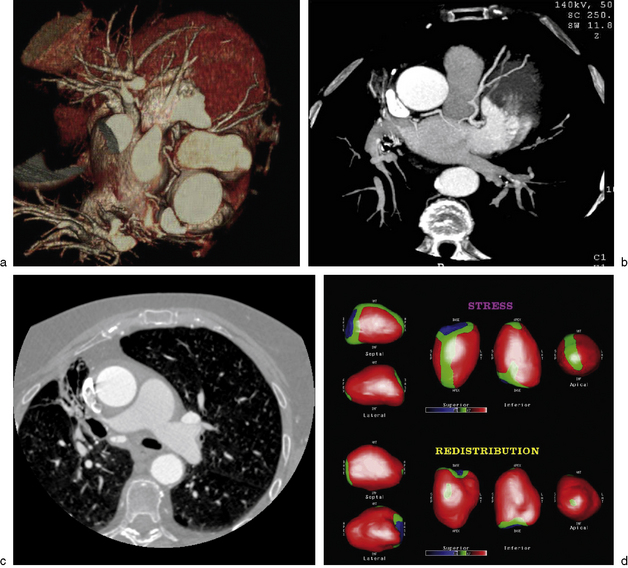
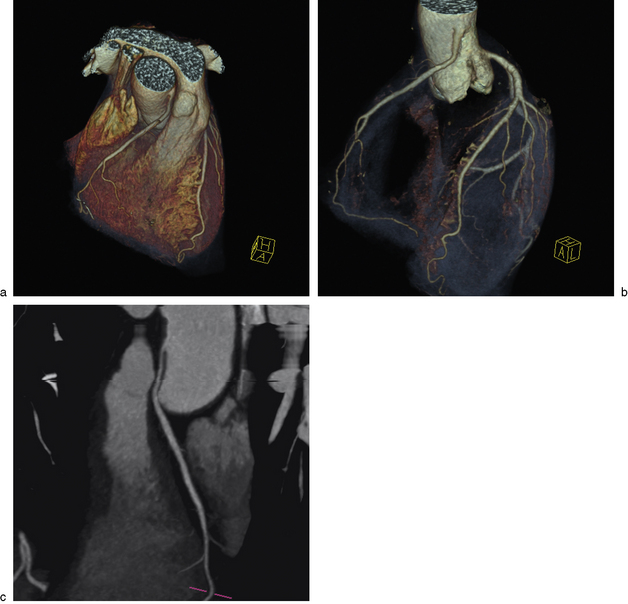
a,b. Le rendu 3D du coroscanner met en évidence un fin vaisseau tortueux naissant depuis la CX proximale puis cheminant derrière le tronc de l’artère pulmonaire vers le hile pulmonaire droit. c. Il existe un important foyer de bronchectasie lobaire moyen avec des remaniements parenchymateux d’aspect séquellaire chronique (![]() vidéo 8.3). La coronarographie de contrôle confirme la naissance d’un vaisseau artériel depuis la CX, vascularisant le foyer de bronchectasie par de fines anastomoses artérielles avec la vascularisation artérielle systémique bronchique. d. Une scintigraphie myocardique (reproduite avec l’autorisation de Nicolas Fourquet, clinique Pasteur, Toulouse) objective une hypoperfusion dans le territoire IVA à l’effort, réversible au repos. Ces anomalies peuvent s’expliquer par un vol coronarien IVA à l’effort causé par l’hyperartérialisation bronchique.
vidéo 8.3). La coronarographie de contrôle confirme la naissance d’un vaisseau artériel depuis la CX, vascularisant le foyer de bronchectasie par de fines anastomoses artérielles avec la vascularisation artérielle systémique bronchique. d. Une scintigraphie myocardique (reproduite avec l’autorisation de Nicolas Fourquet, clinique Pasteur, Toulouse) objective une hypoperfusion dans le territoire IVA à l’effort, réversible au repos. Ces anomalies peuvent s’expliquer par un vol coronarien IVA à l’effort causé par l’hyperartérialisation bronchique.
). Cette communication peut également être responsable d’infarctus pulmonaire lors d’embolisation thérapeutique bronchique pour hémoptysie [1,4].
Anévrisme
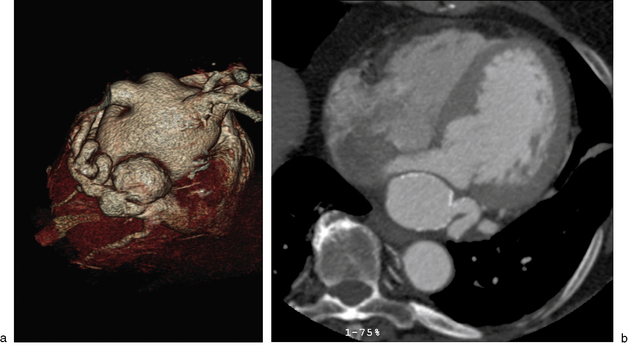
Le diamètre moyen du tronc commun est de 5 mm, puis les artères diminuent régulièrement de diamètre vers la distalité. Un anévrisme peut compliquer l’évolution de la maladie athéromateuse (fig. 8.7). Il peut également être causé par une maladie inflammatoire comme dans la maladie de Takayasu, par une anomalie du tissu élastique (Ehler-Danhlos ou Marfan), ou compliquer l’évolution d’une vascularite infectieuse (Kawasaki post-streptococcique ou aortite syphilitique). Enfin, il peut révéler un hyperdébit causé par une fistule coronarienne. Le plus souvent asymptomatiques, les anévrismes peuvent être responsables d’embolisation distale ou d’hémopéricarde par fissuration ou rupture.
Pont intramyocardique
Les artères coronaires cheminent à la face épicardique du myocarde. Parfois, un segment artériel peut cheminer dans le myocarde, réalisant un pont intramyocardique. Dans ce cas, toute la circonférence du segment artériel est entourée de fibre musculaire myocardique (fig. 8.8). La contraction systolique du myocarde peut entraîner une réduction de calibre de la coronaire qui reprendra son calibre habituel en diastole (![]()
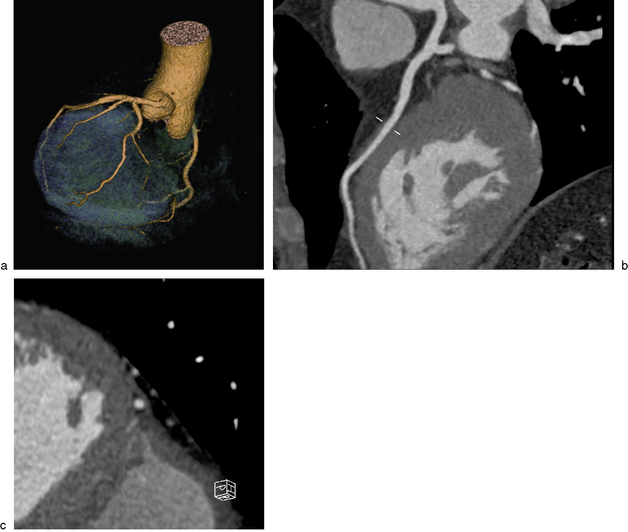
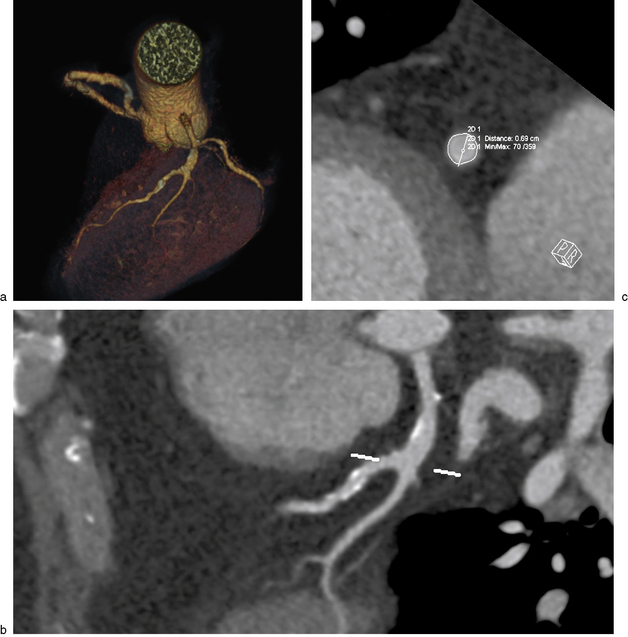
Fig. 8-8 Homme de 58 ans présentant une douleur thoracique atypique et un bloc de branche gauche.
a. La vue 3D retrouve un réseau coronaire globalement sain avec un aspect rectiligne du deuxième segment de l’IVA. b. Ce segment rectiligne correspond à un passage intramyocardique à la face superficielle du ventricule gauche. c. Le muscle myocardique engaine toute la circonférence de l’artère sur les coupes petit axe (![]() vidéo 8.4).
vidéo 8.4).
). La prévalence de cette anomalie dans une population standard est estimée à 1–2 %. Elle est exceptionnellement symptomatique [2].