8 Développement du Système Nerveux
8.1 Formation de la plaque neurale, du tube neural et de la crête neurale
8.3 Développement du tube neural et formation de la crête neurale
8.4 Développement des axones périphériques
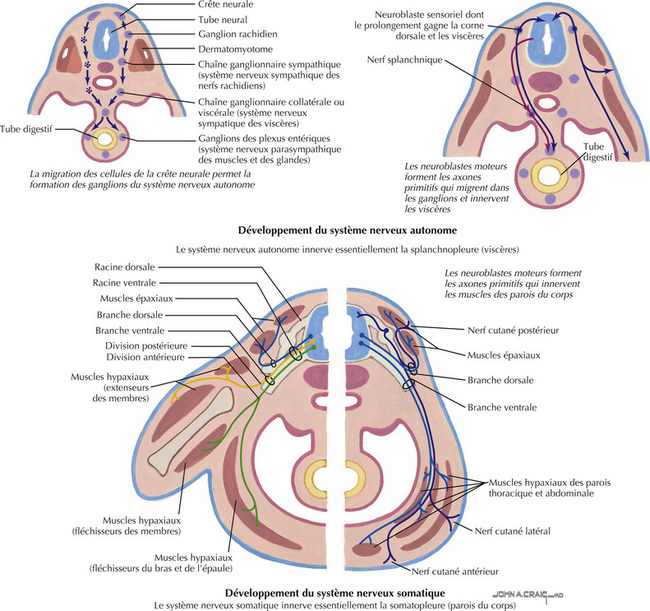
8.5 Développement des nerfs du système nerveux autonome (nerfs splanchniques) et du système nerveux somatique
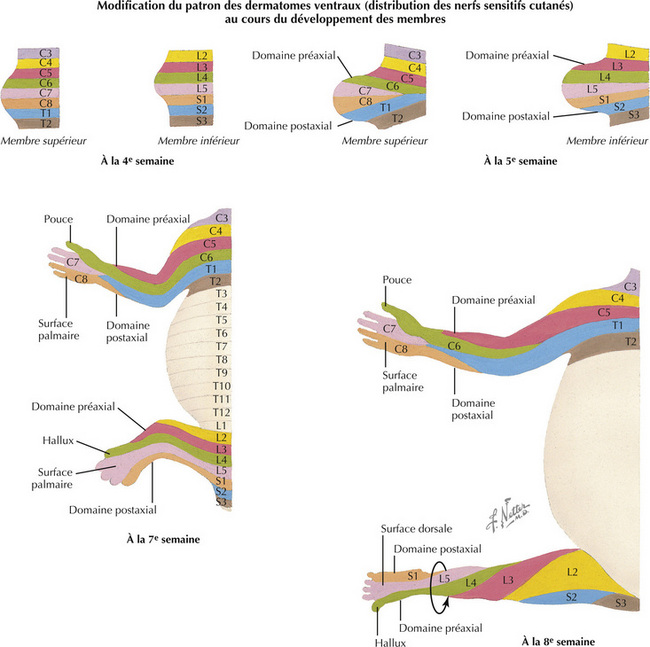
8.6 Rotation des membres et dermatomes
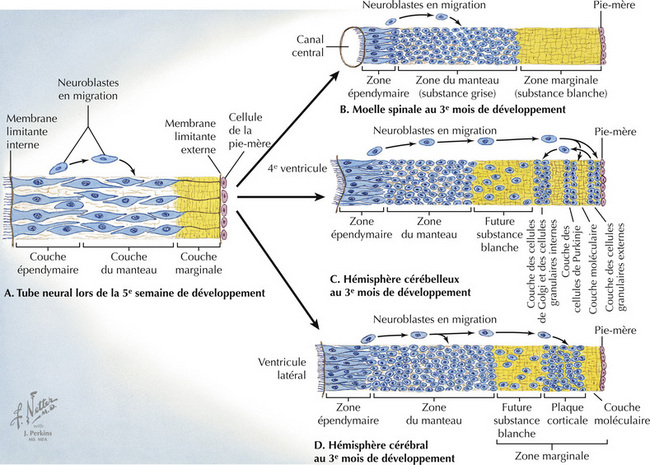
8.7 Prolifération et différenciation neurales : les parois du tube neural
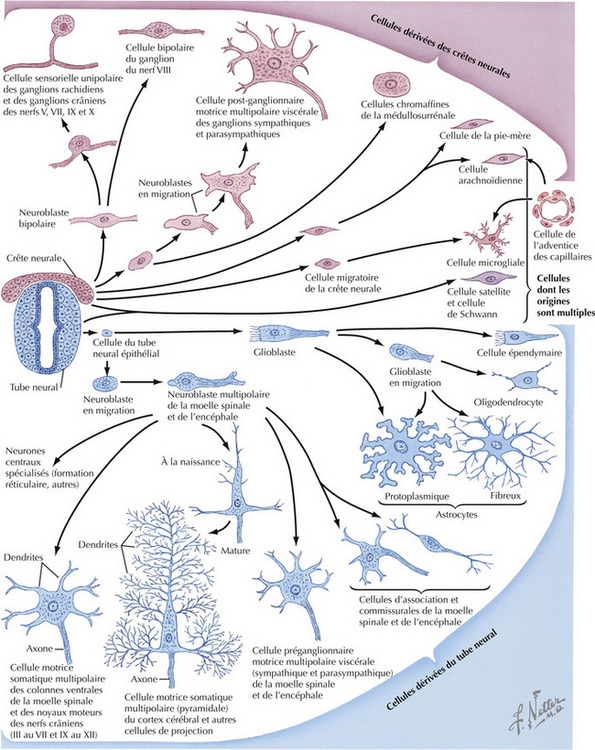
8.8 Dérivés du tube neural et de la crête neurale
8.9 Développement précoce du SNC : l’embryon au 28e jour de développement
8.10 Développement précoce du SNC : l’embryon au 36e jour de développement
8.11 Développement précoce du SNC : l’embryon au 49e jour et au 3e mois de développement
8.12 Développement du cerveau antérieur :de la 7e semaine au 3e mois du développement
8.13 SNC au 6e et au 9e mois de développement
8.14 Comparaison des régions du SNC à 5 semaines et demi du développement et à l’âge adulte
8.15 Dérivés des plaques alaire et basale du tronc cérébral
8.16 Dérivés adultes du prosencéphale, du mésencéphale et du rhombencéphale
8.17 Ébauches embryonnaires des nerfs crâniens
8.18 Composants neuronaux des nerfs crâniens
8.19 Développement des noyaux moteurs et préganglionnaires autonomes du tronc cérébral et de la moelle spinale
8.20 Développement de l’œil et de l’orbite
8.21 Développement de l’oreille
8.22 Développement de la glande hypophysaire
8.23 Développement des ventricules
8.24 Développement du quatrième ventricule
8.25 Malformations du tube neural
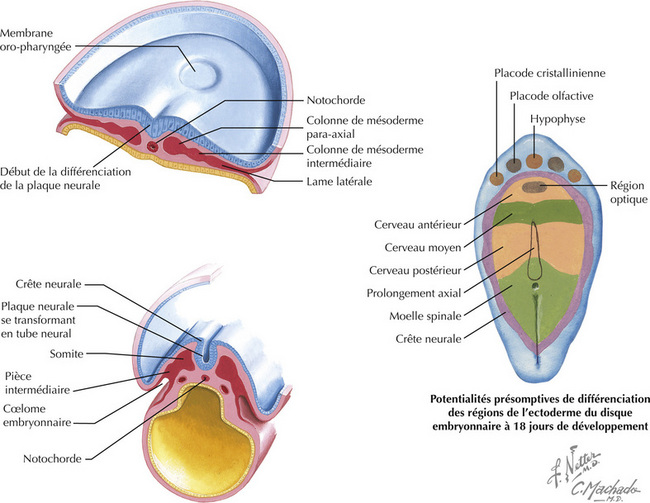
La plaque neurale, le tube neural et la crête neurale se forment au 18e jour du développement embryonnaire. La notochorde sous-jacente induit la plaque neurale et un sillon neural médian apparaît. Les bords latéraux de la plaque constituent les bourrelets neuraux destinés à former les crêtes neurales. Ces crêtes formeront de nombreux composants du système nerveux périphérique (SNP). À ce stade très précoce, les précurseurs neuraux peuvent être lésés par des substances toxiques ou d’autres formes d’agressions.
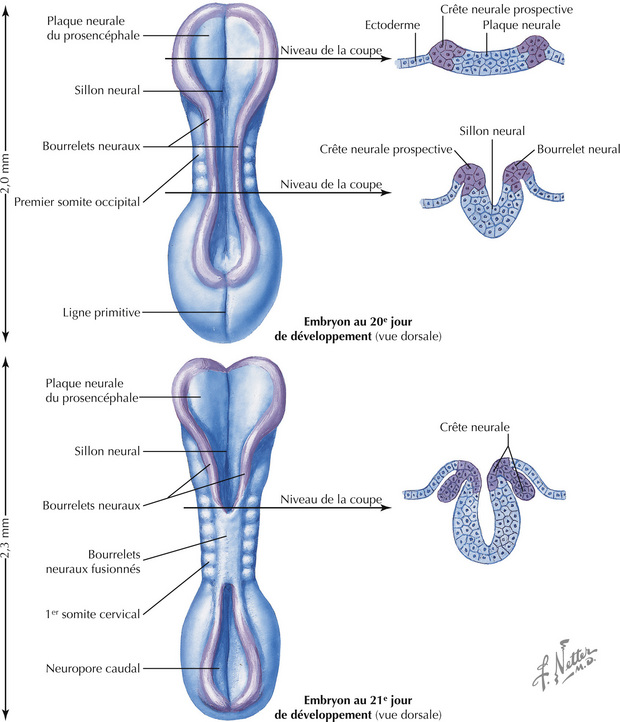
Chez l’embryon de 21 ou 22 jours de développement, la plaque neurale et son sillon médian s’épaississent et commencent à s’élever de chaque côté, si bien que les deux bords latéraux fusionnent sur la ligne médiane pour former le tube neural. Le canal central, futur système ventriculaire, constitue le centre du tube neural. Ce processus de neurulation progresse vers l’avant et vers l’arrière. Un défaut de neurulation peut entraîner une anomalie de formation du tube neural au niveau caudal (spina bifida) ou rostral (anencéphalie).
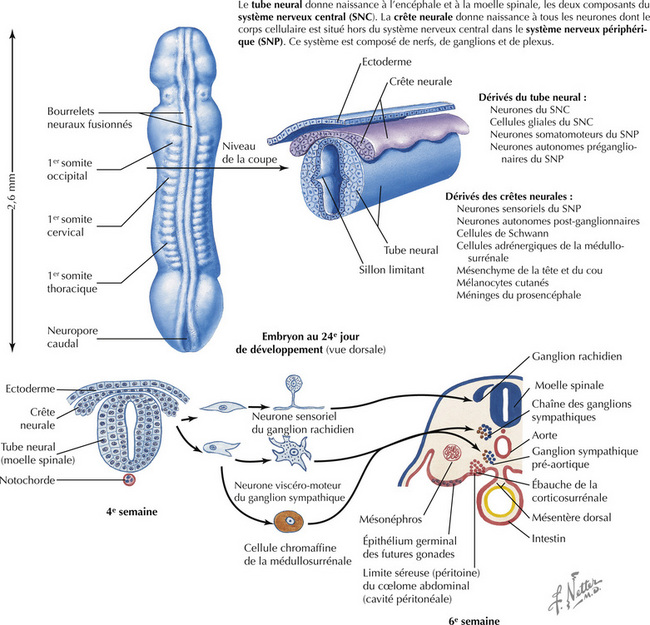
Les moitiés dorsale et ventrale du tube neural sont séparées par le sillon limitant, un élargissement externe du canal central qui marque la limite entre les plaques alaire et basale. Cette structure importante subsiste dans certaines régions du système ventriculaire de l’adulte. La plaque alaire est à l’origine de nombreux neurones sensoriels. La plaque basale donne naissance à de nombreux neurones moteurs soma- tiques ou autonomes de la moelle spinale ou du tronc cérébral. Les cellules de la crête neurale situées sur le bord des bourrelets neuraux s’unissent pour former une crête dorsale. La crête neurale se constitue ainsi au-dessus du tube neural. Ce dernier et la crête neurale se détachent de l’ectoderme dont ils sont issus.
Le développement des axones périphériques est un processus complexe qui fait intervenir l’extension des neurites centraux et périphériques, des facteurs trophiques et chémotactiques, le guidage axonal et le maintien des axones par les tissus cibles. Les cellules des ganglions spinaux sont bipolaires ; le prolongement périphérique axonal s’associe à des cellules réceptrices sensorielles simples ou complexes, tandis que le prolongement axonal central s’étend dans le système nerveux central (SNC) pour faire synapse avec les neurones sensoriels secondaires. Les motoneurones périphériques envoient leurs axones, par les racines ventrales ou les nerfs moteurs crâniens, vers les fibres musculaires striées squelettiques, constituant les jonctions neuromusculaires aux sites synaptiques. Les motoneurones qui n’établissent pas de contact avec les fibres musculaires squelettiques meurent. Les axones centraux préganglionnaires empruntent les racines ventrales et se terminent sur les cellules des ganglions sympathiques de la chaîne sympathique latérale ou sur les ganglions parasympathiques intramuraux qui se trouvent près des organes à innerver. Les axones post-ganglionnaires ont pour cible les fibres musculaires lisses, les fibres musculaires cardiaques, les glandes sécrétoires, quelques cellules métaboliques (comme les hépatocy- tes ou les adipocytes) et les cellules immunitaires des organes lym- phoïdes. Des signes sensoriels, moteurs ou autonomes peuvent être observés au cours des neuropathies périphériques lorsque ces voies sont lésées.
La somatopleure et la splanchnopleure sont les bases embryonnaires qui permettent le développement des systèmes nerveux périphériques somatique et splanchnique (autonome). La somatopleure se développe entre I ’ectoderme et la portion somatique des I ames latérales. Les myoblastes du domaine hypaxial du somite migrent dans la somatopleure pour former les cellules musculaires striées squelettiques des parois latérales et ventrale du corps ainsi que les cellules musculaires striées squelettiques des membres. La splanchnopleure se développe entre I ’endoderme et la portion somatique des lames latérales pour former les viscères. Les branches nerveuses ventrales migrent vers la somatopleure et les nerfs splanchniques (autonomes) dans la splanchnopleure. Les nerfs splanchniques thoraciques et lombaires ont des composants sympathiques et sensoriels. Les nerfs splanchniques pelviens (S2-S4) ont des composants parasympathiques et sensoriels.
La rotation du membre inférieur est la conséquence de l’inversion des régions pré- et postaxiales, conduisant à un arrangement spinal spécifique des dermatomes. Les segments nerveux spinaux de la face antérieure du membre inférieur s’étendent sur les faces médiane et inférieure, si bien que l’hallux est innervé par un dermatome plus rostral (L4) que celui du cinquième orteil (S1). L’extrémité inférieure est une extension du tronc et les dermatomes les plus caudaux (sacral et coccygien) innervent le périnée et non le pied. Les dermatomes cervicaux gardent une distribution relativement ordonnée au membre supérieur, avec une rotation minime.
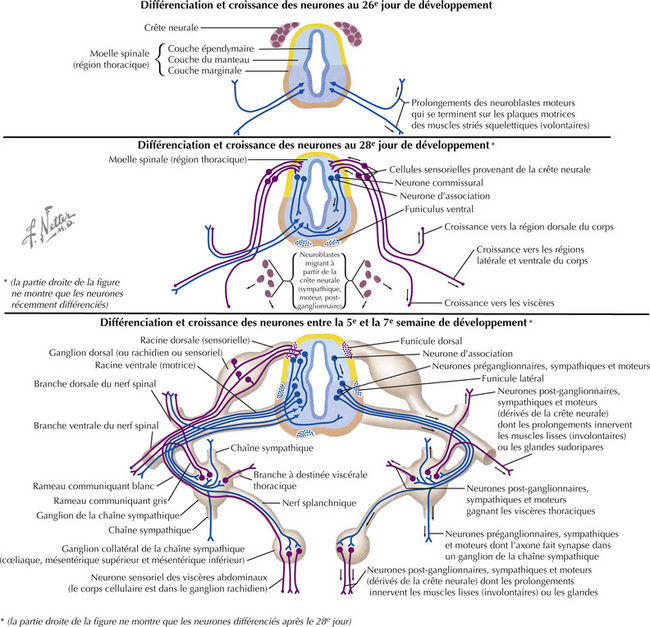
Dès un stade précoce du développement (5e semaine), les neuroblastes de la couche épendymaire qui limite le canal central subissent des mouvements de va-et-vient entre les surfaces épendymaire et piale et se divisent au cours de ces mouvements. Cette migration neurale suit des schémas différents selon la région du tube neural. Au niveau de la moelle spinale, les neurones migrent dans la couche interne du manteau, la couche marginale externe contenant les prolongements axo- naux. Au niveau du cortex cérébelleux, quelques neurones migrent en dehors dans la surface piale et forment la couche granulaire externe, à partir de laquelle les cellules granulaires migrent en profondeur pour former des synapses avec d’autres neurones présents dans les couches profondes du cortex cérébelleux. Dans le cortex cérébral, les neurones migrent vers la zone externe, où la substance grise (corps cellulaires des neurones) reste en surface et recouvre la substance blanche (fibres nerveuses). Ces schémas de développement préfigurent l’organisation anatomique des structures matures, leur vascularisation et leur vulnérabilité à différentes formes d’agression, telles que les tumeurs, les traumatismes et les atteintes ischémiques.
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree