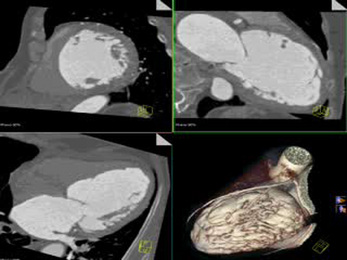
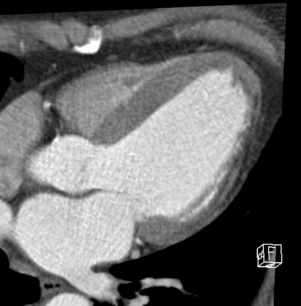
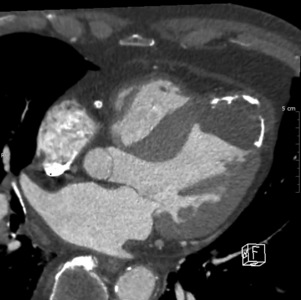
Chapitre 22 Cœur et thorax
Quand le scanner thoracique doit-il être d’emblée un scanner cardiaque ?
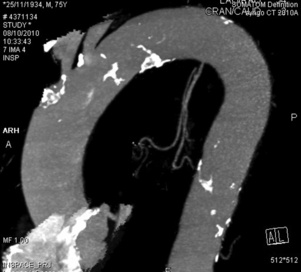
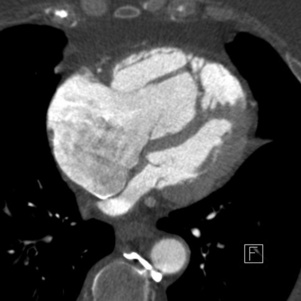
En revanche, le bilan d’hémoptysie, qui est une situation moins fréquente, bénéficie d’une acquisition d’emblée avec synchronisation, car cette technique améliore de façon très nette la qualité des reconstructions qui permettent une identification précise de la naissance et du trajet des artères bronchiques, soumises à une grande variabilité anatomique, dans le but de guider leur cathétérisme si un geste d’embolisation s’avérait nécessaire (fig. 22.1). Il permet aussi parfois la découverte d’anastomoses à risque, comme les fistules coronarobronchiques. En cas de saignement d’origine artérielle pulmonaire, le diagnostic est également facilité par l’absence d’artéfacts cinétiques liés à la masse cardiaque dans les régions proximales.
Connaître les images pièges
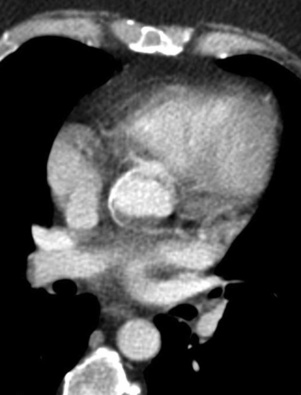
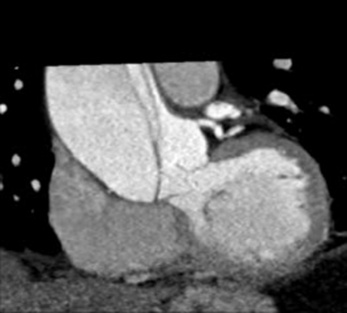
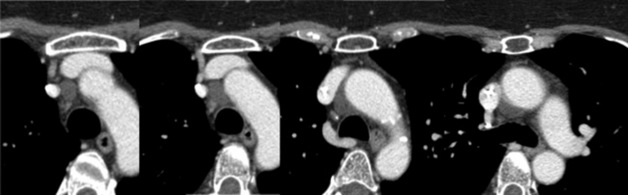
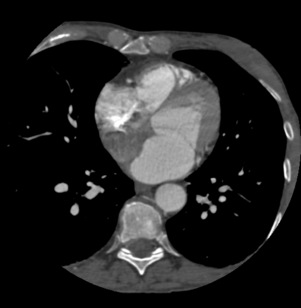
Parmi les images artéfactuelles, certaines sont connues de longue date, comme l’artéfact de pulsatilité aortique qu’il faut différencier d’un flap intimal sur l’aorte thoracique initiale (fig. 22.2, ![]() vidéo 22.1), ou comme certains artéfacts de flux au sein de l’oreillette droite, à différencier d’un thrombus (fig. 22.3).
vidéo 22.1), ou comme certains artéfacts de flux au sein de l’oreillette droite, à différencier d’un thrombus (fig. 22.3).
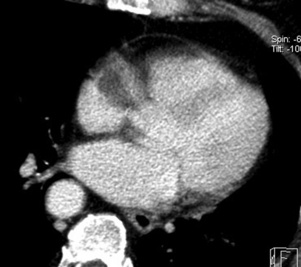
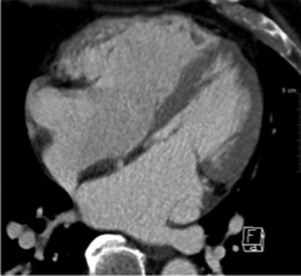
Fig. 22-3 TDM thoracique APC sans synchronisation ECG.
Hypodensité au sein de l’oreillette droite correspondant à un artéfact de flux.
En ce qui concerne les variantes anatomiques, on rappellera :
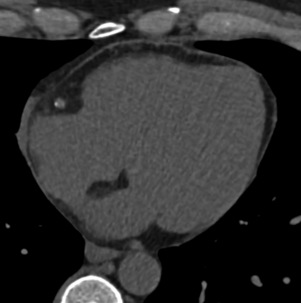
Fig. 22-6 TDM thoracique SPC.
Petit lipome du septum interauriculaire caractérisé par des densités graisseuses.
Cardiopathies méconnues à révélation pneumologique
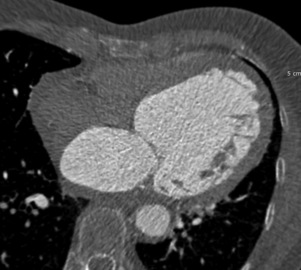
L’œdème cardiogénique se traduit par un œdème interstitiel avec infiltration septale périlobulaire, œdème péribronchique souvent associé à des opacités alvéolaires périhilaires, un épanchement pleural et des adénopathies médiastinales de « résorption lymphatique ». Son diagnostic nécessite une analyse cardiaque concomitante et permet la découverte de cardiomyopathies primitives ou secondaires affectant le ventricule gauche, parfois méconnues. Certaines cardiomyopathies dilatées peuvent ainsi être suggérées sur l’existence d’une franche dilatation du ventricule gauche avec un myocarde d’épaisseur normale ou réduite (fig. 22.9). Une analyse en mode ciné-IRM dans les différents plans cardiaques de référence permet d’objectiver les troubles de la cinétique à type d’hypokinésie globale homogène (![]() vidéo 22.2).
vidéo 22.2).
Il faut également citer ici les cardiopathies méconnues dont le clinicien n’a pas eu connaissance ou qu’il a oublié de signaler sur la demande d’examen, comme les séquelles ischémiques d’infarctus du myocarde ou les anévrismes ventriculaires. La cica trice d’une nécrose myocardique se traduit par un amincissement pariétal et une plage de métaplasie graisseuse [2] qui peut être aisément reconnue, même sur un examen non synchronisé, en raison de sa franche hypodensité, surtout si elle est assez étendue (fig. 22.10).
L’anévrisme ventriculaire gauche apical est parfois difficile à détecter en échocardiographie. En scanner, il se présente sous la forme d’une ectasie sphérique de la pointe du ventricule gauche qui perd sa forme triangulaire, avec une paroi nettement amincie contenant de la graisse et souvent des calcifications arciformes. L’analyse cinétique objective une akinésie, voire une dyskinésie localisée, et parfois un thrombus hypodense tapissant l’apex (fig. 22.11).
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree