Chapitre 21 Explorations électrophysiologiques
Du point de vue des définitions et de la compréhension de la physiopathologie, les tachycardies atriales relèvent d’un mécanisme entièrement localisé au sein des oreillettes. Selon leur physiopathologie, certaines tachycardies sont régulières et d’autres pas. Parmi ces dernières, la fibrillation atriale (FA) a des caractéristiques épidémiologiques et des implications thérapeutiques suffisamment importantes pour qu’un chapitre particulier lui soit consacré.
Le mécanisme de la FA n’est pas encore clairement compris. La théorie prédominante du XXe siècle était basée sur l’existence de plusieurs circuits de rentrée, chaotiques et variant constamment, en fonction des lignes du bloc de conduction, générant la FA (fig. 21.1).
Ce concept a été contesté, cependant, par le fait que chez certains patients sans anomalies cardiaques structurelles, un tracé électrocardiographique (ECG) de FA était constaté, en rapport avec une source précise générant une tachycardie auriculaire irrégulière, et issue d’une veine pulmonaire (VP) [1]. Cette notion de FA focale est à l’origine du traitement par ablation endocavitaire de la FA [2].
Ces deux mécanismes ne devraient pas être considérés comme des entités distinctes. Au fil du temps, cependant, en raison d’épisodes récurrents de tachycardie, il se produit un remodelage du tissu auriculaire (altération de la conduction et de propriétés structurelles), avec dilatation des oreillettes. Ce phénomène peut gérer plusieurs fronts d’onde de réentrée sans nécessiter une source focale à l’origine de la FA [3]. Cette progression pathologique (remodelage des oreillettes) est reflétée par l’existence d’observations cliniques où la FA paroxystique devient permanente lorsqu’elle n’est pas traitée. Il est également possible que, même chez les patients atteints de FA permanente, il existe des foyers focaux, participant à l’entretien permanent de cette FA.
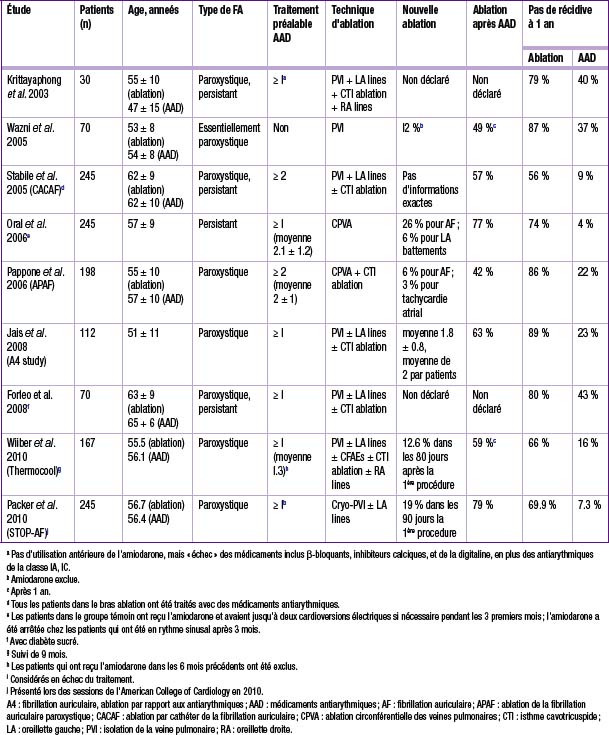
Les recommandations récentes de l’European Society of Cardiology (ESC) ont clairement établi le bénéfice des techniques d’ablation dans la FA paroxystique ou persistante comparativement au traitement médical [4], augmentant considérablement les indications d’ablation jusque-là réservées aux patients symptomatiques avec FA paroxystique [5]. Le tableau 21.1 résume les études et donne les résultats des travaux comparatifs publiés.
Ainsi, l’ablation curative de la FA a deux buts mécanistiques :
Procédures d’ablation
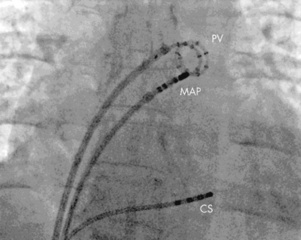
Depuis le début des années 1980, les techniques ablatives ont permis d’améliorer la prise en charge thérapeutique des patients présentant des arythmies cardiaques. Il s’agit d’un type d’intervention en pleine expansion. L’ablation consiste en la destruction d’une partie limitée du muscle cardiaque. Celle-ci est réalisée grâce à des électrodes situées sur la partie distale de cathéters dédiés à ce type de thérapie. Dans la majorité des cas d’ablation endocavitaire, ces cathéters sont positionnés au niveau de l’endocarde après ponction fémorale artérielle ou veineuse selon l’arythmie à traiter. La procédure est réalisée dans un laboratoire d’électrophysiologie sous contrôle radioscopique (fig. 21.2). L’objectif est d’éliminer le tissu myocardique servant de substrat à l’arythmie.
Le principe de l’ablation a été découvert fortuitement à l’hôpital de la Pitié-Salpêtrière en 1977 [6]. Il s’agissait en fait d’une complication d’une exploration électrophysiologique réalisée dans le cadre du bilan de syncope chez un patient de 47 ans porteur d’une cardiopathie ischémique. Un bloc auriculoventriculaire complet a été constaté après la délivrance d’un choc électrique externe pour réduire une tachycardie ventriculaire. La formation d’un arc électrique entre les électrodes endocavitaires et les palettes de défibrillation a généré les lésions myocardiques responsables du bloc auriculoventriculaire. Ce n’est que quelques années plus tard que des études expérimentales et cliniques ont permis de développer la technique de fulguration à des fins thérapeutiques [7]. Cette procédure devait être faite sous anesthésie générale. Rapidement, d’autres énergies se sont développées, d’utilisation plus facile et d’efficacité supérieure. Il s’agit principalement de la radiofréquence, mais aussi des ultrasons et de la cryoablation.
Procédure de Maze
Les chirurgiens cardiaques ont été les pionniers de l’ablation curative de la FA. En 1992, la procédure de Cox’s Maze III était réalisée avec succès. Elle dérivait d’une longue expérience chirurgicale de cartographies réalisées chez l’animal puis chez l’homme pour améliorer la technique d’ablation [8]. Au départ, les lésions ont été créées par des incisions sous vision directe dans laquelle la transmuralité était certaine. Par conséquent, cette technique était extrêmement efficace, avec maintien du rythme sinusal déclaré par Cox à plus de 97 % et à 84,9 % après un examen systématique de 1553 patients dans toutes les séries publiées jusqu’à 2004 [9]. Une autre caractéristique importante de l’approche chirurgicale est le démantèlement ou la fermeture de l’auricule gauche, qui conduit à un taux très faible d’accidents vasculaires cérébraux peropératoires (0,5 %) et dans le suivi (0,3 % à 12 ans dans cette étude).
Autres procédures d’ablation
Le succès et le développement de l’ablation endocavitaire de la FA ont été rendus possibles par la découverte qu’une activation ectopique auriculaire venant des VP pouvait déclencher la FA. Ainsi, l’ablation de ces sites pouvait prévenir la récidive de la FA chez les patients très symptomatiques [1]. Cette technique s’est extrêmement développée, et a connu une croissance exponentielle du nombre d’ablations par cathéters réalisées depuis les années 1990.
Prise en charge multidisciplinaire
La pratique d’explorations électrophysiologiques nécessite d’une part des connaissances rythmologiques spécifiques, d’autre part une infrastructure suffisante en matériel et en personnel. Il est notamment indispensable de disposer d’un matériel de réanimation et d’un défibrillateur externe en bon état de marche. Nous ne reviendrons pas sur la technique du cathétérisme cardiaque droit, qui doit être parfaitement maîtrisée. Un plan d’exploration méthodique et rigoureux doit être suivi, sans oublier toutefois que l’exploration électrophysiologique n’est que le complément d’une analyse clinique rigoureuse et qu’elle doit être adaptée au cas particulier de chaque patient, et vue comme un complément de l’ECG de surface. Pour les explorations courantes, deux ou trois sondes sont en général utilisées, introduites dans une veine fémorale, pour enregistrer les potentiels intracardiaques et réaliser une stimulation. Elles sont placées dans l’oreillette droite (OD), à la jonction auriculoventriculaire et dans le ventricule droit. Dans le cas particulier de l’ablation de la FA, un cathétérisme trans-septal est nécessaire, afin d’avoir accès aux VP qui s’abouchent dans l’oreillette gauche (OG). En effet, la voie d’abord privilégiée est la veine fémorale droite (ou gauche), diminuant les complications au point de ponction et les risques emboliques systémiques [10].
Préparation de la procédure d’ablation
En raison des risques potentiels d’ablation de la FA (tableau 21.2), nous évaluons normalement tous les patients en ambulatoire, afin de discuter des approches alternatives thérapeutiques. C’est le moment où tous les détails pertinents de l’histoire médicale du patient doivent être étudiés attentivement : le type et la durée de la FA (paroxystique, persistante ou permanente) à l’ablation préalable, les antécédents chirurgicaux, les maladies éventuelles associées, les médicaments et les allergies. Certains de ces facteurs peuvent augmenter la morbidité de la procédure ou la probabilité de récidive de FA après ablation. Par exemple, la présence de barres dans la colonne vertébrale de chirurgie de la scoliose peut rendre la visualisation de l’OG extrêmement difficile en scopie. En outre, une évaluation complète doit être effectuée, semblable à celle d’un patient consultant devant l’apparition d’une FA, y compris la détermination des causes réversibles de la FA. Les derniers résultats biologiques de laboratoire devraient être revus afin d’exclure des anomalies qui pourraient compliquer la procédure ou la période postopératoire, comme l’existence d’une anémie, d’une thrombocytopénie, d’une coagulopathie importante, d’infections, d’insuffisance rénale et de troubles électrolytiques.
Tableau 21-2 Résumé des complications de l’ablation par cathéter.
| Complications | Incidence |
|---|---|
| AVC et AIT | 1,0 % |
| Tamponnade | 1,2 % |
| Sténoses VP > 50 % | 1,3 % |
| Fistule atrio-œsophagienne | Peu de c as dans le monde |
| Résultats issus de la publication de Cappato et al. [33]. | |
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree