2 Classes médicamenteuses en ophtalmologie
ANTISEPTIQUES ET ASTRINGENTS
On peut distinguer dans cette catégorie trois types de produits :
ANTISEPTIQUES ET ASTRINGENTS PROPREMENT DITS
SOLUTIONS DÉSINFECTANTES DE LA PEAU DES PAUPIÈRES ET DES CONJONCTIVES
Elles sont utilisées en préparation chirurgicale sur ces structures fragiles qui ne supporteraient pas les solutions de désinfection habituellement utilisées pour la préparation cutanée en chirurgie.
CICATRISANTS
IMMUNOGLOBULINES
Il s’agit simplement d’homosérum conservé au réfrigérateur, instillé quatre fois par jour, dont l’action anticollagénasique est reconnue.
ANTIBIOTIQUES
CHOIX D’UN ANTIBIOTIQUE
Il répond à deux critères principaux.
Examen complet des structures oculaires
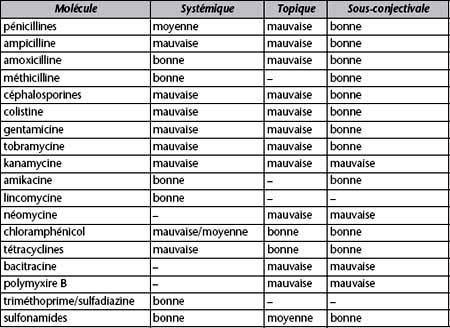
Il faut d’abord, à la faveur de l’examen clinique, identifier la structure infectée et si possible porter un diagnostic étiologique (examens complémentaires souvent nécessaires : examens bactériologique, cytologique et sérologique ; immunofluorescence directe ; PCR…). L’examen bactériologique avec antibiogramme, contrairement à ce qui est assez souvent mis en œuvre, ne s’impose d’emblée que s’il y a risque pour la fonction visuelle (et il faut dans ce cas mettre en œuvre un traitement antibiotique d’attente avant d’avoir le résultat de l’examen), ou si une affection chronique non résolue le justifie. Avec un peu d’expérience clinique, en fonction de la structure intéressée et de l’aspect de la lésion qui peut être typique (chémosis unilatéral de chlamydophilose, ulcère à collagénases de brachycéphale), un premier choix d’antibiotique peut être fait selon la sensibilité présumée du germe (tableau 2.I). L’antibiogramme permet de déterminer la CMI (concentration minimale inhibitrice) d’une souche bactérienne par un antibiotique : c’est la plus faible concentration d’antibiotique capable de provoquer une inhibition complète de la croissance d’une bactérie donnée, appréciable à l’œil nu après une période d’incubation. Une CMI comprise entre les deux concentrations critiques qualifie la souche bactérienne en cause comme de sensibilité intermédiaire (entre souche sensible et souche résistante), c’est-à-dire que le choix de l’antibiotique testé sera aléatoire quant au résultat clinique in vivo. Les associations d’antibiotiques (framycétine-polymyxine B, néomycine-polymyxine B par exemple) sont élaborées dans les spécialités topiques disponibles de façon à ce que ces dernières soient le moins tributaire possible des limites du spectre antibactérien de chaque antibiotique pris individuellement.
Tableau 2.I Choix d’un antibiotique en fonction de la sensibilité présumée du germe
| Germe | Molécule de référence | |
|---|---|---|
| Cocci Gram positifs | Staphylococcus spp | néomycine |
| bacitracine | ||
| amoxicilline | ||
| céphalosporines | ||
| fluoroquinolones | ||
| Staphylococcus aureus | gentamicine | |
| oxacilline | ||
| méthicilline | ||
| céphalosporines | ||
| fluoroquinolones | ||
| Staphylococcus epidermidis | néomycine | |
| gentamicine | ||
| fluoroquinolones | ||
| Streptococcus spp | pénicillines | |
| chloramphénicol | ||
| amoxicilline | ||
| céphalosporines | ||
| Cocci Gram négatifs | Neisseria spp | pénicillines |
| tétracyclines | ||
| sulfonamides (± triméthoprime) | ||
| Bacilles Gram positifs | Corynebacterium spp | pénicillines |
| tétracyclines | ||
| sulfonamides (± triméthoprime) | ||
| Bacilles Gram négatifs | Pseudomonas aeruginosa | polymixine B |
| gentamicine | ||
| tobramycine | ||
| amikacine | ||
| fluoroquinolones | ||
| Escheria coli | chloramphénicol | |
| tétracyclines | ||
| gentamicine | ||
| fluoroquinolones | ||
| Enterobacter spp | amoxicilline (± streptomycine) | |
| Proteus spp | gentamicine | |
| fluoroquinolones | ||
| tobramycine | ||
| amikacine | ||
| chloramphénicol | ||
| Hemophilus spp | amoxicilline | |
| tétracyclines | ||
| Moraxella spp | pénicillines | |
| tétracyclines | ||
| Actinomycètes | Actinomyces spp | pénicillines |
| tétracyclines | ||
| Nocardia spp | chloramphénicol (± streptomycine) | |
| Chlamydophila | Chlamydia spp | doxycycline |
| tétracyclines | ||
| chloramphénicol | ||
| Mycoplasmes | Mycoplasma spp | tétracyclines |
| chloramphénicol | ||
(modifié d’après D. Slatter, Fundamentals of veterinary ophtalmology, 3rd ed., Philadelphia : WB Saunders, 2001).
Connaissance des propriétés pharmacocinétiques et pharmacologiques des principes actifs
La pénétration des antibiotiques est soumise au passage de barrières anatomiques :
Chaque famille thérapeutique sera étudiée en respectant cet ordre de présentation et en présentant les principaux antibiotiques utilisés. La rifamycine, qui bloque la synthèse de l’ARN-polymérase ADN dépendante des bactéries, et l’acide fusidique, apparenté tantôt aux macrolides, tantôt aux aminosides, seront présentés séparément.
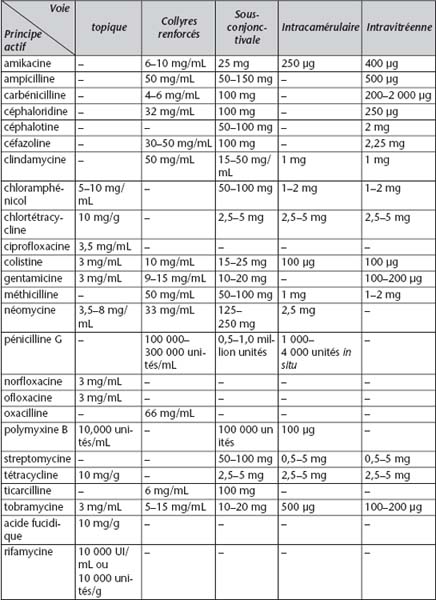
Les concentrations en principe(s) actif(s) des différentes spécialités topiques disponibles sont en principe optimales, mais on peut être amené, dans certains cas, à prescrire une préparation magistrale, où la concentration de l’antibiotique choisi sera augmentée pour des raisons d’efficacité sur certains germes (gentamicine par exemple). Le tableau 2.III fournit une synthèse des données utiles en matière de concentration, posologie et voies d’administration des principes actifs.
PÉNICILLINES
Propriétés pharmacocinétiques et pharmacologiques
Les pénicillines sont actives conte les bactéries Gram positives, mais seules celles qui sont lactamases résistantes (méthicilline, oxacilline, cloxacilline, dicloxacilline) sont efficaces contre les souches de Staphylococcus aureus et Staphylococcus epidermidis qui produisent ce type d’enzyme. Les spectres d’activité de l’ampicilline et de l’amoxicilline sont les plus larges et l’ajout d’un inhibiteur des lactamases (acide clavulanique, clavulanate, sulbactam, tazobactam) permet de les employer dans ce cas. Carbénicilline, pipéracilline et ticarcilline sont utilisables contre Pseudomonas aeruginosa et certaines souches de Proteus et Enterobacter.
CÉPHALOSPORINES
Indications
BACITRACINE
Propriétés pharmacocinétiques et pharmacologiques
La bacitracine est hydrosoluble et est efficace contre la plupart des bactéries Gram positives. Instable en solution, elle est seulement disponible en pommade ; sa toxicité rénale par voie générale limite considérablement ce dernier usage, ce qui fait que peu d’antibiorésistances sont connues chez les bactéries contre lesquelles elle est efficace.
AMINOSIDES
Propriétés pharmacocinétiques et pharmacologiques
Cette famille d’antibiotiques est potentiellement efficace contre de nombreuses bactéries Gram négatives : Pseudomonas aeruginosa, Proteus, Klebsiella, Escherichia coli, Enterobacter, Serratia et de nombreuses souches de staphylocoques. Le large spectre d’activité de la néomycine, incluant bactéries Gram négatives et Gram positives à l’exception de Pseudomonas, présente un grand intérêt topique. Ces substances agissent en se liant aux ribosomes bactériens, inhibant la synthèse protéique et, de ce fait, sont l’objet d’antibiorésistances fréquentes liées soit à l’altération des ribosomes bactériens, soit à une diminution des prises, soit le plus souvent à l’inactivation enzymatique du principe actif par la bactérie ; les résistances croisées (gentamicine-tobramycine) sont possibles et souvent complètes (d’où l’intérêt de l’antibiogramme lors d’ulcère cornéen à Pseudomonas) et les pénicillines mélangées aux aminoglycosides par voie topique inactivent ces derniers (bien que l’association des deux soit synergique).
Hydrosolubles, elles pénètrent le stroma cornéen ulcéré mais passent mal la barrière hémato-aqueuse.
Tobramycine
Les indications sont les mêmes que celles de la gentamicine, à la même concentration et si besoin en solution renforcée à 15 mg/mL (irritation locale possible), mais elle est plus active in vitro contre Pseudomonas que la gentamicine avec laquelle des résistances croisées existent. Cependant, si un germe est résistant à la tobramycine, il l’est en général à la gentamicine, l’inverse n’est pas toujours vrai. Pour ces raisons, la tobramycine fait partie des antibiotiques topiques de tout premier choix lors d’infection à germes Gram négatifs, notamment à Pseudomonas (Tobrex collyre, 3 à 8 instillations/j ; Tobrex pommade, 2 à 3 fois/j).
MACROLIDES
Ils sont peu utilisés en médecine vétérinaire (passent mal la barrière hématoaqueuse, induisent facilement des résistances bactériennes), sont actifs sur les cocci Gram positifs (Staphylococcus, Streptococcus) et les bacilles Gram positifs (Chlamydophila, Mycoplasma, Rickettsia). Le seul d’entre eux parfois utilisé est l’érythromycine en collyre ou pommade à 0,5 % (non disponible en spécialité).
TRIMÉTHOPRIME, PYRIMÉTHAMINE
Il s’agit de deux 4-diaminopyridines inhibitrices de la synthèse de l’acide folique à une étape postérieure à celle bloquée par les sulfonamides, en association avec lesquelles un effet synergique est observé. On utilise par voie générale des associations triméthoprime-sulfaméthoxypyridazine (Septotryl) ou triméthoprime-sulfaméthoxazole (Sultrian). Actives contre les germes Gram négatifs et Gram positifs (Staphylococcus, Streptococcus), ces deux molécules le sont aussi contre Pseudomonas (triméthoprime 1 % et polymyxine B à 10 000 UI/mL en collyre, non disponible en spécialité) et Toxoplasma (en association avec la sulfadiazine par voie générale).
RIFAMYCINE
Présenté en collyre en solution à 1 000 000 UI/100 mL et en pommade à 1 000 000 UI/100 g (Rifamycine Chibret), il est instillé 4 fois/j en collyre et appliqué 2 fois/j en pommade. Son administration peut rarement dépasser une semaine quelle que soit la forme utilisée car, selon notre expérience, à l’irritation transitoire suivant l’application des premiers jours succède fréquemment une irritation constante et assez intense pour que le traitement soit suspendu. Nous n’avons jamais constaté les possibles réactions d’hypersensibilité aux conservateurs de la forme collyre (disulfite de K et thimersal) décrites chez l’homme.
ANTIVIRAUX
À RETENIR
VIROSTATIQUES
Aciclovir 5 (ACV)
C’est celui dont le mode d’action a été le mieux étudié, compte tenu de son large emploi chez l’homme : l’ACV, analogue de la guanine (base identique, un radical 3’OH en moins), interrompt la croissance du brin d’ADN viral en se comportant comme l’élément obligatoirement terminal de la chaîne nucléotidique dès qu’il y est incorporé, le nucléotide suivant étant attaché au précédent par le radical 3’OH. Il doit subir trois phosphorylations successives dans la cellule hôte pour passer du stade de nucléoside à celui actif de nucléotide : la première sous dépendance de la thymidine kinase virale, la seconde et la troisième sous dépendance des kinases de la cellule hôte.
PRODUITS NON ANALOGUES AUX NUCLÉOSIDES DU VHF-1
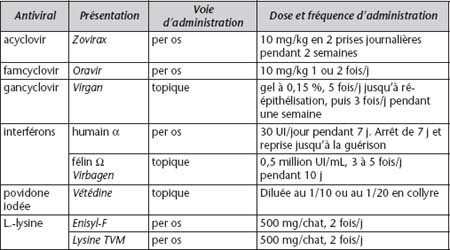
Ils sont également présentés au tableau 2.IV.
Povidone iodée
Elle est utilisée en diluant au 1/10 (1 %) ou au 1/20 (0,5 %) la solution du commerce (Vétédine) utilisée en collyre, efficace contre le VHF-1 durant sa courte phase extracellulaire.
ANTIFONGIQUES
Les antifongiques sont classés selon leur structure et leur mode d’action :
KÉRATITES MYCOSIQUES
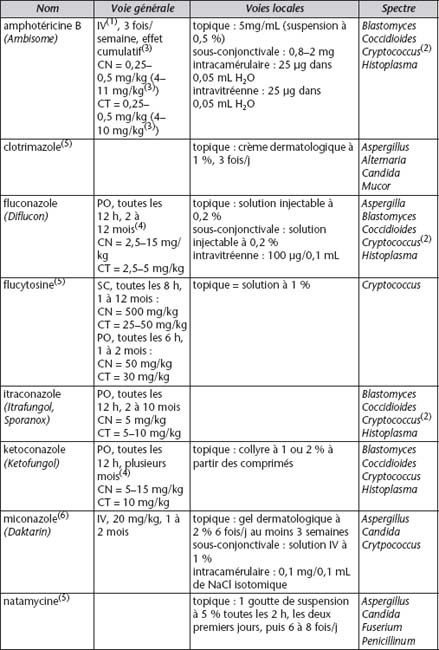
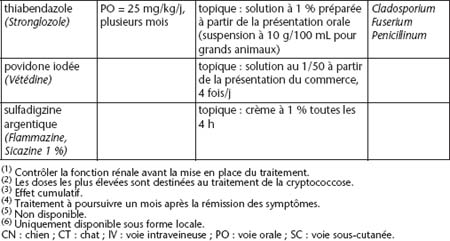
Rares chez les carnivores par rapport à la fréquence observée chez le cheval (les levures font partie de la flore conjonctivale normale des équidés), on sait qu’elles sont la conséquence d’une plaie de cornée ou d’un traitement corticoïde topique prolongé. Le traitement topique antifongique (tableau 2.V) en association à un traitement antibiotique peut être efficace, mais le recours à une solution chirurgicale (kératectomie avec ou sans greffe conjonctivale ou cornéenne lamellaire associée, voire kératoplastie transfixiante) est souvent nécessaire.
MYCOSES SYSTÉMIQUES
Ce sont essentiellement des signes d’uvéite qui sont observés, avec uvéite antérieure, choriorétinite, décollements rétiniens, glaucome secondaire. Les quatre principaux agents de mycoses systémiques avec signes oculaires des carnivores, telles que rapportées par la littérature nord-américaine (ces affections sont fréquentes aux États-Unis, rares en France), sont les suivants : Blastomyces dermatitis, Coccidioides immitis, Cryptococcus neoformans, Histoplasma capsulatum. Le traitement est effectué par voie générale (tableau 2.V), le traitement spécifique de l’uvéite et du glaucome secondaire mis en place s’il y a lieu.
ANTI-INFLAMMATOIRES
À RETENIR
Les affections oculaires à caractère inflammatoire ou à médiation immune sont nombreuses chez les carnivores domestiques. Quelle que soit la classe thérapeutique à laquelle ils appartiennent, l’emploi des anti-inflammatoires s’intègre dans de nombreux protocoles de traitement où ils contribuent à la sauvegarde de la fonction visuelle et au confort des animaux traités. Cette utilisation ne doit pas se substituer à la formulation d’un diagnostic étiologique. Ils sont divisés en deux catégories :
RAPPELS SUR LES MÉCANISMES DE L’INFLAMMATION OCULAIRE
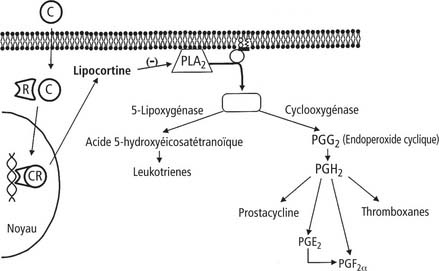
Une lésion de membrane cellulaire se traduit par la libération d’acide arachidonique (AA) membranaire. L’AA est métabolisé par deux voies (fig. 2.1) : celle des cyclo-oxygénases et celle des lipo-oxygénases, actives dans les cellules de la conjonctive, de la cornée et du tractus uvéal. Ces deux voies métaboliques sont initiatrices de la formation de médiateurs chimiques pro-inflammatoires : prostaglandines (PGs) et thromboxanes pour la voie des cyclo-oxygénases (COX), leucotriènes pour la voie des lipooxygénases. Ces molécules ont des effets chimiotactiques pour les cellules de l’inflammation, et les leucotriènes augmentent spécifiquement la perméabilité vasculaire.
Note : voir en annexe le diagnostique différentiel des inflammations oculaires, p. 173.
AIS (CORTICOSTÉROÏDES)
Propriétés pharmacocinétiques et pharmacologiques
Les AIS sont des 21-carboprotéines lipophiles dérivées du cholestérol qui se lient aux récepteurs glucocorticoïdes du cytoplasme cellulaire : la liaison avec un AIS modifie la structure tertiaire de ces récepteurs ubiquistes qui sont transférés au noyau, où ils se lient à des séquences d’ADN spécifiques de la réponse à l’administration d’AIS, elle-même matrérialisée par la synthèse d’une enzyme : la lipocortine, inhibitrice de la phospholipase A2 (donc protectrice membranaire), inhibitrice de la PGE-isomérase (donc de la synthèse de PGE) et protectrice de l’endothélium vasculaire (fig. 2.1). Cela se traduit par une diminution de l’exsudation cellulaire et fibrineuse, une inhibition de l’activité fibroblastique et de la synthèse de collagène, un effet stabilisateur sur les membranes lysosomales et la barrière hémato-oculaire.
Effets bénéfiques
Anti-inflammatoires : outre les effets protecteurs membranaires déjà évoqués, les AIS bloquent la dégranulation des neutrophiles, basophiles et mastocytes ; ils réduisent par leur effet cytoprotecteur la libération de protéases, d’histamine et de bradykinines.
Indications, contre-indications
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree