CHAPITRE 19 PARTICULARITÉS PÉDIATRIQUES 19.1 PARTICULARITÉS PÉDIATRIQUES DE L’EXPLORATION DU THORAX CHEZ L’ENFANT L’exploration du thorax en pédiatrie relève des mêmes techniques que celles employées chez l’adulte, allant de la radiographie simple du thorax qui reste le premier examen réalisé à l’imagerie par résonance magnétique (IRM) dont les indications encore limitées (paroi, vaisseaux et médiastin postérieur) s’élargissent à l’étude des voies aériennes. La tomodensitométrie est l’examen de deuxième intention et est particulièrement bien adaptée à l’exploration du thorax permettant, d’étudier avec une bonne résolution spatiale et une bonne résolution en contraste tous les éléments constitutifs du thorax. En raison de la plus grande susceptibilité de la population pédiatrique aux effets des rayonnements ionisants [10], cette imagerie doit être justifiée. L’échographie, de réalisation facile, peut être utile dans l’exploration des tissus mous, de la plèvre et du médiastin de nourrisson. La réalisation d’une radiographie du thorax se distingue de celle de l’adulte d’une part du fait de son incidence antéro-postérieure et d’autre part du fait de l’absence de grille antidiffusante. L’incidence antéro-postérieure est nécessaire chez le nourrisson en raison de l’utilisation de certains statifs dédiés, permettant une bonne contention, et est indispensable chez l’enfant plus âgé qui acceptera de ne pas bouger s’il peut voir ce qui se passe autour de lui. Chez l’enfant de moins de 4 ans, la coopération peut être difficile à obtenir et une contention s’avère souvent nécessaire [7]. L’absence d’utilisation du potter et de grille antidiffusante permet de réduire l’exposition de l’enfant aux rayonnements ionisants. L’incidence de face est considérée par la plupart des équipes comme suffisante pour répondre à l’immense majorité des questions posées. Le profil est donc une incidence complémentaire demandée par le radiologue. La radiographie en expiration est demandée systématiquement devant une dyspnée aiguë. Elle facilite la recherche d’un pneumothorax ou la mise en évidence d’un trappage expira-toire (emphysème obstructif) lors de l’inhalation d’un corps étranger (fig. 19-1). Cette incidence est également utile pour déterminer le côté pathologique devant une asymétrie de volume pulmonaire. Le côté pathologique est celui dont le volume ne diminue pas en expiration. Fig. 19-1 Radiographie de thorax de face en inspiration (a) et en expiration (b) pour syndrome de pénétration. Le décubitus latéral est une incidence de moins en moins réalisée. Elle permettait d’affirmer l’existence d’un épanche-ment quand le diagnostic était incertain sur l’incidence de face, ou de déterminer le caractère libre ou cloisonné d’un épanchement pleural. Actuellement, la réalisation d’une échographie pleurale a supplanté ces indications. Le décubitus latéral rayon horizontal permet d’obtenir chez un nourrisson une radiographie en expiration du côté où l’enfant est tourné. Les côtes, dont la portion antérieure est cartilagineuse, ne sont pas visibles chez l’enfant. Lorsque la radiographie est prise en hyperlordose, on observe une horizontalisation des côtes qu’il ne faut pas interpréter comme un signe de distension thoracique ; en outre, les clavicules qui se projettent normalement à la partie supérieure des deux poumons sont au-dessus des apex pulmonaires (fig. 19-2) [4]. Fig. 19-2 Radiographie de thorax de face prise en hyperlordose. Le sternum se projette sur le médiastin et le rachis ; il est donc difficilement individualisable. Si la radiographie est prise en discret oblique, les pièces sternales peuvent alors devenir visibles et ne doivent pas être interprétées comme des opacités anormales (fig. 19-3). Fig. 19-3 Radiographie prise en oblique postérieur gauche. Chez le nouveau-né, la peau se plisse facilement, ce qui peut être à l’origine d’images linéaires évoquant à tort un pneumothorax. Généralement, cette ligne sort du thorax osseux et une vascularisation du parenchyme pulmonaire peut être visualisée sur son versant externe (fig. 19-4). Fig. 19-4 Radiographie de thorax au lit d’un nouveau-né. Chez le nourrisson, la trachée qui en inspiration est recti-ligne se coude vers la droite en expiration (fig. 19-5). Cette coudure physiologique de la trachée est visible uniquement à cet âge. Avec la croissance, la trachée se rigidifie et reste rectiligne tout au long du cycle respiratoire. Fig. 19-5 Radiographie de thorax de face en inspiration (a) et en expiration (b) chez un nourrisson. Le médiastin, en raison de la présence du thymus, présente un aspect particulier chez le nourrisson, souvent source d’erreurs, de doutes et d’interrogations en pratique courante. Il est donc essentiel d’en connaître les principales caractéristiques radiologiques. Le thymus est un organe lympho-épithélial constitué de deux lobes reliés par un isthme situé au niveau du médiastin antérieur et supérieur. Le thymus apparaît comme une opacité de tonalité hydrique, homogène et non compressive du médiastin antéro-supérieur dont les limites externes sont ondulées (fig. 19-6) et dont le raccordement à la masse cardiaque peut être visualisé sous la forme d’une encoche (incisure cardiothymique). Sa forme se modifie entre l’inspiration (diminution) et l’expiration (augmentation) [11]. Ce phénomène s’explique d’une part du fait du caractère mou du thymus et d’autre part par le changement d’orientation de la glande thymique entre le temps inspiratoire et le temps expiratoire [6]. Fig. 19-6 Radiographie de thorax de face chez un nourrisson. Le thymus peut avoir une extension inférieure jusqu’au diaphragme, simulant alors une cardiomégalie (fig. 19-7), une extension postérieure ne pouvant être différenciée d’une masse du médiastin postérieure sur les données de la radiographie simple et nécessitant une exploration par une autre imagerie en coupes (fig. 19-8). Le thymus peut avoir un développement asymétrique avec une hypertrophie de son lobe droit, dont le bord inférieur s’appuie sur la petite scissure appelée généralement thymus en « voile latine ». Chez le nourrisson, en cas de pneumomédiastin, les deux lobes thymiques se soulèvent et réalisent l’aspect de thymus volant (fig. 19-9). Fig. 19-7 Radiographie de thorax de face d’une hypertrophie thymique descendant jusqu’au diaphragme. Fig. 19-8 Tomodensitométrie avec injection de produit de contraste passant à hauteur de la crosse de l’aorte. La tomodensitométrie est la technique d’imagerie la plus utilisée pour explorer le thorax de l’enfant après la radiographie simple. L’apparition du scanner multibarrettes a permis une étude multiplanaire et tridimensionnelle du médiastin, des voies aériennes et du parenchyme pulmonaire. La très grande majorité des examens est maintenant acquise en mode spi-ralé [5]. Le mode incrémental tend à disparaître, y compris pour certains dans l’étude de la pathologie infiltrative diffuse. Cependant, ce mode autorise une diminution importante de la dose délivrée quand un échantillonnage du parenchyme pulmonaire est suffisant. L’utilisation des reconstructions itératives permet de diminuer l’irradiation délivrée aux enfants. Le choix des paramètres d’acquisition doit être adapté à l’enfant. Le lecteur pourra retrouver sur le site de la Société francophone d’imagerie pédiatrique et prénatale (www.sfipp-radiopediatrie.org) les recommandations dosimétriques en scanographie pédiatrique établies en collaboration avec l’Institut de radioprotection et de sûreté nucléaire. Les progrès technologiques, en permettant une réalisation rapide de l’examen, ont permis de diminuer le nombre de sédations réalisées [9] et en particulier dans notre expérience chez les enfants de moins de 4 ans. Le recours à l’anesthésie générale est exceptionnel. L’endormissement naturel après la prise du biberon est utilisé chez l’enfant de moins de 6 mois. De même, les enfants scolarisés de plus de 3 ans dont l’examen est réalisé sans injection ou ayant une voie d’abord mise bien en amont de la réalisation de l’examen ne nécessitent pas de sédation. Cette dernière peut être réalisée par les radiologues. Les molécules utilisées réalisent une sédation consciente (hydroxyzine, hydrate de chloral, pentobarbital). Les contre-indications à la prémédication sont les obstructions des voies aériennes supérieures, l’insuffisance cardiaque, hépatique ou rénale, et l’hypertension intracrânienne. Une surveillance clinique et un monitorage de la fréquence cardiaque et de la saturation en oxygène doivent être assurés. Un protocole de sédation doit également être établi. L’injection d’un produit de contraste n’est pas systématique ; elle est utile à l’étude du médiastin, des gros vaisseaux thoraciques, des hiles pulmonaires et de la paroi thoracique. L’échographie, technique non invasive dont les principaux avantages sont l’absence d’irradiation et de sédation, est limitée dans son utilisation par le défaut de transmission des ultrasons à travers les structures osseuses (gril costal et sternum) et aériques (parenchyme pulmonaire normal). Elle permet l’étude de la plèvre, du médiastin, du diaphragme et du parenchyme pulmonaire pathologique [8]. L’échographie permet l’étude de la plèvre ; elle affirme la présence d’une minime lame d’épanchement pleural suspecté sur la radiographie, confirme un épanchement pleural massif ou un hémithorax opaque et élimine une lésion tumorale [1]. Elle précise l’aspect de l’épanchement (transsonore ou échogène, existence de dépôts de fibrine ou de cloisons). Elle permet également de choisir le site le plus adapté pour une ponction pleurale, surtout en cas d’épan-chement multiloculé (fig. 19-10). Fig. 19-10 L’échographie pleurale met en évidence l’épanchement pleural, son abondance et la présence de cloisons. L’échographie du médiastin peut être réalisée devant un élargissement de la silhouette cardiomédiastinale pour confirmer une hypertrophie thymique (l’échostructure du thymus est suffisamment caractéristique), mais quand un thymus est éliminé, le recours à une autre imagerie en coupes est indispensable pour mieux caractériser la masse tumorale [3]. L’échographie peut en revanche être proposée dans certains cas pour guider une biopsie percutanée. Depuis quelques années, l’IRM fait l’objet de recherches cliniques pour valider de nouvelles applications. Ce regain d’intérêt vient de la volonté de diminuer l’exposition de la population pédiatrique aux rayonnements ionisants, en particulier les patients qui devront être surveillés régulièrement et dont l’espérance de vie progresse rapidement. La mucoviscidose est l’exemple le plus marquant (fig. 19-11). La surveillance par tomodensitométrie semble, selon certaines publications, pouvoir être effectuée par l’IRM [2]. L’IRM est également en cours d’évaluation par certaines équipes pour l’étude de la perfusion pulmonaire grâce à l’injection intraveineuse d’un complexe de gadolinium et l’utilisation de séquences rapides. D’autres pistes de recherche se dessinent aussi concernant, notamment, l’étude de la ventilation pulmonaire. Ces études sont prometteuses mais leur mise en œuvre est difficile car elle nécessite, par exemple, de disposer d’hélium polarisé dont la demi-vie est courte et de faire l’acquisition d’une chaîne radiofréquence spécifique onéreuse. Ces contraintes limitent la diffusion de ces techniques. 1. Durand C, Garel C, Nugues F, Baudain D. L’échographie dans la pathologie thoracique de l’enfant. J Radiol. 2001;82:729–737. 2. Eichinger M, Optazaitea DE, Kopp-Schneiderb A, et al. Morphologic and functional scoring of cystic fibrosis lung disease using MRI. Eur J Radiol. 2012;81:1321–1329. 3. Enriquez G, Aso C, Serres X. Chest US. In: Lucaya J, Strife JL, eds. Pediatric chest imaging. Berlin: Springer Verlag; 2008:1–35. 4. Enriquez G, Garcia-Peña P, Lucaya J. Pitfalls in chest imaging. Pediatr Radiol. 2009;39:S356–S368. 5. Garcia-Pena P. Helical chest CT. In: Lucaya J, Strife JL, eds. Pediatric chest imaging. Berlin: Springer Verlag; 2007:47–78. 6. Hassan M, Valois P. Le thymus. In: Hassan M, Valois P, eds. Guide d’interprétation de la radiographie thoracique de l’enfant. Paris: Flammarion Médecine-Sciences; 2005:84–102. 7. Hedlund GL, Griscom NT, Cleveland RH, Kirks DR. Respiratory system. In: Kirks DR, ed. Practical pediatric imaging. Diagnostic radiology of infants and children. Philadelphia: Lippincott-Raven; 1998:619–819. 8. Kim OH, Kim WS, Kim MJ, et al. US in the diagnosis of pediatrics chest diseases. RadioGraphics. 2000;20:653–671. 9. Pappas JN, Donnelly LF, Frush DP. Reduced frequency of sedation of young children with multisection helical CT. Radiology. 2000;215:897–899. 10. Pearce MS, Salotti JA, Little MP, et al. Radiation exposure from CT scans in childhood and subsequent risk of leukaemia and brain tumours : a retrospective cohort study. Lancet. 2012. 11. Swischuk LE. Respiratory system. The thymus : normal and abnormal. In: Swischuk LE, ed. Imaging of the newborn, infant and young child. Philadelphia: Lippincott Williams & Wilkins; 2004:17–29. 19.2 MALFORMATIONS BRONCHOPULMONAIRES : DIAGNOSTIC PRÉ- ET POSTNATAL Les malformations pulmonaires forment un groupe complexe de lésions dans lesquelles peuvent coexister des anomalies de l’arbre trachéobronchique, du parenchyme pulmonaire, de la vascularisation artérielle et de la vascu-larisation veineuse. Les associations malformatives sont fréquentes. Les classifications sont nombreuses et controversées. Clements et Warner [6] ont utilisé le terme de mali-nosculation (connexion congénitale anormale) pour décrire les différentes malformations et associations malformatives touchant ces quatre secteurs. Nous décrirons les principales malformations que sont les malformations adénomatoïdes kystiques ou malformations congénitales des voies aériennes pulmonaires, les séquestrations, les kystes bronchogé-niques, l’emphysème lobaire géant, l’atrésie bronchique, le syndrome CHAOS (congenital high airway obstruction syndrome), les agénésies ou aplasies pulmonaires et lobaires, les hypoplasies pulmonaires et les bronches glissées. L’approche diagnostique des malformations pulmonaires s’est modifiée depuis une dizaine d’années en raison du développement de l’imagerie anténatale et de la découverte de plus en plus fréquente de ces malformations in utero [8, 10, 11]. Toutefois, certaines malformations ne sont découvertes qu’après la naissance, en période néonatale ou plus tard dans l’enfance ou à l’âge adulte. Lorsque la malformation est dépistée in utero, le dossier est présenté au CPDPN (centre pluridisciplinaire de diagnostic prénatal). Le CPDPN propose aux parents : – des examens complémentaires, en fonction de la pathologie (caryotype, IRM fœtale, échocardiographie par un réfé-rent) ; – un entretien prénatal avec les pédiatres et chirurgiens pédiatriques qui expliquent les modalités de prise en charge néonatale, les indications et les techniques chirurgicales ; – une naissance en maternité de niveau 3 lorsqu’il existe un risque de détresse respiratoire néonatale. Le rôle de l’imagerie anténatale est d’évoquer un diagnostic, de rechercher des malformations associées, d’évaluer la gravité et d’assurer un suivi tout au long de la grossesse [3, 4]. En postnatal, le diagnostic de malformation étant posé, le rôle du radiologue est de préciser le type de malformation, son extension, de rechercher des complications et de planifier les examens complémentaires en fonction de la symptomatologie clinique. Le développement de l’arbre trachéo-broncho-pulmonaire est d’une grande complexité dont la finalité est de permettre, à la naissance, l’adaptation à la vie extra-utérine. Nous rappellerons quelques points essentiels [1, 2, 6, 12]. L’origine de l’arbre trachéo-broncho-pulmonaire est double : l’épithé-lium est d’origine endodermique et le mésenchyme d’origine mésodermique. Des études récentes montrent l’existence de nombreux gènes et facteurs de croissance qui jouent un rôle dans les interactions cellulaires entre dérivés endodermiques et mésodermiques. Le développement de l’arbre trachéo-broncho-pulmonaire est indissociable de l’environnement locorégional. Pendant la vie fœtale, des travaux expérimentaux [16] ont démontré l’existence d’un liquide pulmonaire sécrété par l’épithélium pulmonaire. Ce liquide, contenu dans les voies aériennes, peut être évacué dans le liquide amniotique par la trachée ou être dégluti. La rétention du liquide pulmonaire fœtal est responsable d’une distension pulmonaire, décrite dans les ligatures trachéales utilisées dans le traitement in utero des hernies diaphragmatiques.
RADIOGRAPHIE SIMPLE
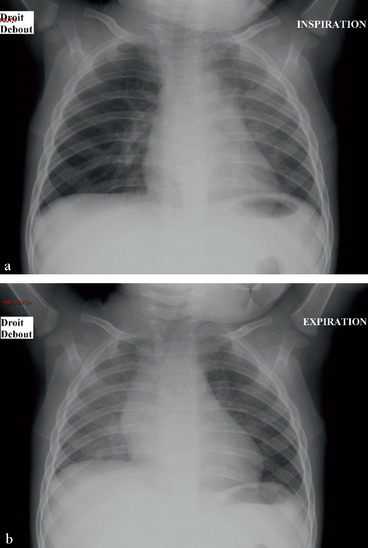
La radiographie en inspiration montre une hyperclarté du poumon droit. En expiration, le trappage s’effectue au niveau du poumon gauche, le corps étranger est donc situé dans la bronche souche gauche, comme l’a confirmé l’endoscopie.
Dans cette incidence les clavicules sont projetées au-dessus des apex pulmonaires.
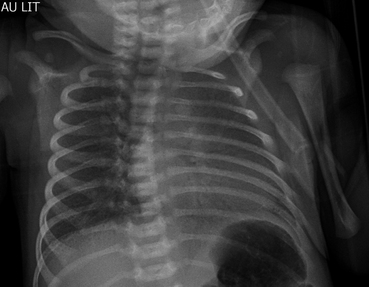
Dans cette incidence, les pièces sternales deviennent visibles et ne doivent pas être interprétées comme des masses anormales calcifiées intrathoraciques.
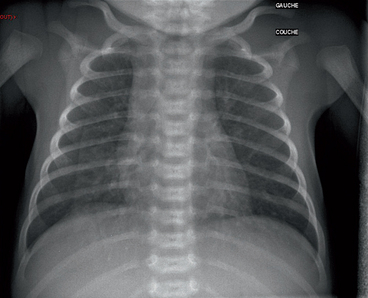
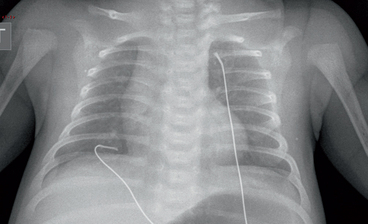
Présence d’un pli cutané se projetant sur le tiers externe du poumon droit, simulant un pneumothorax. Noter la présence d’une vascularisation pulmonaire entre cette ligne et la paroi thoracique.
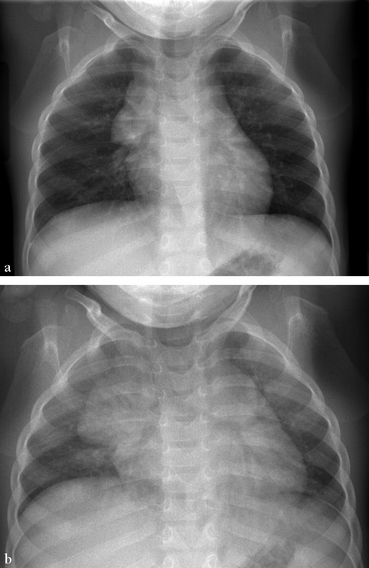
En inspiration, la trachée est rectiligne, mais en expiration elle se coude vers la droite. Le médiastin semble élargi en expiration.
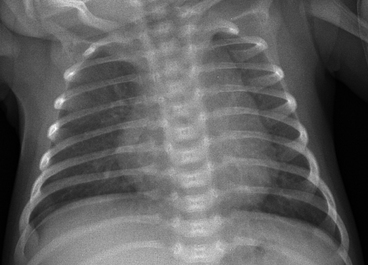
L’ondulation du bord gauche du médiastin est liée à l’invagination du thymus dans les espaces intercostaux.
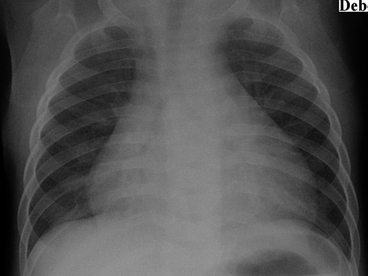
La vascularisation normale du parenchyme pulmonaire et la position normale des hiles pulmonaires à travers l’opacité thymique permettent d’éliminer le diagnostic de cardiomégalie.
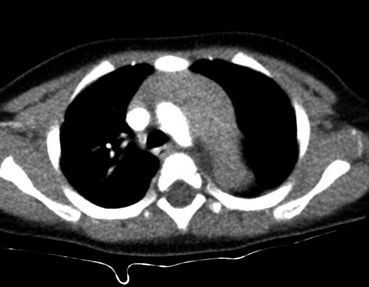
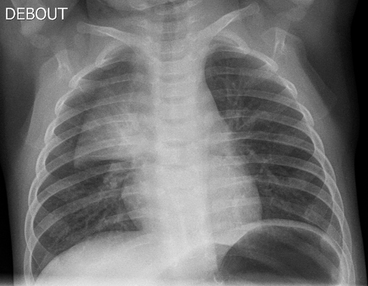
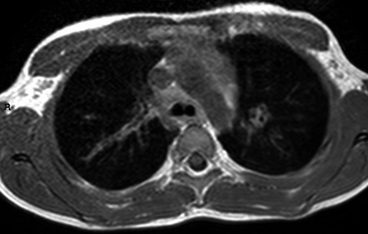
L’élargissement du médiastin supérieur gauche est dû au prolongement postérieur du thymus.
TOMODENSITOMÉTRIE
ÉCHOGRAPHIE
IMAGERIE PAR RÉSONANCE MAGNÉTIQUE
BIBLIOGRAPHIE
RAPPELS EMBRYOLOGIQUES
Développement de l’arbre trachéobronchique
![]()
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree


19: PARTICULARITÉS PÉDIATRIQUES