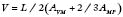Chapitre 19 Imagerie des flux et des valves
La mesure quantitative des flux par résonance magnétique à l’aide des séquences sensibles à la vélocité (SSV) est utilisée depuis les années 1980 [1] et a retrouvé un regain d’intérêt ces dernières années, depuis l’arrivée de gradients puissants et la réduction du temps d’acquisition qui en découle, permettant d’ajouter une information fonctionnelle indispensable à toute imagerie par résonance magnétique (IRM) cardiaque morphologique [2].
La stratégie diagnostique dans les valvulopathies a complètement changé depuis le développement de l’échocardiographie-doppler couleur, qui permet d’obtenir une information quasi complète pour planifier les options thérapeutiques [3–5]. De plus, elle reste la seule technique fiable permettant d’apporter une information morphologique, comme le nombre de feuillets valvulaires, l’épaississement valvulaire et les végétations dans les endocardites.
Les méthodes invasives telles que le cathétérisme et l’angiographie cardiaques sont maintenant limitées à l’évaluation préopératoire des artères coronaires, à l’exploration hémodynamique ou aux cas où il existe des discordances entre les données cliniques et les résultats de l’échocardiographie [6].
L’échocardiographie-doppler est habituellement très performante pour quantifier la sévérité des sténoses valvulaires, mais reste limitée dans la quantification des régurgitations où l’évaluation par doppler couleur est semi-quantitative et peut être gênée par des facteurs techniques ou hémodynamiques [7].
Ainsi, une méthode non invasive capable d’apporter toutes les informations nécessaires pour la surveillance et la planification de la chirurgie est toujours nécessaire avant l’apparition de la dysfonction ventriculaire. Des études récentes ont démontré que l’IRM pouvait être une technique alternative ou complémentaire à l’échocardiographie [8–12]. Cette technique apporte des informations anatomiques et fonctionnelles tridimensionnelles et, potentiellement, une mesure plus fiable et reproductible de la fonction ventriculaire que l’échocardiographie [13]. Les SSV autorisent une estimation exacte des profils de vélocité à travers une valve ou toute structure vasculaire permettant une quantification plus précise des flux et des valvulopathies que l’échocardiographie-doppler [14,15]. De plus, l’IRM n’est pas limitée par les problèmes de pénétration acoustique et permet une meilleure visualisation de la morphologie et des flux valvulaires dans les structures cardiovasculaires.
Techniques d’imagerie
Imagerie par résonance magnétique
Séquences spin-écho et fast spin-écho
Les séquences spin-écho et fast spin-écho synchronisées à l’électrocardiogramme (ECG) constituent encore la première étape dans l’évaluation des maladies valvulaires et des maladies caractérisées par une anomalie des flux telle qu’un shunt ou une sténose sur un gros vaisseau [16]. Les anomalies morphologiques des valves telles qu’une bicuspidie ou un épaississement valvulaire pourront être visualisées, de même que les conséquences d’une valvulopathie ou d’une anomalie congénitale telle qu’une dilatation d’une cavité ou une hypertrophie.
Habituellement, des images axiales transverses sont d’abord réalisées, suivies par un ou deux plans additionnels coronal et sagittal oblique dans le plan du court axe du cœur. Les séquences classiques tendent à être remplacées par les séquences turbo spin-écho en apnée avec la technique d’acquisition parallèle permettant de diminuer le temps d’acquisition en conservant la même résolution spatiale [17].
Séquences ciné-IRM
Dans ces séquences, le sang circulant est en hypersignal (sang blanc). Les flux anormaux rencontrés dans les valvulopathies (aussi bien les sténoses que les régurgitations), les sténoses vasculaires et les shunts sont responsables d’un déphasage des spins se traduisant par un hyposignal. Cet hyposignal est dû aux turbulences et accélérations du flux au sein du sang circulant normal en hypersignal [18]. Mais il est dépendant de facteurs techniques : les paramètres de visualisation de l’image, l’angle de bascule et surtout le TE. Il est bien visible sur les séquences avec TE longs (12 ms) alors qu’il tend à disparaître sur les séquences avec TE courts [19].
Actuellement, ces séquences ont été remplacées par les techniques ultrarapides « balancées » permettant de renforcer l’aimantation transversale résiduelle (imagerie à l’état d’équilibre) avec des TR de 4 à 8 ms et des TE de 2 à 4 ms. Ces séquences (Truefisp™, Fiesta™ ou Balanced FFE™) associées aux techniques d’acquisition parallèle (SENSE) permettent de réduire considérablement le temps d’acquisition compatible avec une apnée, éliminant ainsi les artéfacts respiratoires, et sont caractérisées par un meilleur contraste entre le myocarde et le sang circulant [17]. Elles sont moins performantes pour démontrer les anomalies de flux rencontrées dans les valvulopathies, les sténoses vasculaires et les shunts à cause du TE court employé, mais sont idéales pour évaluer la fonction ventriculaire globale et segmentaire, calculer les volumes ventriculaires, la fraction d’éjection et la masse cardiaque [20].
Séquences sensibles à la vélocité
Les SSV ou imagerie de phase sont basées sur le principe que la phase des spins mobiles (sang circulant), par rapport aux spins stationnaires le long d’un gradient de champ magnétique, change en directe proportion avec la vélocité du flux. La méthode permet la quantification des profils de vélocité du sang à différents moments du cycle cardiaque [21,22].
Le changement de phase, proportionnel à la vélocité, est visualisé sous la forme de variations d’intensité de pixels sur l’image de phase. Les tissus stationnaires apparaîtront en gris alors que les flux ayant une direction positive ou négative apparaîtront sous la forme de pixels blancs ou noirs. Ainsi, il est possible de différencier les flux antérogrades des flux rétrogrades [23]. L’encodage de la vélocité peut se faire soit dans un plan perpendiculaire à la direction du flux en utilisant la direction du gradient de sélection de coupe (mesure de la vélocité à travers le plan de coupe), soit dans un plan parallèle à la direction du flux en utilisant la direction du gradient de codage de phase ou de fréquence (mesure de la vélocité dans le plan de coupe) ou, plus récemment, dans les trois dimensions [2].
La mesure de la vélocité sera d’autant plus précise que la vélocité encodée est proche de la vélocité réelle de la structure vasculaire ou valvulaire d’intérêt. Plusieurs mesures sont ainsi souvent nécessaires avec des seuils de vélocité différents. Le gradient de pression à travers une sténose valvulaire ou vasculaire sera calculé grâce à l’équation de Bernoulli modifiée : ΔP = 4 · (Vmax)2 [1,24,25]. Des études récentes ont montré une bonne corrélation entre les mesures de vélocité maximales effectuées au doppler et en imagerie de phase, avec toutefois une tendance à la surestimation des vélocités au doppler jusqu’à 25 % [26,27]. Les reconstructions en magnitude de ces séquences à TE court, limitant le phénomène d’hyposignal en rapport avec l’anomalie de flux, seront également très utiles pour étudier la morphologie d’une valve anormale et le calcul direct de la surface valvulaire par planimétrie.
Scanner multicoupes
Pour explorer les valves en scanographie multicoupe, on va utiliser les mêmes paramètres techniques que pour l’exploration des coronaires. L’utilisation d’un scanner avec 64 à 320 barrettes sera bien sûr préférable, permettant l’acquisition des données en quelques secondes, compatible avec une apnée dans la majorité des cas. La synchronisation avec l’ECG est obligatoire et il sera préférable d’utiliser la synchronisation rétrospective plutôt que prospective, permettant la reconstruction de coupes chevauchées à de multiples phases du cycle cardiaque. Ainsi, des images statiques reconstruites à une phase donnée du cycle seront utiles pour l’étude morphologique (en général à 60–75 % du cycle lorsque le cœur est momentanément « arrêté ») alors que la reconstruction en multiphase offre une approche dynamique et fonctionnelle [28].
Actuellement, les scanners les plus performants permettent l’acquisition de 64 à 320 coupes de 0,65 mm d’épaisseur avec un temps de rotation du tube inférieur à la seconde, couvrant 140–160 mm en hauteur avec un pitch de 0,24–0,3 et une vitesse de déplacement de table d’environ 7 mm/s, 100–120 kV et 300–400 mAs. Des coupes sans injection de produit de contraste sont réalisées dans un premier temps afin d’évaluer les éventuelles calcifications des valves et des artères coronaires. Ensuite, une série de coupes injectées est pratiquée avec 80 à 100 ml de produit de contraste non ionique hypo-osmolaire (350–400 mgI/ml) avec un débit de 5 ml/s suivi d’un bolus de sérum physiologique pour minimiser les artéfacts de contraste au niveau de la veine cave supérieure [29].
Les reconstructions des images natives seront ensuite effectuées en rendu de volume mono- et multiphase, avec création d’une boucle cinéma, de même qu’en MPR (multiprojection reformat) dans le plan de la valve et selon les axes traditionnels du cœur (quatre cavités, deux cavités, long axe, court axe). Là aussi, la reconstruction dans ces différents plans en multiphase permet une analyse fonctionnelle de la valve elle-même, ainsi que de l’évaluation de la fonction globale et régionale des ventricules [30].
Applications cliniques
Valves cardiaques et valvulopathies
Anatomie des valves cardiaques
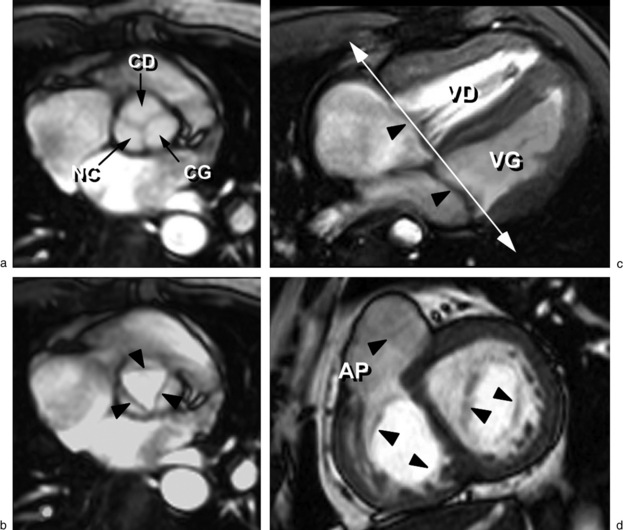
Les valves semi-lunaires aortique et pulmonaire sont pourvues de trois valvules sigmoïdes caractérisées par de minces replis membraneux qui réalisent des poches en nid-de-pigeon avec la paroi artérielle sur laquelle elles sont insérées. Sur des coupes transverses de l’orifice aortique ou pulmonaire, elles apparaissent sous la forme d’un Y lorsqu’elles sont fermées. Au niveau de l’orifice aortique, la valvule sigmoïde coronaire droite se situe en avant, la coronaire gauche se situe en arrière et à gauche alors que la sigmoïde non coronaire se situe en arrière et à droite (fig. 19.1).
Les valves auriculoventriculaires sont au nombre de deux. À droite, la valvule tricuspide comprend trois feuillets, antérieur, postérieur et septal, présentant des insertions sur le septum interventriculaire. À gauche, la valvule mitrale comprend deux feuillets, antérieur et postérieur, sans aucune attache septale. La valvule mitrale présente deux muscles papillaires bien individualisés : les muscles papillaires postéromédian et antérolatéral, alors que la valvule tricuspide présente de multiples muscles papillaires dont un est mieux individualisé : le muscle papillaire antérieur. Il existe une continuité directe entre l’anneau mitral et l’anneau aortique, alors que la valvule tricuspide est séparée de la valve pulmonaire par l’infundibulum, chambre de chasse du ventricule droit (fig. 19.1).
Insuffisance aortique
La conséquence hémodynamique majeure d’une insuffisance aortique progressive est une augmentation du volume télédiastolique du ventricule gauche, qui reste longtemps asymptomatique. La chirurgie doit être décidée avant ou dès l’apparition des symptômes, mais surtout avant le développement de la dysfonction ventriculaire gauche. Ainsi, une surveillance rapprochée des patients permettant une mesure précise de la sévérité de la régurgitation ainsi que l’évaluation de la fonction ventriculaire sont fondamentales.
Le cathétérisme cardiaque et l’angiographie demeurent les examens de référence pour apprécier la sévérité d’une insuffisance aortique, et restent pour l’instant nécessaires pour l’évaluation préopératoire des artères coronaires dans la pratique courante. Toutefois, le cathétérisme est invasif, la gradation de la régurgitation reste imprécise et il existe une sous-estimation de la régurgitation dans les insuffisances aortiques sévères. Ainsi, le besoin d’une méthode non invasive capable d’évaluer directement le volume de régurgitation aussi bien que la fonction ventriculaire reste nécessaire, et l’IRM est reconnue depuis plusieurs années comme la méthode susceptible de jouer ce rôle [7].
L’insuffisance aortique peut être due à des anomalies des valves sigmoïdes, une lésion de l’anneau et/ou une dilatation de la racine aortique. Les causes les plus fréquentes sont la maladie annuloectasiante associée ou non à un syndrome de Marfan, la bicuspidie aortique congénitale, les séquelles d’endocardite ou de rhumatisme articulaire aigu. L’insuffisance aortique aiguë peut être due à une endocardite infectieuse, une dysfonction d’une prothèse, un traumatisme ou une dissection aortique.
Méthodes d’évaluation de l’insuffisance aortique
Mesure de la surface et de la longueur de l’hyposignal sur les images de ciné-IRM
Les flux anormaux rencontrés dans les régurgitations sont dus à un déphasage des spins en rapport avec les turbulences et hautes vélocités rencontrées se traduisant par un hyposignal au sein du sang circulant normal en hypersignal [19].
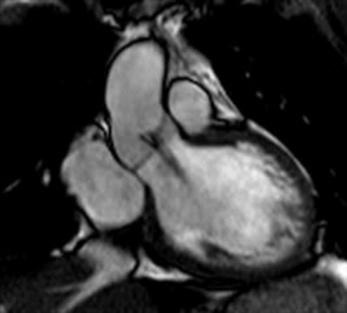
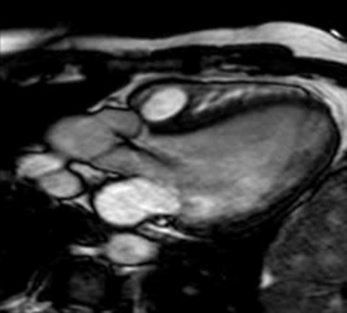
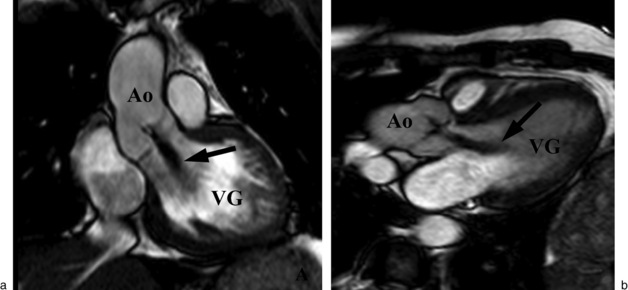
La régurgitation aortique est identifiée par la mise en évidence d’un hyposignal se propageant depuis la valve aortique incompétente dans le ventricule gauche pendant la diastole ventriculaire. Elle sera le mieux démontrée dans les deux plans suivants : le plan coronal centré sur la chambre de chasse du ventricule gauche et le long axe du ventricule gauche (fig. 19.2, ![]() vidéos 19.1a et 19.1b). Ce flux anormal de régurgitation est une structure tridimensionnelle qui peut changer de forme et de direction d’un patient à l’autre, en fonction du type d’altération valvulaire rencontrée et au cours du cycle cardiaque chez le même patient. Ainsi, la taille apparente de l’hyposignal peut varier d’un plan à un autre, il est donc recommandé d’utiliser plusieurs incidences pour évaluer sa taille [10].
vidéos 19.1a et 19.1b). Ce flux anormal de régurgitation est une structure tridimensionnelle qui peut changer de forme et de direction d’un patient à l’autre, en fonction du type d’altération valvulaire rencontrée et au cours du cycle cardiaque chez le même patient. Ainsi, la taille apparente de l’hyposignal peut varier d’un plan à un autre, il est donc recommandé d’utiliser plusieurs incidences pour évaluer sa taille [10].
Toutefois, ces mesures ne représentent que des indices semi-quantitatifs de la sévérité de la régurgitation [9,31,32].
Les limites de l’hyposignal sont tracées manuellement sur l’image où le jet de régurgitation apparaît le plus important dans l’espace RR. Ce dernier peut donc varier considérablement en fonction des paramètres de visualisation de l’image et d’un observateur à l’autre, de même qu’en fonction d’éventuelles modifications physiopathologiques (modifications de la distribution du jet de régurgitation dues aux changements de volume et de pression dans la cavité réceptrice), expliquant les limites de la méthode. D’autre part, il est bien visible sur les séquences en écho de gradient avec TE longs (12 ms), alors qu’il tend à diminuer voire disparaître sur les séquences ciné-IRM avec TE courts [19] ultrarapides « balancées » (imagerie à l’état d’équilibre) utilisant des TE de 2 à 4 ms.
Calcul de la fraction de régurgitation à partir de la mesure des volumes ventriculaires sur les images de ciné-IRM
Une méthode très pratique pour mesurer les volumes ventriculaires est d’utiliser la formule de Simpson modifiée où la surface des ventricules est mesurée sur deux courts axes et la longueur des cavités est mesurée sur l’incidence des quatre chambres [33]. La formule utilisée est la suivante :
Dans un cœur normal, le volume d’éjection ventriculaire droit (VEVD) et le volume d’éjection ventriculaire gauche (VEVG) sont identiques. Le volume d’éjection ventriculaire est la différence entre le volume télédiastolique (habituellement calculé sur la première image du cycle après l’onde R) et le volume télésystolique (calculé sur l’image du cycle cardiaque où la plus petite surface ventriculaire est visualisée). La différence de volume d’éjection entre un ventricule régurgitant (ventricule gauche dans les régurgitations mitrale et aortique) et un ventricule normal (ventricule droit) représente le volume de régurgitation (VReg). La fraction de régurgitation (FR) est ainsi le VReg divisé par le volume d’éjection systolique du ventricule régurgitant. La FR a été utilisée pour évaluer la sévérité de la régurgitation : légère : FR = 15–20 %, modérée : FR = 20–40 %, sévère : FR > 40 % [33].
Calcul de la fraction de régurgitation à partir de la mesure des volumes d’éjection ventriculaires sur les SSV
Une autre façon de calculer les volumes d’éjection des ventricules droit et gauche consiste à mesurer le flux dans l’aorte ascendante et l’artère pulmonaire dans un plan perpendiculaire à ces vaisseaux grâce aux SSV [24]. Le flux (débit) est le produit de la vélocité moyenne dans le vaisseau considéré par la surface du vaisseau sur chaque phase du cycle cardiaque. L’intégration du flux pour toutes les images pendant la systole permet la mesure du flux systolique. Ainsi, les volumes d’éjection systolique des ventricules droit et gauche peuvent être calculés respectivement.
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree