Chapitre 18 Pathologies du péricarde
L’échocardiographie détient une place fondamentale dans la détection et dans la prise en charge des pathologies du péricarde, permettant à la fois une analyse morphologique et une évaluation précise de la fonction cardiaque. Sa très grande disponibilité, sa faisabilité au lit du patient et l’absence d’utilisation de rayonnements ionisants en font un examen de première intention. Mais le caractère peu échogène de certains patients, les fenêtres acoustiques réduites ne permettant pas une exploration de la totalité du péricarde, et l’imprécision pour la détection d’épaississement péricardique attestent des limites de cet examen. L’échocardiographie par voie transœsophagienne a permis d’améliorer la résolution, mais le champ de vue étroit est une de ses principales limites [1].
Anatomie
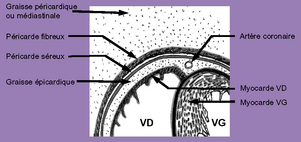
Le péricarde est un sac conique de moins de 2 mm d’épaisseur, contenant le cœur et la racine des gros vaisseaux. Il est composé de deux enveloppes, l’une fibreuse, le péricarde pariétal, qui est en continuité avec l’autre, une membrane séreuse recouvrant la totalité des cavités cardiaques, le péricarde viscéral ou épicarde (fig. 18.1). La ligne de réflexion de ces deux feuillets se situe à 2 cm au-dessus des anneaux pulmonaire et aortique. La cavité ainsi délimitée contient le liquide péricardique (de 20 à 30 ml), apparaissant comme un ultrafiltrat du plasma sanguin, avec un taux faible de protéine et une pression osmotique basse (un peu moins du quart de la pression plasmatique) [2].
Le péricarde assure essentiellement deux fonctions :
Le scanner et l’IRM offrent une excellente visualisation du péricarde, grâce notamment au contraste naturel apporté par la graisse médiastinale d’une part, et la graisse épicardique d’autre part. Ce contraste permet une visualisation constante du péricarde en regard des cavités droites [4]. En revanche, la sensibilité est de seulement 61 % en regard de la paroi latérale du ventricule gauche, de par le plus faible contraste apporté par le poumon [5]. L’épaisseur du péricarde mesurée en tomodensitométrie (TDM) ou en IRM est variable en fonction de la phase du cycle cardiaque. En IRM, son épaisseur varie de 1,2 mm en diastole à 1,9 mm en systole [5]. L’insertion du ligament phrénopéricardique dans le diaphragme majore l’épaisseur du péricarde sur des coupes axiales [6]. La mesure de l’épaisseur péricardique doit être réalisée en regard de la partie moyenne des ventricules aussi bien en TDM qu’en IRM, et doit être inférieure à 2 mm [5,7]. En TDM, il apparaît comme un fin liseré dont la densité est proche de celle de l’eau. En IRM, il apparaît en hyposignal sur les séquences pondérées T1 et T2. La connaissance des différents replis anatomiques est fondamentale pour éviter des interprétations de fausses images de dissection aortique, d’adénomégalies ou de masses médiastinales [8,9] :
Épanchement péricardique
Le scanner et l’IRM permettent non seulement d’apprécier la quantité de liquide, mais aussi de caractériser la nature de l’épanchement. Les causes les plus fréquentes sont les infections (virales ou bactériennes), les causes tumorales (cancer du sein, du poumon, ou lymphome malin), l’infarctus du myocarde, l’insuffisance cardiaque, l’insuffisance rénale, l’hypoprotidémie, l’hypothyroïdie, le chylopéricarde, et les traumatismes. Un épanchement est de quantité modérée quand l’épaisseur mesurée est supérieure à 5 mm et de grande abondance quand l’épaisseur mesurée est supérieure à 20 mm [5]. Les épanchements cloisonnés sont bien individualisés en TDM et surtout en IRM en raison de leur large champ de vue.
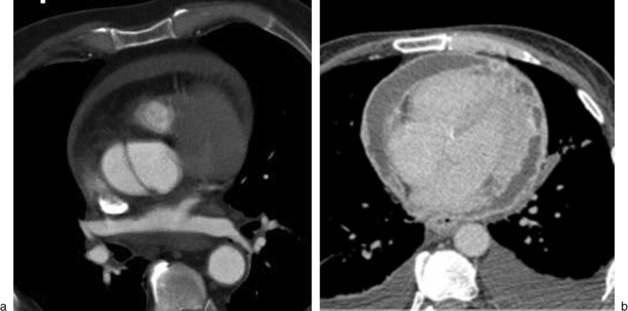
La caractérisation du liquide péricardique en TDM, par la mesure de densité, permet de préciser la nature étiologique de l’épanchement : une densité strictement liquidienne oriente vers un épanchement de nature bénigne (type péricardite virale ou idiopathique le plus souvent) ; une densité plus élevée (supérieure à 20 unités Hounsfield [UH]) sera plus en faveur d’un épanchement de nature néoplasique, d’un hémopéricarde, d’un exsudat purulent ou d’un épanchement intégré dans le cadre d’une hypothyroïdie ; enfin, une densité négative sera en faveur d’un épanchement intégré dans le cadre d’un chylopéricarde [13]. La présence d’un épaississement irrégulier du péricarde, voire de nodules ou de masses péricardiques associés, sera en faveur d’un épanchement néoplasique (fig. 18.2).
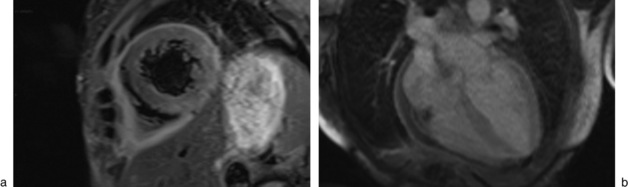
L’IRM permet aussi une caractérisation de la nature du liquide péricardique : un épanchement hémorragique apparaît en hypersignal sur les séquences pondérés T1 alors qu’un épanchement non hémorragique apparaît en hyposignal sur ces séquences pondérées T1 (et en hypersignal sur les séquences pondérées T2) [14]. En revanche, l’analyse du signal ne peut distinguer un épanchement exsudatif et transsudatif. L’IRM est très utile pour le diagnostic des péricardites aiguës (fig. 18.3) en montrant un péricarde en hypersignal T2 et se rehaussant après injection de gadolinium.
Péricardites constrictives
Les causes sont multiples (tableau 18.1). Les plus fréquentes actuellement sont les péricardites constrictives secondaires à la chirurgie cardiaque et à la radiothérapie, puis viennent les étiologies infectieuses avec notamment la tuberculose (étiologie la plus fréquente dans les pays du tiers-monde), les maladies de système, les péricardites néoplasiques, l’insuffisance rénale, les péricardites métaboliques avec notamment la péricardite urémique, et enfin les péricardites idiopathiques [15,16].
Tableau 18-1 Principales étiologies des péricardites constrictives.
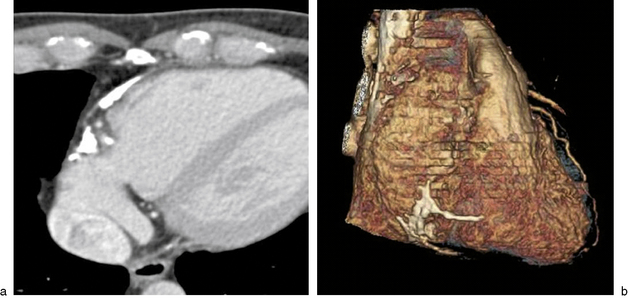
La présence d’un épaississement péricardique, défini par une épaisseur péricardique supérieure à 4 mm [5,17], associée à un tableau clinique évocateur, est très suggestive d’une péricardite constrictive, approchant une sensibilité diagnostique de 93 % [17]. Cet épaississement peut être focal ou diffus (le plus souvent bien visualisé sur le bord droit du cœur) [18]. Le scanner peut apporter des arguments supplémentaires en retrouvant des calcifications péricardiques, souvent associées dans les péricardites constrictives (fig. 18.4). D’autres signes peuvent être retrouvés, comme un volume ventriculaire droit réduit avec aspect tubulé (notamment en diastole où la fibrose péricardique empêche la bonne expansion ventriculaire), la présence d’une dilatation de la veine cave inférieure et des veines sus-hépatiques, et une hépatomégalie. Enfin, un mouvement paradoxal du septum est souvent retrouvé en ciné-IRM (fig. 18.5, ![]() vidéo 19.1). Ce mouvement du septum vers les cavités gauches en début de diastole est un signe relativement sensible, mais qui se voit dans d’autres circonstances. Il est indispensable de réaliser des séquences en temps réel ou en fin d’expiration pour sensibiliser la visualisation de ce mouvement septal anormal, parfois non visible en inspiration. Des séquences de tagging sont également recommandées pour rechercher des adhérences péricardiques qui se traduisent par une absence de rupture des lignes de marquage par opposition au péricarde libre qui glisse lors du cycle, entraînant une cassure nette des lignes de tagging (fig. 18.5,
vidéo 19.1). Ce mouvement du septum vers les cavités gauches en début de diastole est un signe relativement sensible, mais qui se voit dans d’autres circonstances. Il est indispensable de réaliser des séquences en temps réel ou en fin d’expiration pour sensibiliser la visualisation de ce mouvement septal anormal, parfois non visible en inspiration. Des séquences de tagging sont également recommandées pour rechercher des adhérences péricardiques qui se traduisent par une absence de rupture des lignes de marquage par opposition au péricarde libre qui glisse lors du cycle, entraînant une cassure nette des lignes de tagging (fig. 18.5, ![]() vidéo 19.2).
vidéo 19.2).
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree