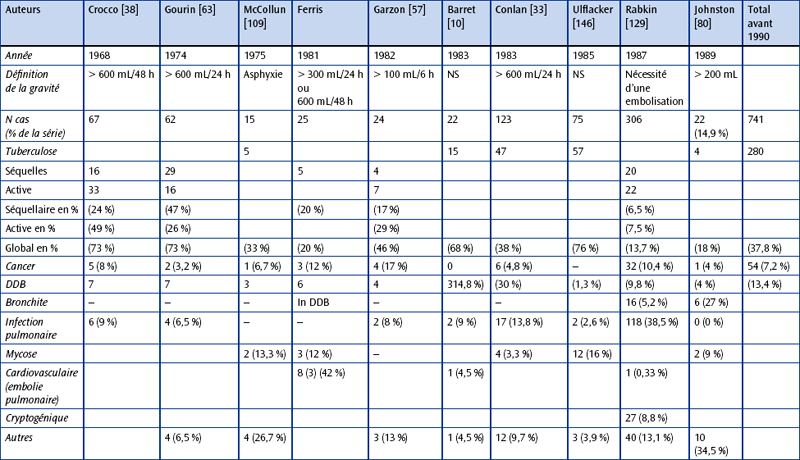
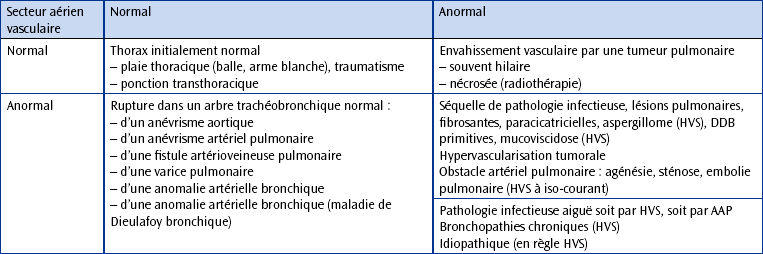
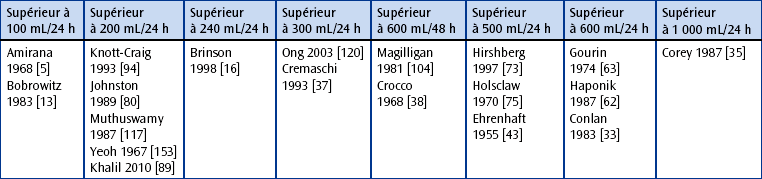
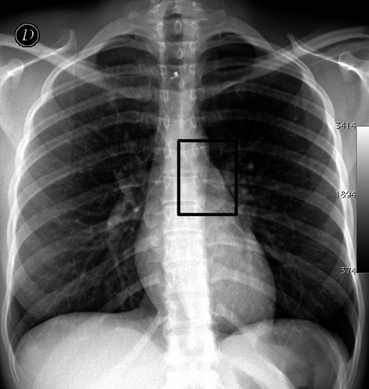
CHAPITRE 18 ASPECTS PARTICULIERS DES HÉMOPTYSIES : PHYSIOPATHOLOGIE, DIAGNOSTIC ET TRAITEMENT L’hémoptysie est l’extériorisation de sang à partir du secteur aérien sous-glottique. Elle correspond au passage de sang du secteur vasculaire thoracique vers le secteur aérien sous-glottique. L’abord des différents mécanismes physiopathologiques des hémoptysies, et en particulier des hémoptysies graves [24], demande une bonne connaissance de l’ensemble de la vascula-risation intrathoracique normale et de ses modifications pathologiques. L’apport de l’imagerie dans l’hémoptysie est diagnostique et thérapeutique. Sur le plan diagnostique, c’est l’utilisation récente de l’angiographie par tomodensitométrie volumique (ATDMV) qui permet, en plus de la localisation et de l’appréciation de la gravité du saignement, la visualisation du mécanisme artériel bronchique ou pulmonaire orientant ainsi la thérapeutique endovasculaire ou chirurgicale [26, 90]. Sur le plan thérapeutique, l’artériographie bronchique avec embolisation ainsi que la vaso-occlusion artérielle pulmonaire sont devenues les modalités thérapeutiques de première intention chez la majorité des patients admis pour hémoptysie en réanimation. Dans ce chapitre, nous allons détailler la clinique, l’angio-anatomie vasculaire bronchique normale et pathologique, les principales étiologies, la technique et l’apport de l’ATDMV, notamment sur le mécanisme, et enfin le traitement endovasculaire. – une hématémèse : faite de sang plus noir, parfois mêlée à des aliments et s’accompagnant d’efforts de vomissements ; – un saignement d’origine ORL : une épistaxis, en général retrouvée à l’interrogatoire et confirmée par un examen ORL. Certains patients atteints de la maladie de Rendu-Osler sont susceptibles d’avoir soit des épistaxis, soit des hémoptysies par rupture de malformations artérioveineuses pulmonaires (MAVP), mais les épistaxis sont infiniment plus fréquentes. D’autres types de saignement ORL peuvent être très trompeurs : c’est le cas de rupture ou fissuration d’anévrisme carotidien chez des malades ayant des antécédents de cancer ORL. On propose chez ces patients d’inclure l’exploration des vaisseaux cervicaux en même temps que l’exploration du thorax en ATDMV. Plus rare que le type précédent, elle correspond à une hémoptysie dont les caractéristiques la rendent menaçante pour la vie du patient, réclamant un traitement spécifique, même si sa valeur symptomatique reste identique au type précédent, conduisant à une enquête étiologique si cette étiologie n’est pas évidente ou connue, éventuellement différée par rapport au traitement propre de l’hémoptysie. La caractéristique clinique qui conditionne le classement en hémoptysie « maladie » est l’abondance de cette hémoptysie, estimée à plus de 50 mL de sang expectoré. Ce critère est pris ici arbitrairement, au vu de notre expérience de plus de 1 500 hémoptysies traitées à l’hôpital Tenon depuis 20 ans. Au-delà de ces 50 mL qui réclament de mettre le patient en milieu spécialisé (au mieux, réanimation respiratoire), le second seuil de 200 mL ou une mauvaise tolérance sera pris pour critère de gravité incluant le patient dans une filière de prise en charge thérapeutique d’urgence multidisciplinaire. La quantification du volume étant difficile, nous pratiquons dans notre centre une échelle en fonction des ustensiles disponibles (fig. 18-1) qu’on présente au patient lors de l’interrogatoire [123]. La gravité selon le volume et le débit dans la littérature est très variable, avec un débit allant de 100 mL724 h à 1 000 mL/24 h (tableau 18-1). Ainsi, pour un volume supérieur à 600 mL/16 h, Crocco et al. [38] rapportaient une mortalité opératoire de 23 % comparativement à 78 % chez les patients opérables mais qui avaient été traités médicalement. De plus, ce volume par 24 heures est à corréler avec la réserve respiratoire des patients. Tableau 18-1 Estimation de la gravité d’une hémoptysie en fonction de la quantité selon la littérature. Fig. 18-1 Échelle de quantification du volume de l’hémoptysie utilisée dans l’unité de réanimation à l’hôpital Tenon. Source : adaptée de Parrot et al. [122]. Par ailleurs, la gravité de l’hémoptysie n’est pas uniquement fonction du volume ou du débit de sang émis, mais également du terrain sur lequel elle survient et de ses conséquences. En effet, une hémoptysie de faible abondance chez un patient insuffisant respiratoire chronique ou aux capacités de toux altérées peut rapidement conduire à une détresse respiratoire et doit être considérée comme grave. De même, toute hémoptysie est grave, quel que soit son volume, lorsqu’elle entraîne une hypoxémie ou un état de choc [103]. Certains auteurs ont proposé une définition plus « fonctionnelle » de la gravité, prenant en compte, outre le débit de l’hémoptysie, les comorbidités du patient, le retentissement clinique de l’hémoptysie et la nécessité d’administrer un traitement vasoconstricteur par voie générale [48, 105, 109]. Ainsi, pour Mal et al. [105], l’hémoptysie « menaçant la vie » est définie par un débit de sang supérieur à 200 mL/h en cas de fonction respiratoire normale, 50 mL/h chez un patient ayant une insuffisance respiratoire chronique ou plus de deux épisodes d’hémoptysie modérée malgré la prescription de terlipressine par voie générale. Bien que la définition de la gravité paraisse utile pour homogénéiser la prise en charge, elle est cependant limitée par la difficulté d’évaluer précisément le volume ou le débit de sang émis en pratique clinique, et peu d’auteurs proposent une méthode d’évaluation standardisée [48]. Angio-anatomie thoracique normale La vascularisation intrathoracique normale est formée de deux systèmes circulatoires à visée bronchopulmonaire, l’un nourricier (artères bronchiques), l’autre fonctionnel (artères pulmonaires). En pathologie, d’autres vaisseaux participeraient à la genèse de l’hémoptysie tels les artères systémiques non bronchiques (ASNB) et plus rarement les gros vaisseaux de trajet intrathoracique. En cas d’hypervascularisation systémique avec symphyse pleurale, les ASNB sont recrutées dans l’hypervascularisation systémique, participant ainsi à l’hémoptysie. Les gros vaisseaux sont rarement à l’origine d’un saignement. Leur participation se fait soit par érosion tumorale ou infectieuse, soit par rupture traumatique, mais aussi pour l’aorte thoracique par fissuration d’un anévrisme ou d’une dissection dans les voies aériennes. C’est la circulation nourricière du poumon, où règne un régime de haute pression. À l’état normal, la circulation bronchique est grêle avec des capacités d’adaptation considérables [47]. Les artères bronchiques mesurent moins de 1,5 mm à leur origine, leur calibre diminue à 0,75-0,50 mm à leur entrée dans un segment pulmonaire. Cela explique que les artères bronchiques normales peuvent être visibles à leur naissance sans être visibles au-delà lorsqu’il n’y a pas d’hypervascularisation systémique (HVS). Elles se résolvent en un réseau nourricier pour les éléments du hile, le péricarde, l’œsophage, la plèvre médiastinale, la paroi aortique et, enfin, pour les parois des bronches, des artères et des veines pulmonaires et pour les parois alvéolaires. Les artères bronchiques naissent habituellement de la face antérieure de l’aorte thoracique descendante (fig. 18-2), en regard de la bronche souche gauche [26, 27, 101]. Le niveau de naissance des artères bronchiques en ATDMV est visualisé au niveau de la paroi antérieure et latérale droite de l’aorte thoracique descendante, sur les coupes passant par la bronche souche gauche (T5) ou un peu au-dessus (fig. 18-3a). L’ostium est plutôt visible en latéral droit pour la naissance d’un tronc broncho-intercostal droit (TBICD) ou d’une artère bronchique droite (ABD), plutôt antérieur pour les troncs bronchiques communs droit/gauche (TBCDG) et les artères bronchiques gauches (ABG) qui peuvent être également légèrement antérieures gauches, mais il faut aussi les chercher venant franchement de la région antéro-latérale droite (fig. 18-3b), voire d’un tronc commun avec un tronc broncho-intercostal droit (fig. 18-4). Chaque arbre bronchique droit et gauche est vascularisé par trois artères bronchiques : une supérieure, une moyenne ou lingulaire et une inférieure (fig. 18-5 et 18-6). Les troncs artériels donnant naissance à ces branches de division naissent de façon variable de l’aorte, au nombre moyen de 2,7. Nous distinguons quatre grands types de naissance : par un TBICD, par un TBCDG et/ou par un tronc bronchique droit et/ou bronchique gauche ; chaque artère peut également naître isolément, directement de l’aorte. Fig. 18-2 Radiographie thoracique de face, la zone au sein du cadre étant celle où se trouve l’origine des artères bronchiques eutopiques. Fig. 18-3 Coupes TDM dans le plan axial en fenêtre médiastinale. Fig. 18-4 Artère bronchique gauche naissant de la partie initiale d’un tronc broncho-intercostal droit. Fig. 18-5 Variabilité de l’origine des artères bronchiques. Source : adaptée de Cauldwell et al. [27]. Fig. 18-6 Visualisation chez un patient de l’ensemble de la vascularisation bronchique. Le TBICD (fig. 18-7) correspond à un tronc commun donnant un tronc bronchique droit et un tronc intercostal droit ou une artère intercostale (AIC), quasiment toujours à destinée supérieure droite (le plus souvent 2e à 5e AIC droites). Le tronc bronchique donne souvent l’artère bronchique supérieure. La fréquence globale du TBICD varie de 81 à 97,5 %. Il n’est pas facilement appré-hendable en MIP fin car, naissant de la face latérale droite de la portion initiale de l’aorte thoracique, après un trajet initial assez rectiligne vers le haut et le dehors, le tronc donne naissance, lors de sa division, à une intercostale ou à un tronc d’intercostales supérieures droites qui part vers l’arrière en poursuivant vers le haut le trajet initial, tandis que le tronc bronchique part vers l’avant, faisant une crosse pour rejoindre la partie supérieure de la paroi postérieure de la bronche souche droite, passant initialement en arrière de la partie basse de la trachée. Dans la majorité des cas, ce tronc bronchique va donner les trois artères bronchiques droites. On le suit donc le plus souvent sur plusieurs coupes et son aspect est souvent très évocateur ; aussi, il est rarement utile de faire une reconstruction en 3D-VRT pour le reconnaître (fig. 18-7c). Fig. 18-7 Tronc broncho-intercostal droit. Le TBCDG correspond à un tronc donnant des artères bronchiques à destinées droite et gauche (fig. 18-8). Au maximum, ce tronc peut donner l’ensemble de la vascularisation bronchique, mais ce cas est rare (< 4 % des cas). Les troncs bronchiques, droits ou gauches, donnent des artères bronchiques exclusivement à droite ou à gauche. La répartition la plus fréquente (27 à 41 %) serait la naissance, à droite, d’un TBICD donnant toutes les artères bronchiques droites, avec à gauche deux troncs bronchiques gauches isolés (tableau 18-2). Quelle que soit la disposition, un TBICD est présent chez plus de 80 % des patients. Cette disposition n’est pas anodine car le rameau spinal antérieur médian du territoire dorsal moyen peut naître des intercostales naissant du TBICD (fig. 18-9). En effet, le rameau spinal antérieur médian naît en règle des 2e, 3e ou 4e intercostales droites ou gauches (le plus souvent gauches). Tableau 18-2 Nombre et fréquence des artères bronchiques chez 126 patients explorés par angio-TDM volumique et angiographie bronchique (série personnelle). Notez la fréquence élevée des troncs broncho-intercostaux et des troncs bronchiques communs. Fig. 18-8 Tronc bronchique commun (TBC) avec une sténose ostiale. Fig. 18-9 Opacification d’un tronc broncho-intercostal droit (TBICD). La naissance des artères bronchiques peut être atypique, toujours au niveau du plancher de l’arche aortique (fig. 18-10), position que nous avons retrouvée pour 45 (75 %) des 60 artères ectopiques trouvés chez 55 soit 43 % des 126 patients chez qui 283 artères étaient visualisées [91] ; c’est pourquoi nous les qualifierons seulement d’atypiques. Ce fait est retrouvé par Hartmann et al. [68] qui, chez 251 patients étudiés, en trouvent 36 % ayant au moins une artère bronchique ectopique, soit 77 patients, chez qui étaient observés 124 troncs ou artères bronchiques en position ectopique. Sur ces 124 positions ectopiques, 92 soit 74 % venaient de la concavité ou paroi inférieure ou « plancher » de l’arc aortique. Il peut s’agir aussi de sa paroi latérale droite, postérieure, localisation très voisine de la position normale, plus rarement de la portion médiane de l’arc aortique. Cette disposition doit être systématiquement recherchée car elle n’est pas rare dès lors que l’anatomie artérielle bronchique n’est pas complète ; elle réclame l’utilisation d’une sonde particulière permettant de pouvoir « racler » ce plancher de l’arche aortique. En pratique, la sonde utile est de type coronaire gauche. Fig. 18-10 Artère bronchique droite (ABD) naissant de la paroi latérale droite de l’arc aortique. Cette naissance peut être totalement ectopique, se faisant du tronc artériel brachiocéphalique, de la sub-clavière, du tronc thyro-bicervico-scapulaire ou cevicothoracique, de la thoracique interne, de la carotide commune gauche, voire de la vertébrale ou des artères coronaires (fig. 18-11). Ce caractère ectopique ne peut être affirmé que si l’artère en question n’est pas retrouvée en position normale, si le calibre de l’artère est régulier, sans disparité, et qu’elle pénètre par le hile pulmonaire. Il ne faut pas les confondre avec des anastomoses devenues fonctionnelles en raison d’un ostium occlus ou sténosé qu’on repère bien par la disparité de calibre ; en effet, dans ce cas, l’anastomose initiale d’origine ectopique est de plus petit calibre que le réseau bronchique qui lui fait suite. Le véritable ostium est alors parfois visible par un flux rétrograde. On pourra repérer des artères bronchiques ectopiques sur les coupes axiales médiastinales hautes jusqu’au niveau de l’arc aortique ; on peut les visualiser à gauche de la trachée, à droite ou à gauche de l’arc aortique, ou à droite de la trachée. Il peut s’agir d’une artère volumineuse, ou plus petite qu’il faut bien rechercher. Une fois repérées, on pourra alors suivre leur trajet jusqu’à leur origine en amont et jusqu’au hile en aval, réaliser si besoin une reconstruction et utiliser les données pour l’embolisation bronchique. Fig. 18-11 Patient de 34 ans suivi pour une dilatation des bronches lobaires inférieures gauches et hémoptysies récidivantes de l’ordre de 100 mL. Le trajet des artères bronchiques ne peut être étudié en TDM qu’en cas d’hypertrophie de celles-ci. Ce trajet est certainement mieux appréhendable sur des reconstructions en 3D (fig. 18-12). Ce trajet est aussi fonction du mode et du lieu de naissance, et si dans la majorité des cas les artères bronchiques sont rétro-bronchiques, elles peuvent être aussi prébronchiques. Fig. 18-12 Reconstruction en mode rendu de volume segmentaire. L’artère bronchique supérieure droite naît dans la majorité des cas d’un TBICD, reste le plus souvent au-dessus de la bronche souche droite et suit vers le haut la bronche lobaire supérieure. Elle peut aussi naître de l’artère bronchique moyenne une fois qu’elle est en dehors du tronc intermédiaire, pour remonter en dehors de la bronche lobaire supérieure. Les artères bronchiques gauches naissent le plus souvent par deux ostia, le supérieur donnant un tronc bronchique supérieur et moyen. Ce tronc bronchique gauche en position normale rejoint le hile au bord supérieur de la bronche souche gauche. L’artère bronchique supérieure gauche longe le bord supérieur de la bronche souche gauche puis la bronche lobaire supérieure gauche et suit la paroi inférieure de la crosse de l’aorte dont elle donne les vasa vasorum, non visibles sur l’angioscanner. L’artère bronchique moyenne gauche descend en dehors de la bronche lobaire inférieure. Ces artères bronchiques plus distales ne sont le plus souvent pas discernables des autres structures injectées ou des calcifications hilaires. Les artères bronchiques sont anastomosées entre elles, de façon homo- ou controlatérale (fig. 18-13 et 18-14). Cela explique qu’il ne faut pas se contenter d’opacifier les artères homolatérales au saignement et/ou de pratiquer une occlusion purement ostiale (ligature, mais aussi ressort proximal isolé). En effet, l’occlusion proximale est le plus souvent vouée à l’échec avec disparition de la porte d’accès à l’embolisation, sans empêcher pour autant la reprise en charge du réseau bronchique sous-jacent par les anastomoses ; cette reprise en charge peut être très rapide (image). Il existe également une possibilité d’anastomoses avec d’autres artères systémiques dangereuses et l’on en décrit en particulier avec les artères coronaires, particulièrement fréquentes dans la maladie de Takayasu, source d’accident d’embolisation. Les anastomoses avec les branches des artères sub-clavières sont fréquentes (fig. 18-15), notamment dans l’atteinte inflammatoire et infectieuse chronique des apex pulmonaires. Il existe aussi des anastomoses avec les artères pulmonaires (voir plus loin). Fig. 18-13 Patient hospitalisé pour une hémoptysie avec indication d’embolisation. Le saignement provient du lobe supérieur droit. Fig. 18-14 Hémoptysie de 300 mL provenant du culmen. Fig. 18-15 Hémoptysie apicale gauche sur des séquelles de tuberculose. Certaines collatérales des artères bronchiques sont importantes à connaître : un rameau trachéal, venant en règle d’une artère bronchique droite, les vasa vasorum aortiques, naissant le plus souvent d’une artère bronchique supérieure gauche et enfin un rameau œsophagien, issu en règle d’une artère bronchique inférieure gauche (fig. 18-16). Les deux premières ne posent pas de problème d’embolisation, mais l’embolisation d’une artère œsophagienne peut être source d’une ischémie œsophagienne. On a souligné récemment la possibilité de rameau à destinée du nerf phrénique dont l’embolisation pourrait être source d’une paralysie phrénique [30]. Fig. 18-16 Hémoptysie provenant du lobe inférieur gauche. Ces anastomoses sont nombreuses et se situent à plusieurs niveaux. Fig. 18-17 Vascularisation bronchique normale. Les anastomoses bronchopulmonaires sont décrites au niveau des bronches de 3,5 à 1,6 mm de diamètre. Elles ont un calibre d’environ 72 à 325 μ. Ce sont des anastomoses entre les artères bronchiques et pulmonaires termino-terminales ou termino-latérales. Elles ont été décrites par Von Hayek comme des segments « sperrartériens » ou comme des segments d’arrêt permettant de réguler la circulation bronchique. Les anastomoses précapillaires sont décrites au niveau des lobules pulmonaires. Leur calibre est de 24 à 48 μ et leur structure est différente des anastomoses précédemment décrites. Ce sont des anastomoses termino-terminales ou termino-latérales des branches des artères bronchiques et des artères pulmonaires. Fig. 18-18 Exemple d’un obstacle sur l’artère pulmonaire, par exemple une embolie pulmonaire (EP). La destruction du lit capillaire pulmonaire peut être réalisée par un processus inflammatoire ou infectieux ou par la fibrose aboutissant au développement d’une hypervascularisation systémique bronchique empruntant essentiellement les anastomoses bronchopulmonaires. Le lit capillaire artériel pulmonaire d’aval étant obstrué, la circulation se fait à contre- courant dans le segment artériel pulmonaire concerné. Si cette zone reste limitée, rapidement, ce flux a contrario reprend à iso-courant une branche artérielle pulmonaire voisine sans destruction du lit capillaire, donnant un drainage veineux pulmonaire. En cas de destruction du lit capillaire très distale et limitée, le drainage veineux est la seule anomalie observée. Au contraire, en cas de destruction importante, la totalité d’une branche artérielle pulmonaire, voire une artère pulmonaire entière, peut être visualisée par un flux à contre-courant à partir de l’artère bronchique ; cela est observé au maximum en cas de poumon détruit. Ce shunt à contre-courant peut être à l’origine de faux diagnostic d’embolie pulmonaire ou de mauvaise opacification des branches d’artères pulmonaires en cas d’acquisition d’un angioscanner thoracique à la recherche d’une embolie pulmonaire au temps artériel pulmonaire sans opacification de la circulation systémique (fig. 18-20). Les étiologies responsables de ce type d’hypervascularisation systémique sont la tuberculose évolutive ou séquellaire, les destructions parenchymateuses par une infection à pyogènes, les dilatations des bronches et les pneumoconioses. Cette hypervascularisation systémique peut être momentanément aggravée par un facteur infectieux surajouté, à pyogènes (suppuration des dilatations des bronches), tuberculeux (reprise évolutive) ou mycosique (aspergillome). Fig. 18-19 Exemple de destruction du parenchyme pulmonaire. Fig. 18-20 Aggravation d’une dyspnée chez un patient suivi pour des séquelles majeures de tuberculose du lobe supérieur gauche ; indication d’un angioscanner thoracique à la recherche d’une embolie pulmonaire. Elle est observée en règle de façon modérée pour le cancer bronchique ou sur un mode plus profus comme pour les tumeurs car-cinoïdes (fig. 18-21) ou certaines métastases (cancers du rein, de la thyroïde ou mélanomes). Elle semble correspondre à une prolifération vasculaire angiomateuse qui ne donne pas lieu en règle à la visualisation d’un shunt. Fig. 18-21 Hémoptysie massive chez un homme de 46 ans. La circulation systémique non bronchique peut être affectée de la même manière que la circulation bronchique. Cette hypervascularisation systémique non bronchique acquise peut se faire aux dépens de pédicules vasculaires déjà existants dans le thorax, comme l’artère du ligament triangulaire, ou plus fréquemment par la création de néovaisseaux transpleuraux à l’occasion d’une symphyse pleurale. La distinction de ces vaisseaux non bronchiques par rapport à d’authentiques artères bronchiques est faite sur la notion que seules ces dernières abordent le poumon par un trajet hilaire. Cette hypervascularisation systémique non bronchique est pratiquement toujours associée à une hypervascularisation systémique bronchique ; elle est le plus souvent régionale et doit être recherchée en fonction de la localisation de la pathologie sous-jacente. En cas d’atteinte apicale, de nombreuses artères peuvent venir contribuer à l’hypervascularisation, venant des troncs supra-aortiques, des artères sous-clavières, des artères thoraciques (mammaires) internes et externes, et des intercostales supérieures. Toutes les intercostales peuvent être impliquées dans une atteinte postérieure ; elles apparaissent alors hypertrophiques et sinueuses. En cas d’atteinte antérieure, quel que soit son niveau, on comparera la taille des deux artères thoraciques internes ; si l’une d’elle est augmentée de calibre, une artère bronchique ectopique ou une artère systémique non bronchique hypertrophique en naît très certainement. En cas d’atteinte des bases, l’étude portera sur la région des ligaments triangulaires, sur la région diaphragmatique et sur l’espace infra-médiastinal postérieur. On peut ainsi visualiser une augmentation de calibre d’une artère du ligament triangulaire, une grosse artère diaphragmatique inférieure. Notons que l’on peut également visualiser à ce niveau une séquestration, mais l’artère sys-témique anormale visualisée a un aspect qui ne correspond pas à celui d’une artère systémique ; son mode de ramification est différent, beaucoup plus semblable à celui d’une artère pulmonaire (dichotomique). Elles sont à rapprocher de la pathologie acquise par le risque d’hémoptysie. Elles semblent exceptionnelles. Ainsi décrit-on des angiomes et hémangiomes bronchiques sans étiologie apparente [79]. Des anévrismes artériels bronchiques et des shunts entre des malformations artérielles bronchiques et les artères pulmonaires, puis les veines pulmonaires, peuvent être observés en dehors de tout facteur source d’une hypervascula-risation systémique et semblent sans rapport, contrairement à ce qui avait été évoqué, avec la maladie de Rendu-Osler [127]. Les séquestrations correspondent à la vascularisation d’une partie, exclue ou non, du parenchyme pulmonaire, par une artère systémique anormale, le plus souvent par voie trans-diaphragmatique (voir chapitre IV) Le drainage veineux est pulmonaire dans la plupart des cas, les séquestrations intralobaires étant les plus fréquentes ; le drainage est veineux systémique dans les séquestrations extralobaires. Des fistules systémopulmonaires non bronchiques sont aussi décrites. L’hémoptysie est un symptôme fréquent en pneumologie ; elle est à l’origine de 7 % des consultations et de 11 % des admissions d’un service de pneumologie et de 38 % d’admission dans un service de chirurgie thoracique [4, 41]. Les étiologies sont nombreuses et leur répartition s’est modifiée au cours du temps, avec régression de l’origine tuberculeuse après 1980 et augmentation de fréquence du cancer bronchique (tableaux 18-3 et 18-4). On observe également des variations en fonction de l’origine géographique des malades [4, 73], du type de recrutement et de l’abondance de l’hémoptysie (tableaux 18-3 à 18-6) [24, 141]. L’amélioration des techniques a modifié ce paysage. La TDM en haute résolution a pu majorer la proportion des dilatations bronchiques au détriment des groupes « bronchite » et « sans étiologie », et l’ATDMV a majoré le nombre reconnu des étiologies ayant pour origine la vascularisation pulmonaire [88]. Le classement des étiologies peut être effectué en fonction du secteur initialement atteint, le secteur vasculaire, le secteur aérien ou aucun (tableau 18-7). Tableau 18-3 Étiologies des hémoptysies tout-venant (avant 1980). Séries de la littérature ayant plus de 100 cas. Source : d’après Carette et al. [24]. Tableau 18-4 Étiologies des hémoptysies tout-venant (après 1980). Séries selon la littérature ayant plus de 100 cas. Source : d’après Carette et al. [24]. Tableau 18-6 Cause des hémoptysies massives dans la littérature (après 1990). Source : d’après Carette et al. [24]. L’hémoptysie est un symptôme fréquent en pathologie tumorale thoracique, estimé entre 5 et 35 % des cas, restant le plus souvent d’abondance minime (hémoptysie symptôme). Des hémoptysies massives sont cependant possibles et représentent 10 % des cas [73]. Cette origine néoplasique représente de 0 à 43 % des étiologies des hémoptysies graves (voir tableaux 18-5 et 18-6). Leur pronostic est plus sombre que pour les autres étiologies [35, 50], surtout en cas de masses proximales en dehors de toute ressource chirurgicale [39] avec un pourcentage de décès pouvant aller jusqu’à 59 % [35]. Les mécanismes de l’hémoptysie dans les tumeurs sont nombreux : angiogenèse tumorale, hypervascularisation systémique secondaire à une occlusion artérielle pulmonaire avec un shunt à iso-courant, érosion d’un gros vaisseau systémique (aorte ou ses branches) ou pulmonaire ou secondaire à un geste percutané (biopsie transthoracique ou traitement par radiofréquence). L’hypervascularisation systémique tumorale est en rapport avec une angiogenèse anormale ; cette angiogenèse ne donne pas lieu habituellement à un shunt systémopulmonaire et elle est le plus souvent d’origine artérielle bronchique [141]. Il faut en tenir compte lorsque l’on décide de réaliser une biopsie transthoracique à visée diagnostique et vérifier l’intensité de la prise de contraste du nodule avant biopsie. Une hypervascularisation systémique peut se développer en cas de sténose tumorale des branches artérielles pulmonaires si les artères bronchiques ne sont pas également envahies. Enfin, les tumeurs sont aussi le siège de lacs veineux mais, surtout, elles créent des ulcérations des gros vaisseaux qui sont à leur contact, et le risque de rupture peut être accru par l’apparition d’une nécrose post-radique ou post-chimiothérapie ciblée anti-angiogénique (fig. 18-22). Fig. 18-22 Hémoptysie massive chez une patiente suivie pour un cancer bronchique non à petites cellules en cours de chimiothérapie.
CLINIQUE
Diagnostic différentiel
Diagnostic du type d’hémoptysie et facteurs pronostiques
Hémoptysie « maladie »

ANGIO-ANATOMIE THORACIQUE NORMALE ET PATHOLOGIQUE
Circulation systémique bronchique
Origine des artères bronchiques
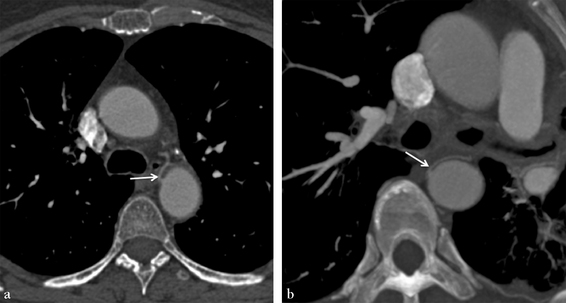
(a) Origine d’un tronc bronchique droit/gauche (flèche) au-dessus de la carène et en antéro-latéral droit. (b) Origine de l’artère bronchique inférieure gauche (flèche) très latéralisée à droite.
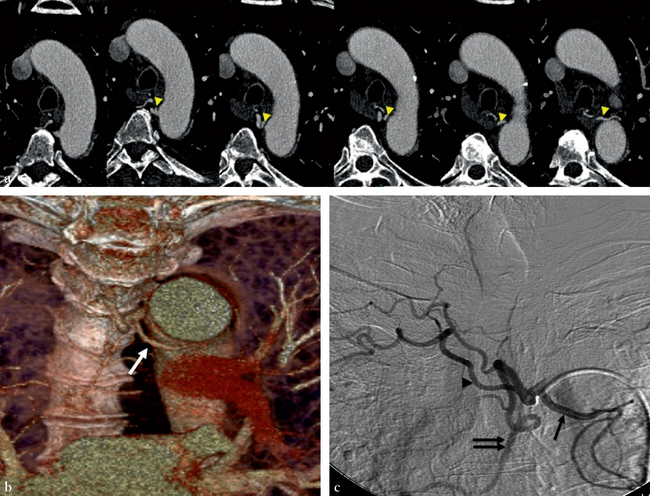
(a) Coupes sériées TDM en MIP fin de 3 mm d’épaisseur au niveau de la crosse de l’aorte montrant l’origine de l’artère bronchique gauche (tête de flèche) d’un tronc commun avec un tronc broncho-intercostal. (b) Reconstruction dans le plan frontal en VRT montrant d’une façon nette l’artère bronchique gauche (flèche) naissant par un tronc commun avec le tronc broncho-intercostal droit. (c) Opacification de l’artère identifiée en scanner. Artère bronchique gauche (flèche) ; artère bronchique droite (double flèche) ; artère intercostale droite (tête de flèche).
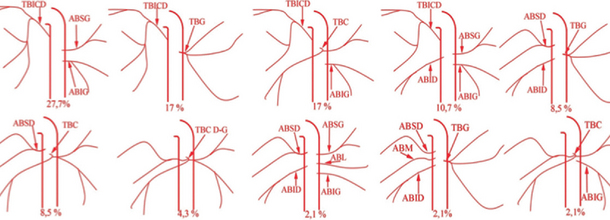
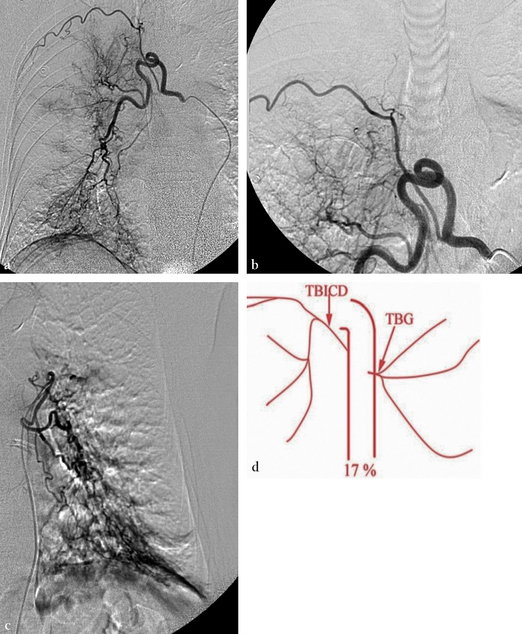
(a) Tronc broncho-intercostal droit donnant l’ensemble de la vascularisation bronchique droite. (b) Série centrée sur le rachis à la recherche d’un rameau spinal antérieur (le rameau est absent sur cet examen), (c) Artère bronchique gauche avec un dessin montrant l’ensemble de la vascularisation bronchique (d). Cette situation n’est trouvée que chez 17 % des patients.
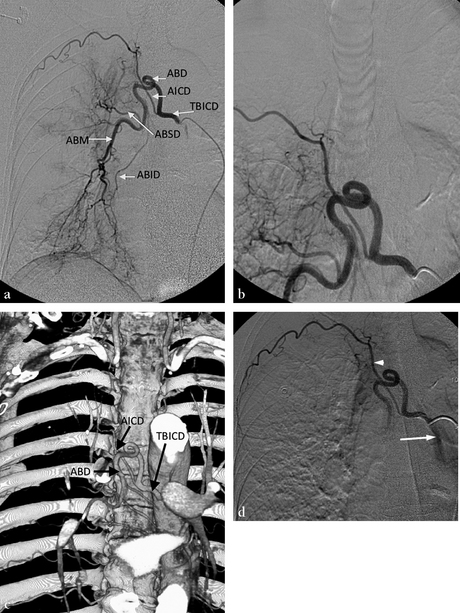
(a) L’opacification d’un TBICD montre l’artère bronchique droite (ABD) et l’artère intercostale droite (AICD). Noter l’hypertrophie majeure de l’ABD en comparaison avec l’AICD. De plus, la majeure partie de l’hypervascularisation est destinée au lobe moyen par l’artère bronchique moyenne en comparaison avec les autres artères bronchiques droites, supérieure (ABSD) et inférieure (ABID). (b) L’opacification d’un TBICD est toujours complétée par une série centrée sur la jonction cervicodorsale à la recherche d’un éventuel rameau spinal antérieur. (c) Reconstruction en VRT dans le plan coronal montrant la bonne corrélation entre les images TDM et l’angiographie. (d) Le contrôle, après embolisation avec des particules via un cathétérisme hypersélectif (non montré), montre une occlusion satisfaisante de l’artère bronchique avec respect de l’artère intercostale droite (tête de flèche) ; notez le reflux du contraste dans l’aorte lors de l’opacification.
Artère bronchique
Nombre
Pourcentage (n = 126)
Tronc broncho-intercostal droit
91
72,2
Tronc bronchique commun
68
54,0
Tronc bronchique gauche
33
26,2
Artère bronchique supérieure gauche
24
19,0
Artère bronchique inférieure gauche
31
24,6
Tronc bronchique droit
6
4,8
Artère bronchique supérieure droite
3
2,4
Artère bronchique inférieure droite
15
11,9
Tronc bronchique commun complet
7
5,6
Autres
5
4,0
Total
283
2,2 artères/patient
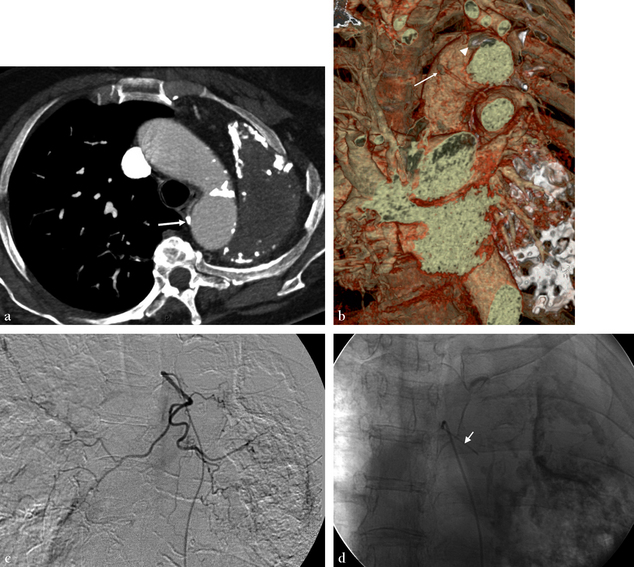
(a) Coupe dans le plan axial en MIP de 5 mm montrant la calcification (flèche) à l’origine d’un TBC. (b) Reconstruction dans le plan coronal en VRT montrant la calcification à l’origine du TBC (flèche) et d’autres calcifications de la paroi aortique (tête de flèche). (c) Cathétérisme instable avec fuite de produit de contraste lors de l’opacification du TBC qui donne la vascularisation de l’ensemble de l’arbre bronchique droite et du lobe supérieur gauche. (d) Cathétérisme hypersélec-tif avec un microcathéter (flèche) permettant une embolisation satisfaisante avec de particules.
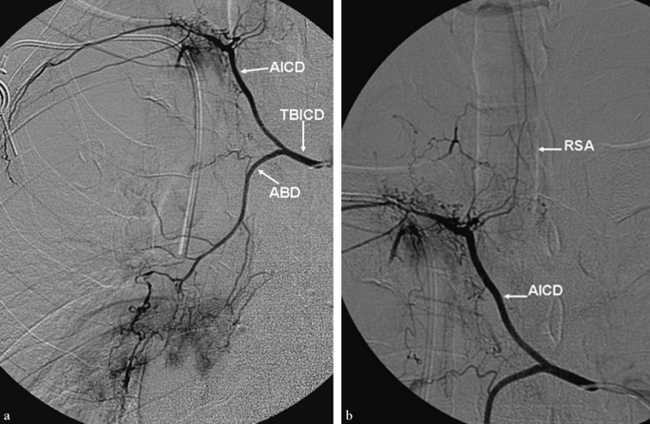
(a) Opacification avec centrage sur l’hémithorax droit montrant une artère intercostale droite (AICD) avec une légère hypervascularisation apicale droite mais surtout une hypervascularisation d’allure tumorale lobaire inférieure droite par l’artère bronchique droite (ABD). (b) L’opacification de la même artère avec un centrage médian sur la jonction cervicothoracique montre une image en épingle à cheveux correspondant au rameau spinal antérieur médian (RSA).
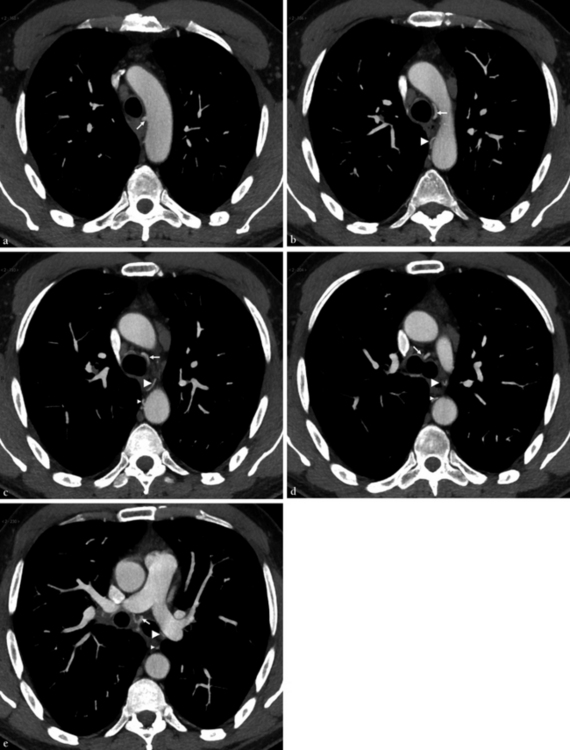
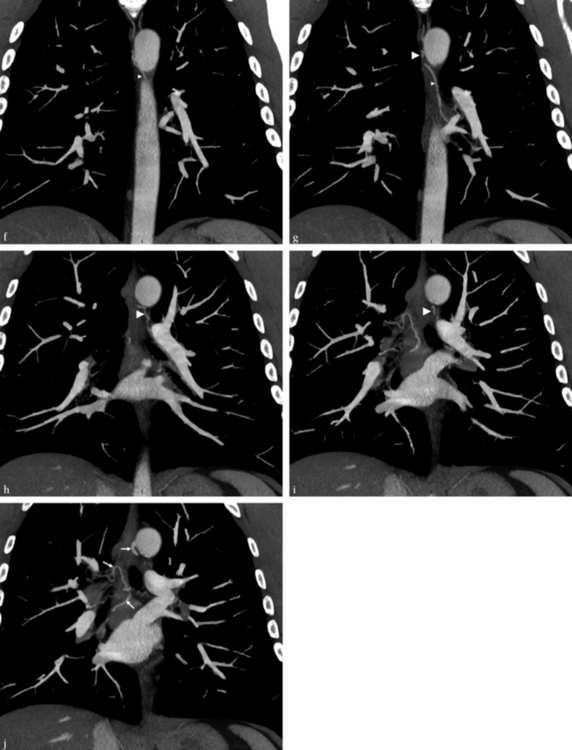
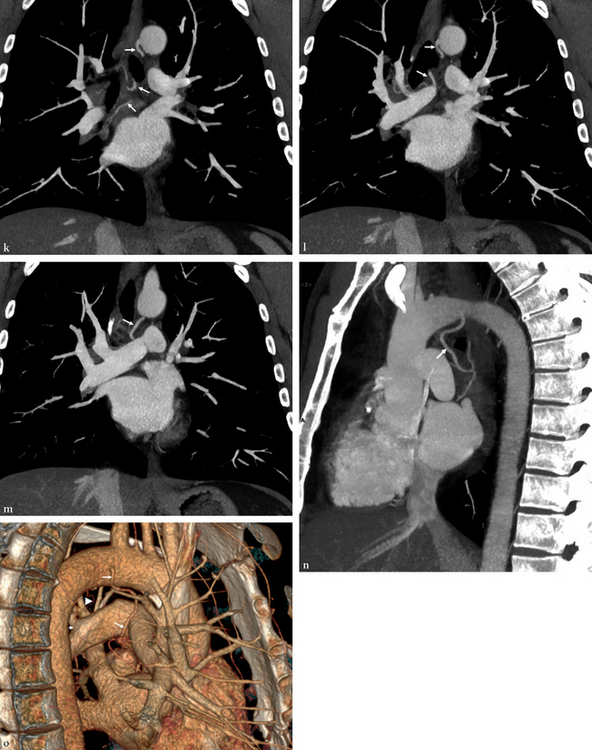
(a-e) Coupes en MIP fin de 3 mm d’épaisseur de l’arc aortique vers la région sous-carénaire ; nous suivons l’ABD (flèche) naissant de la crosse et passant en avant de la bifurcation trachéale avant sa division en deux branches. À noter la visualisation de deux artères bronchiques gauches, l’une supérieure (tête de flèche épaisse) et l’autre inférieure (tête de flèche fine). (f-m) Reconstruction dans le plan frontal en MIP fin de 5 mm d’épaisseur d’arrière en avant montrant l’origine et le trajet des artères bronchiques droite (flèche), supérieure gauche (tête de flèche épaisse) et inférieure gauche (tête de flèche tmontrant l’artère bronchique droite (flèche). (o) Reconstruction dans le plan sagittal en VRT avec une visualisation du côté droit montrant d’une façon nette l’anatomie complexe des AB chez ce patient.
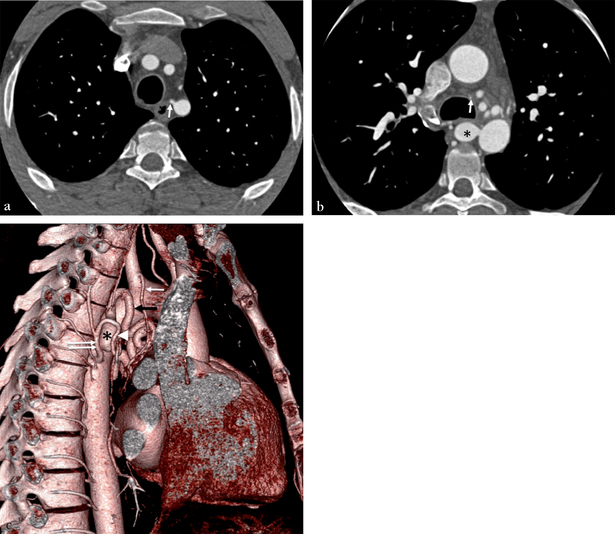
(a,b) Coupes dans le plan axial montrant l’origine ectopique d’une artère bronchique inférieure droite (flèche) du pied de l’artère sub-clavière gauche. Hypertrophie majeure des artères bronchiques à destinée gauche avec un anévrisme d’hyperdébit (astérisque) à l’origine de l’artère bronchique gauche. (c) La reconstruction en VRT avec une vue latérale droite montre mieux cette anatomie complexe associant un tronc broncho-intercostal droit (double flèche blanche) avec l’artère bronchique droite partant en avant (tête de flèche), l’anévrisme (astérisque) à l’origine de l’artère bronchique gauche (flèche noire) et l’artère bronchique inférieure droite ectopique (flèche blanche).
Trajet des artères bronchiques
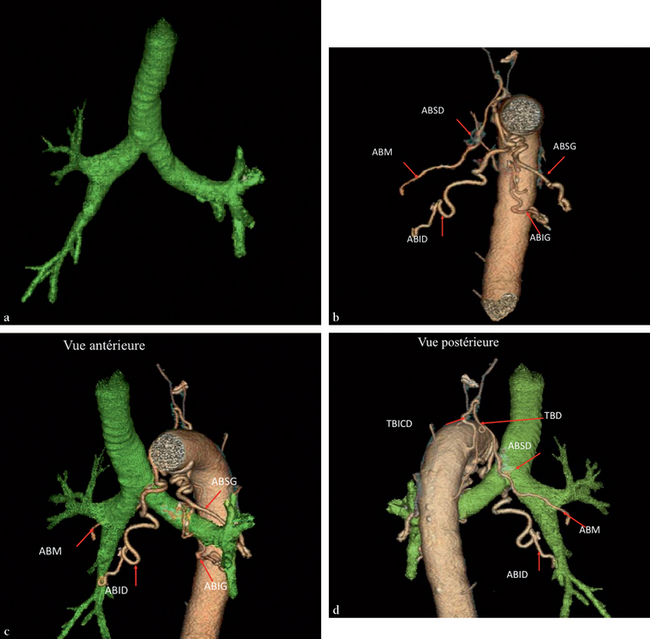
Nous avons effectué une propagation des pixels de densité très faible pour l’arbre bronchique (a) et les plus élevés pour les artères bronchiques (b), puis nous avons fusionné les deux structures et nous les visualisons en vues antérieure (c) et postérieure (d).
Le tronc broncho-intercostal (TBICD) se divise en une artère intercostale et un tronc bronchique droit (TBD) ; ce dernier se divise en une artère à destinée lobaire supérieure droite (ABSD : artère bronchique supérieure droite) et en une artère bronchique moyenne (ABM) qui passent en arrière de la trachée et la bronche souche droite, et en une artère bronchique inférieure droite (ABID) qui passe devant la bifurcation trachéale.
À gauche, le tronc bronchique gauche se divise en une artère bronchique supérieure gauche (ABSG) passant en arrière de la trachée et une artère bronchique inférieure gauche (ABIG) passant en avant de le trajet et a un trajet en dessous de la bronche souche et inférieure gauche .
Anastomoses et collatérales
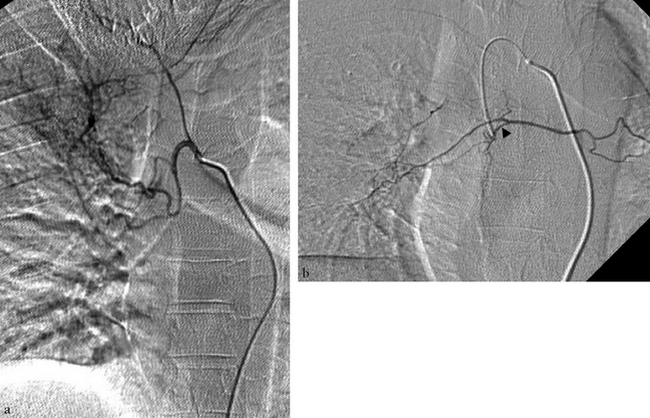
(a) Opacification d’un tronc broncho-intercostal droit montrant une hypervascularisation lobaire supérieure droite. (b) Le cathétérisme hypersélectif avec un microcathéter révèle une anastomose (tête de flèche) avec un tronc bronchique commun droit/gauche donnant l’ensemble de la vascularisation gauche et l’artère bronchique inférieure droite.
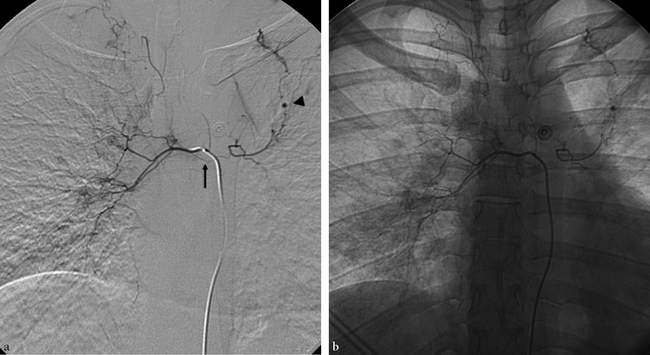
Lors de l’opacification d’une artère bronchique droite complète (a : image soustraite ; b : image non soustraite), nous opacifions l’artère bronchique du lobe supérieur gauche via une anastomose (flèche) et nous identifions un micro-anévrisme bronchique distal (tête de flèche).
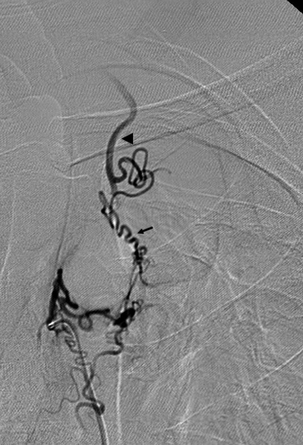
L’opacification de l’artère bronchique supérieure gauche montre l’artère thoracique interne gauche (tête de flèche) via une large anastomose (flèche).
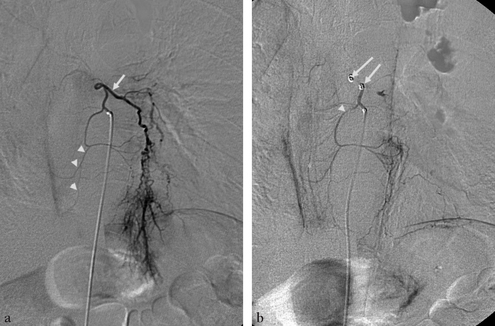
L’opacification de l’artère bronchique inférieure gauche (a) montre l’hypervascularisation du lobe inférieur gauche avec hypertrophie de l’artère bronchique inférieure gauche (flèche) et la présence d’une collatérale (têtes de flèche) allant vers le médiastin ; doute sur une parenchymographie œsophagienne. Le contrôle (b) après cathétérisme sélectif de l’artère bronchique inférieure gauche et occlusion avec deux microressorts (flèches), montre de façon nette le rameau œsophagien (tête de flèche) et la parenchymographie œsophagienne (astérisque).
Anastomoses entre le système pulmonaire et le système bronchique (fig. 18-17)
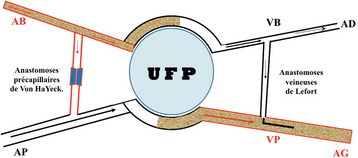
L’unité fonctionnelle pulmonaire peut correspondre à un segment ou à un lobe. Le sang pulmonaire non oxygéné arrive dans l’unité fonctionnelle pulmonaire et ressort oxygéné par les veines pulmonaires (VP) vers l’atrium gauche (AG). Les artères bronchiques (AB) cheminent le long des axes bronchiques avec des anastomoses bronchopulmonaires (entre le système artériel bronchique et pulmonaire) assez proximales (diamètre des bronches de 3,5 à 1,6 mm) de Von Hayeck et des anastomoses bronchopulmonaires précapillaires au niveau du lobule pulmonaire. Enfin, les anastomoses de Lefort entre le réseau capillaire veineux bronchique distal et le réseau capillaire veineux pulmonaire distal.
Angio-anatomie thoracique pathologique
Hypertrophie de la circulation bronchique
Défaut de la circulation pulmonaire (fig. 18-18)
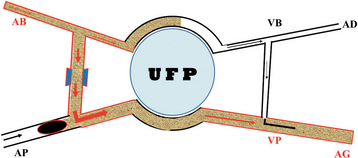
Hypertrophie des artères bronchiques avec ouverture des shunts bronchopulmonaires suivie par un shunt systémopulmonaire à iso-courant vers l’unité fonctionnelle pulmonaire.
Destruction du lit capillaire pulmonaire (fig. 18-19)
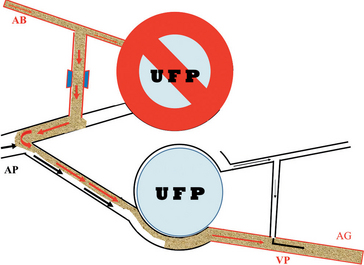
Hypertrophie des artères bronchiques avec ouverture des anastomoses bronchopulmonaires et apparition d’un shunt à contre-courant allant jusqu’à une artère pulmonaire irrigant un territoire fonctionnel (flèche courbe). Dans le territoire fonctionnel, le sang circule à iso-courant.
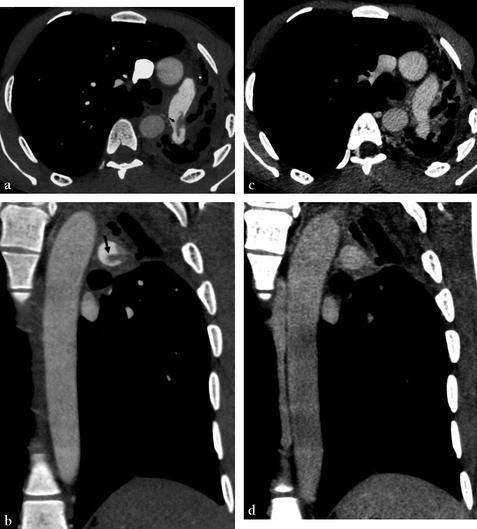
Coupe dans le plan axial (a) et reconstruction dans le plan coronal (b) montrant une lacune endovasculaire dans le tronc de l’artère pulmonaire gauche faisant évoquer le diagnostic d’un thrombus. (c,d) Les mêmes images que a et b mais à un temps plus tardif montrent la disparition des lacunes. La lacune correspond à du sang non rehaussé circulant à contre-courant et se jetant dans le tronc de l’artère pulmonaire gauche ; ce phénomène n’est plus visible après un rehaussement homogène (temps tardif).
Hypervascularisation tumorale
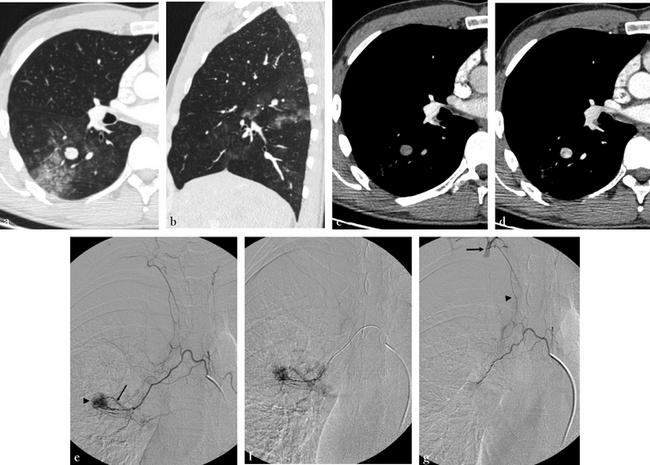
Coupe dans le plan axial (a) et reconstruction dans le plan sagittal (b) en fenêtre parenchymateuse montrant un nodule entouré par des surdensités en verre dépoli. (c,d) Coupes dans le plan axial avec injection de produit de contraste aux temps précoce (a) et tardif (b) montrant une prise de contraste intense. (e,f) Angiographie sélective (e) et hypersélective (f) d’une artère bronchique droite visualisant le nodule avec un rehaussement intense sans shunt systémopulmonaire. (g) Le contrôle après embolisation avec des particules et occlusion avec un ressort montre un dévascularisation complète. À noter la meilleure visualisation de l’anastomose (tête de flèche) avec le tronc thyro-bicervico-scapulaire droit (flèche).
Hypertrophie de la circulation systémique non bronchique
Anomalies congénitales de la circulation bronchique
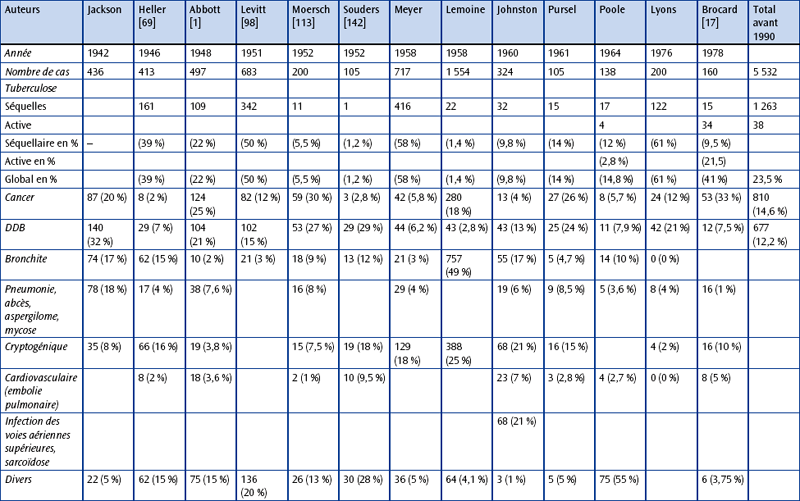
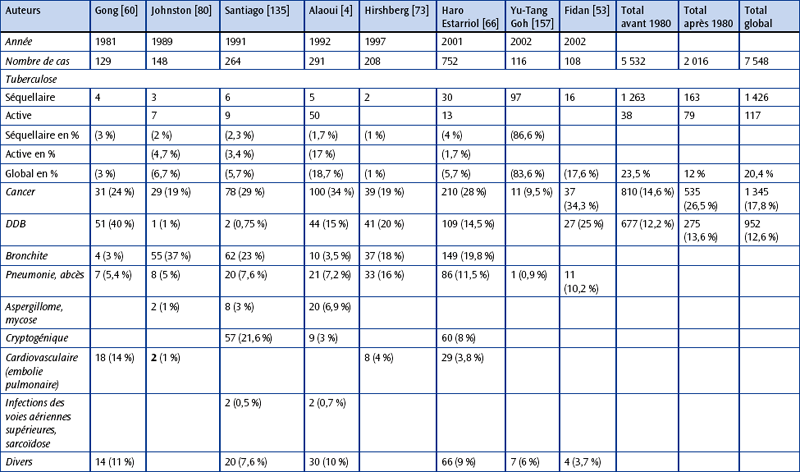
PRINCIPALES ÉTIOLOGIES DES HÉMOPTYSIES
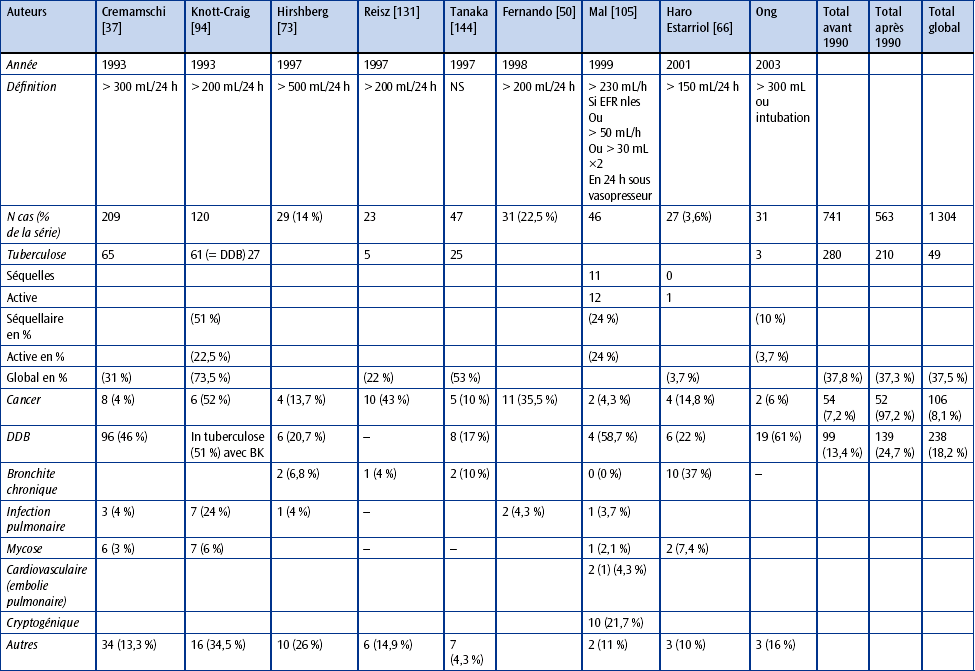
Hémoptysie d’origine bronchopulmonaire
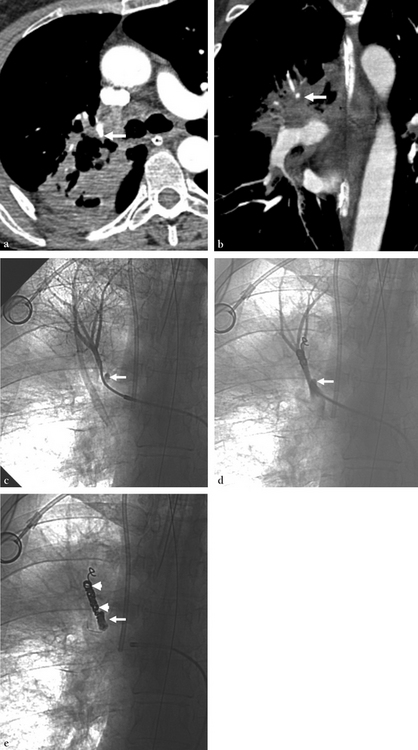
(a) Coupe dans le plan axial en MIP de 5 mm montrant l’interruption d’une branche artérielle pulmonaire (flèche) par la nécrose tumorale. (b) Reconstruction dans le plan coronal en MIP de 5 mm montrant l’image du faux anévrisme entouré par de la nécrose (flèche). (c) L’opacification de la segmentaire A1 visualise le faux anévrisme (flèche) avec un aspect normal de la partie distale. Le faux anévrisme est trop proximal du tronc de l’artère médiastinale droite et son occlusion sélective est dangereuse. L’option thérapeutique était d’occlure la partie distale normale avec des ressorts (prévenir la propagation de l’Onyx®) et de remplir le reste du tronc de la segmentaire A1 avec de l’Onyx® jusqu’à l’abouchement dans le tronc de l’artère médiastinale droite. (d) Contrôle après largage d’un premier ressort Nester® 35-14-4 montrant la persistance du passage en distalité du produit de contraste et le faux anévrisme (flèche). (e) Occlusion de la vascularisation distale avec deux ressorts Nester® 35-14-4 et du faux anévrisme avec de l’Onyx® jusqu’à l’abouchement de l’artère porteuse dans le tronc de l’artère médiastinale.![]()
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree


18: ASPECTS PARTICULIERS DES HÉMOPTYSIES : PHYSIOPATHOLOGIE, DIAGNOSTIC ET TRAITEMENT