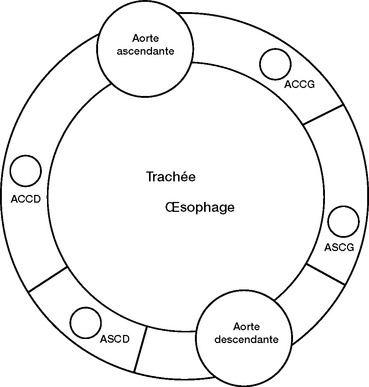
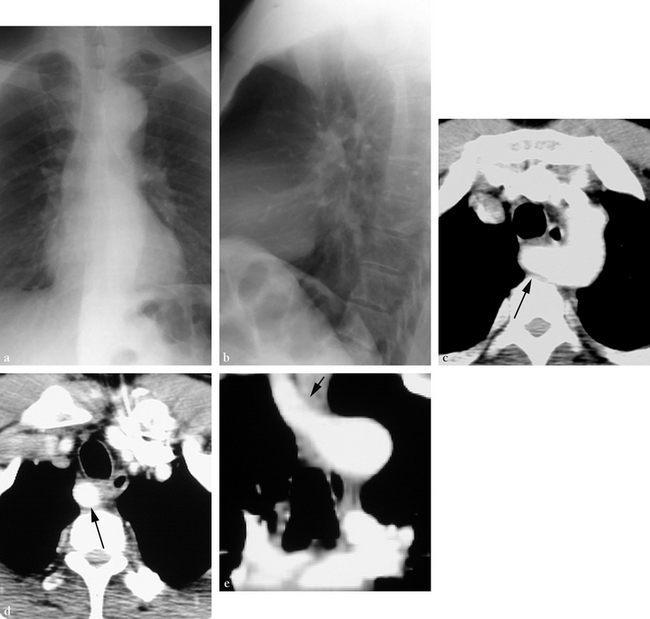
CHAPITRE 16 IMAGERIE DE L’AORTE THORACIQUE M. El Hajjam, M. Bensalah, C. Beigelman, J.-P. Pelage, Y. Badachi, C. Lagrange, A. Demir and P. Lacombe Les développements permanents de l’imagerie non invasive – TDM hélicoïdale, IRM et échocardiographie transœsophagienne (ETO) – ouvrent de plus en plus de champs d’application dans le domaine des explorations vasculaires, notamment de l’aorte thoracique. Ces techniques permettent une étude vasculaire non seulement morphologique, mais aussi fonctionnelle. L’analyse concerne la totalité de l’aorte. Elle doit intégrer également l’étude du cœur, des artères coronaires et de la valve aortique. Ce bilan est primordial pour la prise en charge thérapeutique. Le système du double arc aortique décrit par Edwards et al. est un modèle de référence [21]. Dans ce modèle, il existe un arc aortique et un ductus arteriosus (canal artériel) de chaque côté avec une aorte médiane unique ascendante et descendante. Une artère carotide commune et une artère sub-clavière naissent séparément de chaque arc aortique (figure 16-1). Le développement normal consiste en l’accroissement de l’arc aortique gauche, qui comporte en fait le quatrième arc aortique et l’aorte dorsale gauches, avec une involution de l’arc droit en aval de l’artère sub-clavière. En fait, cette involution concerne l’aorte dorsale droite située en aval de l’artère sub-clavière, qui disparaît. Il ne reste de l’arc droit que le tronc artériel brachiocépha-lique. Ce dernier donne naissance aux artères carotide commune et sub-clavière droites. La constitution normale est donc celle d’un arc aortique gauche avec une aorte descendante et un ligament artériel gauches. Fig. 16-1 Schéma simplifié du double arc aortique. ACCD et ACCG : artères carotides communes droite et gauche ; ASCD et ASCG : artères sub-clavières droite et gauche. (d’après Edwards [21]) L’orientation du truncus conoseptal détermine dans le même temps le développement correct du système artériel pulmonaire et aortique. La portion ventrale du 6e arc aortique forme les artères pulmonaires, le segment dorsal de ce même arc étant le futur ductus arteriosus [45]. C’est le flux préférentiel dans l’artère pulmonaire gauche qui détermine le développement de l’aorte descendante gauche via le ductus arteriosus homolatéral perméable. Le terme d’anneau vasculaire reflète l’existence d’une relation anormale des structures vasculaires avec la trachée et l’œsophage responsable d’une compression, d’une dysphagie ou de problèmes respiratoires. Le scanner, l’IRM et l’échographie trans-œsophagienne sont les techniques d’imagerie diagnostique de référence. L’angiographie est réalisée dans le bilan préthérapeutique [44]. L’aorte est l’un des meilleurs champs d’application du scanner spiralé. La rapidité d’acquisition des coupes, le balayage volumique, la possibilité d’injecter le produit de contraste à haut débit permettent une acquisition à visée angiographique [22, 56, 73, 79, 88, 105]. Les paramètres d’acquisition dépendent des objectifs diagnostiques, des caractéristiques techniques du système d’imagerie et de la dose de rayons X délivrés. L’acquisition est idéalement réalisée en apnée, dans le sens cranio-caudal. Avec les scanners multi-détecteurs (16, 64, 256 coupes…), il est possible d’explorer l’aorte thoracique avec une collimation submillimétrique (0,625 mm) en un temps de rotation très court de l’ordre de 0,3 seconde. L’acquisition synchronisée rétrospective à l’électrocardiogramme (ECG), permet de s’affranchir des artefacts de battement de l’aorte (dédoublement de la paroi aortique du segment 0 et I pouvant prêter à confusion avec une dissection) [54, 72, 78]. Le but est d’obtenir un rehaussement vasculaire suffisamment dense et homogène sur la totalité du volume exploré [79, 88]. L’utilisation d’un produit de contraste de concentration supérieure ou égale à 300 mg d’iode/mL, injecté à un débit de 3 à 5 mL/s, est recommandée. Compte tenu de ces débits d’injection élevés, les produits de contraste de faible osmolarité sont préférables car leur toxicité en cas d’extravasation est moindre. En outre, ces produits sont fortement recommandés chez les patients aux conditions hémodynamiques précaires [22, 73]. L’usage des scanners multibarrettes et des injecteurs automatiques à double corps permettent une réduction du volume de produit contraste. Pour l’exploration de l’aorte thoracique, l’injection se fait au pli du coude droit afin d’éviter les artéfacts vasculaires de la veine innominée gauche sur l’origine des troncs supra-aortiques. L’injection dans une veine du pied paraît idéale, mais elle est de réalisation pratique difficile et potentiellement source de douleur et de thrombose. Le délai entre le début de l’injection et celui de l’acquisition est d’une importance capitale. Plusieurs facteurs interviennent dans le rehaussement vasculaire : facteurs patient-dépendants (taille, poids, âge, fonction cardiaque, hydratation) et facteurs patientindépendants (site d’injection, concentration et viscosité du produit de contraste, volume et débit d’injection). Une injection bi-phasique (bolus de produit de contraste suivi d’un bolus de sérum physiologique) permet de limiter les artéfacts de renforcement dans la veine cave supérieure. Plusieurs approches pour déterminer le délai optimal ont été proposées. « Jadis », ce délai était fixé de façon empirique. Pour l’aorte thoracique, il est de 18 à 20 secondes pour un site d’injection antécubital droit à 4 mL/s [73]. Actuellement, les scanners sont tous équipés de procédés de détection de l’arrivée du bolus iodé intravasculaire, permettant l’acquisition des images au moment idéal [16]. Il reste à l’appréciation du radiologue le choix entre le déclenchement automatique de l’acquisition et la visualisation en temps réel du bolus avec un déclenchement manuel lors du rehaussement de l’aorte. Les acquisitions en coupes submillimétriques avec un pixel isotropique permettent des reconstructions d’une qualité identique aux coupes axiales natives [31]. Les reconstructions multiplanaires bidimensionnelles (MPR) sont utiles pour préciser certains détails difficiles à analyser sur les coupes axiales [104]. Le plan de reconstruction est défini de manière interactive et peut être orthogonal aux coupes axiales, oblique dans l’axe de l’aorte horizontale ou curviligne. Ces reconstructions sont quasi-instantanées et peuvent être utilisées en situation d’urgence, mais elles ne doivent en aucun cas retarder la prise en charge thérapeutique du patient. Les reconstructions tridimensionnelles, qu’elles soient de type surfacique ou volumique, pseudo-angioscopique ou projec-tif (Maximum Intensity Projection [MIP], technique de rendu volumique [VRT]), ont un intérêt diagnostique limité, mais donnent une excellente cartographie vasculaire, facilitant la compréhension des images par les cliniciens et sont très utiles pour les chirurgiens en pré- et peropératoire. Les reconstructions de type MIP peuvent être très utiles dans l’analyse des troncs supra-aortiques. Par ailleurs, les différents logiciels de modélisation aortique, permettent au scanner multibarrette de se substituer à l’aortographie avec cathéter gradué, pour les indications d’endoprothèses aortiques [9, 71]. L’angio-IRM est une excellente méthode d’exploration de l’aorte thoracique. Elle associe les avantages de l’imagerie en coupes et des techniques de projection, permettant une étude à la fois anatomique et fonctionnelle. Les séquences tridimensionnelles (3D) en écho de gradient avec injection intraveineuse de chélate de gadolinium, réalisées en apnée et couplées à l’ECG, associées aux séquences ciné-IRM et aux séquences en écho spin T1, constituent la technique de choix pour l’étude de l’aorte thoracique [1]. Les séquences de ciné-IRM permettent également une étude globale et segmentaire de la fonction ventriculaire gauche et la recherche d’anomalies constitutionnelles type bicuspidie aortique [64]. Ce sont les séquences de base pour l’analyse du médiastin. Elles sont pondérées en T1 avec un TR et un TE courts et sont réalisées dans le plan axial et sagittal oblique. Ces séquences sont couplées à l’ECG (gating cardiaque) et à la respiration (gating respiratoire) pour supprimer les arté-facts dus aux battements cardiaques et aux mouvements respiratoires [19]. Les séquences tridimensionnelles en écho de gradient (EG-3D) avec injection, pondérées en T1, permettent une excellente visualisation de l’aorte et de recueillir un hypersignal intra-vasculaire. Le temps d’acquisition est court. La séquence 3D est constituée d’une partition de coupes fines acquises avec un TR (3 à 5 ms) et TE (1,2 à 2 ms) très courts au cours d’une apnée (inférieure à 30 s) et un couplage à l’ECG [1]. Une injection biphasique (bolus de 0,2 mmol/kg de chélate de gadolinium suivi d’un bolus de 20 mL de sérum physiologique) est nécessaire afin d’obtenir un contraste suffisant entre les structures vasculaires et les tissus avoisinants [19]. L’analyse s’effectue sur les coupes natives, les reconstructions MPR et MIP. L’acquisition débute par des coupes axiales strictes ce qui permet de programmer facilement les autres plans d’analyse. Le plan sagittal oblique est parallèle à l’aorte horizontale. Le plan coronal oblique est perpendiculaire au précédant. En utilisant ces deux derniers plans, une acquisition perpendiculaire au plan du sinus de Valsalva permet une mesure précise de l’anneau aortique, du sinus de Valsalva, de la jonction sino-tubulaire et une étude anatomique de la valve aortique à la recherche d’une éventuelle bicuspidie [64]. Une dilatation du sinus de Valsalva peut être en rapport avec : – une maladie annulo-ectasiante ; – ou une maladie génétique de surcharge à type de maladie de Fabry, surtout s’il existe une hypertrophie ventriculaire gauche associée [4]. Des séquences ciné-IRM en haute résolution temporelle permettent d’accéder à des indices de rigidité aortique grâce à des logiciels dédiés, permettant l’estimation de la surface diastolique et systolique combinée à la mesure simultanée de la pression artérielle et calculer ainsi la compliance aortique [74]. L’acquisition en contraste de phase permet d’accéder à des paramètres de la rigidité aortique par le calcul de la vitesse de l’onde de pouls (VOP) entre deux segments de l’aorte thoracique. L’acquisition se fait à hauteur de la bifurcation pulmonaire entre l’aorte ascendante et descendante et grâce à des logiciels dédiés, on peut estimer le temps de transit (T) de la colonne sanguine entre les deux segments aortiques [41, 74]. Les images natives doivent toujours être analysées. Les reconstructions ne peuvent être étudiées seules, afin d’éviter les pièges et les artéfacts [1]. La série est reconstruite selon différents algorithmes : MIP, MPR, 3D surfacique ou technique d’addition-soustraction d’images comme en angiographie numérisée [11, 19]. La reconstruction MIP produit une image similaire à l’angiographie. Cette technique a cependant des limites, à savoir la surestimation des sténoses vasculaires et la non-visualisation des portions thrombosées d’un anévrisme ou d’un faux chenal de dissection. Les reconstructions MPR sont très utiles pour les structures vasculaires tortueuses permettant une meilleure évaluation de leur diamètre. Le 3D surfacique réalise une image de l’aspect extérieur des vaisseaux, mais se heurte aux difficultés de seuillage des vaisseaux par rapport aux structures adjacentes. Il repose sur les éléments suivants : Tableau 16-1 Différentes séquences en IRM pour l’exploration de l’aorte thoracique et leurs applications. La pathologie de l’aorte thoracique a largement bénéficié de cette technique qui est facilement réalisable au lit ou au bloc opératoire chez des patients hémodynamiquement instables [57]. L’utilisation de sondes multiplans permet une analyse satisfaisante des trois segments de l’aorte thoracique : la racine et la partie initiale de l’aorte ascendante, l’aorte horizontale et l’aorte descendante. Cependant, en raison de l’interposition de l’arbre trachéobronchique, il persiste deux zones aveugles que sont la partie haute de l’aorte ascendante sur 3 cm environ et l’origine des troncs supra-aortiques. Les anomalies congénitales de l’aorte peuvent être diagnostiquées de façon fortuite sur une radiographie standard chez des patients asymptomatiques ou être révélées par une symptomatologie clinique très variable dépendant de l’existence d’anneaux vasculaires ou de cardiopathies congénitales associées. Auparavant, leur détection et leur évaluation étaient effectuées en radiologie conventionnelle (clichés standard et transit œsophagien) et par angiographie. Si l’apport de l’IRM dans la détection et l’évaluation préchirurgicale de ces anomalies est indéniable, la TDM hélicoïdale autorise actuellement un bilan aussi exhaustif par la qualité des reformations bi- et tridimensionnelles. Ce bilan a pour but de détecter l’ensemble des anomalies positionnelles et de calibre de l’aorte et de l’origine des troncs supra-aortiques [87]. Les anomalies associées sont explorées au cours du même examen. Arcs aortiques gauches avec artère sub-clavière droite aberrante Les arcs aortiques gauches avec artère sub-clavière droite aberrante sont les malformations des arcs aortiques les plus fréquentes avec une prévalence rapportée de 0,4 à 2,3 % [92]. Cette anomalie peut être isolée ou associée à des anomalies cardiaques congénitales. Elle est en règle générale asympto-matique (figure 16-2). Néanmoins, avec l’âge, l’artère sub-clavière droite aberrante devient tortueuse, ectasique, athé-romateuse, et peut entraîner une compression trachéale et œsophagienne responsable de dysphagie, dénommée dans ce cas dysphagia lusoria [97] (figure 16-3). La connaissance d’une telle anomalie est importante en endoscopie œsophagienne et en cas de cathétérisme cardiaque, car le cœur et les coronaires sont inaccessibles par voie artérielle brachiale droite [70]. Fig. 16-2 Arc aortique gauche avec diver-ticule de Kommerell et artère sub-clavière droite aberrante asymptomatique (flèches). a. b. L’aorte est de situation anormalement haute. a. Cliché de face et b. de profil. c. et d. TDM avec injection en coupes axiales. e. reconstruction coronale. Dans la classification proposée, il s’agit d’une anomalie positionnelle caractérisée par une composante transversale à type d’interruption de l’arc mineur entre les artères carotide commune et sub-clavière droites et une composante verticale à type d’aorte cervicale de grade I, le niveau supérieur de la crosse se projetant juste en dessous du manubrium sternal. Fig. 16-3 Arc aortique gauche avec diverticule de Kommerell et artère sub-clavière droite aberrante rétro-œsophagienne athé-romateuse (flèche) révélée par une dysphagie. Embryologiquement, l’arc aortique gauche avec artère sub-clavière droite aberrante rétro-œsophagienne résulte de l’interruption de l’arc aortique droit entre l’artère carotide commune et l’artère sub-clavière droites. L’artère sub-clavière droite peut émerger d’un diverticule de Kommerell persistant de la portion la plus distale de l’arc aortique droit [97]. Un anneau vasculaire est rarement constitué en cas de défaut de régression du ductus arteriosus droit. La découverte d’un arc aortique gauche avec artère sub-clavière droite aberrante rétro-œsophagienne est généralement fortuite, éventuellement dans le cadre d’une opacité ou d’une masse médiasti-nale anormale. Une compression trachéale antérieure a été décrite chez les patients ayant une artère sub-clavière rétro-œsophagienne en association avec un tronc bicarotidien (origine commune des artères carotides) ou une artère carotide commune droite tortueuse, l’artère sub-clavière droite aberrante générant une compression trachéale postérieure et œsophagienne. L’aspect en i magerie est caractéristique. Sur la radiographie thoracique de face, l’artère sub-clavière aberrante se présente sous la forme d’une opacité oblique en haut et à droite, avec un bombement antérieur de la trachée sur l’incidence de profil. Cette opacité naît en regard du bord supérieur du bouton aortique et traverse le médiastin avec une angulation de 70° et une topographie caractéristique rétro-œsophagienne. En TDM, l’artère sub-clavière droite aberrante est le vaisseau supra-aortique le plus postérieur. À son origine, un diverticule de Kommerell est fréquemment visible, d’un calibre égal ou inférieur à celui de la crosse de l’aorte et s’implantant largement sur cette dernière. Des complications du diverticule à type d’ectasie ou d’anévrisme peuvent être rencontrées. Des anomalies mineures, ou de découverte fortuite, ne générant pas de compression trachéale peuvent être rencontrées. Elles consistent en la naissance de l’artère vertébrale gauche de l’aorte horizontale entre les artères carotide commune et sub-clavière gauches et l’existence d’un tronc commun entre le tronc artériel brachiocéphalique et l’artère carotide commune gauche [45]. Les arcs aortiques droits surviennent chez 0,05 à 0,1 % des adultes [70]. De nombreuses variations dans les classi-fixations des arcs aortiques droits ont été décrites. Le type d’anomalie va dépendre des points d’interruption en regard de l’arc aortique gauche. Au moins cinq variétés sont possibles, les plus classiques étant les arcs aortiques droits avec image en miroir, les arcs aortiques droits avec artère sub-clavière gauche aberrante, et les arcs aortiques droits avec artère sub-clavière gauche isolée. L’arc aortique droit avec image en miroir est en règle générale détecté précocement, une cardiopathie congénitale cyanogène étant retrouvée dans 98 % des cas [70], essentiellement représentée par des tétralogies de Fallot, un truncus arteriosus, ou des ventricules droits à double issue. Moins fréquemment, il s’agit d’atrésie tricuspidienne ou de transposition complète des gros vaisseaux avec défect septal ventri-culaire [85]. Inversement, 25 % des sujets ayant une tétralogie de Fallot et 35 % de ceux ayant un truncus arteriosus ont ce type de malformations [48, 92]. Embryologiquement, l’arc aortique droit avec image en miroir est le plus souvent dû à un développement dominant de l’arc primitif droit avec une interruption de l’arc primitif gauche en aval de l’artère sub-clavière et du ductus arteriosus gauches. Il n’y pas d’anneau vasculaire dans ce cas et les cardiopathies congénitales y sont fréquemment associées. Beaucoup plus rarement, l’interruption siège entre l’artère sub-clavière gauche et le ductus arteriosus. Dans ce cas, un anneau vasculaire est constitué, avec une anatomie cardiaque normale [46]. Dans la forme la plus fréquente, le premier vaisseau supra-aortique est un tronc artériel innominé gauche donnant naissance aux artères carotide commune et sub-clavière gauches, puis vers l’arrière naissent respectivement l’artère carotide commune et l’artère sub-clavière droites. Il n’existe ainsi aucune structure vasculaire rétro-œsophagienne, aucun anneau vasculaire ni compression des voies aériennes. En radiographie standard, une crosse droite générant une empreinte trachéale droite et une déviation gauche de la trachée est notée, le bouton aortique gauche habituel étant absent. L’aorte descendante est généralement située à droite du rachis avec un passage normal du hiatus diaphragmatique [97]. Le transit œsophagien est normal. La forme rare où un anneau vasculaire est constitué par les structures vasculaires et le ductus gauche peut être symptomatique [85]. Dans ce cas, un piégeage pulmonaire gauche, de même qu’une large empreinte œsophagienne postérieure peuvent être mis en évidence [85]. L’arc aortique droit avec artère sub-clavière gauche aberrante est une anomalie de découverte non rare chez l’adulte, rapportée dans 0,06 à 0,1 % de la population [97]. Il s’agit de la forme la plus fréquente des arcs aortiques droits (figures 16-4 et 16-5). L’arc droit avec artère sub-clavière gauche aberrante peut être symptomatique ou non, en fonction de l’étroitesse de l’anneau vasculaire créé. Il s’agit de la deuxième cause la plus fréquente d’anneau vasculaire après le double arc [97]. Cette forme d’arc aortique droit est présente chez environ 5 % des patients porteurs de cardiopathies congénitales, en particulier les défects septaux ventriculaires, et rarement les tétralogies de Fallot [85]. Embryologiquement, il existe une interruption en regard de l’arc primitif gauche, entre l’artère carotide commune et l’artère sub-clavière gauches. Différents sous-types sont décrits selon le côté du ligament artériel non involué. Si le ligament artériel siège à droite, aucun anneau vasculaire n’est créé. S’il siège à gauche, un anneau vasculaire est constitué [26]. Très fréquemment, l’origine de l’artère sub-clavière gauche aberrante fait suite à un diverticule de Kommerell, de longueur et de calibre variables, toujours inférieur à celui de la crosse. L’anneau vasculaire est complété par le ductus ou ligament artériel connectant le diverticule ou la portion proximale de l’artère sub-clavière à l’artère pulmonaire gauches. Le degré de traction créé par le ductus arteriosus est responsable du degré d’obstruction de l’anneau vasculaire [45]. Rarement, une sténose ou une atrésie de la portion proximale de l’artère sub-clavière gauche aberrante est observée, avec possible phénomène de vol sub-clavier [85]. Fig. 16-4 TDM d’un arc aortique droit avec diverticule de Kommerell et artère sub-clavière gauche aberrante (flèche). a. Composante cervicale, attestée par le siège anormalement haut de l’aorte horizontale, b. dont le sommet se projette immédiatement en dessous du manubrium sternal. Elle peut ainsi être classée dans le groupe des aortes cervicales ou des arcs aortiques de type II. c. L’aorte descendante est à gauche, réalisant de surcroît une aorte circonflexe dans les descriptions classiques. Dans la nouvelle classification, il s’agit d’une malformation purement positionnelle dont les composantes transversales sont une anomalie de côté de l’aorte horizontale (arc aortique droit), une interruption de l’arc mineur entre les artères carotide commune et sub-clavière gauches (artère aberrante avec diverticule de Kommerell), une aorte descendante croisée et dont la composante verticale est une aorte cervicale de grade I. Fig. 16-5 Double arc aortique. a. b. Coupes TDM sans injection. c. Transit œsophagien de profil. d. Artériographie de face. e. f. Coupes axiales en IRM : l’arc droit est le plus haut (d) volumineux, et le plus postérieur (b, c) responsable de la compression œsophagienne postérieure. Les quatre vaisseaux naissent des deux arcs. Dans la nouvelle classification, les caractéristiques transversales sont un double arc (arc droit dominant) et une aorte descendante gauche ; la composante verticale est de grade I pour l’arc droit. L’aspect radiographique standard de face est celui d’un bouton aortique à droite avec empreinte trachéale droite, latéro-déviation gauche de la trachée et déplacement à droite de la veine azygos. Le diverticule de Kommerell peut être visualisé sous la forme d’une opacité latéro-trachéale gauche. Sur l’incidence de profil, une opacité avec refoulement antérieur de la trachée et de l’œsophage anormalement aéré est mise en évidence. Le transit œsophagien retrouve une compression extrinsèque postérieure de l’œsophage par une structure tubulée d’orientation inverse à celle décrite dans les arcs aortiques gauches, avec possible dilatation œsophagienne sus-jacente. L’aorte descendante est en règle générale droite, avec un passage normal du hiatus diaphragmatique à gauche de la ligne médiane [70], mais l’aorte peut être parfois médiane ou gauche [85]. Arc aortique droit avec artère sub-clavière gauche isolée: Cette anomalie rare n’est pas responsable de la création d’un anneau vasculaire. Elle peut générer un syndrome de vol subclavier, l’artère sub-clavière isolée étant vascularisée via un ductus arteriosus perméable par l’artère pulmonaire ou par voie rétrograde par l’artère vertébrale gauche via le polygone de Willis en cas d’atrésie du ductus [45]. Le double arc est la cause la plus fréquente d’anneau vasculaire complet symptomatique. La plupart des patients présentent un stridor, des infections respiratoires ou une dysphagie dans les six premiers mois de la vie (figure 16-6). Le traitement est alors chirurgical. Des cardiopathies congénitales associées sont rares. Parfois, les doubles arcs sont de découverte systématique chez des sujets asymptomatiques. Cette malformation résulte de la persistance du double arc aortique embryonnaire. Elle peut être subdivisée en doubles arcs aortiques avec perméabilité persistante des deux crosses ou avec atrésie de l’arc aortique gauche [45]. La première de ces formes, la plus fréquente est volontiers associée à des infections pulmonaires récidivantes [85]. Un arc droit et gauche arrive de l’aorte ascendante et les deux branches se rejoignent vers l’arrière, chacun des arcs donnant respectivement l’artère carotide et sub-clavière homolatérale pour former une aorte descendante unique. En règle générale, l’arc aortique droit est le plus haut et le plus large, et de topographie postérieure expliquant la compression œsophagienne, pour rejoindre l’aorte descendante du côté gauche dans 70 % des cas environ. En cas d’aorte descendante droite, les deux arcs sont symétriques ou ont tendance à avoir une composante antérieure droite et postérieure gauche [45]. En cas d’atrésie de l’arc aortique gauche en distalité de l’artère carotide ou sub-clavière avec simple persistance d’un cordon fibreux, le diagnostic de double arc est parfois impossible. De façon caractéristique, il s’agit de deux crosses aortiques avec un petit arc gauche, donnant naissance directement à quatre vaisseaux supra-aortiques. L’aorte descendante est le plus souvent gauche, de même que le ductus. L’aspect en imagerie conventionnelle est similaire à celui des arcs aortiques droits avec artère sub-clavière gauche rétro-œsophagienne ou des arcs aortiques droits avec aorte circonflexe. Une indentation trachéale bilatérale est caractéristique avec possible sténose de la trachée distale, en particulier chez les sujets symptomatiques [45]. Le degré de compression trachéale et œsophagienne est bien précisé en imagerie. Fig. 16-6 Double arc aortique. Nourrisson de 2 mois. Gêne respiratoire et vomissements. Détresse respiratoire après une fibroscopie œsophagienne. a. Cliché de face ne montrant pas d’anomalie. TDM après injection montrant un double arc aortique emprisonnant la trachée et l’œsophage (b, c. MIP axial et coronal, d. 3D surfacique, e, f. coronal et sagittal mlP, g. VRT). Le traitement chirurgical a consisté en une section de l’arc droit après la naissance des artères carotide commune et sub-clavière droites. Cet arc était dominé (l’épreuve de son clampage n’entraînait pas d’hypotension d’aval contrairement à l’arc gauche). Elles sont définies par une aorte descendante controlatérale à l’aorte horizontale, avec croisement de la ligne médiane en rétro-œsophagien. À gauche, les aortes circonflexes sont volontiers associées à une artère sub-clavière droite rétro-œsophagienne. Ce type d’anomalie est volontiers associé à une tétralogie de Fallot, une veine cave supérieure gauche persistante, une sténose aortique et un défect ventriculaire [97]. La symptomatologie est généralement celle d’un anneau vasculaire. Les arcs aortiques droits avec artère sub-clavière rétro-œsophagienne peuvent être également concernés [97]. Des anévrismes athéromateux de la portion postérieure de la crosse ont été rapportés dans ce cadre [94]. Une ectasie de l’artère sub-clavière droite responsable d’un syndrome de Horner a également été décrite [18]. L’aorte cervicale est une anomalie rare, d’étiologie inconnue, caractérisée par une situation anormalement haute de l’aorte horizontale, le plus souvent à droite [39, 70]. Une masse pulsatile du cou ou de la région sus-claviculaire peut être révélatrice [97]. Les symptômes, lorsqu’ils sont présents, consistent en un stridor, des infections du tractus respiratoire ou une dyspnée d’effort. La dysphagie est plus rare, en rapport avec la portion rétro-œsophagienne de l’aorte thoracique descendante. Les aortes cervicales peuvent être associées à des cardiopathies congénitales de Fallot, pseudo-truncus, ventricule droit à double issue ou défect ventriculaire. Les aortes cervicales sont expliquées par une régression anormale du quatrième arc dominant, avec la persistance anormale des premier, deuxième et/ou troisième arcs ou par une fusion des troisième et quatrième arcs et/ou un défaut de migration caudale du quatrième arc à la septième semaine de gestation [29, 39]. Une implantation directe des artères carotides interne et externe du côté de la crosse sans artère carotide commune peut être observée [39, 85], l’artère carotide commune étant normalement originaire du troisième arc aortique. Une artère sub-clavière aberrante est fréquemment observée. De façon occasionnelle, on peut également observer une artère vertébrale homolatérale naissant directement de l’aorte horizontale. Des anévrismes de l’aorte ont été rapportés dans le cadre d’aortes cervicales [68]. L’aorte horizontale entre l’artère carotide commune et l’artère sub-clavière gauches est le plus souvent affectée, région la moins touchée par les ané-vrismes aortiques classiques, à un moindre degré l’aorte descendante ou la crosse et l’aorte descendante. Des calcifications athéromateuses en regard de l’anévrisme aortique peuvent être retrouvées [42]. Une nécrose médiale kystique avec dégénérescence basophile a été rapportée chez de jeunes patients, des remaniements athéroscléreux ayant été retrouvés chez des sujets plus âgés [27, 67]. Un défaut de développement embryologique, une anomalie du tissu conjonctif, une altération de l’hémodynamique, une contrainte de la paroi aortique et un mécanisme traumatique ont été incriminés [34]. En radiographie standard, un élargissement du médiastin supérieur est noté, le bouton aortique n’étant pas en situation normale. L’arc aortique droit est responsable d’un déplacement trachéal vers la gauche et l’avant [45]. Un élargissement de l’espace rétropharyngé peut être noté. Une compression postérieure de l’œsophage de niveau variable est objectivée sur le transit œsophagien. La position anormalement haute de l’arc aortique est identifiée sur toutes les imageries (voir figures 16-2 et 16-4), l’implantation des différentes branches étant parfaitement précisée. L’IRM permet de surcroît d’effectuer un bilan des cardiopathies congénitales associées. Les coarctations sont définies par une sténose hémodynami-quement significative de l’aorte thoracique en règle générale juste en aval de l’artère sub-clavière gauche, en regard de l’origine du ductus arteriosus [2]. Des formes d’extension variable du fait de leur association à d’autres anomalies de calibre de la crosse aortique, en particulier de type hypoplasie, sont décrites. La forme ductale ou diffuse, la plus sévère, est de présentation généralement précoce en raison de l’obstruction aortique marquée [70]. Cette forme est caractérisée par une hypoplasie de l’arc aortique entre l’artère carotide commune et l’artère sub-clavière gauches ainsi que de l’isthme aortique avec coarctation juste en amont de l’insertion du ductus [45]. Il s’agit donc de formes préductales. Les cardiopathies congénitales associées sont fréquentes, en particulier les bicuspidies aortiques dans plus de 85 % des cas, des lésions obstructives du cœur gauche, des valvulopathies mitrales congénitales, des défects septaux ventriculaires et la persistance de la perméabilité du ductus. Cette entité est fréquemment rencontrée chez les patients avec syndrome de Turner [45]. La seconde forme est localisée, juxta-ductale, se révélant dans l’enfance tardive ou l’adolescence par les signes classiques d’hypertension artérielle et de diminution des pouls fémoraux [70]. Une bicuspidie aortique y est associée dans 80 % des cas. En cas d’artère sub-clavière aberrante distale à la coarctation, l’artère aberrante peut servir de vaisseau collatéral. Un phénomène de vol sub-clavier droit (arc aortique gauche avec artère sub-clavière droite aberrante) peut ainsi être observé avec un flux rétrograde dans l’artère sub-clavière droite, puis l’aorte descendante en aval de la coarctation. Des encoches costales droites sont alors absentes. Si l’artère sub-clavière aberrante naît en amont de la coarctation, le flux reste antérograde et les encoches costales sont présentes. L’aspect en radiographie standard est caractérisé par une image en double contour du bouton aortique en regard de l’arc supérieur gauche. Le contour supérieur correspond à la portion proximale de l’artère sub-clavière gauche dilatée, l’encoche répondant à la coarctation sur l’incidence de profil, le contour inférieur répondant à la dilatation post-sténotique de l’aorte descendante. Des encoches du bord inférieur des côtes supérieures sont également retrouvées (figure 16-7). Le diagnostic formel de coarctation et la dilatation des vaisseaux collatéraux thoraciques internes et intercostaux sont aisément faits en TDM ou IRM [86]. Les complications des coarctations à type d’ectasie ou de dissection sont également facilement objectivées [70]. Fig. 16-7 Illustrations de coarctation aortique. Bilan d’hypertension artérielle. a. Le cliché montre une interruption de la ligne para-aortique (flèche), un aspect marqué de l’arc supérieur gauche en rapport avec l’hypertrophie de l’artère sub-clavière gauche (flèche courbe) et des encoches costales en rapport avec l’hypertrophie des artères intercostales (tête de flèches). L’ensemble est hautement évocateur d’une coarctation aortique. Autre patient : (b) angio-TDM : plan sagittal. Sténose très serrée de l’aorte après la naissance de l’artère sub-clavière gauche avec dilatation des artères intercostales. c. Plan coronal montrant la dilatation des artères thoraciques internes (courtoisie de J.-L. Sablayrolles). Autre patient : (d) angio-IRM : coupe sagittale oblique montrant la sténose aortique (flèche) et la collatéralité surtout thoracique interne. Elles seraient, pour certains auteurs, une forme mineure de coarctation, sans sténose aortique significative. Aucune circulation collatérale n’est mise en évidence. Elles consistent en une indentation de l’aorte horizontale en regard du ligament artériel, fixant l’aorte à l’artère pulmonaire, avec une convexité angulaire à direction antéro-inférieure. La portion de l’aorte située en amont du kinking est de situation anormalement haute [8]. La plupart des sujets sont asymptomatiques, bien qu’une hypertension artérielle soit volontiers retrouvée et que des anévrismes et des dissections aient été rapportés [8]. Des malformations congénitales cardiovasculaires ont également été décrites en association avec des pseudo-coarctations [97]. L’aspect radiographique de face consiste en une opacité visible au-dessus du bouton aortique normal, ce dernier étant de situation anormalement basse. De profil, les anomalies de courbure sont retrouvées. En TDM, la situation anormalement haute de la crosse aortique au-dessus des articulations sterno-claviculaires est bien mise en évidence [70] (figure 16-8). Les arcs aortiques interrompus sont des lésions congénitales rares, toujours associées à d’autres anomalies cardiovasculaires. Il s’agit d’une des formes les plus rapidement létales de maladie cardiovasculaire congénitale [45]. Ces malformations sont caractérisées par une interruption de l’arc aortique entre l’aorte ascendante proximale et l’aorte descendante distale. Elles se différencient des atrésies par l’existence d’une interruption complète entre l’aorte horizontale et l’aorte descendante. En cas d’atrésie, un cordon fibreux connecte la portion proximale aortique avec l’aorte thoracique descendante. Ces anomalies concernent essentiellement les arcs aortiques gauches [97]. Les classifications sont fondées sur le site d’interruption : – type A (42 %) en aval de l’artère sub-clavière ; – type B (53 %) entre l’artère carotide et l’artère sub-clavière ; – type C (4 %) entre l’artère carotide commune droite et gauche. Ces trois types peuvent être subdivisés en : – sous-type 1 : artère sub-clavière normale ; – sous-type 2 : artère sub-clavière aberrante rétro-œsophagienne ; – sous-type 3 : artère sub-clavière isolée, arrivant du ductus arteriosus homolatéral. La position de l’aorte descendante est importante à définir parce qu’une aorte descendante droite associée à une interruption aortique est quasiment toujours associée à un syndrome de DiGeorge. Ces patients ont en règle générale une interruption de type B. Des aortes horizontales et descendantes gauches peuvent également être visualisées. Les anomalies cardiaques les plus fréquemment rencontrées sont un défect large du septum ventriculaire mal orienté. Observé dans 73 % des cas, il est responsable d’une obstruction par sténose musculaire sous-valvulaire aortique et d’un large shunt gauche-droite [45]. Une valve aortique déformée ou bicuspide est fréquente. Pour des raisons hémodynamiques, il existe une relative diminution du flux dans l’aorte ascendante avec un flux préférentiel dans les vaisseaux carotidiens, le flux en regard de l’arc aortique étant diminué, entraînant une régression en raison du manque de pression. Des truncus arteriosus, transpositions complètes et corrigées des gros vaisseaux et ventricules droits à double issue, peuvent être rencontrés [45]. L’aorte descendante est en continuité avec le ductus arteriosus perméable et est vas-cularisée via l’artère pulmonaire [45].
RAPPEL EMBRYOLOGIQUE
TECHNIQUES D’IMAGERIE
TDM
Paramètres d’acquisition
Paramètres d’injection
Traitement des images
IRM
Séquences en écho de spin T1
Séquences angio-IRM
Séquences cinétiques (SSFP)
Séquences en contraste de phase
Traitement des images
Protocole d’IRM de l’aorte thoracique (tableau 16-1)
Approche
Séquences
Application
Morphologie
Écho de spin T1 et T2
Anatomie des structures
Cinétique
Ciné-IRM : écho de gradient
Cinétique pariétale et du flux sanguin
Débimétrie
Contraste de phase
Quantification des flux
Angiographie
Angio-IRM avec gadolinium
Imagerie vasculaire
Échocardiographie transœsophagienne
MALFORMATIONS CONGÉNITALES
Arcs aortiques gauches
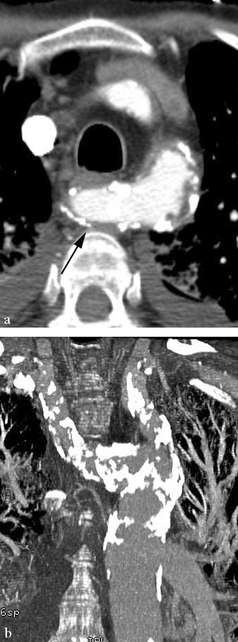
TDM avec injection. a. Coupe axiale. b. Reconstruction oblique en MPVR. Dans la classification proposée, il s’agit d’une anomalie caractérisée par une composante transversale unique à type d’interruption de l’arc mineur entre les artères carotide commune et sub-clavière droites.
Arcs aortiques droits
Double arc aortique
Aortes circonflexes
Aorte cervicale
Coarctations
Pseudo-coarctations
Arcs aortiques interrompus et atrétiques
![]()
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree


Medicine Key
Fastest Medicine Insight Engine