Chapitre 15 Cardiomyopathies et myocardites
Le terme « myocardiopathie » est général et regroupe de nombreux processus pathologiques qui n’ont qu’une caractéristique commune : leur capacité à diminuer la fonction myocardique de façon significative. La classification la plus reconnue est celle de l’Organisation mondiale de la santé (OMS) [World Health Organization (WHO)], pour qui le vocable « myocardiopathie » est réservé aux maladies myocardiques de cause inconnue, les autres étant regroupées sous le terme de « maladies myocardiques spécifiques » (Tableau 15.1) [1]. Néanmoins, et compte tenu de leur présentation clinique similaire, le terme de « myocardiopathies secondaires » est souvent utilisé dans ce dernier cas, incluant les myocardiopathies associées à l’ischémie, la dysfonction valvulaire, l’hypertension, les myocardites, les maladies métaboliques, les maladies systémiques, les dystrophies musculaires, les pathologies neuromusculaires, d’origine toxique, et liées au post-partum. À côté de ces formes chroniques, il existe également des cardiomyopathies aiguës, essentiellement représentées par les myopéricardites.
Tableau 15-1 Principales causes de myocardiopathies spécifiques.
| Infectieuses : virales (VIH), bactériennes, rickettsiennes, fungiques, parasitaires… |
| Inflammatoires non infectieuses : collagénoses, granulomatoses |
| Métaboliques : nutritionnelles (thiamine, carnitine, sélénium, vitamine D, obésité), endocriniennes (acromégalie, thyrotoxicose, myxœdème, Cushing, phéochromocytome), trouble métabolique (oxalose, goutte) et électrolytique |
| Toxiques : cobalt, alcool, adriamycine, mercure, paracétamol, cocaïne, lithium… |
| Agents physiques : brûlure, hypothermie, irradiation… |
| Infiltratives : amylose, hémochromatose, sarcoïdose, néoplasie, mucopolysaccharidoses |
| Fibreuses : fibrose endomyocardique, Loffler, carcinoïde |
| Hématologiques : leucémie, purpura thrombopénique |
| Hypersensibilité : pénicilline, tétracyclines, phénylbutazone, antituberculeux, myocardite à cellules géantes, rejet de greffe |
| Génétiques : myocardiopathie hypertrophique, maladies neuromusculaires (Steinert, Duchenne, Friedreich…) |
| Diverses acquises : postpartum, obésité |
| Idiopathiques : |
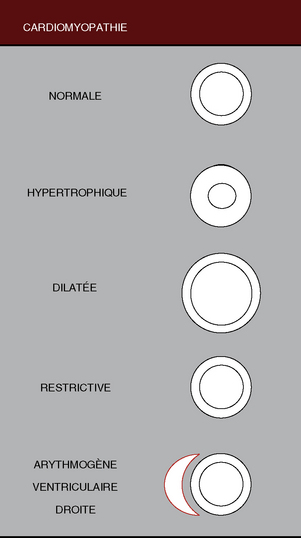
Quatre catégories sont définies sur des bases morphologiques et hémodynamiques : la myocardiopathie hypertrophique, la myocardiopathie dilatée, la myocardiopathie restrictive, et une forme particulière d’atteinte ventriculaire droite, la myocardiopathie ventriculaire droite arythmogène (fig. 15.1). En pratique, la cardiomyopathie est actuellement volontiers classée selon le type de dysfonction : les cardiomyopathies avec dysfonction systolique, parmi lesquelles les cardiopathies ischémiques et postvalvulaires, et les cardiopathies avec dysfonction diastolique liées à un trouble de la compliance myocardique du ventricule gauche (VG), dont font partie les cardiopathies restrictives et hypertrophiques (tableau 15.2). Les principales indications ont été rappelées dans une récente mise à jour (tableau 15.3) publiée par Pohost [2].
Tableau 15-2 Principales étiologies des myocardiopathies.
| Classification actuelle | Ancienne classification | Étiologies |
|---|---|---|
| Myocardiopathie avec dysfonction systolique | Cardiopathies dilatées | Cardiopathies ischémiques et postvalvulaires, cardiopathies hypertensives |
| Myocardiopathie avec dysfonction diastolique | Cardiopathies restrictives et hypertrophiques |
Tableau 15-3 Indications de l’IRM.
| Indications | Classe |
|---|---|
| Évaluation fonction VD-VG | I |
| DAVD | I |
| Cardiomyopathie hypertrophique | I |
| Cardiomyopathie dilatée | I |
| Cardiomyopathie restrictive (diagnostic différentiel de péricardite chronique constrictive) | I |
| Myocardites aiguës | I |
| Sarcoïdose et maladies de système | I |
I : utilité indiscutable ; II : utile mais indication moins bien établie ; IIa : nombreuses données en faveur de l’utilité ; IIb : données insuffisantes.
D’après Pohost (1).
Protocole IRM
Les images dynamiques essentielles à l’analyse des paramètres fonctionnels globaux (fraction d’éjection, mesures de volume, d’épaisseur) et segmentaires (score de cinétique segmentaire) sont réalisées en écho de gradient équilibré (steady state free precession [SSFP] : Truefisp™, Fiesta™ ou Balanced FFE™), en petit axe de l’apex au plan valvulaire. Ces acquisitions peuvent être complétées par des images dynamiques acquises avec des bandes ou des grilles de présaturation (tagging) qui permettent de quantifier la fonction contractile.
Protocole scanner multicoupe
Il est réalisé une première acquisition en contraste spontané pour rechercher des calcifications myocardiques, puis une acquisition type coroscanner habituel pour l’étude des artères coronaires (voir le chapitre 2). Enfin, on procède à un passage tardif à 5 minutes en baissant les kilovolts (80 kV en dessous de 75 kg et 100 kV au-dessus de 75 kg, par exemple), avec une épaisseur de coupes de 1,5 mm et des reconstructions en 3 mm tous les 1,5 mm, après réinjection de produit de contraste iodé (double dose).
Cardiomyopathie hypertrophique
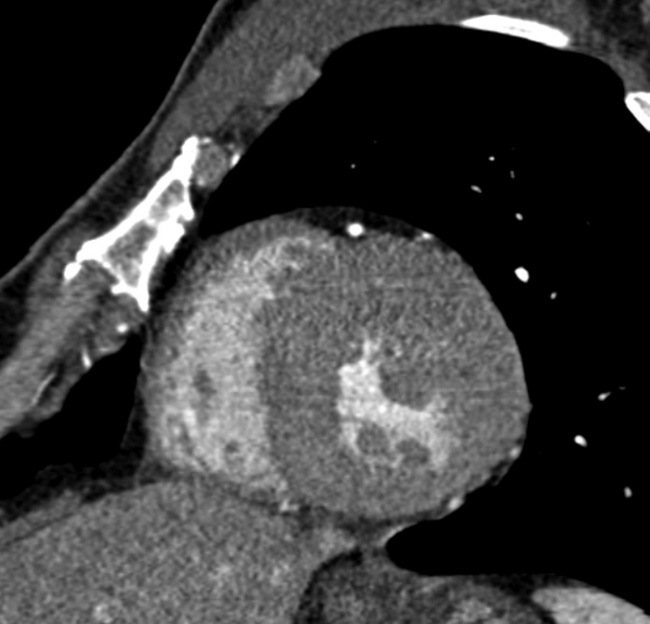
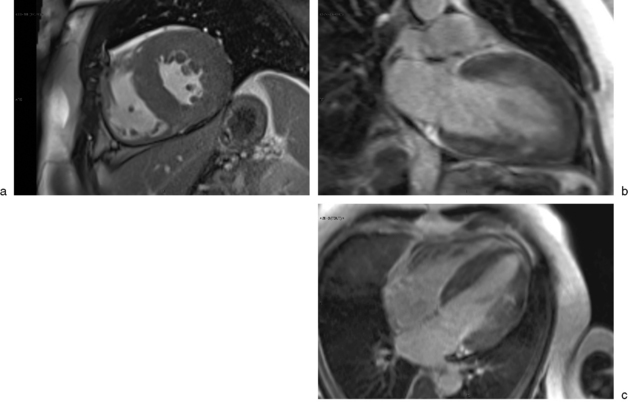
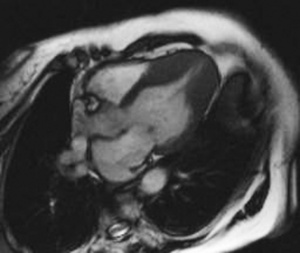
La cardiomyopathie hypertrophique (CMH) est définie par une hypertrophie myocardique primitive, non expliquée par une cause sous-jacente, comme un rétrécissement aortique ou une hypertension artérielle systémique. Une désorganisation des fibres myocardiques est associée à l’histologie [3,4]. Elle touche 0,2 % des adultes jeunes et représente la première cause de mort subite chez les athlètes. Un déterminisme génétique est présent dans 50 % des cas, avec une transmission autosomique dominante à pénétrance variable. L’histoire naturelle est variable, pouvant parfois aboutir à une mort subite par arythmie. La topographie et l’importance de la zone hypertrophique sont également variables (fig. 15.2 à 15.4).
Les séquences ciné-IRM segmentées sont indispensables pour évaluer les volumes d’éjection ventriculaire et la fraction d’éjection [5,6]. Dans les CMH, il existe une diminution des volumes ventriculaires télésystolique, télédiastolique et une augmentation fréquente de la fraction d’éjection du VG du fait de l’hypertrophie myocardique. Le rapport épaisseur pariétale/volume diastolique ou masse/volume du VG est un bon indicateur pour distinguer l’hypertrophie du sportif de l’hypertrophie primitive (dilatation ventriculaire chez l’athlète). Ces modifications s’accompagnent d’une dilatation et d’une diminution de la fraction d’éjection de l’oreillette gauche. Le myocarde hypertrophique est également moins compliant, ce qui se traduit par une diminution du pourcentage d’épaississement systolique, du raccourcissement circonférentiel et de la fraction d’épaississement.
L’injection de gadolinium peut amener des informations intéressantes en mettant en évidence des défauts de perfusion dans les zones hypertrophiques, probablement liés à des atteintes ischémiques régionales. L’existence de zones ischémiques est une des hypothèses avancées pour expliquer les morts subites observées chez des patients avec CMH. Surtout, les acquisitions tardives après injection de gadolinium peuvent mettre en évidence des prises de contraste anormales, surtout à la jonction septum et ventricule droit (VD), qui correspondent aux remaniements fibreux et à la désorganisation myofibrillaire [6]. Ces prises de contraste sont en général plutôt éparses, en mottes (patchy), médiopariétales, prédominant dans les régions les plus hypertrophiées, et sans distribution coronaire systématisée. Très fréquentes (7 à 8 fois sur 10), elles sont liées au phénotype (progression de l’hypertrophie) et non au génotype. La valeur pronostique de ces rehaussements tardifs est clairement établie (évolutivité de la maladie, fonction diastolique et systolique, risque de mort subite) et la corrélation entre l’étendue de ces prises de contraste « fibreuses » et la survenue de troubles du rythme a été démontrée par plusieurs auteurs [7].
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree