Chapitre 10 La médecine nucléaire
Techniques et principales utilisations
La médecine nucléaire est la seule technique d’imagerie fonctionnelle qui est le reflet direct du métabolisme cellulaire ou de voies métaboliques. En imagerie mammaire, si sa place dans le diagnostic des lésions mammaires néoplasiques apparaît limitée, elle a un rôle très important dans le bilan d’extension, la surveillance du traitement et la recherche de récidives. Mais c’est surtout dans l’évaluation de la réponse aux traitements que sa place ne cesse de croître notamment avec la tomographie par émission de positons (TEP) au FDG. Nous vous présentons dans ces quelques pages un instantané des indications actuelles de l’imagerie isotopique en pathologie mammaire néoplasique qui se veut volontairement très pratique et simple. En effet, les indications vont évoluer rapidement en raison du développement de nouvelles molécules pour l’imagerie TEP (permettant d’appréhender encore mieux la réponse tumorale aux traitements) et l’amélioration des matériels de détection : TEP temps de vol entre autre, caméras semi-conducteurs en imagerie scintigraphique monophotonique. Ces nouvelles caméras en plus d’augmenter de façon très significative la résolution spatiale ont une sensibilité accrue ce qui permet de diminuer de façon majeure les doses administrées aux patients donc de réduire l’irradiation de ces derniers.
Mammoscintigraphie (MMS)
Cette technique d’imagerie est apparue dès le milieu des années 1970 pour connaître un véritable essor, avec la parution de nombreux articles durant les années 1990. Elle est née des insuffisances des autres techniques d’imagerie utilisées durant cette période. Dans certaines études, explorant les performances de la mammographie, il était retrouvé des taux de faux négatif variant de 25 à 45 %, et donc une faible spécificité et valeur prédictive positive.
Nous allons passer en revue les différents radio-pharmaceutiques qui ont été utilisés en MMS.
Thallium 201 (Tl201)
Résultats cliniques
Le premier cas de captation du Tl201 par un cancer du sein a été rapporté par l’équipe de Hisada et al. [1] en 1978 chez deux patientes.
Cimitan et al. [2] avaient inclu 72 patientes présentant des masses mammaires anormales dépistées en mammographie ou en échographie. La sensibilité et la spécificité de la MMS étaient respectivement de 91 % et 95 %. La sensibilité variait en fonction de la taille de la lésion, 97 % quand la tumeur mesurait plus de 1,5 cm et 80 % pour des lésions de moins de 1,5 cm. La plus petite lésion dépistée mesurait 0,6 cm. La sensibilité dans le dépistage de l’envahissement ganglionnaire était de 27 %. Ces auteurs ont remarqué que l’intensité de la captation du Tl201 était plus dépendante de la taille et de la vascularisation de la tumeur que du grade, du statut hormonal ou de la présence d’emboles lymphatiques ou vasculaires.
Vaxman et al. [3] avaient inclu 81 patientes présentant des masses mammaires anormales palpables. La sensibilité et la spécificité étaient respectivement de 95 % et 91 %. La plus petite lésion dépistée mesurait 0,9 × 1,3 cm. La sensibilité dans le dépistage de l’envahissement ganglionnaire était de 57 %. Ils concluaient en soulignant que la MMS au Tl201 était une méthode efficace dans l’exploration des masses mammaires de plus de 1,5 cm.
Limites de la MMS au Tl201 et critères d’interprétation
• demi-vie longue (73 heures);
• dose injectée limitée en raison de son rayonnement;
• statistique de comptage faible limitant la résolution tant en mode planaire qu’en mode tomographique;
• artéfacts liés à la fixation physiologique du Tl201 au niveau du cœur, des muscles et du foie, limitant son utilisation dans les tumeurs du sein proches de ces organes.
MMS au Sestamibi marqué au technétium 99m
Technique
• Dose injectée (IV) : 740 MBq ajustés au poids.
• Images planaires décubitus et/ou procubitus (avec matelas d’examen adapté) : face antérieure, profils et éventuellement obliques antérieur et postérieur. Les acquisitions tomoscintigraphiques n’augmenteraient pas la sensibilité de la technique par rapport aux images planaires et en plus pourraient diminuer sa spécificité.
• Délai d’acquisition des images : images précoces 5 à 15 minutes après injection (les images tardives peuvent être source de faux négatifs quand la tumeur exprime le gène MDR). La durée de l’acquisition est généralement de 10 minutes (à augmenter dans les petites tumeurs).
Résultats cliniques
C’est en 1992, qu’Aktolum et al. [4] ont décrit pour la première fois l’utilisation de la MMS au 99mTc-Sestamibi dans le cancer du sein (étude comparant la MMS au 99mTc-Sestamibi à la MMS au Tl201).
La première série utilisant la MMS au 99mTc-Sestamibi seule dans la détection des cancers du sein est celle de Khalkhali et al. en 1994 [5]. Il s’agissait d’une série de 59 patientes présentant une mammographie et un examen clinique sénologique anormaux. Les résultats de cette étude sont les suivants : sensibilité 96 %, spécificité 87 %, valeur prédictive positive (VPP) 82 %, valeur prédictive négative (VPN) 97 %.
La plus grosse série était une étude multicentrique nord-américaine regroupant plus de 30 centres avec 673 patientes incluses [3]. Parmi les 673 patientes, 286 avaient une tumeur palpable et 387 avaient une tumeur non palpable. Les résultats de cette étude sont les suivants : sensibilité globale 85 %, spécificité globale 81 %; pour les tumeurs palpables : sensibilité 95 %, spécificité 74 %; pour les tumeurs non palpables : sensibilité 72 %, spécificité 86 %.
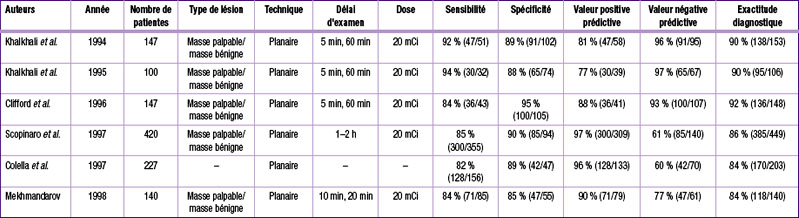
Les résultats des autres séries présentant une population étudiée de plus de 100 patientes sont présentés dans le tableau 10.1.
Tiling et al. [6] ont comparé la MMS au 99mTc-Sestamibi à l’IRM avec et sans injection dans le dépistage de cancer du sein chez 56 femmes suspectes de cancer. L’IRM est plus sensible que la MMS (91 % versus 88 %) mais moins spécifique (52 % versus 88 %).
Mammoscintigraphie à la tétrofosmine marquée au technétium 99m
Résultats cliniques
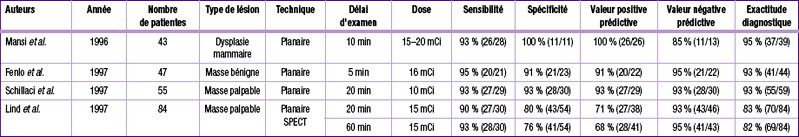
Ces résultats sont comparables à ceux obtenus avec le 99mTc-Sestamibi pour des lésions mammaires supracentimétriques. Les résultats des principales études sont présentés dans le tableau 10.2.
Mammoscintigraphie au méthylène diphosphonate (MDP) marqué au Technétium 99m
Mode de captation
La captation dans les cellules tumorales des tissus mous du 99mTc-MDP dépend :
• de la vascularisation du tissu tumoral (néovascularisation);
• de la teneur intracellulaire et intratumorale en calcium;
• des perturbations de la membrane cellulaire (souvent retrouvées dans les cellules tumorales);
• des modifications de l’espace extracellulaire et du pH dans les tissus tumoraux;
Résultats cliniques
C’est l’équipe de Piccolo, Lastoria et al. [7–9] du Centre national du cancer de Milan en Italie qui a la plus grande expérience de la MMS au 99mTc-MDP.
Mammoscintigraphie au 99mTc-MDP et critères d’interprétations
• MMS normale ou négative : fixation diffuse et homogène du 99mTc-MDP dont l’intensité correspond au bruit de fond mammaire (augmente pendant les menstruations);
• MMS avec aspect diffus : fixation diffuse mais dont l’intensité est supérieure au bruit de fond mammaire. Aspect noté dans les cancers inflammatoires et les carcinomes in situ diffus mais également dans les dysplasies diffuses;
• MMS avec aspect focal : fixation intense et focale du 99mTc-MDP. Aspect très souvent associé à un cancer;
• MMS avec aspect multifocal : fixation intense focale multiple. Aspect presque toujours associé à un cancer du sein.
Mammoscintigraphie utilisant d’autres radio-pharmaceutiques
• MMS utilisant des anticorps monoclonaux ou des peptides marqués. L’interprétation des résultats de ces études est rendue encore plus complexe en raison de la diversité des radio-isotopes utilisés pour le marquage (In111, Tc99m, I123, I131). De plus, il existe de nombreux facteurs limitants : le coût, une fixation non spécifique par le système réticulo-endothélial, une cinétique de fixation lente, la possibilité de développement de réaction immunogénique après injection du radio-traceur (anticorps antimurin);
• MMS utilisant des analogues de récepteurs. Récepteur à la somatostatine (octréotide marqué à l’In111). En effet 50 à 70 % des cancers du sein possèdent des récepteurs à la somatostatine;
• MMS utilisant des ligands ayant une forte affinité pour les récepteurs aux œstrogènes;
Lymphoscintigraphie mammaire avec détection du ganglion sentinelle (technique du ganglion sentinelle)
Introduction
En France depuis 1989, date du dépistage systématique du cancer du sein, la maladie est diagnostiquée à un stade de plus en plus précoce, donc la taille tumorale au moment du diagnostic est limitée. Le risque d’envahissement ganglionnaire, étant corrélé à la taille tumorale, est donc faible quand la tumeur est de petite taille. Par ailleurs, le statut ganglionnaire, élément de pronostic majeur sur la survie (spécifique et globale), guide la stratégie thérapeutique. La méta-analyse de Carter et al. en 1989 [10] montrait que 70 % des cancers du sein de moins de 2 cm sont N0. Ces constatations ont conduit à reconsidérer le caractère systématique du curage axillaire, ceci d’autant que l’impact sur la survie du curage axillaire n’est pas démontré, alors qu’il a un rôle très important pour permettre une stadification (TNM). Par ailleurs, le curage axillaire est source d’une morbidité élevée (environ 70 % des personnes ayant eu un curage ont des séquelles).
C’est dans ce contexte que la technique du ganglion sentinelle (GS) a connu un regain d’intérêt. En effet, il s’agit d’un concept ancien introduit en 1977 par Cabanas [11] et appliqué au cancer du sein à partir de 1994 par l’équipe de Giuliano et al. en validant ce principe sur une série de 107 patientes avec un taux d’identification du GS de 94 %.
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree