31 Microgreffes de cheveux
Introduction
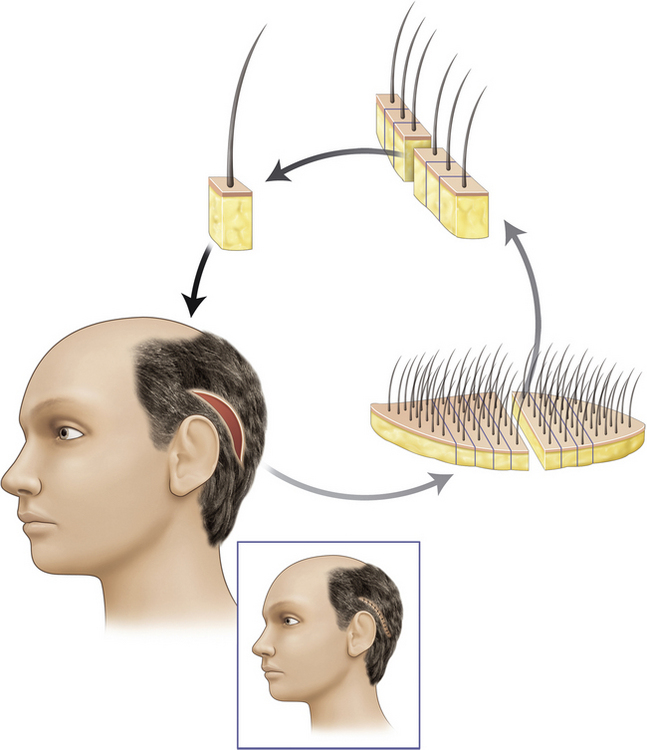
Les prémices de la greffe de cheveux furent observées au Japon en 1939. Le docteur Shoji Okuda publia 200 cas de reconstruction d’alopécie cicatricielle et congénitale par transplantation autologue de cheveux [1]. Cependant, la paternité de la greffe de cheveux dans la reconstruction de l’alopécie androgénique revient au Dr Orentreich, dermatologue new-yorkais, qui décrivit le principe de l’aire dominante en 1959 [2]. Ce dernier établit que les cheveux prélevés en zone occipitale puis, transplantés en zone alopécique, continuaient leur croissance sans souffrir de la chute des cheveux de la zone d’implantation, même à long terme. Puis c’est à partir de la description histologique des unités folliculaires (UF) par Headington [3] qu’apparaîtront les nouveaux standards de la microgreffe de cheveux, réduisant la taille des greffons en unités folliculaires par la découpe de la bandelette occipitale au microscope, puis leur transplantation se fera dans des microfentes [4], reprenant le dessin d’une implantation « naturelle » [5] (Figure 31.1).
Les techniques de prélèvements de la zone donneuse ont également permis de rendre la cicatrice occipitale imperceptible, que ce soit en réalisant une suture dite « trichophytique » [6], ou grâce à l’extraction des unités folliculaires (FUE) [7].
Consultation préopératoire
Un temps majeur, indispensable
La consultation permet d’établir :
 les données médicales du patient concernant son problème capillaire, avec la liste des interventions déjà effectuées, ainsi que la prise des traitements en cours (finastéride, minoxidil, etc.) ;
les données médicales du patient concernant son problème capillaire, avec la liste des interventions déjà effectuées, ainsi que la prise des traitements en cours (finastéride, minoxidil, etc.) ; les contre-indications opératoires devant nécessiter une prise en charge particulière lors de l’intervention : prévention d’une endocardite, prise d’anticoagulant ou d’aspirine qui risque de majorer le saignement peropératoire, diabète, immunosuppression, etc.
les contre-indications opératoires devant nécessiter une prise en charge particulière lors de l’intervention : prévention d’une endocardite, prise d’anticoagulant ou d’aspirine qui risque de majorer le saignement peropératoire, diabète, immunosuppression, etc.Cette consultation permet d’exposer au patient :
 le type de procédure chirurgicale proposée, avec toutes ses modalités ainsi que les suites opératoires habituelles et les effets secondaires, même les plus rares ;
le type de procédure chirurgicale proposée, avec toutes ses modalités ainsi que les suites opératoires habituelles et les effets secondaires, même les plus rares ;Plusieurs points importants sont à préciser au patient :
 la chirurgie ne permet pas de multiplier les cheveux ni d’obtenir plus de cheveux qu’il n’en existe sur le cuir chevelu, il s’agit d’une technique de répartition ;
la chirurgie ne permet pas de multiplier les cheveux ni d’obtenir plus de cheveux qu’il n’en existe sur le cuir chevelu, il s’agit d’une technique de répartition ; le patient doit comprendre que l’alopécie androgénique ou AAG est un processus évolutif dont il est difficile d’apprécier le stade tardif ;
le patient doit comprendre que l’alopécie androgénique ou AAG est un processus évolutif dont il est difficile d’apprécier le stade tardif ; ce résultat ne se résume pas uniquement à la densité capillaire obtenue, mais dépend pour une grande partie de la configuration morphologique redonnée au visage du patient. La restauration des contours entre le visage et le cuir chevelu prend ici toute sont importance ;
ce résultat ne se résume pas uniquement à la densité capillaire obtenue, mais dépend pour une grande partie de la configuration morphologique redonnée au visage du patient. La restauration des contours entre le visage et le cuir chevelu prend ici toute sont importance ; en dépit d’une appréciation minutieuse du résultat de l’intervention, une certaine part d’inconnu existe, en particulier de par l’absence de donnée quant à la rapidité de l’évolutivité et des futures zones atteintes par le processus androgénique. Le patient devra bien en prendre conscience et accepter cette incertitude ;
en dépit d’une appréciation minutieuse du résultat de l’intervention, une certaine part d’inconnu existe, en particulier de par l’absence de donnée quant à la rapidité de l’évolutivité et des futures zones atteintes par le processus androgénique. Le patient devra bien en prendre conscience et accepter cette incertitude ; compte tenu de cet aspect évolutif de l’alopécie, le patient doit être prévenu qu’il sera possible d’envisager d’autres séances dans le futur afin de maintenir le résultat esthétique obtenu.
compte tenu de cet aspect évolutif de l’alopécie, le patient doit être prévenu qu’il sera possible d’envisager d’autres séances dans le futur afin de maintenir le résultat esthétique obtenu.Une ordonnance pour un bilan sanguin préopératoire ainsi qu’une prescription de prémédication seront remises au patient. Un document d’information consentement, ainsi qu’un devis précisant le montant exact de l’intervention sera établi. Un délai de réflexion de 15 jours avant l’intervention devra être respecté.
Sélection des bonnes indications opératoires
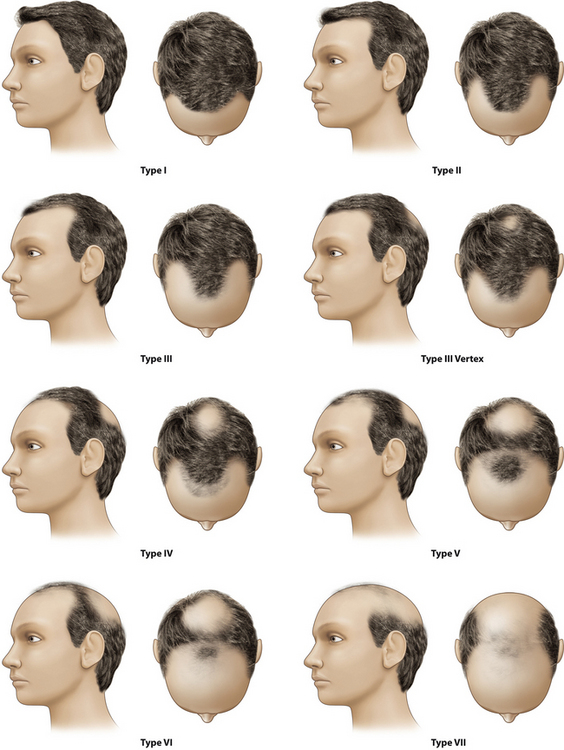
 dans la grande majorité des cas, les bonnes indications opératoires chez l’homme sont pour les stades III à V. Les stades précoces I et II ne donnent pas d’amélioration esthétique conséquente et risquent de ne pas satisfaire le patient. Les stades Va à VII sont généralement des stades trop avancés, ils sont le plus souvent de mauvaises indications à la microgreffe de cheveux ; (cf. Figure 31.8)
dans la grande majorité des cas, les bonnes indications opératoires chez l’homme sont pour les stades III à V. Les stades précoces I et II ne donnent pas d’amélioration esthétique conséquente et risquent de ne pas satisfaire le patient. Les stades Va à VII sont généralement des stades trop avancés, ils sont le plus souvent de mauvaises indications à la microgreffe de cheveux ; (cf. Figure 31.8) la souplesse du cuir chevelu au niveau occipital sera évaluée par l’examen physique de cette zone. Une bonne souplesse est indispensable à la bonne fermeture sans tension de la zone donneuse et au résultat cicatriciel ;
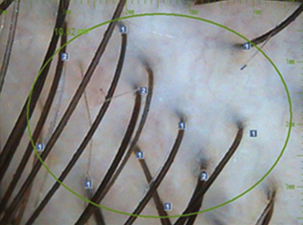
la souplesse du cuir chevelu au niveau occipital sera évaluée par l’examen physique de cette zone. Une bonne souplesse est indispensable à la bonne fermeture sans tension de la zone donneuse et au résultat cicatriciel ; la densité de la région occipitale, ainsi que le calibre des cheveux, seront mesurés avant toute intervention. La densité moyenne chez l’homme est supérieure à 55 UF\cm2. En dessous de 40 UF\cm2, le patient n’est pas une bonne indication opératoire (Figure 31.2).
la densité de la région occipitale, ainsi que le calibre des cheveux, seront mesurés avant toute intervention. La densité moyenne chez l’homme est supérieure à 55 UF\cm2. En dessous de 40 UF\cm2, le patient n’est pas une bonne indication opératoire (Figure 31.2).
Fig. 31.2 Cheveux de la zone donneuse très fins, en dessous de 40 µm, mauvaise indication opératoire.
Le problème de la tonsure
La demande de réparation esthétique la concernant est fréquente chez l’homme et ce à tout âge.
Cette demande doit être tempérée pour de nombreuses raisons :
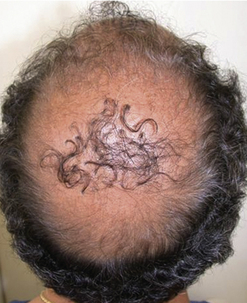
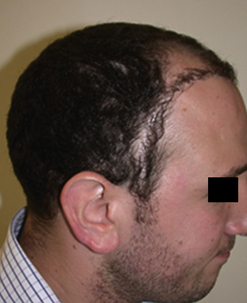
 son extension évolutive est difficilement prévisible avant 40 ans. La progression de l’alopécie se fait de façon centrifuge, risquant de donner un aspect inesthétique (Hare Krishna Syndrome) [8] lors d’une correction trop précoce avec poursuite de l’évolution alopéciante (Figure 31.3) ;
son extension évolutive est difficilement prévisible avant 40 ans. La progression de l’alopécie se fait de façon centrifuge, risquant de donner un aspect inesthétique (Hare Krishna Syndrome) [8] lors d’une correction trop précoce avec poursuite de l’évolution alopéciante (Figure 31.3) ; sa réparation nécessite un grand nombre de microgreffes, et plusieurs séances, ce qui ampute le réservoir de la zone donneuse au détriment de la zone frontopariétale plus importante esthétiquement à réparer ;
sa réparation nécessite un grand nombre de microgreffes, et plusieurs séances, ce qui ampute le réservoir de la zone donneuse au détriment de la zone frontopariétale plus importante esthétiquement à réparer ; l’orientation capillaire y est divergente (tourniquet), rendant la réparation par implantation difficile ;
l’orientation capillaire y est divergente (tourniquet), rendant la réparation par implantation difficile ; la chirurgie de réduction assistée ou non d’extenseur était de ce fait souvent proposée pour en limiter la surface. Les complications et les cicatrices résiduelles parfois importantes qui accompagnent cette technique en font aujourd’hui une procédure moins pratiquée.
la chirurgie de réduction assistée ou non d’extenseur était de ce fait souvent proposée pour en limiter la surface. Les complications et les cicatrices résiduelles parfois importantes qui accompagnent cette technique en font aujourd’hui une procédure moins pratiquée.Médicaments
En aucun cas la microgreffe de cheveux n’arrête le processus évolutif alopéciant de l’AAG comme peuvent le penser certains patients qui demandent à se faire opérer pour pouvoir arrêter leurs traitements. Le minoxidil [9] et le finastéride [10] ont montré leurs effets positifs sur la correction de l’alopécie, tant sur l’amélioration de la densité que sur l’augmentation des diamètres des cheveux. Le finastéride a également prouvé son efficacité [11] en association à la microgreffe de cheveux, en augmentant la densité et la qualité des cheveux préexistants autour des microgreffons. Ces traitements permettront de stabiliser l’AAG, d’augmenter la densité visuelle de façon importante et de maintenir le résultat de la microgreffe de façon prolongée.
Examen vidéomicroscopique
Signes dermoscopiques spécifiques de l’alopécie androgénique
 Variabilité des diamètres supérieure à 20 % [12], qui reflète la miniaturisation des cheveux (Figure 31.4).
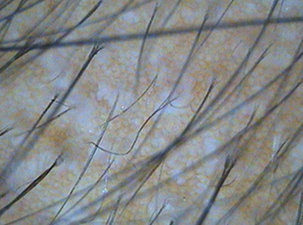
Variabilité des diamètres supérieure à 20 % [12], qui reflète la miniaturisation des cheveux (Figure 31.4). Présence de points jaunes, correspondant à un aspect visible de la glande sébacée et de la kératinisation de l’ostium vacant (Figure 31.5).
Présence de points jaunes, correspondant à un aspect visible de la glande sébacée et de la kératinisation de l’ostium vacant (Figure 31.5). Présence d’un réseau pigmenté cutané, due à l’exposition de la peau directe au soleil (Figure 31.6) [13].
Présence d’un réseau pigmenté cutané, due à l’exposition de la peau directe au soleil (Figure 31.6) [13].
Fig. 31.5 Points jaunes visibles, correspondant à des ostiums vides dus au retard de la phase anagène.
Aujourd’hui, certains logiciels couplés à une vidéocaméra (Figure 31.7) permettent de déterminer avec une grande précision les différentes données relatives au cuir chevelu [14].
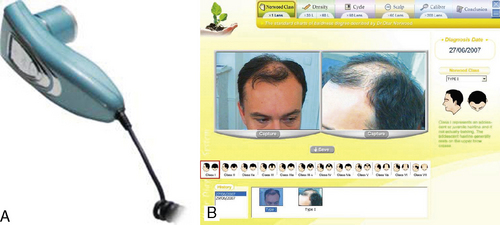
Fig. 31.7 Folliscope : logiciel avec caméra USB permettant de réaliser une vidéomicroscopie du cuir chevelu.
Ces logiciels réalisent des photographies standards qui définissent le stade de l’alopécie dans la classification de Norwood (Figure 31.8).
Dans tous les cas, l’étude du cuir chevelu en vidéomicroscopie sera un préalable indispensable à tout acte chirurgical de microgreffe. Ces images par vidéomicroscopie ont aujourd’hui montré leur intérêt dans la pose des indications opératoires [15]. Ils déterminent les densités de cheveux par cm2 sur les zones receveuses et sur la zone donneuse (Figure 31.9).
Intérêt de la mesure du taux de miniaturisation
 Sur la zone receveuse, la mesure d’un taux de miniaturisation supérieur à 20 % permet de confirmer le diagnostic d’AAG par la présence de cheveux miniaturisés. Si le taux de miniaturisation est supérieur à 50 %, cela indique une activité importante de miniaturisation et donc une atteinte importante et rapide de l’alopécie. Dans ce cas, le risque et l’importance d’un effluvium postopératoire est majeur et le ou la patiente doit en être informé(e). Ce phénomène est particulièrement observé chez la femme. La prescription préventive de minoxidil dans les périodes pré et postopératoire luttera contre cette chute de cheveux [16].
Sur la zone receveuse, la mesure d’un taux de miniaturisation supérieur à 20 % permet de confirmer le diagnostic d’AAG par la présence de cheveux miniaturisés. Si le taux de miniaturisation est supérieur à 50 %, cela indique une activité importante de miniaturisation et donc une atteinte importante et rapide de l’alopécie. Dans ce cas, le risque et l’importance d’un effluvium postopératoire est majeur et le ou la patiente doit en être informé(e). Ce phénomène est particulièrement observé chez la femme. La prescription préventive de minoxidil dans les périodes pré et postopératoire luttera contre cette chute de cheveux [16]. Sur la zone donneuse occipitale, la mesure de la densité permet de déterminer la quantité d’unités folliculaires et de cheveux par cm2 disponible au prélèvement. Cette mesure est extrêmement importante afin de déterminer la quantité de greffons disponibles pour recouvrir et densifier la zone receveuse. La majorité des patients caucasiens ont une densité de 60 à 100 unités folliculaires\cm2 [17].
Sur la zone donneuse occipitale, la mesure de la densité permet de déterminer la quantité d’unités folliculaires et de cheveux par cm2 disponible au prélèvement. Cette mesure est extrêmement importante afin de déterminer la quantité de greffons disponibles pour recouvrir et densifier la zone receveuse. La majorité des patients caucasiens ont une densité de 60 à 100 unités folliculaires\cm2 [17]. Si le taux de miniaturisation de cette zone est élevé, supérieur à 20 %, cela signifie que les cheveux de la zone donneuse sont également atteints par le processus de miniaturisation. L’indication opératoire devient alors à risque car le patient présente une alopécie diffuse et extensive à tout le cuir chevelu [18]. Les cheveux implantés vont évoluer vers une miniaturisation et une chute définitive, faisant perdre le caractère permanent de la transplantation.
Si le taux de miniaturisation de cette zone est élevé, supérieur à 20 %, cela signifie que les cheveux de la zone donneuse sont également atteints par le processus de miniaturisation. L’indication opératoire devient alors à risque car le patient présente une alopécie diffuse et extensive à tout le cuir chevelu [18]. Les cheveux implantés vont évoluer vers une miniaturisation et une chute définitive, faisant perdre le caractère permanent de la transplantation.Recommandations pour les patients de moins de 30 ans [19]
L’indication la plus controversée reste celle du sujet jeune, de moins de 30 ans. Plus l’alopécie débute tôt dans la vie et plus longue sera son évolution et plus avancé sera son stade. C’est dans ces cas qu’une bonne prise en charge médicale est souvent nécessaire, afin de freiner l’évolution et de stabiliser l’évolution. L’indication opératoire est le plus souvent contre-indiquée, car on ne peut prédire l’évolution future de l’alopécie (Figure 31.10).
Indications
Alopécie androgénique
C’est la principale indication de la microgreffe de cheveux. Elle se définit par la raréfaction diffuse et par la diminution de la densité des cheveux chez des patients génétiquement prédisposés. Il se produit sur les follicules pileux un processus de miniaturisation qui transforme les cheveux terminaux en cheveux à type de duvets fins et courts, sous l’influence de facteurs héréditaires et androgéniques.
Chez l’homme, sa prévalence a été bien documentée et rapportée par Hamilton [20] et Norwood [21]. Ils ont, les premiers, décrit une classification en 7 stades évolutifs (cf. Figure 31.8).
Chez la femme, la classification établie par Ludwig [22] est aujourd’hui la plus utilisée, même si elle n’est pas réellement adaptée aux différentes situations cliniques rencontrées. Le début de l’AAG féminine se fait préférentiellement vers la fin de la 20e année jusqu’à la quarantaine. Deux principales formes cliniques ont été décrites :
 la première, la plus fréquente, est celle décrite par Ludwig, avec une raréfaction diffuse de la chevelure sur le vertex et la partie frontale mais qui respecte le plus souvent une fine bandelette chevelue antérieure ;
la première, la plus fréquente, est celle décrite par Ludwig, avec une raréfaction diffuse de la chevelure sur le vertex et la partie frontale mais qui respecte le plus souvent une fine bandelette chevelue antérieure ; la deuxième est la même forme que celle décrite chez l’homme avec le classique recul frontotemporal qui représente respectivement 15 % des femmes en préménopause, puis 30 % en post-ménopause [23].
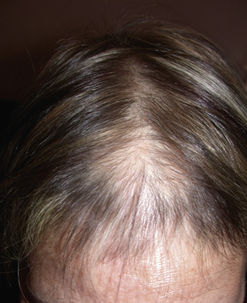
la deuxième est la même forme que celle décrite chez l’homme avec le classique recul frontotemporal qui représente respectivement 15 % des femmes en préménopause, puis 30 % en post-ménopause [23].Une troisième forme dite « en arbre de Noël » a également été décrite par Olsen [24]. Celle-ci dégarnit la chevelure de la partie médiofrontale de la femme en forme de triangle, à l’image d’un sapin (Figure 31.11). Enfin, il existe une quatrième forme extrêmement diffuse à l’ensemble du cuir chevelu et qui atteint également la zone occipitale, habituellement préservée par le processus androgénique. Le diagnostic de cette forme diffuse (25 % chez la femme) est une contre-indication à une intervention de transplantation capillaire (Figure 31.12). Plus de 30 % des femmes, après la ménopause, sont atteintes d’alopécie androgénique. Cependant, chez la femme, l’alopécie peut être multifactorielle et on s’assurera bien de la réalité du diagnostic d’alopécie androgénique par un bilan clinique et biologique qui permettra d’éliminer une autre cause parfois associée à cette alopécie, comme une carence vitaminée, ou en fer, ainsi qu’un dysfonctionnement hormonal.
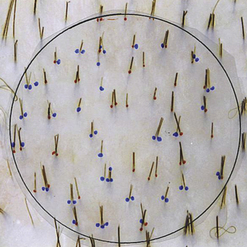
Fig. 31.12 AAG avec atteinte diffuse occipitale : densité totale 144 ; taux de miniaturisation 54,2 %.
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree