Chapitre 4 Traitement cœliochirurgical de la grossesse extra-utérine 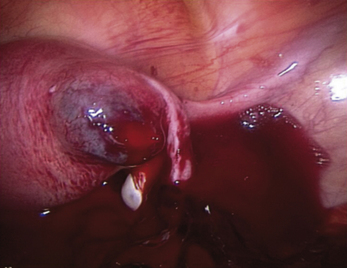
– traiter par cœlioscopie les GEU rompues ou à risque important de rupture ;
– toujours informer la patiente du risque de conversion en laparotomie et du risque de salpingectomie ;
– le choix entre salpingotomie et salpingectomie dépend de facteurs pré- et peropératoires ;
– pour la salpingotomie, utiliser une pointe fine monopolaire ;
– inciser toute l’épaisseur de la paroi tubaire sur son bord antimésial en regard du sac ectopique ;
– attention, le sac ectopique est toujours plus proche de l’utérus que l’hématosalpinx ;
– utiliser une canule de 10 mm pour aspirer efficacement tout le trophoblaste ;
– en cas de traitement conservateur proscrire les préhensions intempestives de la trompe ou des coagulations étendues sur sa muqueuse ;
– pour la salpingectomie, réaliser les séquences de coagulation-section du mésosalpinx au plus près de la trompe pour épargner la vascularisation de l’ovaire.
Avec environ 14 000 cas annuels en France, la grossesse extra-utérine (GEU) demeure l’urgence gynécologique par excellence, de par sa fréquence mais également de par sa gravité, puisqu’elle peut mettre en péril le pronostic vital [14]. Réalisé pour la première fois en 1973 par Bruhat et Manhès à Clermont-Ferrand, le traitement cœliochirurgical de la GEU est actuellement considéré comme le traitement de référence [2]. Il s’agit en fait d’un des tous premiers gestes chirurgicaux réalisés par cœlioscopie. Le traitement laparoscopique de la GEU tubaire peut être conservateur (salpingotomie) ou radical (salpingectomie). Les GEU extratubaires sont rares et leur traitement n’est pas codifié.
Indications du traitement chirurgical
Le choix d’un traitement médical ou chirurgical repose sur un faisceau d’arguments à la fois cliniques, échographiques et biologiques [3, 12, 17]. En pratique, l’indication d’un traitement chirurgical est retenue, soit d’emblée devant un tableau évocateur d’une GEU rompue ou à risque important de rupture, soit après échec du traitement médical. Par ailleurs, le traitement médical est également contre-indiqué en cas de difficultés de compréhension du protocole par la patiente ou du fait d’un éloignement géographique. Dans tous les cas, les modalités du traitement et de sa surveillance doivent recevoir l’adhésion complète de la patiente.
Cœlioscopie ou laparotomie ?
Une étude tirée du registre auvergnat, qui est actuellement le plus important registre des GEU, rapporte qu’entre 1992 et 1996, sur 835 GEU étudiées, 83 % ont été traitées exclusivement par cœlioscopie, 10 % par laparotomie et 7 % par méthotrexate [1]. Le traitement cœlioscopique de la GEU s’est imposé comme une technique fiable et parfaitement reproductible. Jouissant des avantages indéniables de cette voie d’abord, par rapport à la laparotomie en termes de qualité de vie pour les patientes, de coût pour la collectivité (réduction des adhérences et des douleurs postopératoires, le rétablissement rapide permettant un raccourcissement du séjour, bénéfices esthétiques) mais également sur le plan technique [18]. La cœlioscopie comporte, en fait, une seule contre-indication absolue : l’inexpérience du chirurgien en laparoscopie. Les autres contre-indications habituelles, comme un hémopéritoine massif et un état hémodynamique instable, une obésité morbide, une volumineuse hématocèle enkystée ou une GEU interstitielle ne sont plus considérées comme indiscutables par les équipes disposant d’une bonne expérience cœliochirurgicale et d’un matériel adapté. Le facteur limitant résidera plus dans les problèmes liés à l’anesthésie que dans ceux liés à la cœlioscopie elle-même : une bonne concertation préopératoire, au cas par cas, entre le chirurgien et l’anesthésiste permettra de définir au mieux la voie d’abord.
Approche cœliochirurgicale de la grossesse extra-utérine
Installation et matériel
L’insufflation de la cavité péritonéale est effectuée après réalisation des tests de sécurité habituels (voir chapitre 1). Dans la majorité des cas, l’optique est introduite par un trocart de 10 mm en transombilical et les instruments par trois trocarts opérateurs qui sont placés de la manière suivante : un de 5 mm dans chaque fosse iliaque et un de 10 mm en sus-pubien avec un capuchon réducteur de 5 mm. Le placement des voies d’abord pourra être modifié en fonction des caractéristiques de la GEU, des difficultés opératoires et des habitudes des opérateurs. Il est important de disposer d’un système d’aspiration efficace et de diamètre suffisant. Dans notre pratique, nous utilisons le plus souvent la canule d’aspiration de 10 mm de diamètre afin d’évacuer rapidement un éventuel hémopéritoine, mais aussi pour aspirer efficacement tout le trophoblaste.
Premiers temps de l’intervention
Les premiers temps de l’intervention comportent toujours :
• l’exposition du pelvis avec une toilette péritonéale ;
• l’aspiration d’un éventuel hémopéritoine qui permettra une bonne visibilité du pelvis ainsi qu’un rétablissement de la luminosité (fig. 4.1) ;
• la mise en position de Trendelenburg et le refoulement délicat des anses digestives au-dessus du promontoire à l’aide d’une pince atraumatique ;
• la confirmation du diagnostic et de la localisation de la GEU ;
• l’hémostase élective en cas de saignement actif ;
• l’exploration abdomino-pelvienne et le recueil des informations nécessaires pour la décision thérapeutique et l’établissement du pronostic de la fertilité.
Diagnostic cœlioscopique de la grossesse extra-utérine
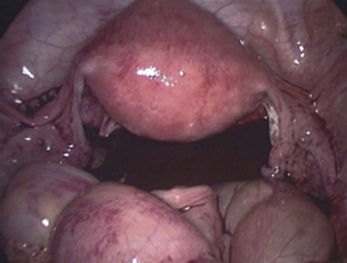
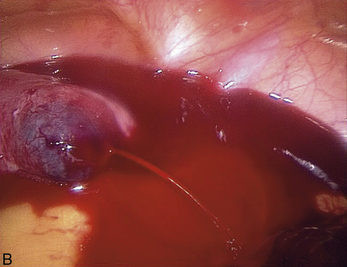
La GEU se présente, dans sa localisation la plus fréquente, au niveau ampullaire sous la forme d’une trompe tendue par le trophoblaste et l’épanchement sanguin intratubaire (hématosalpinx), violacée, pouvant être fissurée, voire rompue et associée à un hémopéritoine de volume variable (fig. 4.2). Parfois, la GEU n’est pas visible, mais « palpable » sous la forme d’une induration tubaire, lorsque la prise en charge chirurgicale a été précoce. En cas d’avortement tubaire pavillonnaire, la GEU expulsée est « noyée » dans l’hémopéritoine. L’exploration pelvienne quantifie l’hémopéritoine. Si le siège tubaire de la grossesse n’est pas établi, il convient d’envisager un siège ovarien ou abdominal (mésentère ou épiploon).
Salpingotomie ou salpingectomie ?
• le désir de la patiente : chez les patientes ayant des enfants et ne désirant plus de grossesse, le traitement logique de la GEU est la salpingectomie, associée ou non à une stérilisation tubaire controlatérale ;
• les antécédents : le risque de récidive de GEU est important en cas d’antécédent de plastie tubaire homolatérale ou de GEU ;
• l’état tubaire homolatéral et controlatéral : en cas de trompe altérée, la salpingectomie est le traitement de choix ;
• les difficultés opératoires : un saignement tubaire non maîtrisable peut mener à une salpingectomie.
Nous utilisons un score [20] qui affecte un coefficient à chacun des facteurs influençant de façon significative la fertilité après GEU (tableau 4.1). L’élévation de ce score va de pair avec une élévation du risque de récidive de GEU et une altération du pronostic de la fertilité.
• En cas de score inférieur à 4, un traitement conservateur offre de grandes chances de GIU spontanée par la suite.
• En cas de score égal à 4, nous optons pour un traitement radical. En effet, les chances de GIU et les risques de GEU s’avèrent à peu près identiques mais dans la mesure où les récidives sont essentiellement homolatérales, en cas d’antécédents tubaires, cette attitude permettrait d’augmenter les chances de GIU (en diminuant les risques de GEU).
• En cas de score supérieur à 4, nous réalisons une salpingectomie avec, le plus souvent, une stérilisation controlatérale car le taux de récidive de GEU est largement supérieur au taux de GIU. La patiente est ensuite orientée en fécondation in vitro en cas de désir de grossesse.
Tableau 4.1 Score préthérapeutique de Pouly.
| Antécédents | Points |
|---|---|
| GEU | 2 |
| Adhésiolyse | 1 |
| Microchirurgie tubaire | 2 |
| Trompe unique | 2 |
| Salpingite | 1 |
| Laparoscopie | Points |
|---|---|
| Adhérences homolatérales | 1 |
| Adhérences controlatérales | 1 |
| Score décisionnel | Total |
|---|---|
| Traitement conservateur | 1 à 3 |
| Salpingectomie | 4 |
| Salpingectomie et stérilisation tubaire controlatérale | > 4 |
Par ailleurs, il est démontré que les patientes n’ayant aucun antécédent de chirurgie tubaire ou d’infertilité et ayant une trompe controlatérale saine, présentent une fertilité comparable après un traitement radical ou conservateur [9].
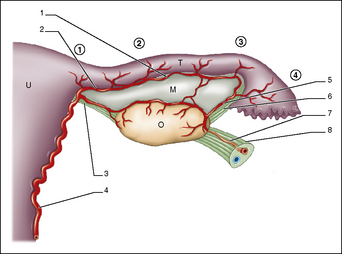
Anatomie
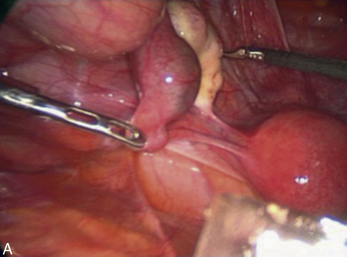
La trompe utérine est composée de quatre segments (fig. 4.3) : la jonction interstitielle ou intramurale, l’isthme, l’ampoule – site naturel de la fécondation – et l’infundibulum. La vascularisation de la trompe est assurée par deux artères : l’artère tubaire médiale, branche terminale de l’artère utérine et l’artère tubaire latérale, branche terminale de l’artère ovarique. Ces deux artères s’anastomosent au niveau de l’arcade infratubaire.
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree









 : jonction interstitielle ;
: jonction interstitielle ;  : isthme de la trompe ;
: isthme de la trompe ;  : ampoule tubaire ;
: ampoule tubaire ;  : infundibulum.
: infundibulum.





