Chapitre 4 Scanner cardiaque
principes, protocole d’acquisition et dosimétrie
En dépit d’une qualité d’image désormais tout à fait satisfaisante, les évolutions du scanner cardiaque multicoupe continuent, passant notamment par le développement d’un nombre accru de détecteurs coupant plus fin et d’un temps de rotation du tube de plus en plus rapide, améliorant ainsi les résolutions spatiale et temporelle (tableau 4.1). D’autre part, le champ d’action du scanner cardiaque s’élargit : il ne se limite plus à l’analyse morphologique, mais propose également une analyse fonctionnelle (étude de la plaque athéromateuse et évaluation de la perfusion myocardique) avec l’introduction de la biénergie et de l’imagerie spectrale.
Tableau 4-1 Résolutions spatiale et temporelle en fonction des différentes évolutions technologiques des scanners multicoupes : comparatif avec la coronarographie.
| Type d’imagerie | Résolution spatiale (mm) | Résolution temporelle (ms) |
|---|---|---|
| Scanner 4 coupes | 1,0–1,25 | 250 |
| Scanner 16 coupes | 0,75 | 165–188 |
| Scanner 64 coupes monotube | 0,5–0,6 | 165 |
| Scanner 64 coupes bitube | 0,5–0,6 | 75–83 |
| Scanner 256/320 coupes | 0,5–0,6 | 135–175 |
| Coronarographie | 0,2 | 20 |
Principes
L’exploration du cœur, et notamment des artères coronaires, impose des résolutions spatiale et temporelle élevées [1]. En effet, le petit calibre des vaisseaux étudiés (de 4 à 1 mm de diamètre) et les mouvements cardiaques entraînent de nombreuses contraintes. Pour obtenir une qualité d’image satisfaisante permettant une analyse fiable de la lumière des vaisseaux coronaires, il est nécessaire d’acquérir une image permettant la visualisation d’un voxel isotropique inframillimétrique et s’affranchissant des artéfacts de flou cinétique. De plus, l’acquisition doit être synchronisée avec le rythme cardiaque du patient et être la plus courte possible, afin que celui-ci puisse tenir une apnée raisonnable et de réduire les risques d’artéfacts respiratoires, de survenue de trouble de rythme ou de rehaussement veineux qui pourraient gêner l’interprétation.
La qualité d’image d’un examen dépend donc de différents critères, certains prédéfinis par les constructeurs (temps de rotation du tube, type et nombre de détecteurs), d’autres opérateurs-dépendants (voltage et tension du tube, acquisition prospective ou rétrospective, protocole d’injection, volume d’acquisition), et c’est le compromis entre ces différents critères qui permettra d’obtenir une image interprétable en limitant au maximum l’irradiation du patient [2].
Protocole d’acquisition
Préparation du patient
Le patient sera ensuite installé en décubitus dorsal sur la table d’examen. Une voie veineuse de bon calibre sera posée au pli du coude (cathlon vert si possible). Les électrodes seront appliquées sur une peau nettoyée et sèche. Leur positionnement devra donner un tracé adéquat avec une amplitude de l’onde R suffisante. Si la fréquence cardiaque est trop élevée, l’administration d’un β-bloquant par voie orale 1 à 2 heures avant l’examen (par exemple le métoprolol [Lopressor®]), qui a un taux plasmatique maximal 1,5 heure après administration de 100 mg en sublingual) ou par voie intraveineuse immédiatement avant l’acquisition (par exemple l’aténolol [Ténormine®], 1 ampoule de 50 mg en IVL), peut être conseillée. Ces produits ont les contre-indications classiques des β-bloquants, à savoir bradycardie spontanée inférieure à 50/min, insuffisance cardiaque sévère, blocs auriculoventriculaires, asthme et bronchopneumopathie obstructive. Certaines équipes recommandent également l’utilisation de trinitrine pour vasodilater les artères coronaires (une pulvérisation sublinguale de Natispray® avant l’acquisition).
Modes d’acquisition
En cas d’arythmie, la prise en compte de celle-ci peut se faire de façon prospective ou rétrospective en fonction des constructeurs : de façon prospective, les battements cardiaques erratiques sont éliminés en temps réel lors de l’acquisition des données (fig. 4.1), alors que de façon rétrospective, des logiciels d’édition d’ECG permettent de modifier les fenêtres de reconstruction a posteriori en cas de variation de rythme cardiaque pour éliminer une extrasystole.
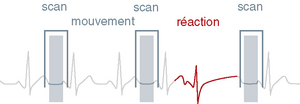
Fig. 4-1 Prise en compte prospective des arythmies.
Les battements cardiaques erratiques sont éliminés en temps réel lors de l’acquisition des données.
Reproduit avec l’autorisation de Siemens.
Par ailleurs, la rapidité des nouveaux scanners offre la possibilité de réaliser des acquisitions sur un seul battement cardiaque, soit par une couverture très large (Aquilion™ 320 détecteurs, Toshiba), soit par une acquisition spiralée bitube permettant un pitch large et une vitesse de rotation élevée pour une acquisition en 250 ms sur une diastole (mode Flashspiral™ chez Siemens) [fig. 4.2]. L’acquisition sur une seule diastole diminue considérablement le risque d’arythmie. L’élargissement de la couverture permet donc une acquisition séquentielle rapide, faiblement irradiante (peu de paliers, appareil Philips 256 coupes).
Acquisition des images
Certaines équipes préconisent la réalisation d’une acquisition sans injection de produit de contraste pour calcium scoring. Ceci permet d’évaluer les calcifications coronariennes. On utilise alors une synchronisation prospective avec des coupes plus épaisses, de l’ordre de 2,5 mm d’épaisseur, en diastole. Un post-traitement spécifique permet une évaluation globale de la charge calcique selon un procédé dérivé du score d’Agatston [3] : un score inférieur à 100 traduit une charge calcique faible, un score compris entre 101 et 400 traduit une charge calcique modérée, et un score supérieur à 400 traduit une charge calcique élevée. La valeur prédictive de cette charge calcique sur des événements ischémiques ultérieurs demeure très controversée. Cependant, cette première acquisition permet d’ajuster au mieux le champ d’acquisition nécessaire à l’exploration désirée (paramétrage du début de la boîte d’acquisition au niveau des ostiums des artères coronaires et de la fin de la boîte d’acquisition à la sortie du ventricule gauche).
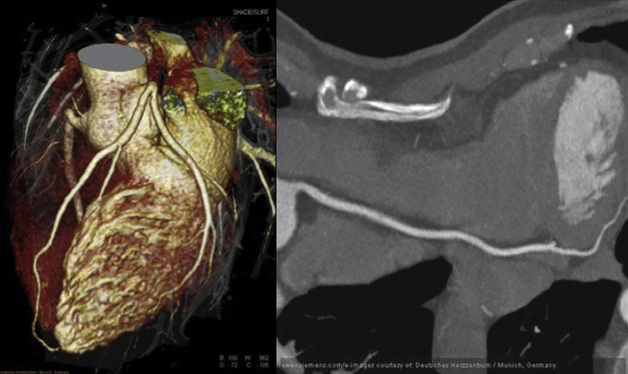
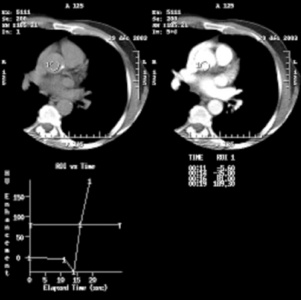
Une fois le type d’acquisition choisi et le volume d’acquisition déterminé, le déclenchement de l’acquisition proprement dite se fait sous contrôle fluoroscopique dès qu’un rehaussement de 100 UH (unités Hounsfield) est obtenu dans une région d’intérêt prédéfinie au niveau de l’aorte ascendante ou de l’aorte isthmique, pour éviter les artéfacts liés à la forte concentration de produit de contraste dans la veine cave supérieure (fig. 4.3).
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree