Chapitre 3 Ce que le radiologue doit savoir de la pathologie du sein
Lésions principales
Lésions bénignes principales
Mastopathie fibrokystique (MFK)
C’est la lésion bénigne la plus fréquente, décrite sous de multiples appellations (états fibrokystiques, mastose sclérokystique, mastite chronique, maladie de Reclus, etc.). Elle répond à la présence de l’une au moins des lésions microscopiques suivantes : fibrose, adénose, kyste et hyperplasie. Cet ensemble lésionnel est de nature dystrophique et se caractérise par un grand polymorphisme, à la fois en quantité et en qualité, des lésions qui la constituent.
La fibrose, hyaline ou élastosique est d’aspect histologique normal, mais sa répartition dans le tissu mammaire n’est pas harmonieuse. Lorsqu’elle est abondante, elle peut simuler une tumeur.
Les kystes résultent de la distension du lobule mammaire, liée à un obstacle mécanique ou fonctionnel de la lumière du galactophore de drainage. Extrêmement fréquents, leur taille varie de microscopique à de larges formations palpables, mais ils ne sont considérés pathologiques que lorsqu’ils dépassent 1 cm. Ils sont bordés, comme les structures épithéliales mammaires normales, par une double assise cellulaire, myoépithéliale et épithéliale, constituée de cellules régulières, parfois aplaties ou métaplasiques, apocrines voire cylindriques.
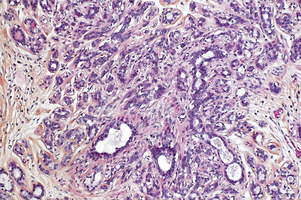
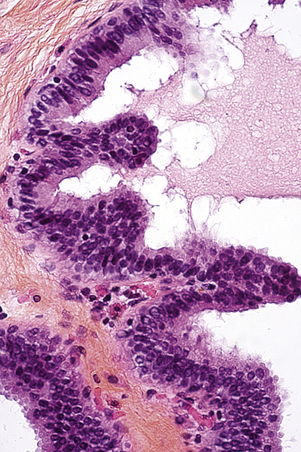
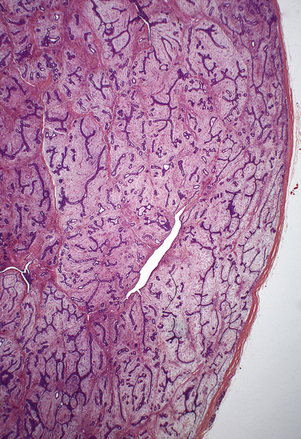
L’adénose correspond à une augmentation du nombre des acini d’un ou de plusieurs lobules adjacents et un accroissement de leur tissu de soutien ou palléal. Différentes variétés sont identifiées : lorsque l’augmentation des acini et du tissu palléal est harmonieuse, il s’agit d’une adénose simple qui conserve la forme régulière du lobule normal. Lorsque l’augmentation prédomine sur le tissu palléal, il s’agit d’adénose sclérosante. La fibrose lui confère une forme étoilée à contours irréguliers. La taille de la lésion peut parfois atteindre 1 cm ce qui la rend détectable, correspondant à une adénose nodulaire ou pseudo-tumorale. Les acini sont étirés et déformés par la sclérose, constituant des travées et miment ainsi une lésion maligne (fig. 3.1) mais qui, à la différence du carcinome, comporte une assise myoépithéliale, mieux identifiée par immunomarquage. D’autres formes plus rares d’adénoses, tubuleuse, apocrine, sécrétoire et microglandulaire, sont également décrites.
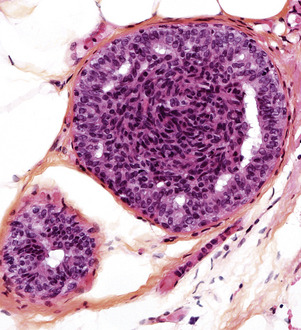
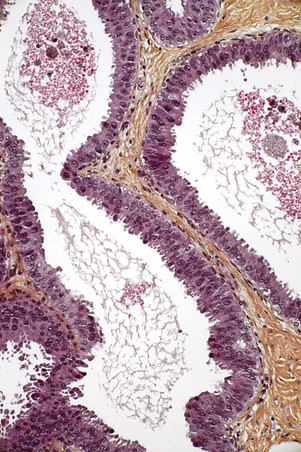
L’hyperplasie répond à la multiplication des cellules épithéliales tapissant la paroi des canaux (épithéliose) et des lobules. Il s’agit généralement d’une découverte microscopique fortuite. Les cellules distendent la lumière et tendent à s’unir en pont ou cordes (fig. 3.2). L’aspect est très variable tant pour l’intensité de la prolifération (quantité) que pour ses caractéristiques cytologiques et architecturales, notamment la présence d’irrégularités cytonucléaires (qualité). Ceci permet de distinguer deux types de proliférations, l’hyperplasie simple et l’hyperplasie atypique qui sont associées à des niveaux de risque différents de développer ultérieurement un cancer du sein (encadré 3.1) [1, 2].
Encadré 3.1
Classement des lésions histologiques élémentaires selon leur niveau de risque relatif de cancer du sein
Risque relatif de cancer du sein = risque de développer ultérieurement un cancer du sein associé à la lésion en comparaison avec le risque de la population générale [1].
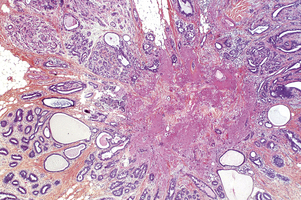
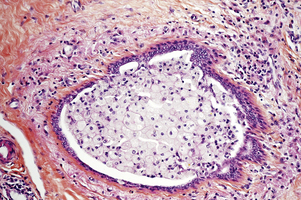
• le centre prolifératif d’Aschoff (CPA) ou cicatrice radiaire (complexe sclérosant papillaire) associe un petit centre fibroélastosique vers lequel convergent de longs spicules où s’observent les différentes lésions, kystes, adénose, métaplasie et hyperplasie (fig. 3.3). Le centre très fibreux et parfois induré induit une attraction du tissu de voisinage responsable de la forme étoilée de la lésion qui simule macroscopiquement un cancer infiltrant. En microscopie, les tubes étirés par la fibroélastose centrale sont similaires à ceux du carcinome tubuleux mais s’en distinguent grâce à la présence d’une couche myoépithéliale, absente dans le carcinome. Dans environ 30 % des CPA macroscopiques, il existe des lésions d’hyperplasie atypique, de carcinome in situ voire infiltrant, situées aussi bien au centre, dans les spicules ou à proximité du CPA ;
• la papillomatose juvénile correspond à un foyer localisé et circonscrit de mastopathie fibrokystique développée chez la jeune femme, souvent de moins de 30 ans. Elle associe de nombreux canaux ectasiés comportant des foyers d’hyperplasie épithéliale floride papillaire, une métaplasie apocrine diffuse ainsi que de nombreux grands kystes responsables de l’aspect macroscopique caractéristique dit « maladie du fromage suisse ». Si elle peut comporter des plages de comédonécrose et d’hyperplasie atypique, son évolution est encore imparfaitement connue.
Lésions à cellules cylindriques
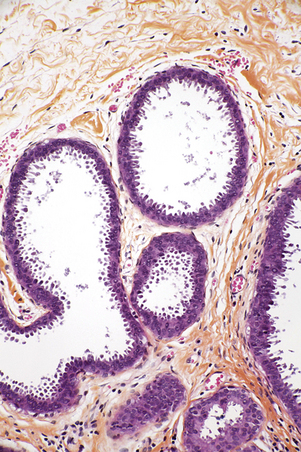
Ces lésions bénignes, connues sous d’autres appellations, ont été récemment regroupées car elles partagent un aspect cytologique commun fait de cellules cylindriques hautes, à noyau ovalaire situé au pôle basal (fig. 3.4). Cet aspect cytologique s’observe aussi dans des lésions atypiques et malignes in situ et infiltrantes et pourrait ainsi être un des éléments du continuum lésionnel de la cancérogenèse mammaire (encadré 3.2). Ceci justifie l’individualisation de ces lésions cylindriques bénignes, entérinée par l’OMS, dans le but de mieux en évaluer l’évolution et le niveau de risque associé. Trois groupes sont distingués microscopiquement :
• métaplasie cylindrique simple : elle touche un ou plusieurs lobules dont les acini sont distendus, avec des lumières souvent irrégulières. Les parois sont recouvertes par une ou deux assises de cellules cylindriques aux noyaux réguliers entre eux (voir fig. 3.4) ;
• hyperplasie régulière à cellules cylindriques : elle touche aussi les lobules dont la lumière des acini est également distendue et irrégulière mais le revêtement comporte une pluristratification dépassant deux assises cellulaires. Les cellules sont toutefois régulières (fig. 3.5) ;
• atypie plane ou métaplasie cylindrique atypique : elle est caractérisée par une pluristratification du revêtement épithélial souvent constitué par des cellules de petite taille, à noyaux volontiers arrondis et hyperchromatiques (fig. 3.6). Le grade nucléaire reste toutefois faible. Bien que le terme atypique soit utilisé dans sa dénomination, le risque relatif de cancer du sein n’est qu’encore imparfaitement connu [3].
Lésions inflammatoires
Cytostéatonécrose
Elle est la conséquence d’un traumatisme physique du sein quelle qu’en soit la nature : chirurgicale, biopsique, radiations, traumatique. Initialement la graisse se nécrose, devenant dure, puis à sa périphérie s’organisent un infiltrat inflammatoire riche en macrophages et cellules géantes et enfin une fibrose dont le caractère rétractile confère un aspect inquiétant. Parfois la zone centrale se liquéfie responsable d’une cavitation (kyste huileux).
Galactophorite ectasiante
Lésion fréquente qui se développe principalement durant la ménopause, elle se caractérise par une inflammation, une fibrose péricanalaire ainsi qu’une distension de la lumière des canaux à des degrés variables (fig. 3.7). Les lésions microscopiques sont bien plus fréquentes que le nombre de patientes symptomatiques. C’est une lésion évolutive qui commence au niveau des canaux galactophores principaux, pour s’étendre progressivement à l’ensemble du lobe correspondant. Différents aspects microscopiques peuvent s’observer et se succéder (tableau 3.1).
Tableau 3.1 Différents stades microscopiques de la galactophorite
| Stades microscopiques | Aspect microscopique |
|---|---|
| Galactophorite aiguë macrophagique | Canaux distendus par un matériel amorphe et des macrophages spumeux |
| Galactophorite chronique | Ectasie marquée. Fibrose et infiltrat lymphocytaire péricanalaire |
| Galactophorite oblitérante | Oblitération plus ou moins complète de la lumière par une fibrose hyaline |
Elle peut se compliquer à tout moment d’une rupture de la paroi du canal induisant une inflammation aiguë qui peut évoluer initialement en abcès ou fistule, puis secondairement en réaction granulomateuse.
Lésions granulomateuses
Elles sont induites par de nombreuses entités (encadré 3.3) comme la galactophorite ectasiante, une réaction à corps étrangers ou une infection. Deux lésions se caractérisent uniquement par des granulomes, la sarcoïdose et la mastite granulomateuse idiopathique.
La localisation mammaire de la sarcoïdose est rare. Elle se caractérise par de multiples granulomes diffus, parfois confluents disposés à l’intérieur ou entre les lobules mammaires et réalisant des nodules. Ils sont constitués de lymphoplasmocytes, de cellules épithélioïdes et géantes mais sans nécrose.
La mastite granulomateuse idiopathique est d’étiologie inconnue. Elle s’observe chez la jeune femme dans les suites d’une grossesse. Les granulomes sont multiples, parfois bilatéraux, intralobulaires et associés à des polynucléaires qui peuvent réaliser des micro-abcès. Son diagnostic comme celui de la sarcoïdose nécessite d’écarter les autres étiologies des lésions granulomateuses.
Mastite lymphocytaire ou mastopathie diabétique
Développée chez de jeunes patientes diabétiques insulino-dépendant de type 1 ou plus rarement avec une maladie auto-immune, elle est caractérisée par l’apparition d’un ou plusieurs nodules, constitués par une fibrose hyaline, dense de type chéloïde renfermant des myofibroblastes épithélioïdes, associée à un infiltrat lymphocytaire périlobulaire et périvasculaire. Elle pourrait correspondre à une réaction auto-immune. Les récidives s’observent dans un tiers des cas.
Tumeurs bénignes
Papillome
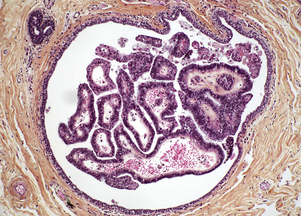
On distingue le papillome unique, central et rétro-aréolaire, et les papillomes multiples ou papillomatose, de siège périphérique. Le papillome unique s’observe entre 30 et 50 ans et se développe dans la lumière d’un canal galactophore. Il est constitué par de nombreuses papilles anastomotiques formées d’un axe fibrovasculaire, recouvertes par un revêtement épithélial et myoépithélial (fig. 3.8). Le papillome solitaire peut obturer totalement la lumière du canal et induire une galactophorite sur le segment en amont ou se nécroser par torsion et saigner. Lésion à faible risque pour le cancer du sein, elle comporte souvent des lésions d’hyperplasie floride, parfois atypique, voire de carcinome in situ. La papillomatose, ou papillomes multiples, est de découverte fortuite ou occasionne des microcalcifications. S’intégrant souvent à des lésions de mastopathie fibrokystique notamment de l’hyperplasie, c’est une lésion à risque modérée pour le cancer du sein (voir encadré 3.2).
Tumeurs fibroépithéliales
Ce groupe de tumeurs associe deux composantes, l’une épithéliale, l’autre mésenchymateuse. Leur proportion respective varie d’une tumeur à l’autre et au sein d’une même tumeur ce qui permet de distinguer deux groupes, les fibroadénomes et les tumeurs phyllodes.
Le fibroadénome, qui serait une hyperplasie d’un lobule et non une tumeur, représente la tumeur du sein la plus fréquente. Elle apparaît chez la femme jeune avant 30 ans et est constituée par une composante mésenchymateuse peu cellulaire et homogène, œdémateuse chez la femme jeune, hyaline après la ménopause et par une composante épithéliale harmonieusement répartie (fig. 3.9). Celle-ci réalise de longs canaux étirés ou de courts tubes, souvent calcifiés. De nombreuses variantes existent. On peut citer la fibroadénomatose formée de multiples fibroadénomes souvent bilatéraux, le fibroadénome cellulaire ou juvénile qui associe une composante conjonctive cellulaire mais homogène et une composante épithéliale hyperplasique, le fibroadénome complexe qui renferme des kystes, de l’adénose sclérosante ou des foyers de métaplasie apocrine.
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree