Chapitre 13 Endométriose : traitement des lésions infiltrantes 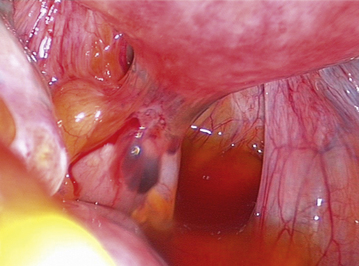
– savoir interroger la patiente ;
– connaître l’importance de l’examen clinique ;
– développer une collaboration efficace avec le radiologue ;
– donner une information complète mais non effrayante à la patiente ;
– organiser correctement le geste avec chacun des spécialistes chirurgicaux ;
– connaître la sémiologie peropératoire ;
– débuter la dissection en tissu sain ;
– enlever la maladie et seulement la maladie ;
– faire une checklist finale pour identifier les complications peropératoires.
Introduction
L’endométriose profonde est connue depuis Cullen et Sampson, elle a été redéfinie par P. Koninckx et D. Martin en 1992. Ils ont fixé la limite à 5 mm d’infiltration [6, 28, 46]. Cette définition est très large, les vrais problèmes sont posés par les lésions de plus de 2 cm de diamètre mais l’apprentissage du traitement des formes les plus volumineuses est long et passe obligatoirement par le traitement de formes moins graves, ce qui justifie cette définition. Ces lésions étaient plus rarement prises en compte et traitées avant le développement de la chirurgie endoscopique. La vision cœlioscopique, bien meilleure du fait de l’effet loupe et de l’axe de vision à partir de l’ombilic, a été essentielle dans cette indication chirurgicale. Elle a permis de voir facilement des lésions et des régions anatomiques très difficiles à voir en laparotomie car situées derrière l’utérus. Ces lésions devenant visibles, il était tentant de les traiter chirurgicalement, c’est ce que de nombreux auteurs et chirurgiens font depuis de nombreuses années.
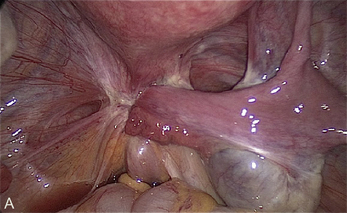
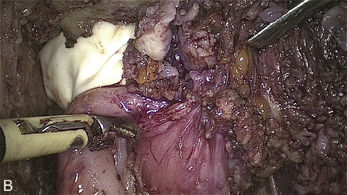
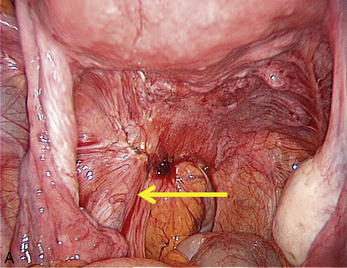
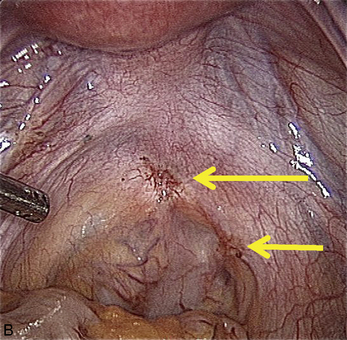
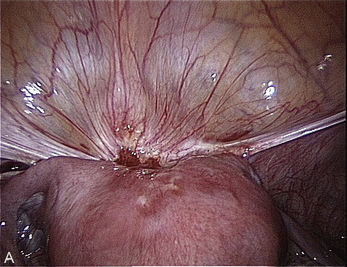
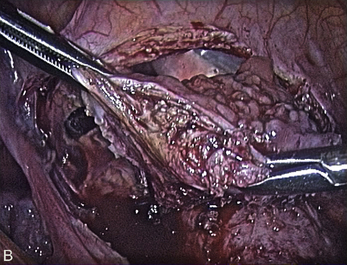
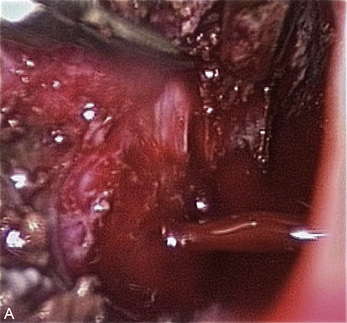
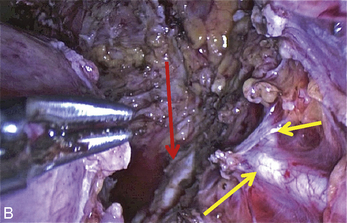
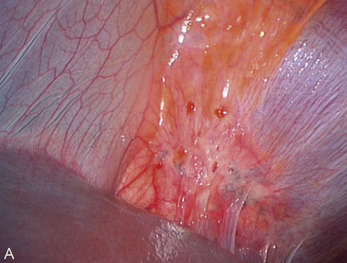
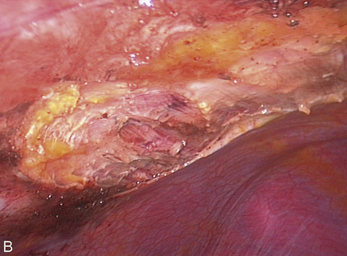
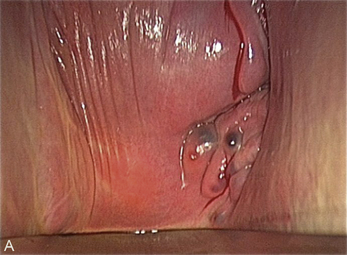
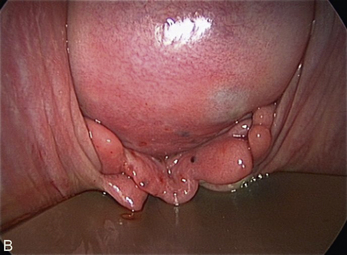
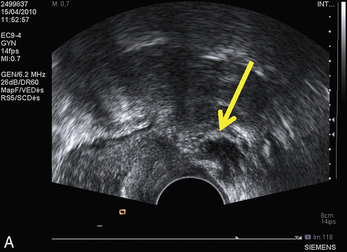
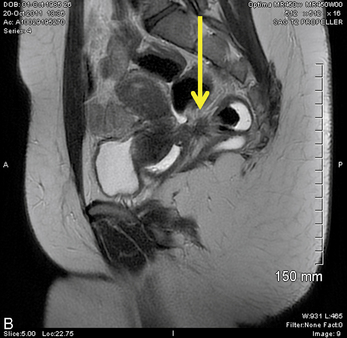
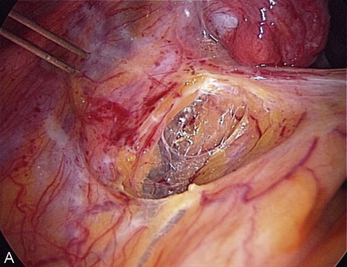
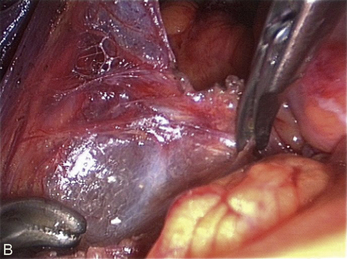
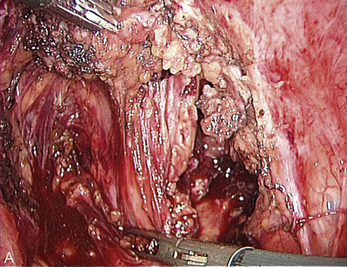
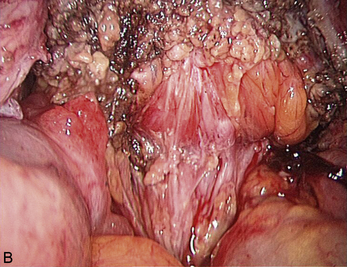
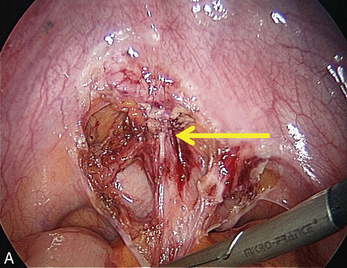
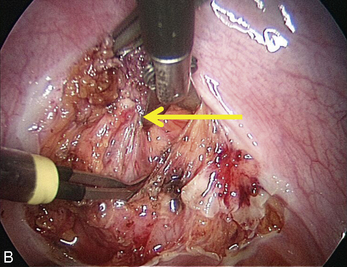
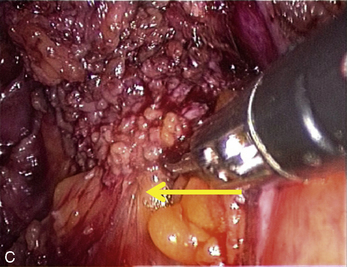
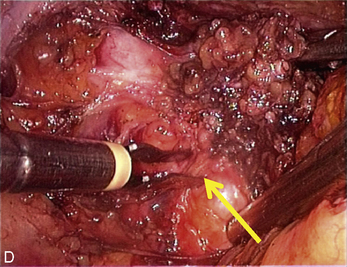
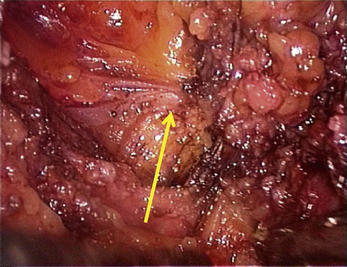
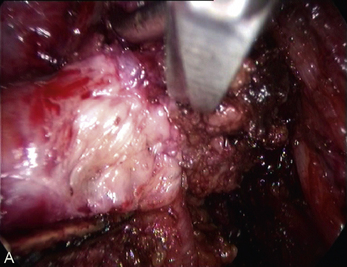
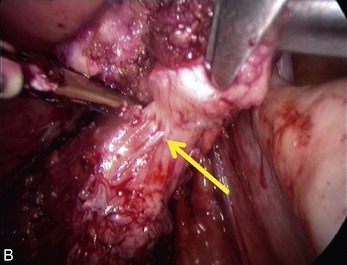
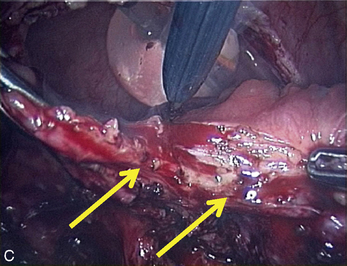
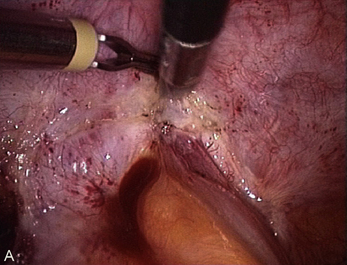
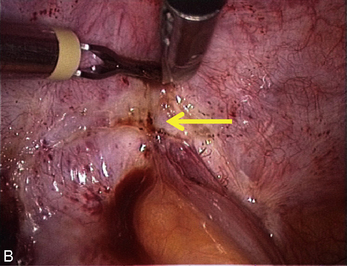
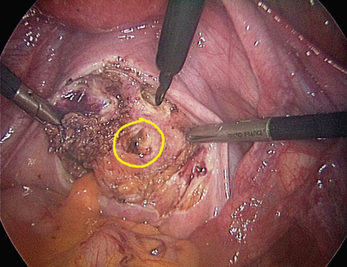
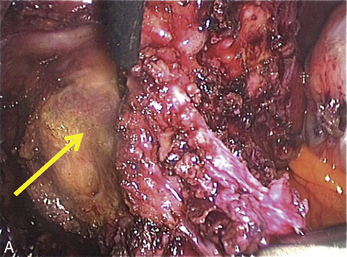
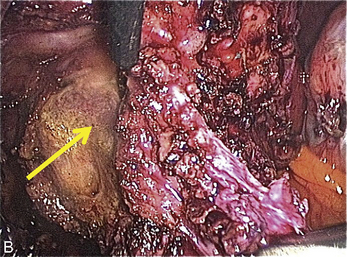
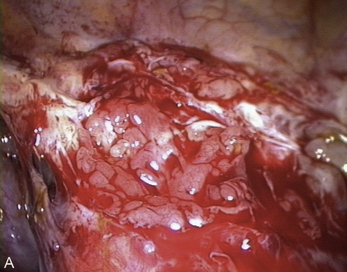
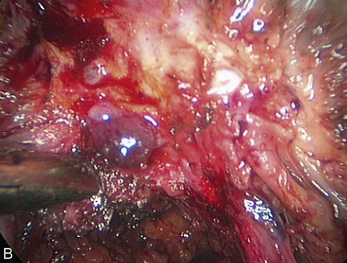
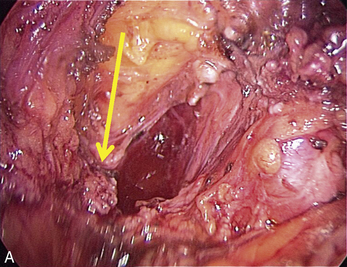
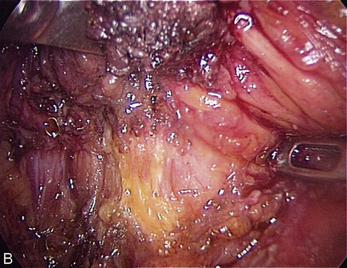
Cependant, la prise en charge de ces lésions pose de nombreuses questions du fait de la difficulté de ces gestes, des risques de complication et de résultats pas toujours parfaits, comme souvent dans la prise en charge des syndromes douloureux chroniques (fig. 13.1 à 13.4).
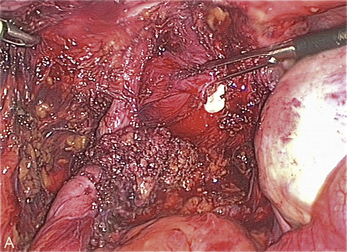
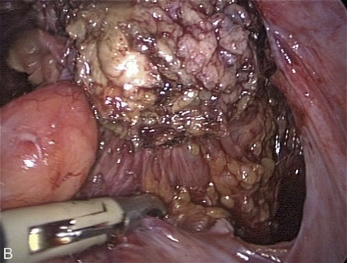
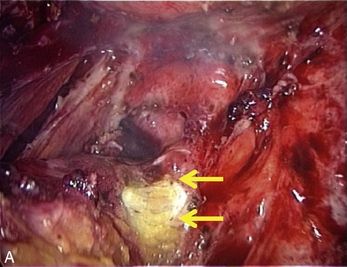
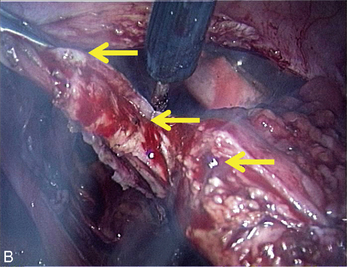
Fig. 13.3 A. Nodule urétéral gauche avant résection-anastomose de l’uretère. B. Nodule enchâssé sur le rectum.
Principes de prise en charge
• Rassurer la patiente : c’est bien souvent la première tâche du chirurgien. Les complications sont bien connues de la plupart des médecins et des gynécologues qui sont amenés à voir ces patientes. Ils présentent de ce fait souvent un tableau dramatique d’une affection qui est et qui reste bénigne. Cette affection est curable sur le plan symptomatique grâce au traitement médical, et/ou sur le plan anatomique grâce à la chirurgie. Si la chirurgie est complète, la récidive est loin d’être la règle. Les reprises évolutives de lésions incomplètement traitées sont beaucoup plus fréquentes que les vraies récidives. Les complications sont gérables en quelques semaines ou quelques mois, ce qui est finalement assez court si on se rapporte aux années de douleur qui précèdent l’intervention ou qui sont à prévoir en cas d’abstention chirurgicale.
• Les lésions asymptomatiques ne doivent pas être opérées. Attention, elles sont rares, les patientes mal interrogées ou mal écoutées sont plus fréquentes, beaucoup plus fréquentes !
• L’abstention chirurgicale est un traitement à part entière. À ce titre, il existe des complications de l’abstention chirurgicale. Si les lésions augmentent de volume, elles peuvent s’étendre latéralement et entraîner une sténose urétérale. Elles peuvent aussi diffuser vers le bas et se rapprocher du tiers moyen du vagin, région au-delà de laquelle il peut être nécessaire de faire une anastomose colo-anale si une résection rectale est nécessaire. Les patientes que l’on n’opère pas doivent avoir une échographie rénale et un examen clinique au moins une fois par an.
• Une équipe plutôt qu’un homme seul. Ces lésions peuvent infiltrer le tube digestif, l’uretère, la vessie ou imposer une excision vaginale très large. Le chirurgien va avoir besoin de compétences chirurgicales multiples. Nous pensons plus logique et plus porteur de progrès de regrouper les chirurgiens de plusieurs spécialités plutôt que de regrouper plusieurs compétences dans un même chirurgien. Toutes les techniques évoluent, il est difficile de suivre l’actualité des techniques chirurgicales dans des spécialités aussi diverses que la chirurgie colique, urologique et plastique. Les compétences du chirurgien omniscient sont plus souvent démodées que celles d’une équipe chirurgicale multidisciplinaire.
• Le gynécologue est le chef d’orchestre de l’équipe parce qu’il connaît la pathologie. C’est lui qui pose les indications, mais il doit tenir compte des conséquences techniques et fonctionnelles de ses décisions. Il doit assumer les complications et en particulier les relations avec la patiente même si les complications sont dues à des gestes réalisés par les autres chirurgiens. Il ne peut pas et ne doit pas être dans la position de « ce n’est pas moi c’est l’autre » ! Sans lui, les autres spécialités chirurgicales ne seraient pas intervenues !
• Le geste doit être autant que possible planifié et organisé. Les chirurgiens non gynécologues qui peuvent être amenés à intervenir doivent être prévenus à l’avance. Ils doivent avoir intégré ce temps d’intervention dans leur planning opératoire.
• Il faut éviter d’appeler les chirurgiens digestifs ou urologues, le vendredi soir à heures pour la gestion d’une complication chez une malade qu’ils ne connaissent pas. Il est préférable de les inviter à venir assister à toute l’intervention, au moins au début de la collaboration ; ils mesureront mieux les difficultés de cette chirurgie et ils comprendront que les complications doivent plus à la maladie qu’à l’incompétence technique du gynécologue !
• Le bilan préopératoire doit être réalisé par des radiologues entraînés à cette pathologie. La sémiologie radiologique de l’endométriose est rarement enseignée. Il est donc fréquent que les radiologues avec lesquels on travaille soient peu ou pas expérimentés. Leur courbe d’apprentissage est de un à deux ans. Il faut l’accepter et continuer de leur adresser les malades, même si les premiers comptes rendus sont très décevants. Il faut leur montrer l’anatomie peropératoire pour qu’ils comprennent leurs erreurs. Ils peuvent aussi se former auprès de spécialistes. C’est à ce prix que les radiologues deviennent capables de prévoir avant l’intervention, et avec une bonne fiabilité, les gestes chirurgicaux peut-être nécessaires.
• La chirurgie de ces femmes jeunes doit être conservatrice. On ne peut pas proposer une hystérectomie et une castration à une femme de moins de 40 ans qui n’a pas d’enfant. La vie est longue : même une femme de 30 ans qui a eu un enfant en FIV doit bénéficier d’une chirurgie conservatrice ; elle peut souhaiter un autre enfant dans quelques années !
• L’endométriose est une maladie bénigne, il faut un traitement aussi complet que possible, mais il n’est pas utile d’avoir des marges de sécurité de plusieurs centimètres. Par ailleurs, quand on réalise ou lorsqu’on propose des gestes très larges, sur le rectum en acceptant des marges nulles, voire un traitement incomplet à la face postérieure de l’utérus, où est la logique ?
• Il faut être aussi respectueux que possible des organes qui paraissent ou qui sont infiltrés.
• Le nerve sparing illustre l’intérêt d’une collaboration entre les spécialités chirurgicales. Les chirurgiens digestifs savent depuis de nombreuses années que, pour préserver l’érection, la dissection et l’excision du rectum et du mésorectum doivent se faire dans un plan aussi proche que possible du rectum [22]. L’endométriose ne respecte pas ces plans et infiltre souvent à distance, c’est pourquoi elle infiltre les nerfs hypogastriques et le plexus hypogastrique inférieur. Si les nerfs sont infiltrés, le sparing des nerfs est un sparing de la maladie ; si les nerfs ne sont pas infiltrés, il faut, dès que l’on est en dessous du nodule, se rapprocher du rectum ou rester au contact du nodule pour préserver les nerfs autant que possible. C’est parce que bien des résections digestives ont été faites par des chirurgiens gynécologues moins au fait de ces notions et qu’ils ont réalisé des exérèses latérales trop importantes guidées par l’extension de la maladie que bien des patientes ont eu des troubles neurologiques vésicaux plus importants que nécessaire.
• Tout le nécessaire mais seulement le nécessaire ! Il faut exciser la maladie mais rien que la maladie. Dès que l’on est en tissu sain, il faut suivre la lésion au plus près et non pas accepter d’exciser tout le tissu normal que les plans ouverts pendant les phases initiales de l’intervention permettraient d’exciser sans difficultés, puisque tout est installé et préparé pour cela. Il faut respecter tout ce qui n’est pas malade, mais l’identification en tissu sain en arrière et au-dessus des lésions de structures nerveuses ne permet pas d’affirmer que l’on sera en mesure de les préserver au moment de l’excision du tissu pathologique.
• La prise en compte des signes cliniques doit guider l’intervention et les décisions peropératoires. Pourquoi faire une résection rectale chez une patiente correctement interrogée qui ne décrit aucun trouble digestif ?
• Pas de dissection systématique de structures vulnérables qui ne sont pas directement infiltrées par la lésion ou rétractées par la fibrose qui entoure les lésions. Par exemple, nous avons acquis la conviction que l’on ne peut pas faire plusieurs urétérolyses difficiles à la même patiente sans risque de fistule urétérale. La troisième dissection difficile d’un uretère est à très haut risque, elle impose la mise en place d’une sonde double « J » qui ne protège pas toujours des fistules induites par l’ischémie du segment distal. Sachant que ces patientes risquent d’être opérées plusieurs fois, et qu’il est impossible de faire la différence entre la fibrose périlésionnelle et la fibrose induite par la maladie, il ne faut pas faire de dissection inutile des organes vulnérables ni ouvrir des espaces que l’on n’a pas besoin d’ouvrir pour faire un traitement complet.
• La prise en compte de la douleur impose la prise en compte de l’atteinte utérine éventuelle, mais aussi de l’histoire personnelle de la patiente. Ne promettons pas la guérison totale, affirmons que l’on peut presque toujours soulager et diminuer les douleurs de manière significative et durable.
• La plupart des complications surviennent lors du traitement de lésions très volumineuses ou lors de réinterventions. Les lésions qui augmentent de volume doivent être opérées. Le traitement initial doit être aussi complet que possible pour limiter les risques liés aux dissections itératives des structures vulnérables comme l’uretère et le rectum. Si on décide que le traitement ne sera pas complet, il faut arrêter le geste tôt avant la dissection des organes qui entourent le nodule.
• Le traitement médical soulage s’il induit une aménorrhée, mais il ne guérit pas les lésions. Les douleurs reprennent en général quelques jours ou quelques semaines après la reprise de l’activité ovarienne. Ce n’est pas une récidive, c’est la reprise évolutive d’une lésion non traitée.
• L’atteinte de toute l’épaisseur du vagin est fréquente (75 %) lorsque les lésions ont un diamètre supérieur à 2 cm [32]. Il n’est pas logique d’éviter l’ouverture du vagin pour privilégier le traitement du rectum dont l’infiltration ne concerne pas toute l’épaisseur et ce, alors que les premiers symptômes ou les symptômes les plus sévères sont gynécologiques.
• Il faut faire d’abord ce qui est facile pour faire plus facilement ce qui est difficile. Cette approche nous a conduit à débuter l’intervention par l’excision des lésions à la face postérieure de l’utérus et au niveau du vagin avant de terminer par le traitement des lésions rectales qui est ainsi réalisé alors que la lésion est mobile et que toutes ses faces peuvent être vues et traitées successivement [26].
• L’endométriose infiltre ou rétracte dans les trois plans de l’espace, il faut prendre cette notion en compte pour extraire progressivement chacune des faces de la maladie. Cette approche permet de n’exciser ou de n’ouvrir la lumière des structures vulnérables que si cela est nécessaire. Le rectum s’enroule autour de la lésion ; en le déroulant progressivement du haut vers le bas, du bas vers le haut et du dehors vers le dedans, il n’est pas rare de découvrir que l’infiltration, qui paraît initialement majeure, n’est finalement que superficielle. Pas de décision hâtive d’exérèse du rectum : sur la figure 13.5, on voit que le nodule ressemble à un oursin dont les piquants auraient tous une longueur différente. Surtout, la distance entre l’extrémité de ces épines ne correspond pas toujours à la même distance sur l’organe infiltré. Une section de 1 mm peut libérer plusieurs millimètres, voire un centimètre à la surface de l’organe infiltré. Les radiologues confirment cette notion que les chirurgiens connaissaient depuis longtemps. Il est fréquent sur les comptes rendus d’échographie de voir qu’un nodule de 2 cm de diamètre rétracte 6 à 8 cm de rectum.
• Sauf exception, pas de décision préopératoire de résection rectale. Une résection réalisée uniquement parce qu’elle a été décidée en préopératoire risque d’apparaître comme un geste trop lourd, voire inutile une fois que le nodule est libre de toutes ses attaches extradigestives ! À l’inverse, la décision est possible si l’atteinte concerne le sigmoïde, le grêle ou le côlon droit, organes au niveau desquels un shaving de la lésion dans l’épaisseur de la paroi digestive n’est pas possible.
• Attention à la dissection de nodules qui infiltrent latéralement et vers l’arrière. Le plus grand risque chirurgical est la blessure d’une veine hypogastrique ou iliaque interne dans la fibrose. Le contrôle du saignement est souvent difficile lorsque cela survient. Il faut savoir disséquer les vaisseaux iliaques en tissu sain avant d’aborder cette région pour faciliter l’hémostase si nécessaire. Autant que possible, cette dissection des vaisseaux doit survenir avant la plaie (fig. 13.6).
Rappels anatomiques
Cul-de-sac postérieur
Kuhn et Hollyock ont montré que la « profondeur » du cul-de-sac de Douglas, distance entre l’insertion des ligaments utéro-sacrés et la partie la plus déclive du cul-de-sac, était de 5,3 cm chez les nullipares et de 5,4 cm chez les multipares [29]. Vercellini et al. ont effectué la même mesure chez les patientes opérées pour une lésion profonde et ont trouvé une distance de seulement 3,6 cm [47]. Chez les patientes avec endométriose, mais sans lésion profonde, la profondeur du cul-de-sac de Douglas était de 5,3 cm. Le terme de nodule de la cloison recto-vaginale est probablement imprécis. La cloison recto-vaginale débute en dessous de la partie inférieure du cul-de-sac de Douglas en regard du tiers moyen du vagin dans plus de 90 % des cas [29] alors que les lésions profondes concernent presque toujours le tiers supérieur du vagin. Ces nodules ne sont donc pas des lésions de la cloison recto-vaginale proprement dite, mais pourraient mériter le qualificatif de recto-vaginaux lorsqu’ils infiltrent à la fois le rectum et le vagin.
Innervation vésicale et rectale : anatomie du plexus hypogastrique inférieur
L’innervation sympathique provient du plexus hypogastrique supérieur, structure médiane située en dessous de la bifurcation aortique en avant et au contact du promontoire. C’est à partir de ce plexus que se forme le nerf hypogastrique, filament de 4 à 7 mm de diamètre [13, 33, 34]. Ce nerf hypogastrique se dirige latéralement vers le bas et vers l’avant en regard de la face antérieure du sacrum en dehors des trous sacrés. Son trajet est concave en dedans. Il se trouve dans la graisse rétropéritonéale en dedans et en dessous des vaisseaux iliaques internes en dehors du rectum. Il rejoint l’angle supérieur du plexus hypogastrique inférieur. Nous avons observé mais sans pouvoir le quantifier que, lorsqu’il existe une rétraction du ligament utéro-sacré induite par l’endométriose, ce nerf paraît plus superficiel. On le trouve plus tôt et plus facilement pendant la dissection du rétropéritoine de la fosse pararectale ou des faces latérales du rectum.
Selon Mauroy et al., le plexus hypogastrique inférieur a une forme triangulaire à base postérieure et à sommet antérieur [33, 34]. On lui décrit trois côtés ou bords, et trois sommets. Le bord supérieur est parallèle au bord postérieur de l’artère hypogastrique, à environ 10ce:hsp sp=”0.25″/>mm en arrière et en dedans. C’est au niveau de son bord postérieur qu’il reçoit les efférences en provenance du plexus sacré. Son bord inférieur va de S4 jusqu’au point d’entrée de l’uretère dans le ligament large. L’angle supérieur correspond au point où ce plexus est rejoint par le nerf hypogastrique, l’angle inférieur au point d’arrivée de l’efférence venant de S4, l’angle antérieur au point urétéral qui marque la fin de la portion rétroligamentaire de l’uretère.
Les efférences qui naissent du plexus sacré, encore appelés nerfs splanchniques, correspondent à l’innervation parasympathique. À partir des trous sacrés, ils se dirigent latéralement jusqu’au bord postérieur des vaisseaux iliaques internes, puis médialement selon une direction parallèle aux vaisseaux recto-moyens vers le plexus hypogastrique inférieur [13]. Mais ce rapport des nerfs splanchniques est inconstant et, dans environ 30 % des cas, ces nerfs rejoignent le plexus hypogastrique inférieur entre 15 et 35 mm en arrière des vaisseaux hypogastriques, indépendamment des vaisseaux rectaux moyens. Les vaisseaux rectaux moyens traversent le plexus hypogastrique inférieur [13].
Le plexus hypogastrique inférieur peut être situé de manière précise par rapport aux vaisseaux du plexus hypogastrique. Nous avons vu les rapports du bord supérieur et de l’artère hypogastrique. L’angle supérieur est située à 10 ± 5 mm en dessous et en avant du confluent veineux hypogastrique et à 35 mm du confluent veineux iliaque externe, iliaque interne [33, 34]. Le plexus hypogastrique inférieur se dirige en bas et en dehors de la face antérieure du sacrum à sa partie latérale, puis en avant et en dedans pour rejoindre le ligament utéro-sacré par en dehors [13] puis la couche postérieure du ligament large. L’uretère est un rapport majeur du plexus hypogastrique inférieur [33, 34]. L’uretère croise le plexus d’arrière en avant et de dehors en dedans. Le plexus se situe en dessous de l’uretère et pénètre dans le ligament large avec lui. Dans tous les cas, l’angle antérieur du plexus se trouve en dessous du point où l’uretère pénètre dans le ligament large. Pour le chirurgien, ce plexus se trouve en dehors du rectum dans la partie latérale du ligament utéro-sacré.
Les nerfs splanchniques sont constamment situés en dessous du trajet de la veine utérine profonde et sont préservés si on ne sectionne pas les tissus situés en dessous de cette veine, que l’on appelle aussi la pars nervosa par opposition à la pars vasculosa que l’on trouve au dessus et en avant de cette veine [17, 18, 30, 34, 45].
Cette anatomie est précise, mais donne peu de vrais repères au chirurgien qui déplace ces structures lorsqu’il ouvre les espaces de dissection du pelvis. Pour cette raison, la connaissance des points fixes proposés par Mauroy et al. paraît utile. De même, il faut savoir avec quelles structures, les structures nerveuses se mobilisent le plus facilement pendant la dissection. L’existence de plan de dissection est l’objet de discussion entre les anatomistes [2, 12, 13, 24]. Ces travaux montrent qu’il existe autour du mésorectum un fascia rectal propre dont la dissection permet d’éviter les plexus nerveux hypogastriques. Ce plan de dissection avait été décrit par Heald comme le holy plane de la chirurgie du cancer rectal [22, 23]. Un travail récent suggère qu’il existe, entre le fascia propria du rectum et le fascia présacré, un fascia qui recouvre le nerf hypogastrique [24]. Le plan situé entre ce fascia du nerf hypogastrique et le fascia propria du rectum est celui de la chirurgie du cancer du rectum avec excision totale du mésorectum ; il est situé trop loin du rectum pour le traitement des lésions bénignes qui n’infiltrent pas les structures latérales. Ainsi, si l’on reste aussi près que possible du rectum ou si l’on se rapproche de lui dès que l’on passe en dessous de la limite latérale d’un nodule, on préserve les nerfs toutes les fois que cela est possible et on fait du nerve sparing sans avoir besoin de disséquer ces structures.
Cette approche est contraire à de nombreux articles récents qui proposent une identification systématique des tissus nerveux en zone saine pour faciliter leur préservation [37, 39]. À cela, on peut opposer deux arguments :
• si ces structures sont infiltrées par la lésion, leur préservation sera incompatible avec un traitement complet de la lésion ;
• la dissection systématique ne risque-t-elle pas de traumatiser des structures dont le diamètre est inférieur au millimètre et dont la fonction peut probablement être altérée par la diffusion d’une coagulation bipolaire parfois nécessaire lors de la dissection d’espaces pelviens qui comportent tout de même de nombreuses variantes anatomiques en particulier vasculaires ?
Bilan préopératoire
Interrogatoire
L’interrogatoire est une étape clé. Le Collège national des gynécologues et obstétriciens français (CNGOF) a recommandé l’utilisation de questionnaire spécifique et d’échelle d’évaluation de la sévérité de la douleur [16]. Cette notion est très importante ; en effet certaines lésions sont difficiles à voir lors du bilan d’imagerie ou de la cœlioscopie. Quelle que soit la méthode d’investigation, on voit mieux ce que l’on recherche et on recherche en particulier les lésions dont la présence est suggérée par l’interrogatoire. Il est capital de rechercher des signes digestifs, urinaires et/ou atypiques de survenue menstruelle ou périmenstruelle.
Certaines douleurs sont très évocatrices de certaines localisations et il faut connaître ces relations bien décrites par les travaux de Chapron et Fauconnier [15]. Mais ces signes peuvent être absents, et il faut rechercher des lésions infiltrantes chez toutes les patientes qui consultent pour une dysménorrhée sévère qui altère leur qualité de vie de manière significative (arrêt de travail, éviction scolaire…) ou qui requiert l’utilisation d’antalgiques puissants plusieurs fois par jour. Il ne faut pas sourire quand une patiente raconte des douleurs scapulaires menstruelles, elle a probablement une atteinte diaphragmatique qui n’est pas vue sur le bilan d’imagerie et qui peut être difficile à voir avec un cœlioscope à 0° introduit par voie ombilicale (fig. 13.7) [40].
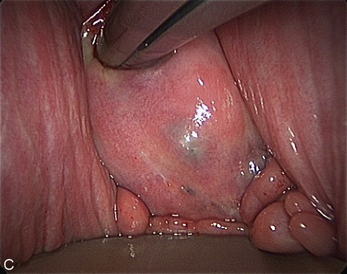
Examen clinique
L’examen clinique est une étape capitale de l’évaluation préopératoire de ces lésions. Pour le chirurgien, quelle que soit la qualité des données de l’imagerie, rien ne remplace aujourd’hui les informations obtenues au cours du toucher vaginal et du toucher rectal. Cet examen doit être doux et patient. L’inspection du fond vaginal peut retrouver des kystes bleutés, des pseudo-polypes, une zone rétractile difficile à distendre avec le spéculum (fig. 13.8). Chez les patientes qui ont des douleurs sévères, le toucher vaginal est souvent plus riche d’enseignement s’il est débuté avec un seul doigt. On recherche, sur la face postérieure du vagin, une zone dure rétractée et sensible, voire exquisément douloureuse. C’est souvent à ce moment-là que la patiente décrit ou reconnaît la dyspareunie occasionnelle qu’elle ne ressent que dans certaines positions. Cette douleur est compréhensible quand on voit, en peropératoire, le saignement parfois induit par un toucher vaginal réalisé en début de cœlioscopie chez une patiente qui présente un volumineux nodule du compartiment.
Pour le nodule, l’examen clinique doit apprécier :
• les extensions inférieures, postérieures et latérales ;
• les rapports avec le vagin (fig. 13.8) et avec le rectum et en particulier, la distance entre l’anus et la limite inférieure de la lésion, l’importance de la résection vaginale qui sera nécessaire.
Bilan paraclinique (fig. 13.9)
Nous utilisons deux techniques d’imagerie : l’IRM et l’échographie endovaginale. L’échographie est indispensable pour le bilan des ovaires. De même, il faut une évaluation des reins quelle que soit la décision chirurgicale. Le travail de Donnez et al. montre que, si un nodule du cul-de-sac postérieur a un diamètre supérieur à 3 cm, le risque de lésion urétérale est de 11 % ce qui justifie la réalisation systématique d’une échographie rénale [9]. Avant l’intervention, l’IRM permet une cartographie des différentes lésions. Elle doit comporter un temps urologique pour rechercher une compression urétérale. Dans notre équipe, c’est avec l’échographie endovaginale que nous avons la meilleure évaluation de la profondeur de l’atteinte digestive [1, 7]. Cette attitude peut être remise en cause au cours des prochaines années grâce à l’apport de nouvelles techniques comme le colo-scanner ou l’élastométrie qui pourraient permettre d’évaluer la mobilité des tissus et des lésions. D’autres approches sont utilisées, il ne faut pas établir de règles trop strictes dans ce domaine, les méthodes sont toutes opérateur-dépendant.
Il semble que, dans les mains des spécialistes, l’échographie endovaginale devienne, comme dans notre pratique, l’examen de référence pour le bilan des lésions digestives et vaginales [1, 7]. Chez les patientes qui n’ont pas subi auparavant de traitement de l’endométriose infiltrante, l’imagerie bien faite est très utile. Sa fiabilité reste à confirmer chez les personnes qui ont déjà subi un geste chirurgical complexe où l’on retrouve presque toujours une cicatrice difficile à distinguer des lésions endométriosiques persistantes ou récidivantes.
Information des patientes
Il faut informer les patientes du risque de laparotomie, d’abcès pelvien, de fistule recto-vaginale, de fistule urétérale, de la mise en place possible de manière transitoire de sondes double « J » ou de colostomie. Il faut également les informer du risque de troubles de la sensibilité vésicale ou de dysurie [11]. Mais il faut adapter cette information à la lésion que l’on va traiter, les risques sont moindres pour une lésion de 1 cm que pour une lésion de 5 cm.
Préparation de l’intervention
L’intérêt de la préparation digestive est discuté comme dans la chirurgie colique, nous l’utilisons presque toujours, elle facilite l’installation peropératoire [21]. Dans notre pratique, elle est indispensable lorsque l’on opère une lésion rectale, cela ne diminue pas le risque de complication, mais cela facilite beaucoup la gestion des complications.
L’intervention doit être organisée.
Installation de la patiente
Sous anesthésie générale, la patiente est allongée sur le dos, les membres inférieurs sont placés en abduction avec une flexion des cuisses sur le bassin d’environ 20°, ce qui permet un accès vaginal et un accès abdominal. Nous utilisons une table qui permet la flexion des cuisses grâce à des bottes montées sur rotules, ce qui facilite la réalisation des sutures réalisées par voie vaginale en fin d’intervention. Ces interventions sont souvent longues, il convient de veiller particulièrement à éviter les troubles dus à la compression ou à l’élongation peropératoire de troncs nerveux. Pour éviter les traumatismes du plexus brachial, nous n’utilisons pas d’épaulière et les deux bras sont placés le long du corps. Les bottes présentées dans le chapitre consacré à l’installation (chapitre 1) nous ont permis d’éviter les troubles de compression des nerfs des membres inférieurs. Si l’on ne dispose pas de cet artifice, l’installation des membres inférieurs doit être très soigneuse pour éviter les compressions du sciatique poplité externe et de la loge postérieure de la jambe.
Sémiologie chirurgicale : ce que les patientes nous montrent !
Pour obtenir l’aide de la patiente, il faut la demander poliment !
Bulles
Grâce à la pression du pneumopéritoine et à une bonne installation du plan à exposer, il est fréquent de voir des bulles apparaître dans les plans de dissection. Ces bulles ont une double signification ; ici existe un plan de dissection et ce plan correspond à une zone de tissu normal. En effet le CO2 ne pénètre pas dans la fibrose des lésions (fig. 13.10).
Flèches
La présence d’une « flèche » n’est pas spécifique de l’endométriose ; on en rencontre dans toutes les dissections et en particulier dans les plans vésico- ou recto-vaginaux pendant le traitement des prolapsus uro-génitaux. Dans le cas de l’endométriose, ces « flèches » sont très utiles. Elles facilitent la dissection des kystes endométriosiques et des implants rétropéritonéaux. Ces flèches se terminent souvent sur les « épines du nodule ». Mais elles ne sont visibles que si l’exposition du plan est bonne. L’hémostase est indispensable, le sang gêne beaucoup la vision dans les espaces rétropéritonéaux. Plusieurs exemples sont présentés dans le chapitre consacré à l’endométriose non infiltrante (chapitre 12). L’exactitude du signe donné par cette flèche est confirmée par la mobilité obtenue après la section.
À l’inverse, si l’on ne situe pas clairement la limite, il faut reprendre l’installation de la dissection en améliorant si possible la traction sur le nodule ou sur les structures qui l’entourent, puis il faut lire l’écran à la recherche des prolongements stellaires du nodule qui sont souvent fléchés par un triangle dont il faut sectionner la pointe pour retrouver le plan (fig. 13.11 à 13.13). Ces signes sont parfois même retrouvés dans l’épaisseur de la musculeuse rectale (fig. 13.14). Dans cette localisation, les flèches montrent le chemin de l’exérèse optimale ; l’opérateur choisit de les suivre ou pas en fonction des données cliniques préopératoires et des risques de lésions digestives qu’il accepte pour cette patiente.
Points noirs
Les points noirs que l’on identifie en périphérie des lésions correspondent à des microkystes, ils signifient que l’exérèse n’est pas complète. Ces lésions correspondent à des kystes de très petite taille (fig. 13.15). Ces kystes peuvent être plus volumineux et il faut alors être vigilant devant tout écoulement de liquide brunâtre même très bref mais dont la signification est la même (fig. 13.16 et 13.17). Ce signe est très fiable, mais il n’a de valeur que si « le petit point noir » est présent immédiatement après la section. Si l’on ne dispose pas de l’élément chronologique, il est difficile, voire impossible, de distinguer les points noirs qui appartiennent au nodule de ceux que l’on crée en coagulant un saignement provenant de petits vaisseaux. Le chirurgien doit mémoriser le champ opératoire pour ne pas exciser inutilement du tissu normal et/ou ne pas laisser en place des zones pathologiques. Il est donc important de ne pas quitter l’écran des yeux, pour se souvenir précisément des zones qui ont été coagulées et où, comme nous le verrons plus loin, l’exérèse est complète. Exciser ces zones coagulées est un geste inutile qui peut conduire à des complications.
Les images de la figure 13.18 illustrent bien l’importance de la qualité de l’image endoscopique. Nous avons appliqué sur une image endoscopique un traitement permettant a posteriori d’améliorer la qualité et la netteté de l’image. Sur la figure 13.18b, après modification, les points noirs sont évidents dans la profondeur de l’ouverture vaginale d’un nodule du ligament utéro-sacré.
Endomètre actif
Il n’est pas rare d’identifier des plages d’endomètre actif lors de l’excision de lésion infiltrante, il faut connaître cet aspect d’endomètre. Cet aspect est peut-être plus fréquent chez les patientes qui ont reçu un traitement progestatif préopératoire et dont l’endomètre est décidualisé (fig. 13.19).
Immobilité ou la mobilité de la lésion
À l’inverse, si après la section, le tissu apparaît blanchâtre ou fibreux et que le nodule bouge peu, il faut se demander s’il n’est pas nécessaire de reprendre l’exérèse plus au large. La réponse est souvent positive, mais un tissu blanchâtre peut aussi correspondre à l’incision de la paroi rectale ou vésicale après une coagulation. Cette notion est d’interprétation difficile dans l’épaisseur des ligaments utéro-sacrés où le tissu blanchâtre peut correspondre à la structure du tissu normal. La figure 13.20 montre une exérèse incomplète au contact d’un releveur de l’anus. Le tissu laissé en place en arrière est blanchâtre, similaire à celui que l’on enlève en avant, l’analyse histologique de la recoupe est positive. On conçoit aisément qu’il aurait été très difficile de retrouver cette zone lors d’une intervention ultérieure si elle avait été laissée en place.
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree