Chapitre 12 Infarctus du myocarde à la phase chronique et complications
En dehors de cette dysfonction ventriculaire gauche postinfarctus, il existe une autre variété : la cardiomyopathie dilatée ischémique, probablement en rapport avec des épisodes de myocytolyse diffus répétés, qui aboutissent à une destruction progressive du myocarde, sans stigmates cliniques ou électriques d’infarctus du myocarde (voir le chapitre Cardiopathies dilatées). Malgré les progrès dans la compréhension et le traitement de ces cardiopathies ischémiques, le pronostic reste réservé avec un taux de survie de seulement 50 à 60 % à 5 ans [1].
Le scanner et surtout l’imagerie par résonance magnétique (IRM) permettent de mettre en évidence et de quantifier les séquelles morphologiques et fonctionnelles d’une ischémie ou d’une nécrose myocardique chronique. Ces techniques sont très intéressantes également pour le diagnostic non invasif des complications d’un infarctus myocardique, souvent plus précisément qu’en échocardiographie. Enfin, l’IRM avec rehaussement tardif permet d’apprécier l’extension de la nécrose (myocarde non viable) [2].
Cette nécrose irréversible sans possibilité de récupération fonctionnelle après revascularisation est à différencier de l’hibernation. Celle-ci est une dysfonction ventriculaire gauche réversible après reperfusion, conséquence d’une ischémie chronique (débit insuffisant par lumière résiduelle ou collatéralité, ou épisodes brefs mais répétés d’ischémie sévère avec sidération). Devant une akinésie, la distinction entre nécrose et hibernation est donc essentielle à titre pronostique, et surtout pour décider de l’attitude thérapeutique. En effet, la distinction entre myocarde viable et non viable permet d’éviter les risques d’une revascularisation à ceux qui n’en tireront aucun bénéfice (pas de myocarde viable), ce d’autant qu’il semble que la mortalité périopératoire soit supérieure d’environ 10 % chez les patients avec du myocarde non viable ; à l’inverse, le taux de mortalité annuelle est 4 fois supérieur chez les patients avec du myocarde viable traités médicalement par rapport à ceux qui ont bénéficié d’une revascularisation [3,4].
Imagerie des cardiopathies ischémiques
Protocole IRM
Protocole scanner multicoupe
Il est réalisé une acquisition type coroscanner habituel pour l’étude des artères coronaires (voir le chapitre 2) puis éventuellement un passage tardif à 5 minutes en baissant les kilovolts (80 kV en dessous de 75 kg et 100 kV au-dessus de 75 kg, par exemple), avec une épaisseur de coupes de 1,5 mm et reconstructions en 3 mm tous les 1,5 mm.
Résultats
Scanner
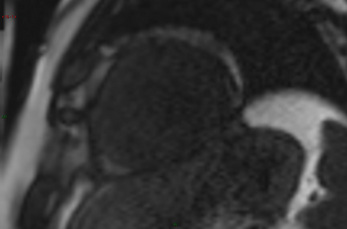
En scanner, l’infarctus du myocarde apparaît sur les acquisitions injectées précoces comme une zone de densité diminuée (défaut de rehaussement) par rapport au myocarde adjacent [5]. Ces hypodensités peuvent être linéaires sous-endocardiques ou transmurales, et sont associées à une diminution de l’épaisseur myocardique en diastole dans les infarctus chroniques (fig. 12.1a). Sur l’acquisition tardive à 5 minutes, le rehaussement tardif de la zone de cicatrice a une signification voisine du rehaussement tardif décrit en IRM avec le gadolinium (augmentation du volume de distribution de l’iode dans l’espace interstitiel) [6].
Fig. 12-1 Infarctus chronique.
Infarctus antérieur en scanner non synchronisé (a) et en IRM en séquence de perfusion (![]()
) et de rehaussement tardif en petit axe. (b) Patients différents. Hypodensité sous-endocardique au scanner de l’apex et hypoperfusion antérieure étendue (vidéo) à l’IRM avec amincissement et hypersignal tardif transmural (noter l’épanchement péricardique lié à un syndrome de Dressler). 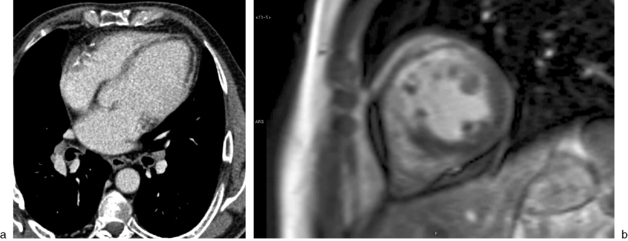
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree