Chapitre 2 Rappels physiopathologiques, cliniques et électriques
Généralités
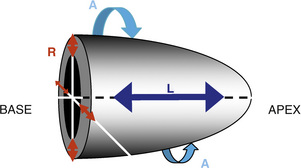
Le muscle cardiaque est essentiellement développé au niveau des ventricules, qui doivent éjecter le sang dans un système à plus haute pression pour le ventricule gauche (VG) que pour le ventricule droit (VD) afin de le distribuer à l’ensemble des artères de l’organisme (le VG est plus épais que le VD). Le remplissage ventriculaire au cours de la diastole s’accompagne d’un relâchement des fibres en diamètre et en longueur. L’éjection systolique des ventricules est un ensemble de contractions et de raccourcissements du myocarde (fibres entrecroisées). La contraction du VG normal (normokinésie) entraîne trois déformations en systole : un raccourcissement circonférentiel, un épaississement radial et un raccourcissement longitudinal (fig. 2.1). Le raccourcissement circonférentiel est lié à un mouvement de rotation que permet l’orientation différente des fibres myocardiques de l’endocarde à l’épicarde. Les altérations de la cinétique se traduisent par une hypokinésie (diminution de l’amplitude du mouvement), une akinésie (absence de mouvement) ou une dyskinésie (mouvements paradoxaux d’expansion en systole) segmentaire ou régionale.
Les mesures normales des volumes ventriculaires gauches rapportées à la surface corporelle sont résumées dans le tableau 2.1.
Tableau 2-1 Normes ventriculaires.
| Diamètre télédiastolique du VG | 56 mm en 4 cavités 60 mm en vertical grand axe (2 cavités) |
|---|---|
| Volume télédiastolique du VG | 52–89 ml/m2 |
| Volume télésystolique du VG | 17–37 ml/m2 |
| Volume d’éjection systolique (stroke volume) du VG | 50–60 ml/m2 |
| Fraction d’éjection du VG | 59–69 % |
| Fraction de raccourcissement | 18–42 % |
| Fraction d’éjection du VD | 51–65 % |
| Épaisseur du myocarde VG | 7–12 mm (sauf pointe ou apex) |
| Épaisseur du myocarde VD | < 4 mm (bord libre) |
| Épaississement systolique | 48 % |
| Masse du VG | 65–92 g/m2 (< 100 chez l’homme, < 95 chez la femme) |
Le myocarde est représenté par le muscle lui-même (environ 75 %), un tissu conjonctif de soutien (environ 15 %), et le volume sanguin myocardique – artères coronaires et microcirculation (environ 10 %). Le muscle myocardique est formé de cellules distinctes (cardiomyocytes) étroitement connectées les unes aux autres. Les cardiomyocytes, qui comptent pour plus de la moitié du poids du cœur, sont grossièrement cylindriques ; ils mesurent 20 μm de long et moins de 10 μm de large dans les oreillettes, 560 à 140 μm de long et 17 à 25 μm de large dans les ventricules. La fonction contractile de ces cardiomyocytes est principalement assurée par deux protéines contractiles, le fin filament d’actine et l’épais filament de myosine. À cette partie contractile du myocarde s’associe une partie anatomique très réduite, le tissu nodal, qui constitue le lieu d’origine de l’automatisme cardiaque et le système de conduction de l’onde d’activation normale. Examinées au microscope, ces cellules musculaires apparaissent striées et ramifiées. Environ la moitié des myocytes ventriculaires sont constitués de myofibrilles et de un quart à un tiers de mitochondries. La myofibre est un groupe de myocytes maintenus par du tissu conjonctif collagène. Ces fibres de collagène lient les myofibres entres elles de telle sorte que leur excès, comme dans l’hypertrophie ventriculaire gauche, peut être à l’origine d’une dysfonction diastolique.
Principales altérations tissulaires et fonctionnelles du myocarde
Bases physiopathologiques
Il a été parfaitement mis en évidence que le myocarde subit des remaniements structurels en réponse aux processus pathologiques qui l’atteignent. Quelle que soit l’étiologie du processus initial, l’atteinte myocardique se caractérise par une diminution de la puissance contractile, puis le myocarde s’adapte pour préserver sa fonction. Cellules hautement différenciées, les myocytes ne peuvent répondre directement à une agression (par exemple liée à une hypertension artérielle). La réponse se limitera à une hypertrophie de ces myocytes (d’où augmentation de la masse du myocarde et hypertrophie pariétale) et à des modifications structurelles du tissu matriciel. L’augmentation des dépôts de collagène et la fibrose sont les meilleurs exemples de ces altérations secondaires. Ce processus de remodelage, qui met en jeu les protéines contractiles et la trame de tissu conjonctif au niveau microvasculaire, comme l’élastine, permet de préserver longtemps la fonction systolique. Un ventricule remodelé et atteint de fibrose peut ne pas répondre à la suppression ou à la correction du facteur déclenchant originel. Le dysfonctionnement systolique ventriculaire, parfois brutal, témoigne de la défaillance de la pompe cardiaque, caractérisée par une diminution de la fraction d’éjection systolique.
Conséquences myocardiques de l’ischémie
Notion de réserve coronaire
La réserve de débit coronaire représente le quotient entre le débit coronaire au maximum de ses possibilités de dilatation artériolaire coronaire et le débit coronaire à l’état basal. Elle peut être étudiée en utilisant un vasodilatateur coronarien comme le dipyridamole ou l’adénosine.
Plusieurs facteurs influent sur le débit coronaire :
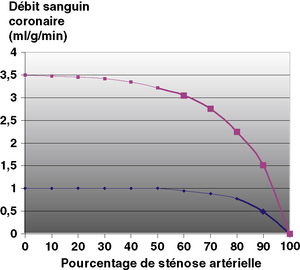
À l’état basal, d’après les données expérimentales, la réduction du débit en aval d’une sténose n’est pas proportionnelle au pourcentage de sténose, mais se manifeste seulement pour des sténoses serrées supérieures à 80 % (voir la courbe de la fig. 2.2). Au contraire, en situation d’hyperhémie (épreuve de stress physique ou pharmacologique), la diminution du débit est plus progressive et débute plus précocement pour des sténoses de 50 %, de sorte qu’il sera plus aisé de mettre en évidence un défaut de perfusion en imagerie avec stress (contraste de perfusion plus élevé entre zones saines et zones en aval d’une sténose modérée).
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree