Chapitre 13 Pathologie des glandes salivaires
Le système glandulaire salivaire comprend:
L’incidence des tumeurs d’origine salivaire est assez faible, moins de 3 % de l’ensemble des tumeurs, 5 à 10 % des tumeurs de la tête et du cou [1, 2]. Le diagnostic d’une masse salivaire, le plus souvent indolore, est essentiellement clinique: découverte à la palpation du fait du caractère superficiel des glandes salivaires.
Imagerie
Échographie [3, 4]
La dilatation des canaux intraglandulaires [3] permet d’affirmer qu’il existe une pathologie canalaire obstructive ; l’exploration échographique permet une évaluation de l’état glandulaire, facteur important à apprécier dans la pathologie inflammatoire.
L’étude des chaînes ganglionnaires jugulocarotidiennes ou cervicales postérieures sera systématique.
Tomodensitométrie et radiographies sans préparation
La suspicion de lithiase salivaire peut faire envisager un cliché simple surtout pour les glandes submandibulaires : cliché occlusal antérieur ou postérieur pour le canal submandibulaire, défilé maxillaire pour la glande car les lithiases sont plus souvent radio-opaques [1, 2].
Les scanners multibarrettes en coupes inframillimétriques sans injection de produit de contraste sont de plus en plus proposés en examen de remplacement du fait de la fréquence élevée de lithiases radiotransparentes [5], tout particulièrement au niveau parotidien, mais aussi submandibulaire [6]. Si l’échographie n’a pas détecté de lithiase, les clichés conventionnels sont peu utiles ne permettant pas (comme le scanner) d’étude canalaire.
Les calcifications recherchées correspondent le plus souvent à des lithiases mais peuvent aussi correspondre à des calcifications tumorales, plus souvent retrouvées pour les adénomes pléomorphes, ou à des phlébolithes pour les « tumeurs » angiomateuses. La TDM a une résolution en contraste tissulaire moins bonne qu’en IRM expliquant son utilisation moindre en pathologie tumorale ; elle sera surtout envisagée pour apprécier une extension osseuse corticale ou pour un bilan d’extension notamment ganglionnaire plus rapide que l’IRM avec exploration thoracique associée (tuberculose, sarcoïdose, bilan métastatique). Si l’examen est réalisé avec injection pour bilan d’une masse salivaire, une étude dynamique [7] pourra être proposée. L’injection permet en cas de pathologie inflammatoire d’apprécier l’état du parenchyme à la recherche d’abcès, de cellulite avec bilan d’extension vers le médiastin.
IRM
Réalisée idéalement avec une antenne superficielle [8, 9] pour améliorer la résolution spatiale, les études axiales T1 et T2 (toujours avoir un T2 sans Fat Sat si on veut caractériser une masse salivaire) et coronales T1 et T2 Fat Sat avant injection permettent une meilleure résolution en contraste tissulaire que la tomodensitométrie pour un bilan d’extension d’une masse.
Les séquences de diffusion [10–13] ont été proposées pour améliorer la distinction entre lésion bénigne et lésion maligne, l’augmentation de la cellularité des tumeurs malignes s’accompagnant d’une baisse du coefficient de diffusion apparent (ADC). La mesure de l’ADC n’étant pas toujours reproductible, la mesure du rapport des valeurs ADC (tumeur/parotide normale) est préconisée.
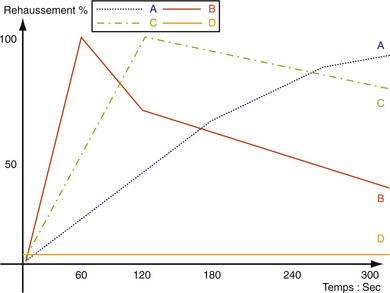
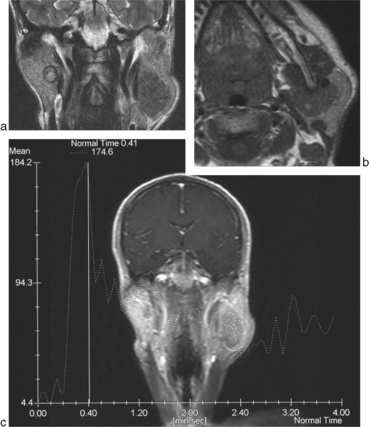
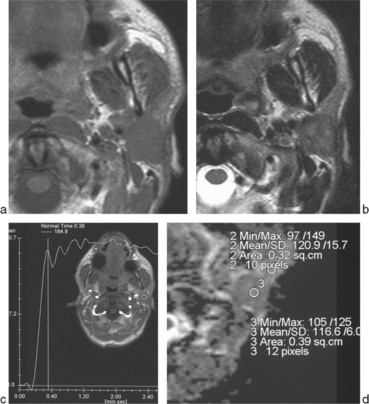
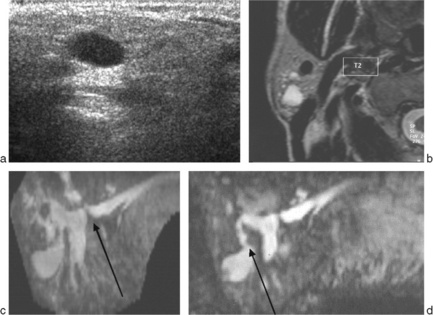
L’injection de gadolinium, indispensable pour apprécier l’extension notamment périnerveuse, peut s’accompagner de séquences dynamiques [13–16], permettant l’étude du pic de rehaussement et le lavage (wash out) de participer à la caractérisation tissulaire (fig. 13-1).
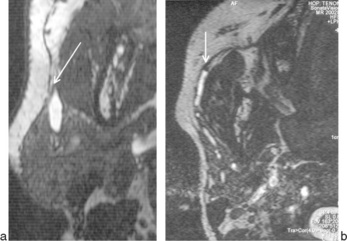
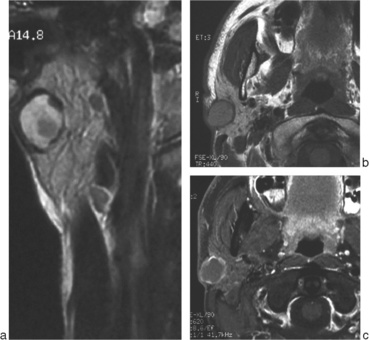
Pour les lésions kystiques, et plus encore pour un bilan canalaire, seront programmées des séquences de sialo-IRM [17] en coupes fines inframillimétriques T2 haute résolution (fig. 13-2). Cette technique non irradiante, sans cathétérisme des canaux salivaires ni injection permet une exploration canalaire satisfaisante même si la résolution est moindre qu’en sialographie [18]. Elle permet une exploration canalaire bilatérale physiologique (pas de remplissage) non invasive tendant à remplacer les indications de sialographie diagnostique dès lors qu’il existe une pathologie canalaire obstructive : une sténose prendra un aspect effilé (fig. 13-2a), un calcul [19] ou un polype (non visible en TDM) seront visibles sous la forme d’un hyposignal ovalaire (fig. 13-2b).
Sialographie [20]
Il s’agit de la technique de référence pour l’étude canalaire permettant également une étude fonctionnelle en appréciant sur le cliché tardif le « lavage » du produit de contraste par le flux salivaire. Un contexte infectieux ou la présence de pus à l’ostium du canal sont les contre-indications classiques ; la présence de lithiase est une contreindication relative à sa réalisation [1].
Le cathétérisme est l’inconvénient de la technique qui présente un taux d’échec global de 5 à 10 % [20]. Elle est plus difficile pour les canaux submandibulaires du fait de la présence d’un sphincter. Des publications récentes montrent des échecs de réalisation de la sialographie submandibulaire dépassant les 15 % [21] voire les 50 % [22], témoignant plus de la perte de l’expérience de réalisation de la sialographie du fait d’indications de plus en plus restreintes.
Tumeurs des glandes salivaires
Les tumeurs de la parotide sont les plus fréquentes (près de 80 %), 10 % atteignant les glandes submandibulaires et 10 % les glandes sublinguales et accessoires avec un risque de malignité inversement proportionnel à la taille de la glande salivaire [23].
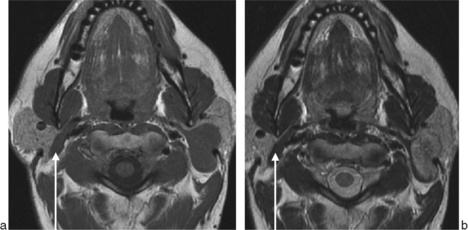
Le rôle de l’imagerie sera d’abord d’affirmer qu’il s’agit bien d’un syndrome de masse développée au sein des glandes salivaires (parotides ou submandibulaires) qui conditionnera la voie d’abord chirurgicale (fig. 13-3) et les risques nerveux liés à la chirurgie. Ainsi une adénopathie du groupe IIA (sous-digastrique) haut située peut poser des problèmes de diagnostic différentiel avec une tumeur du pôle inférieur de la parotide ou de la partie postérieure de la glande submandibulaire.
Tumeurs parotidiennes
Les tumeurs des glandes salivaires sont le plus souvent parotidiennes [1, 2] ; elles sont généralement découvertes par le patient, car palpées pour les tumeurs de la portion superficielle de la parotide, ou au contraire découvertes à un stade souvent tardif de grande taille en cas de localisation à la portion profonde, refoulant l’amygdale en dedans.
Devant une tumeur parotidienne, la technique opératoire comportera un repérage premier du nerf facial au niveau du trou stylomastoïdien avec dissection du nerf et de ses branches, jusqu’à la tumeur, nécessitant d’avoir la certitude que la lésion est bien intraparotidienne (fig. 13-3). Une parotidectomie totale (ou subtotale) conservatrice du nerf facial chaque fois que cela est possible reste souvent préconisée dans la prise en charge des tumeurs malignes mais aussi dans les adénomes pléomorphes. Le traitement peut consister en une parotidectomie exofaciale emportant la tumeur pour les autres lésions bénignes de la portion superficielle ; cette indication de parotidectomie exofaciale superficielle peut se concevoir pour les adénomes plémorphes à condition d’avoir une exérèse suffisamment à distance de la lésion.
Adénome pléomorphe (tumeur mixte)
Dix fois plus fréquente au niveau parotidien que dans la glande submandibulaire, il représente 50 à 60 % des tumeurs parotidiennes bénignes [24] soit plus de 70 % des tumeurs parotidiennes.
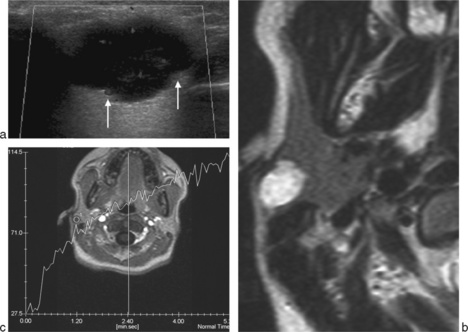
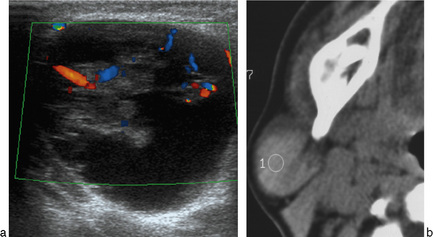
Ces lésions sont appelées tumeur mixte du fait d’une double composante cellulaire (épithéliale et myoépithéliale) avec une composante conjonctive lâche myxoïde. La lésion est solitaire, indolore, d’évolution lente (souvent connue de longues dates du patient, siégeant dans la portion superficielle dans 90 % des cas), d’aspect échographique hypoéchogène avec des contours réguliers mais festonnés, bosselés (absence de capsule), homogène avec renforcement postérieur. L’étude Doppler permet d’écarter un kyste en montrant une vascularisation qui reste modérée (fig. 13-4a) avec possibilité de calcifications [4].
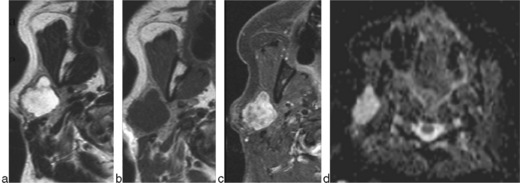
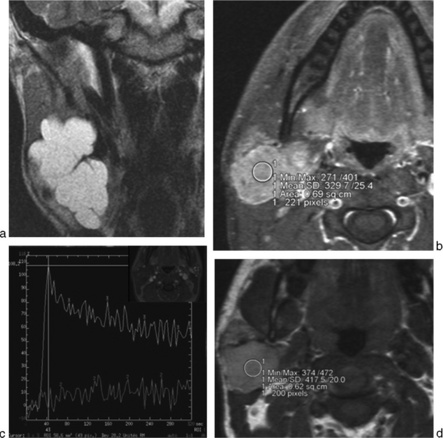
En IRM [25], une lésion aux contours lobulés en franc hypersignal T2 (fig. 13-4b et 13-5a) (stroma fibromyxoïde) homogène majoré sur les séquences avec suppression de graisse est très évocatrice d’un adénome pléomorphe avec hyposignal T1 (fig. 13-5b) non spécifique. L’étude ADC en IRM montre un coefficient élevé (fig. 13-5d) lié au stroma fibromyxoïde prédominant avec un rapport ADC tumeur/parotide normale supérieur à 1,2, souvent proche de 2 (fig. 13-5d).
L’étude dynamique après injection montre un rehaussement progressif (fig. 13-4c) avec un pic retardé supérieur à 120 s et un lavage faible inférieur à 10 % à 5 minutes [15, 16].
La prise de contraste est nette (fig. 13-5c) avec une hétérogénéité augmentant avec la taille de la lésion.
La transformation carcinomateuse sous forme d’adénocarcinome, systématiquement évoquée pour des lésions anciennes de grande taille, est plus proche de 3 à 5 % que des 25 % parfois annoncés : elle est évoquée devant une croissance rapide, des douleurs récentes. En imagerie, une grande taille, la présence d’hypervascularisation Doppler ou un rehaussement hétérogène après injection de contraste doivent faire craindre une dégénérescence. L’hypercellularité liée à la dégénérescence maligne se traduit par une perte du franc hypersignal T2 et une baisse de l’ADC [26] avec un rapport ADC tumeur/parotide inférieur à 1.
Cystadénolymphome (adénolymphome ou tumeur de Whartin)
Il s’agit de la seconde lésion bénigne des glandes parotides représentant plus de 10 % des tumeurs parotidiennes [27]. La lésion est ovalaire de consistance molle souvent située au pôle inférieur, bien limitée bilatérale dans 10 à 30 % des cas (soit de façon synchrone soit métachrone) plutôt chez les hommes de 55 à 65 ans souvent grands fumeurs. Il est caractérisé par un contingent associant des portions kystiques (description de formes kystiques pures) et tissulaires, associant une double composante cellulaire : épithéliale (oncocytaire) et lymphoïde [25].
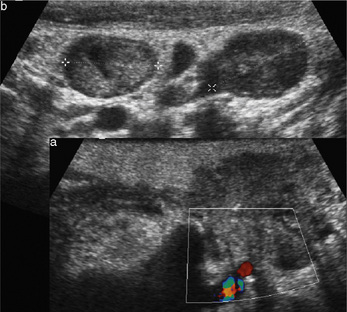
En échographie, le caractère bilatéral bien limité avec double composante (fig. 13-6a) donne un aspect différent de l’adénome pléomorphe avec contingent double :
En TDM, une hyperdensité spontanée (fig. 13-6b) est évocatrice avec prise de contraste hétérogène.
En IRM [13], on retrouve le caractère parfois bilatéral sans hypersignal T2 intense, ce qui est peu en faveur de l’adénome pléomorphe, lésion bénigne la plus fréquente, avec un aspect hétérogène avec hypo-intensités (surinfection, hémorragie, cristaux de cholestérol) (fig. 13-7) associées à des plages kystiques en hypersignal T2 plus ou moins importantes. L’association à un aspect hétérogène en T1 avec des hypersignaux (fig. 13-7b) correspondant aux portions kystiques à forte concentration protidique [25] est très évocatrice de cystadénolymphome.
Les composantes multiples donnent des mesures variables de l’ADC : coefficient apparent de diffusion élevé pour les composantes kystiques ou au contraire bas, voire très bas [11–13] pour la composante tissulaire lymphoïde particulièrement cellulaire.
La partie tissulaire présente un rehaussement rapide (fig. 13-7c), pic inférieur à 120 s [15, 16] avec un lavage rapide (wash out) supérieur à 30 % à 5 min [15, 16]. Les portions kystiques et le lavage rapide expliquent que ces lésions peuvent être considérées comme ne prenant pas ou peu le contraste ou alors comme ayant une prise de contraste périphérique [13].
En l’absence de risque de dégénérescence, une abstention chirurgicale peut s’envisager s’il existe un risque opératoire sur un terrain fragile, à condition que le diagnostic soit suffisamment fiable : concordance des critères morphologiques en imagerie et des données de la cytoponction.
Tumeurs malignes des glandes salivaires
Elles représentent la 3e cause de tumeurs parotidiennes, moins de 20 à 30 % des tumeurs parotidiennes [24] dont plus de la moitié d’origine primitive. Les plus fréquentes sont représentées par :
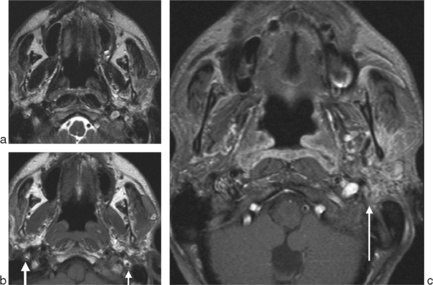
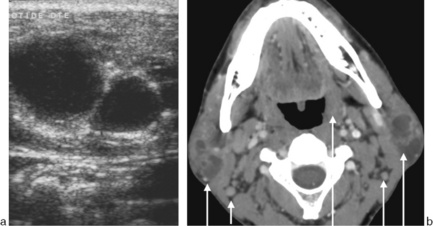
La mesure de la lésion participe au bilan T (encadré) avec bilan ganglionnaire fondamental nécessitant l’association de coupes cervicales (qui rallongent la durée de l’examen) à l’IRM parotidienne ou à une exploration échographique ganglionnaire très performante (fig. 13-8).
Les signes d’envahissement des organes de voisinage (encadré ci-dessus et tableau 13-1a), peau, muscles (faisant passer d’un Ta à Tb), ou surtout du nerf facial (T4) seront mieux évalués en IRM (cf. fig. 13-11, page 205). Le bilan d’extension aux structures osseuses, mandibule (faisant passer d’un Ta à Tb) ou base du crâne (T4) bénéficiera de l’association à l’exploration TDM (tableau 13-1b), qui permet une bonne évaluation ganglionnaire et la recherche dans le même temps de métastases à distance, notamment pulmonaires pour les carcinomes adénoïdes kystiques.
Tableau 13-1a Classification TNM de l’American Joint Committee of Cancer (1993 modifié en 1997)
| T0 | Tumeur non décelable |
|---|---|
| T1 | Tumeur ≤ 2 cm dans sa plus grande dimension sans extension extraglandulaire |
| T2 | 2 cm < tumeur ≤ 4 cm dans sa plus grande dimension sans extension extraglandulaire |
| T3 | 4 cm < tumeur ≤ 6 cm dans sa plus grande dimension (T3a) avec envahissement extraglandulaire sans atteinte du nerf facial (T3b) |
| T4 | Tumeur > 6 cm dans ses plus grandes dimensions (T4a) et/ou envahissant la base du crâne, le nerf facial (T4b) |
| N0 | Pas d’adénopathie |
| N1 | Adénopathie métastatique unique, unilatérale, ≤ 3 cm dans sa plus grande dimension |
| N2a | Adénopathie métastatique unique, unilatérale, > 3 cm mais ≤ 6 cm dans sa plus grande dimension |
| N2b | Adénopathies métastatiques multiples, homolatérales, ≤ 6 cm dans leur plus grande dimension |
| N2c | Adénopathies métastatiques bilatérales ou controlatérales, ≤ 6 cm dans leur plus grande dimension |
| N3 | Adénopathies métastatiques > 6 cm dans sa plus grande dimension |
| M0 | Pas de métastase connue |
| M1 | Métastase(s) à distance |
Tableau 13-1b Classification par stade.
| Stade | TNM | Survie à 5 ans |
|---|---|---|
| I | T1a ou T2a/N0/M0 | 90 % |
| II | T1b, T2b ou T3a/N0/M0 | 55 % |
| III | T3b et T4a/N0/M0 Tous T (sauf T4b)/N1/M0 | 45 % |
| IV | T4b N2 ou N3 M1 | 10 % |
À la classification T(NM) est ajoutée la notion d’envahissement extraglandulaire :
a : pas d’extension extraglandulaire ;
b : extension locale extraglandulaire (autre que le nerf facial ou la base du crâne) : peau, tissus mous, os.
L’absence d’hypersignal T2 (fig. 13-9b) franc sur une lésion rassurante sans signe d’extension ni adénopathie doit remettre en cause le diagnostic d’adénome pléomorphe, lésion la plus fréquente au niveau parotidien, et faire craindre une lésion maligne surtout s’il n’y a pas d’argument pour un cystadénolymphome (hypersignal T1).
L’hypercellularité conduit à une baisse de l’ADC [10–12] avec un rapport : tumeur/parotide normale inférieur à 1 (fig. 13-9d).
L’injection montre un rehaussement plus rapide que dans le cas d’un adénome pléomorphe, mais plus lent que pour un cystadénolymphome, avec un pic entre 60 et 120 s [15, 16] et surtout un lavage lent, wash out, inférieur à 30 % à 5 minutes [15, 16] (fig. 13-9c).
Carcinome muco-épidermoïde
Le carcinome muco-épidermoïde est le plus fréquemment rencontré [24, 25] ; les lésions de bas grade peuvent être le siège de composantes kystiques (hypersignal T2) contenant de la mucine à l’origine d’un hypersignal T1 [25] avec rehaussement pariétal minime après injection (fig. 13-10). Les lésions de haut grade seront plutôt en hyposignal T1 et hyposignal T2 avec rehaussement hétérogène.
L’infiltration périneurale avec atteinte des paires crâniennes est à rechercher systématiquement ; elle est le plus souvent rencontrée avec le carcinome adénoïde kystique. Ceci justifie un bilan en IRM avec injection de gadolinium pour rechercher l’infiltration périneurale (fig. 13-11) le long du nerf facial, du segment VII-3 ou au niveau du V dans la fosse infratemporale avec exploration incluant le foramen ovale.
Carcinomes adénoïdes kystiques
Les carcinomes adénoïdes kystiques (cylindrome) de localisation parotidienne sont classiquement de meilleur pronostic que les autres localisations salivaires avec une évolution lente vers le nerf. On distingue [25] les formes solides (10 %), de moins bon pronostic, plus cellulaires en hyposignal T2 des formes un peu moins cellulaires, glandulaires (cribriforme) (50 %) ou trabéculaires (tubulaire) (30 %), avec possibilité d’hypersignal T2 dans les formes de bas grade de malignité et de meilleur pronostic. Il peut ainsi être difficile en imagerie de différencier un adénome pléomorphe d’un carcinome adénoïde kystique de bas grade : la place de l’ADC et de l’étude des courbes dynamiques pouvant aider à faire la distinction. Les carcinomes adénoïdes kystiques de haut grade peuvent aussi être le siège de nécrose hémorragique à l’origine d’hypersignaux T1 (diagnostic différentiel avec le cystadénolymphome) [25].
Lésions kystiques et pseudokystiques
Kyste parotidien
Il s’agit d’une lésion anéchogène avec renforcement postérieur, sans vascularisation Doppler éliminant un adénome pléomorphe ; elle est parfois cloisonnée en échographie se présentant comme une lésion hypodense, liquidienne non rehaussée après injection de produit de contraste iodé en scanner. L’IRM retrouve un hypersignal T2 et un hyposignal T1 qui pourraient faire envisager un adénome pléomorphe : l’injection de gadolinium permet de différencier les lésions kystiques, qui ne se rehaussent pas, de l’adénome pléomorphe qui se rehausse de façon nette. L’étude de la séquence de diffusion et de l’ADC permettra de reconnaître les exceptionnels kystes dermoïdes décrits au niveau parotidien qui seront en hypersignal b1000 avec baisse de l’ADC [28] contrairement aux structures kystiques liquidiennes pures avec rapport ADC élevé. Ces lésions kystiques ne relèvent pas nécessairement de la chirurgie, sauf complication ou doute diagnostique, notamment certaines présentations pseudokystiques de carcinome muco-épidermoïdes de bas grade (fig. 13-10).
Les lymphangiomes kystiques, rares chez l’adulte (fig. 13-12), surtout visibles chez l’enfant, se présentent sous la forme de lésions kystiques avec cloisons plus ou moins épaisses non vascularisées avec diffusion trans-spatiale multicompartimentale, polylobée. On retrouve cet aspect kystique en IRM [29] avec hypersignal T2 cloisonné, en hyposignal T1 sans rehaussement. Un hypersignal T1 est possible du fait de remaniements hémorragiques ou de contenu protidique élevé avec niveaux liquide/liquide. Le traitement est le plus souvent chirurgical avec possibilité d’alcoolisation sous contrôle échographique [3].
Kyste salivaire ou sialocèle
Kyste acquis, à contenu en règle non muqueux, lié à la dilatation d’un canal excréteur en amont d’une obstruction dont l’étiologie n’est pas toujours évidente : la mise en évidence d’une connexion avec les canaux salivaires (fig. 13-13), en sialographie ou en sialo-IRM [30], permet d’étayer le diagnostic par opposition au kyste simple. Cette lésion n’est classiquement pas chirurgicale sauf complication.
Kyste lympho-épithélial du sujet VIH [31, 32]
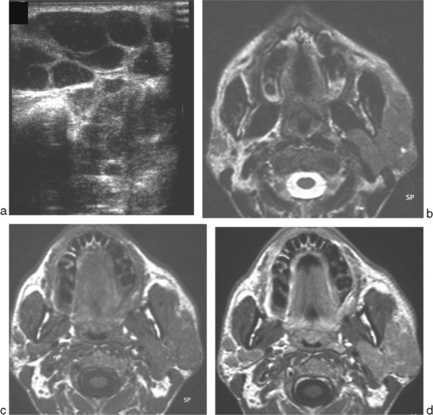
L’échographie est le plus souvent évocatrice montrant des lésions souvent multiples kystiques avec des cloisons épaisses ou à nette prédominance kystique (fig. 13-14a), bilatérales parfois proches de l’aspect du cystadénolymphome auquel il est parfois apparenté.
D’autres lésions liées au VIH, telles que les lymphadénopathies cervicales bénignes persistantes avec aspect hypertrophique des différentes structures lymphoïdes (amygdales, cavum, base de langue), souvent associées, sont retrouvées sur les techniques d’imagerie en coupe retrouvant l’aspect bilatéral pseudokystique prédominant (fig. 13-14b) des lésions parotidiennes.
La chirurgie n’est plus proposée mais la surveillance reste nécessaire du fait du risque de transformation lymphomateuse (fig. 13-15) et du risque de tuberculose parotidienne sur ces terrains d’immunosuppression pouvant donner un aspect proche [32].
« Lésions vasculaires » de la parotide
Hémangiome et malformations veineuses représentent les « tumeurs » salivaires les plus fréquentes chez l’enfant [33, 34].
L’hémangiome infantile est absent à la naissance, en général unilatéral, non capsulé, lobulé, compressible sous la sonde avec un aspect échographique évocateur, une hyperéchogénicité, hétérogène avec plages pseudokystiques comportant des septas présentant une hypervascularisation Doppler avec vitesses systoliques élevées et un index de résistance bas [3] : il s’agit d’une lésion vasculaire à haut débit. Cette lésion prolifère jusque vers l’âge de 9 mois pour régresser et disparaître le plus souvent à l’adolescence. L’IRM n’est indiquée que si l’échographie ne permet pas une extension précise ou en cas de traitement rendu nécessaire par les complications : elle se présente en hypersignal T1 hétérogène, hypersignal T2 hétérogène avec prise de contraste hétérogène après injection de gadolinium.
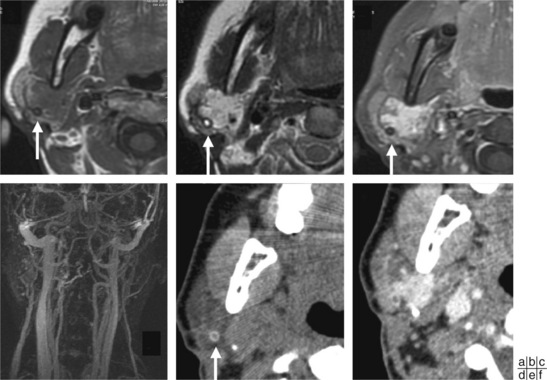
Les angiomes veineux, anomalies vasculaires de développement à débit lent, présents à la naissance, ne vont pas involuer et peuvent se retrouver à l’âge adulte : ils sont caractérisés par des phlébolithes avec hypersignal T2 et rehaussement marqué pouvant faire discuter un adénome pléomorphe en IRM mais avec des contours mal limités – l’hypersignal T1 pouvant à tort orienter vers un cystadénolymphome. La présence de phlébolithes, plus difficiles à visualiser en IRM (hyposignal), à rechercher en TDM, est un bon argument en faveur du diagnostic d’angiome veineux (fig. 13-16).
L’origine vasculaire d’une lésion parotidienne chez l’adulte est rare mais importante à signaler en préopératoire pour le chirurgien pouvant faire surseoir à l’intervention (fig. 13-16).
Autres tumeurs
Les myoépithéliomes [35] correspondent à un adénome pléomorphe avec cellules myoépithéliales exclusives sans la composante épithéliale.
Une lésion ayant certaines des caractéristiques de l’adénome pléomorphe (hyposignal T1 avec prise de contraste rapide et prolongée sur les acquisitions dynamiques) mais avec hyposignal T2 et un aspect rond non lobulé peut faire envisager un adénome à cellules basales [36] dont le diagnostic reste anatomopathologique ; des remaniements kystiques [37] parfois hémorragiques [38] peuvent donner un aspect proche du cystadénolymphome mais la cinétique de rehaussement (prise de contraste rapide et prolongée sur les acquisitions dynamiques) est différente.
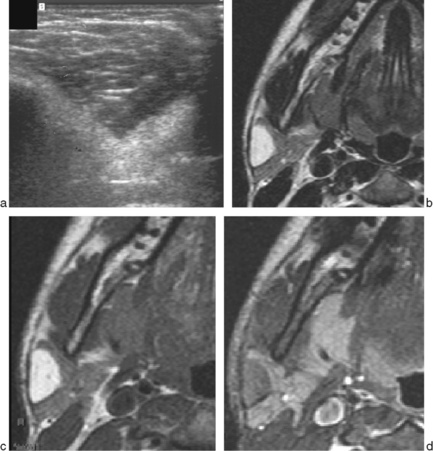
Le lipome[39] peut se développer soit en intrasoit en extraparotidien. L’aspect échographique [3] peut surprendre avec un aspect discrètement hypoéchogène, avec travées fines (fig. 13-17a), sans vascularisation en Doppler nécessitant une confirmation par imagerie en coupes pour affirmer la nature graisseuse (fig. 13-17) : densité négative en scanner, hypersignal T1 (fig. 13-17b) s’effaçant après suppression de graisse en IRM (fig. 13-17d), sans rehaussement significatif après injection de gadolinium. La chirurgie n’est pas indispensable si l’aspect est typique en imagerie.
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree