Diagnostic
• Interrogatoire du patient (âge, terrain immunitaire, contexte géographique et épidémique, vaccinations antérieures).
• Analyse du LCR après ponction lombaire.
• Biologie moléculaire (PCR), recherche d’antigènes solubles ou d’anticorps afin d’identifier le germe responsable.
Ressources et stratégies thérapeutiques
Traitement de la crise (tableau 1.32)
• Situations d’urgence : en cas de purpura fébrile associé à un élément nécrotique ou ecchymotique supérieur à 3 mm de diamètre : antibiothérapie précoce (ceftriaxone : Rocéphine®, Ceftriaxone® ; céfotaxime : Claforan®, Céfotaxime® ou à défaut amoxicilline : Clamoxyl®, Amoxicilline®) en IV ou IM : 1 g chez l’adulte et 50 mg/kg chez l’enfant et le nourrisson, sans dépasser 1 g).
• Méningite virale : traitement uniquement symptomatique (antalgiques voire antipyrétiques).
• Méningite bactérienne communautaire : antibiothérapie IV instaurée le plus rapidement possible :
– pneumocoque (cocci Gram +), méningocoque (cocci Gram−) ou Haemophilus influenzae (bacille Gram−) : céfotaxime ou ceftriaxone ;
– Listeria monocytogenes (bacille Gram +) : amoxicilline et gentamicine (Gentalline®, Gentamicine®) ;
– Escherichia coli (bacille Gram–) : céfotaxime ou ceftriaxone et gentamycine.
• Doses maximales chez l’enfant : 12 g/j de céfotaxime ou 4 g/j de ceftriaxone.
• Association d’une corticothérapie à l’antibiothérapie (dexaméthasone : Dexaméthasone Mylan® : 10 mg chez l’adulte ou 0,15 mg/kg chez l’enfant toutes les 6 heures pendant 4 jours).
• Chimioprophylaxie pour les sujets en contacts par rifampicine en cas d’infection par méningocoque.
Suivi pharmaceutique
• Éduquer le patient sur les bases du traitement symptomatique (rappel des doses maximales, des fréquences d’administration).
• Renforcer l’observance des traitements.
• Rappeler l’importance de poursuivre les antibiotiques sur l’ensemble de la durée prescrite pour éviter le développement de résistances.
• Conseiller des levures ou probiotiques pour limiter les effets secondaires digestifs.
• Indiquer les moyens de prévention pour éviter la contamination de personnes en contact.
• Promouvoir la vaccination (Haemophilus influenzae de type b, méningocoque sérogroupe non B, pneumocoque, oreillons et tuberculose).
Ménopause
Symptomatologie
• bouffées de chaleur : elles sont constatées dans plus de 65 % des cas vers 50–55 ans. Leur intensité est variable depuis la simple rougeur de la face jusqu’à la grande bouffée de chaleur vasomotrice ;
• trouble de l’humeur (irritabilité, état dépressif, anxiété, tristesse) chez 40 % des femmes ;
• sécheresse vaginale, atrophie de la vulve, sensibilité accrue aux infections vaginales…
• modifications de la libido ;
• troubles urinaires : dysurie, incontinence urinaire, impériosité mictionnelle ;
• modification des phanères : ils tendent à se clairsemer dans les zones dépendantes des œstrogènes et augmenter en nombre sur les lèvres supérieures et les joues ;
Les complications de la ménopause sont
Ressources et stratégies thérapeutiques
Traitement hormonal de la ménopause
Les principales contre-indications sont réparties en :
• contre-indications absolues : cancer du sein, maladies thromboemboliques, lupus, tumeur hypophysaire, porphyrie, affections hépatiques graves et évolutives, hyperlipidémies sévères, HTA grave ;
• contre-indications relatives : fibrome, endométriose, mastopathies bénignes, HTA, diabète insulinodépendant, antécédents familiaux de cancer du sein, de l’endomètre, cholestase…
Principales molécules
• Œstrogènes : œstrogènes naturels ou œstrogènes de synthèse (17-bêta-œstradiol) utilisés par voie orale ou par voie cutanée (patch, gel).
• Progestatifs : progestérone naturelle, progestatifs de synthèse. Le progestatif est ajouté au traitement œstrogénique pour éviter le risque de cancer de l’endomètre (12 j/mois au minimum). Chez la femme hystérectomisée, il n’est pas nécessaire d’ajouter au traitement œstrogénique de la progestérone micronisée ou un progestatif. La principale voie d’administration est orale ou intra-utérine par l’intermédiaire d’un DIU.
Éléments de surveillance
• Recherche d’un sur- ou sous-dosage :
– en cas de sous-dosage : bouffées de chaleur et sécheresse vaginale peuvent réapparaître. Dans cette situation, on augmentera la dose d’œstrogènes ;
– en cas de surdosage en œstrogène, les seins sont tendus et les règles sont abondantes. Dans cette situation, on diminuera la dose d’œstrogènes. Les progestatifs peuvent être également responsables de mastodynies.
Principaux effets bénéfiques
• Prévention ou traitement des complications à court et moyen termes :
• Prévention des complications à long terme :
Alternatives thérapeutiques
• Œstrogènes à action locale pour traiter la sécheresse vaginale.
• SERM (modulateur sélectif des récepteurs aux œstrogènes) : actifs sur l’ostéoporose, action préventive sur la survenue d’un cancer du sein mais pas d’action sur les bouffées de chaleur ni la sécheresse vaginale.
• Bisphosphonates : actifs sur la minéralisation.
• Autres traitements disponibles pour l’ostéoporose : l’hormone parathyroïdienne, le ranélate destrontium.
• La tibolone : stéroïde actif sur l’ostéoporose, le vagin, les bouffées de chaleur.
• Parfois des lubrifiants vaginaux pour les rapports sexuels.
Migraine
Symptomatologie
• les facteurs psychologiques : contrariété, anxiété, émotions brusques, stress…
• les habitudes alimentaires : jeûne, rythme de repas irrégulier mais aussi certains aliments tels que : l’alcool, le chocolat, le fromage, les graisses ;
• les facteurs hormonaux : menstruation, pilule contraceptive, traitements hormonaux substitutifs de la ménopause ;
• les changements de mode de vie : fatigue, surmenage, voyages, modifications du rythme de sommeil…
• facteurs neurosensoriels et climatiques : luminosité, bruits, odeurs fortes (parfum), orage, chaleur…
Clinique
• migraine sans aura : c’est la plus fréquente des migraines (environ 80 % des cas). Elle s’exprime sous forme de céphalées, souvent unilatérales, la plupart du temps pulsatiles. Cette céphalée est souvent associée à des nausées ou vomissements, une photophobie et une phonophobie. Dans la majorité des cas, il s’agit de crises qui durent de 4 à 72 heures entrecoupées d’épisodes sans crise ;
• migraine avec aura : les signes cliniques sont similaires à ceux de la migraine sans aura, associés aux signes de l’aura se traduisant par des manifestations neurologiques focales, déficitaires, transitoires et réversibles. Plusieurs types d’aura (visuelle, sensitive, phasique, motrice) peuvent survenir mais l’aura visuelle reste prédominante chez les migraineux.
Diagnostic
• Migraine sans aura : au moins cinq crises de céphalées durant de 4 à 72 heures sans traitement, ayant au moins deux des caractéristiques suivantes (unilatérale, pulsatile, modérée ou sévère, aggravée par les activités physiques de routine, nausées et/ou vomissements).
• Migraine avec aura : au moins deux crises comprenant au moins trois des quatre caractéristiques suivantes : un ou plusieurs symptômes de l’aura, totalement réversibles, le symptôme de l’aura se développe progressivement pendant plus de 4 minutes et si plusieurs symptômes sont associés, ils surviennent successivement, la durée de chaque symptôme n’excède pas 60 minutes, la céphalée fait suite à l’aura après un intervalle libre maximal de 60 minutes, mais parfois commence avant ou pendant l’aura.
Ressources et stratégies thérapeutiques
Traitement de crise
• En première intention : anti-inflammatoires non stéroïdiens (AINS) non spécifiques (kétoprofène : Bi-profénid®, Kétoprofène® ou ibuprofène : Nureflex®, Advil®, Ibuprofène®)
• Si échec : antimigraineux spécifiques de type triptan (almotriptan : Almogran® ; élétriptan : Relpax® ; frovatriptan : Tigréat® ; naratriptan : Naramig® ; rizatriptan : Maxalt® ; sumatriptan : Imigrane®, Sumatriptan® ; zolmitriptan : Zomig®, Zomigoro®, Zolmitriptan®). La prise ne peut être renouvelée que si la première administration a permis de faire régresser les symptômes.
• En cas de nausées ou vomissements associés, utiliser les voies nasale, rectale voire injectable.
Molécules adjuvantes : antiémétiques (métoclopramide : Primpéran®, Métoclopramide®).
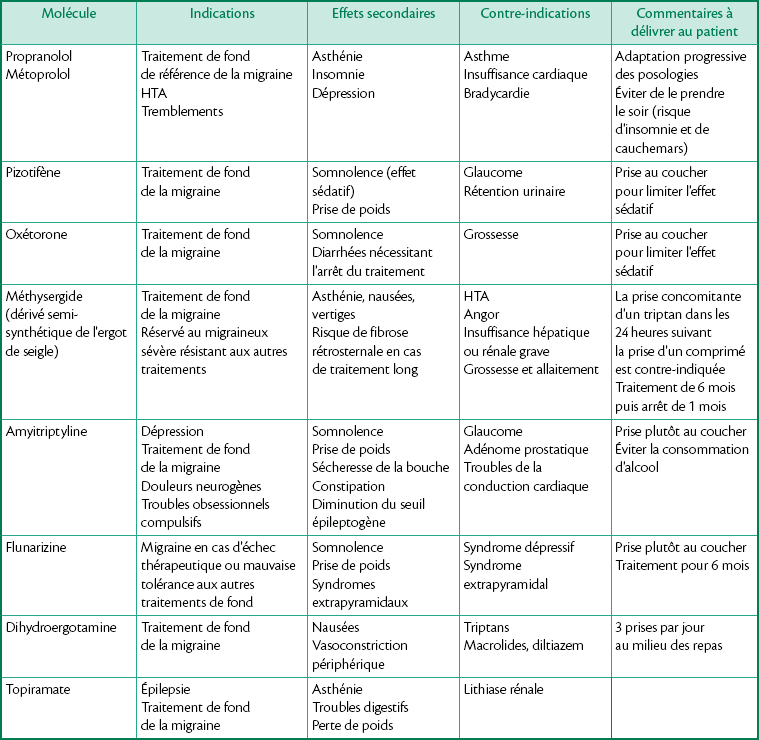
Traitement de fond (tableau 1.33)
– baisse de la fréquence des crises d’au moins 50 % ;
– diminution de la sévérité de la crise ;
– réduction de la consommation médicamenteuse de traitement de crise.
• Durée : le traitement est instauré pour une durée de 6 mois à 1 an suivi d’une diminution progressive des posologies jusqu’à arrêt total.
– bêta-bloquants (propranolol : Avlocardyl®, Propranolol® ou métoprolol : Séloken®, Métoprolol®), traitements de référence ;
– antidépresseurs tricycliques (amitriptyline : Laroxyl®) ;
• Autres classes en deuxième intention, en cas d’échec :
– antisérotoninergiques (pizotifène : Sanmigran® ou méthysergide : Désernil®) ;
– sympatholytiques (indoramine : Vidora®) ;
– inhibiteurs de canaux calciques (flunarizine : Sibélium®) ;
– antiépileptiques (topiramate : Epitomax®, Topiramate® ; valproate de sodium : Dépakine®, Valproate de sodium® ; gabapentine : Neurontin®, Gabapentine®) ;
– dérivés de l’ergot de seigle (dihydroergotamine : Séglor®, Ikaran®, Tamik®).
Suivi pharmaceutique
• Demander au patient de remplir un agenda des céphalées afin de pouvoir adapter au mieux le traitement antimigraineux.
• Rappeler les règles hygiéno-diététiques.
• Vérifier si le patient distingue bien le traitement de fond et le traitement de crise.
• Indiquer les modalités de prise du traitement de crise.
• Renforcer l’observance du traitement de fond.
Myasthénie
Symptomatologie
• La myasthénie acquise, ou auto-immune, est provoquée par la présence d’anticorps antirécepteurs cholinergiques nicotiniques de type IgG au niveau de la plaque motrice.
• Des syndromes myasthéniques congénitaux sont dus à des mutations géniques (gènes codant l’acétylcholinestérase, le récepteur à l’acétylcholine, la choline acétyltransférase…) ou à une transmission transplacentaire des anticorps maternels antirécepteurs nicotiniques.
Clinique
– la principale caractéristique de la myasthénie est la faiblesse et la fatigabilité musculaires (plus marquées en fin de journée, s’aggravant au cours d’un effort physique et améliorées par le repos) ;
– la maladie débute souvent par une atteinte des muscles oculaires se traduisant par une diplopie binoculaire et un ptosis asymétrique. Cette myasthénie oculaire peut se généraliser aux autres muscles striés, à l’origine notamment des symptômes bulbaires (paralysie faciale avec visage inexpressif, difficultés à fermer la paupière, mâchoire tombante, troubles de la phonation, voix nasillarde, syndrome de la « tête tombante »). Le déficit musculaire peut également toucher les muscles des membres proximaux et les muscles respiratoires ;
– la pathologie peut être entrecoupée de manifestations paroxystiques qui constituent le risque majeur de la maladie car elle peut générer détresse respiratoire, faiblesse généralisée pouvant mettre en jeu le pronostic vital.
• Signes négatifs : les sujets myasthéniques ne présentent pas de troubles sensitifs et sensoriels et leurs réflexes ostéotendineux sont conservés.
Diagnostic
• Sérologie : dosage des anticorps antirécepteurs cholinergiques ou antimuscles striés.
• Test pharmacologique : l’administration IV d’anticholinestérasiques (édrophonium, néostigmine) permet une régression des symptômes dans les 15 minutes suivant l’injection.
• Examens électrophysiologiques : mesure du potentiel d’action musculaire à l’aide d’électrodes stimulant de façon répétée un nerf moteur.
Ressources et stratégies thérapeutiques
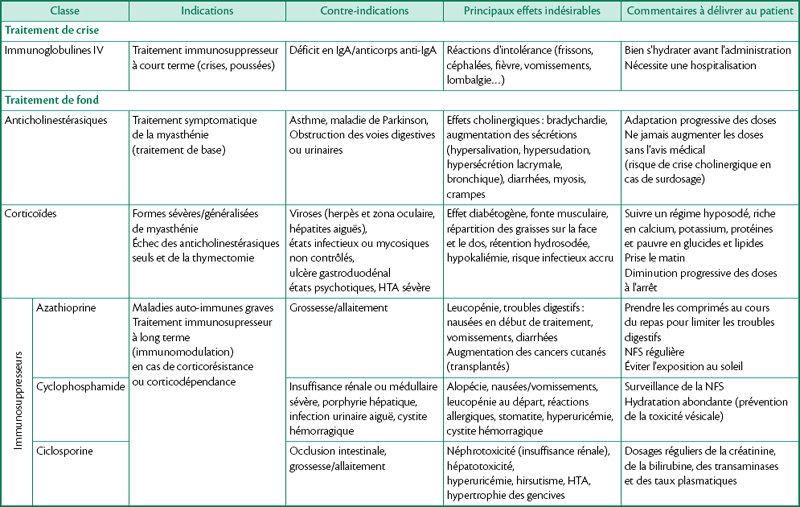
Traitement de la crise (tableau 1.34)
• Plasmaphérèse permettant de diminuer la concentration sanguine en anticorps antirécepteurs à l’acétylcholine (effet durant seulement 2 à 4 semaines).
• Immunoglobulines intraveineuses (Gammagard®, Subcuvia®, Kiovig®, Sandoglobuline®, Privigen®, Vivaglobin®, Tégéline®, Gammanor®, Octagam®) à la posologie de 1 à 2 g/kg par cure en deux jours ou en cinq jours.
Traitement de fond (tableau 1.34)
• Les anticholinestérasiques : trois anticholinestérasiques sont indiqués dans le traitement de la myasthénie : la néostigmine (Prostigmine®), la pyridostigmine (Mestinon®) et l’ambénonium (Mytélase®).
• Les corticoïdes : le principal glucocorticoïde indiqué dans la myasthénie est la prednisone (Cortancyl®) ou son métabolite actif, la prednisolone (Solupred®) à la posologie initiale de 1 mg/kg/j suivie d’une diminution progressive pour atteindre la concentration minimale efficace.
• Les immunosuppresseurs : en cas de réponse insuffisante aux glucocorticoïdes ou s’ils entraînent des effets indésirables trop importants, seront associés des immunosuppresseurs tels que l’azathioprine (Imurel®) le plus souvent, mais aussi le cyclophosphamide (Endoxan®) ou la ciclosporine (Néoral®) afin de diminuer la posologie des corticoïdes voire les arrêter.
Suivi pharmaceutique
• Informer le patient sur sa pathologie.
• Renforcer l’observance du traitement de fond.
• Conseiller un régime alimentaire adapté en cas de prise de corticoïdes (hyposodé, hypoglucidique, hyperprotéique, enrichi en calcium et en potassium).
• Rappeler la surveillance biologique du traitement.
• Prévenir le patient de l’augmentation du risque infectieux et des autres effets secondaires des immunosuppresseurs.
• Inciter le patient à ne pas prendre d’autres médicaments sans avis préalable.
Mycose vaginale
Symptomatologie
Facteurs de risque
• Grossesse (hyperacidité vaginale due à l’imprégnation œstrogénique).
• Prise de certains traitements : antibiothérapie (déséquilibre de la flore de Döderlein), contraception œstroprogestative, progestatif (par atrophie muqueuse) et anticholinergiques (par atrophie muqueuse).
• Hygiène locale inadaptée : toilettes excessives avec douches vaginales, utilisation d’antiseptiques locaux.
• Vêtements favorisant la macération : sous-vêtements en fibres synthétiques, pantalons trop serrés.
Ressources et stratégies thérapeutiques
• Règles hygiéno-diététiques :
– utiliser un savon alcalin pour la toilette intime ;
– ne pas faire de toilette vaginale car cela perturbe la flore de Döderlein ;
– lutter contre les facteurs de risque : ne pas mettre de pantalons trop serrés, porter des sous-vêtements en coton, bien équilibrer le diabète.
• Traitement antifongique local :
– ovule antifongique à base de dérivés azolés, forme LP ou non ;
– associé à une pommade vulvaire antifongique pendant 10 jours.
• Traitement du partenaire : pommade antifongique au niveau du sillon balano-préputial pendant 10 jours si le partenaire est symptomatique ou si mycose récidivante
• Si mycose récidivante : traitement minute par voie systémique per os (Béagyn®), 1 cp/mois pendant 3 mois.
Myélome multiple ou maladie de Kahler
Symptomatologie
• Le myélome multiple est une prolifération maligne de plasmocytes monoclonaux responsables de la sécrétion d’une immunoglobuline monoclonale retrouvée dans le sérum et/ou les urines.
• Les circonstances de découverte sont le plus souvent liées à des douleurs ou des fractures osseuses, parfois de découverte systématique dans le bilan d’une altération de l’état général ou d’une anémie.
Diagnostic
– la mise en évidence d’une immunoglobuline monoclonale dans le sang et/ou les urines (avec également recherche de chaînes légères κ ou λ) ;
– une prolifération plasmocytaire dans la moelle osseuse lors d’un myélogramme ;
– le retentissement sur la fonction rénale et/ou une augmentation de la calcémie ;
– la mise en évidence d’images osseuses lytiques à la radio, au scanner à l’IRM.
Ressources et stratégies thérapeutiques
• inhibiteur du protéasome : bortézomib (Velcade®) ;
• des anti-angiogéniques : thalidomide (Thalidomide®) ; lénalidomide (Revlimid®) ;
• des corticoïdes : prednisolone (Solupred®, Cortancyl®) ou dexaméthazone (Médrol®) ;
• des agents alkylants : melphalan (Alkéran®) ou cyclophosphamide (Endoxan®) ;
• une autogreffe de cellules souches hématopoïétiques périphériques est fréquemment indiquée et est réalisée après mobilisation et recueil de ces cellules souches ;
• il est fréquent de faire appel à d’autres traitements associés de type :
Suivi pharmaceutique
• Les patients doivent être informés d’une plus grande vulnérabilité aux infections et les effets indésirables hématotoxiques de la plupart des médicaments utilisés :
– risques de cytopénies profondes avec le melphalan (Alkéran®). Consulter dans les 24 heures en cas de :
– risques de neuropathies secondaires à l’utilisation des « imides » (thalidomide, lénalidomide : Revlimid®) et du bortézomib (Velcade®) : consulter en cas de paresthésies dans les membres inférieurs ou plus rarement dans les membres supérieures ;
– risques de phlébite avec lénalidomide (Revlimid®) : consulter en cas de douleur du mollet, ou de douleur thoracique brutale (embolie pulmonaire ? ). Ces patients reçoivent souvent soit des antiagrégants plaquettaires, soit des héparines de bas poids moléculaire en prévention de ces risques thrombotiques.
• Il est conseillé d’avoir une bonne hydratation.
• Inciter le patient à une bonne compliance, à un suivi biologique (hémogramme, recherche d’une réapparition de l’immunoglobuline monoclonale circulante, taux des chaînes légères, calcémie, fonction rénale).
Obésité
Symptomatologie
Étiologies
• Génétique et déterminants environnementaux.
• Alimentation (apports énergétiques quantitatifs et qualitatifs).
• Désordre affectif, anxiété ou émotion.
• Troubles endocriniens : hypothyroïdie, hypercorticisme.
• Médicaments : insuline, sulfamides hypoglycémiants, bêtabloquants non cardiosélectifs, antisérotoninergiques, antihistaminiques, corticoïdes, contraceptifs (progestérone), neuroleptiques et antipsychotiques de 2e génération (olanzapine).
Ressources et stratégies thérapeutiques
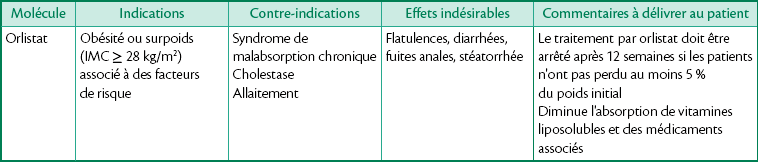
Traitement médicamenteux
La prise en charge de l’obésité est pluridisciplinaire et prend en compte ses dimensions psychologiques et sociales. L’objectif thérapeutique initial est de permettre au patient de perdre 10 % du poids initial (entre 5 et 15 % en général). L’orlistat (Xenical®) peut être proposé (120 mg au milieu de chaque repas) (tableau 1.35).
Chirurgie bariatrique
• en cas d’IMC ≥ 40 kg/m2 ou ≥ 35 kg/m2 associé à au moins une comorbidité susceptible d’être améliorée après chirurgie ;
• après échec d’un traitement médical, nutritionnel, diététique et psychologique bien conduit pendant au moins 6 à 12 mois ;
• en l’absence de perte de poids ou de maintien de la perte de poids ;
• chez des patients bien informés et ayant bénéficié d’une évaluation et d’une prise en charge préopératoire multidisciplinaire ;
• chez des patients ayant bien compris et accepté la nécessité du suivi médico-chirurgical à long terme ;
Suivi pharmaceutique
• Promouvoir une alimentation saine et une activité physique régulière.
• Rassurer les parents obèses et les orienter vers des centres spécialisés.
• Dépister le risque d’obésité chez l’enfant.
• Accompagner le patient d’un point de vue psychologique.
• Dispenser des conseils nutritionnels.
• Contrôler la bonne observance du traitement médicamenteux.
• Prévenir les éventuels effets indésirables.
• Conseiller le patient ayant subi une chirurgie bariatrique.
Œdème aigu du poumon
Symptomatologie
• L’œdème cardiogénique résulte d’une complication d’une cardiopathie connue avec augmentation majeure de la pression capillaire pulmonaire (≥ 18 mmHg) de façon prolongée (≥ 45 minutes). L’insuffisance ventriculaire gauche en est la cause la plus fréquente.
• L’œdème hémodynamique sur cœur sain peut être dû à une surcharge hydrique, hydrosodée ou à des causes neurologiques (traumatismes crâniens, tumeurs…).
• L’œdème lésionnel s’explique notamment par l’altération de façon localisée ou diffuse de la paroi alvéolo-capillaire secondaire à une intoxication par inhalation ou ingestion, à une septicémie…
Clinique
Signes positifs : la crise d’œdème aigu du poumon se caractérise par de nombreux signes :
Examens complémentaires
• Radiologie pulmonaire : dans le cas de l’œdème interstitiel, une redistribution vasculaire aboutit à une visualisation anormale des vaisseaux pulmonaires de la partie supérieure du poumon, avec une dilatation des veines pulmonaires inférieures fréquente. Dans le cas de l’œdème alvéolaire (suivant le stade d’œdème interstitiel), des opacités alvéolaires à contours irréguliers sont dispersées au hasard à travers les poumons.
• Électrocardiogramme : confirmant la tachycardie, il permet la recherche éventuelle des signes de surcharges électriques auriculaires ou ventriculaires gauches.
• Les gaz du sang : les formes simples montrent une hypoxémie accompagnée d’une hypocapnie et d’une alcalose respiratoire due à l’hyperventilation. Cependant, ce n’est pas un examen spécifique car ce tableau se voit également dans l’embolie pulmonaire et dans toute pneumopathie infectieuse.
Diagnostic
• l’auscultation cardiaque met en évidence une tachycardie avec bruit de galop cardiaque ;
• l’auscultation pulmonaire aboutit à la présence de râles crépitants bilatéraux à prédominance basale (ce qui peut constituer une gêne lors de l’examen cardiaque) ;
• la pression artérielle est quant à elle transitoirement élevée au départ.
Ressources et stratégies thérapeutiques
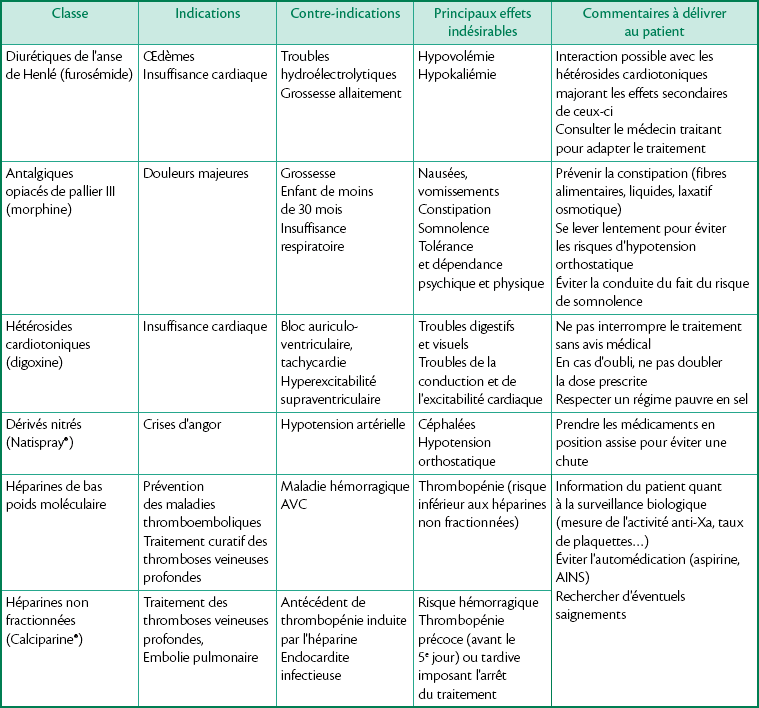
Traitement de crise (tableau 1.36)
• En cas d’OAP important : diurétiques de l’anse de Henlé par voie IV (furosémide 40 mg IV renouvelable : Lasilix®, Furosémide® ou bumétamide 1 à 2 mg en IV : Burinex®).
• Dans le cas où il y a peu ou pas d’œdème et que la pression artérielle systolique est supérieure à 100 mmHg : dérivés nitrés par voie sublinguale (Natispray®).
• La prise en charge hospitalière comprend :
– oxygénothérapie par sonde nasale (2 à 6 L par minute) ou au masque à haute concentration (6 à 12 L par minute) ;
– héparinothérapie préventive avec utilisation des héparines de bas poids moléculaire (Innohep®, Fraxiparine®) ou des héparines non fractionnées (Calciparine®) ;
– éventuellement morphine (Skénan®, Actiskénan®, Morphine®) pour réduire la polypnée et calmer l’anxiété.
Œdème lésionnel
• Corriger l’hypoxémie : oxygénothérapie au masque pour maintenir une paO2 supérieure à 60 mmHg.
• Diminuer l’eau pulmonaire extravasculaire : utilisation de diurétiques en IV rapide (furosémide).
• Traitement étiologique : prise en charge d’éventuelles pathologies infectieuses (antibiothérapie), de foyers septiques.
• Prévention du risque de récidive par une héparinothérapie.
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree