118 Endométriose
Introduction
Affection gynécologique bénigne avec des propriétés invasives occasionnelles rappelant celles des tumeurs malignes, l’endométriose a longtemps frustré les médecins et les patientes. Définie comme la présence et la croissance des glandes et du stroma de l’endomètre en dehors de la cavité utérine, l’endométriose peut conduire à des manifestations symptomatiques de douleur pelvienne cyclique, de dyspareunie, de dysménorrhée et, moins fréquemment, de saignements utérins anormaux et de troubles gastro-intestinaux ou des voies urinaires. La relation entre endométriose et fertilité fait l’objet de spéculations.
Étiologie et pathogénie
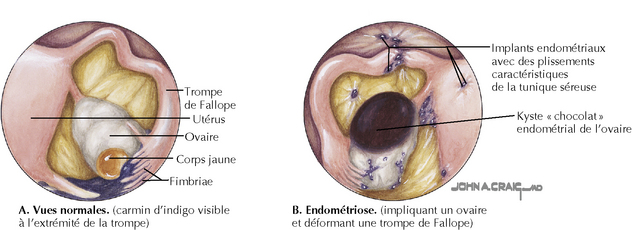
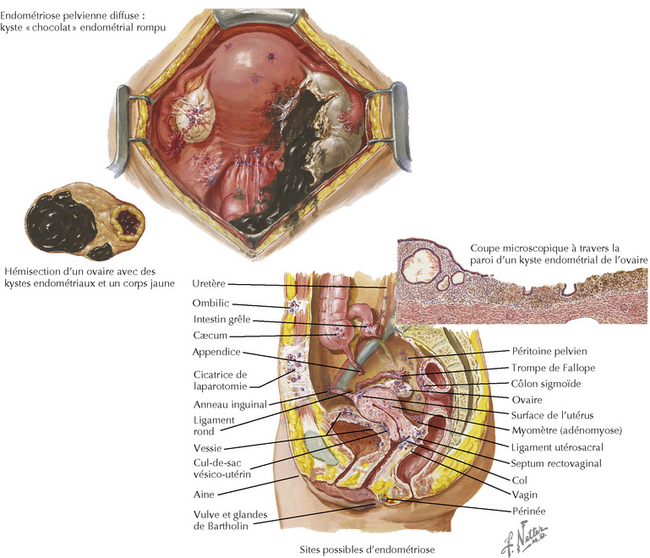
Une menstruation rétrograde, qui survient chez 90 % des femmes dans n’importe quel cycle particulier, est clairement un événement fréquent. L’implantation de cellules endométriosiques pendant la menstruation peut conduire au développement de l’endométriose. Des cellules endométriales viables ont été trouvées à la fois dans les effluents du cycle menstruel et dans le liquide péritonéal des femmes en âge de procréer. À l’appui de cette théorie, on peut citer les travaux démontrant une endométriose chez les femmes ayant une obstruction des voies génitales de sortie (jusqu’à 10 % des adolescentes atteintes d’obstruction congénitale de sortie) et le fait que les implants d’endométriose sont le plus souvent situés dans des zones adjacentes de l’ostium des trompes et dans les régions dépendantes du bassin (figures 118.1 et 118.2).
Tableau clinique
L’hétérogénéité de l’expression des symptômes d’endométriose ne doit pas être négligée, jusqu’à un tiers des patientes étant asymptomatiques. La manifestation classique est celle de la douleur pelvienne cyclique 2 à 4 j avant le début des règles. Un tableau clinique plus traditionnel comprend une dysménorrhée secondaire, une dyspareunie, une infertilité, une rétroversion utérine fixée et une nodularité sensible du cul-de-sac. Toutefois, dans une étude de Brisbane, seulement 5 % de 717 patientes atteintes d’endométriose avaient ce tableau clinique complet. En outre, les cliniciens ont souvent observé une relation inverse entre l’ampleur de la maladie d’endométriose observable et l’intensité de la douleur.
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree