12. Curarisants
INTRODUCTION
Les curares sont connus depuis la découverte de l’Amérique. Dès 1856, Claude Bernard montrait que le curare n’agissait pas directement sur le muscle mais sur la jonction neuromusculaire. En 1935 on isole la D-tubocurarine et en 1943, Griffith et Johnson l’utilisent pour obtenir la relaxation musculaire en anesthésie générale. La gallamine est synthétisée en 1947 et étudiée par Bovet.
Étapes de la curarisation
La curarisation s’établit en plusieurs phases: hypotonie musculaire, atonie par suppression du tonus de posture (atonie de Bremer), paralysie incomplète avec perte de motricité volontaire et réflexe (paralysie de Vulpian), paralysie complète le muscle ne répondant plus à l’excitation électrique du nerf (paralysie de Claude Bernard), mais se contractant par stimulation électrique directe.
La sensibilité des muscles est différente: chez l’homme les premiers muscles atteints sont ceux de la face puis dans l’ordre, membres supérieurs, membres inférieurs, muscles intercostaux, diaphragme. La respiration artificielle évite la mort car l’effet curarisant est fugace. Les muscles redeviennent fonctionnels dans l’ordre inverse de celui selon lequel ils ont été atteints.
MÉCANISME D’ACTION
Rappelons tout d’abord le fonctionnement de la jonction neuromusculaire (fig. 12.1). Au niveau de la plaque motrice l’influx nerveux entraîne la libération d’acétylcholine des vésicules présynaptiques neuronales. L’acétylcholine diffuse dans l’espace sous-neural et dépolarise la membrane postjonctionnelle. La dépolarisation de la plaque motrice entraîne la contraction musculaire par couplage excitation-contraction avec libération du calcium du réticulum sarcoplasmique. La membrane postjonctionnelle et toute la plaque motrice se repolarisent à la suite de l’hydrolyse de l’acétylcholine par l’acétylcholinestérase. On a calculé le nombre de récepteurs de l’acétylcholine dans le diaphragme de rat à l’aide d’une toxine de serpent, α-bungarotoxine, radiomarquée: il est de 4 . 107 par plaque motrice. En l’absence d’influx nerveux l’acétylcholine est sécrétée par petites quantités donnant des «potentiels de plaque miniatures» qui ne sont pas suffisants pour provoquer la contraction musculaire. Sous l’effet de l’influx nerveux du motoneurone, le potentiel de plaque devient suffisant pour provoquer l’apparition du potentiel d’action qui se propage dans la fibre musculaire.
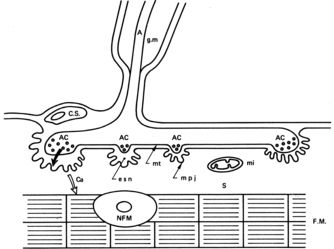 |
| Fig. 12.1 Schéma d’une plaque motrice.A : axone ; FM : fibre musculaire ; NFM : noyau de la fibre musculaire ; CS cellule de Schwann ; AC : acétylcholine ; Ca : calcium ; S : sarcoplasme ; esn espace sous-neural ; mpj : membrane postjonctionnelle ; mt : membrane terminale ; mi : mitochondrie ; gm : gaine de myéline. |
La sécrétion d’acétylcholine dans la plaque motrice peut faire défaut dans la myasthénie grave que l’on pense être une maladie auto-immune.
Les curarisants dits curarimimétiques ou pachycurares ou antidépolarisants bloquent les récepteurs nicotiniques postsynaptiques de la plaque motrice et les rendent insensibles au neuromédiateur. Le blocage de la conduction peut être levé en augmentant la quantité d’acétylcholine dans l’espace sous-neural par inhibition de l’acétylcholinestérase avec de l’ésérine ou de la néostigmine (parasympathomimétiques, anticholinestérasiques). Les curarimimétiques sont des antagonistes compétitifs de l’acétylcholine.
Ils stabilisent la membrane postjonctionnelle. Le type en est la D-tubocurarine.
Les curarisants dits acétylcholinomimétiques ou leptocurares ou dépolarisants, prennent la place de l’acétylcholine dans les récepteurs postsynaptiques de la plaque motrice et entraînent une contraction des fibres musculaires (fasciculations) avant une dépolarisation prolongée de la plaque motrice parce qu’ils ne sont pas hydrolysés par la cholinestérase. La dépolarisation étant prolongée, la conduction neuromusculaire ne se fait plus, les potentiels de plaque miniatures disparaissent, le muscle reste paralysé. L’ésérine et la néostigmine n’antagonisent pas les curarisants dépolarisants mais, au contraire, prolongent leur action. Le type de curarisant dépolarisant est le décamethonium.
CURARISANTS ANTIDÉPOLARISANTS
D-tubocurarine
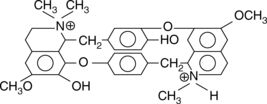 |
La D-tubocurarine est un dérivé de la benzylisoquinoléine retirée du curare en tube et trouvée dans Chondrodendron tomentosum (Ménispermacée). La distance séparant les deux azotes est de 14 angströms.
Action sur le SNC et les muscles
La D-tubocurarine bloque la transmission neuromusculaire et entraîne une paralysie flasque. Elle est plus active sur les muscles rouges (soléaire) que sur les muscles blancs (tibial). Elle déprime la conscience.
Action sur la respiration
Elle diminue la fréquence et l’amplitude respiratoire par action directe sur le bulbe.
Action sur le SNA
Elle présente un effet ganglioplégique à dose très élevée, avec disparition des effets hypertenseurs de la stimulation des nerfs splanchniques chez l’animal surrénalectomisé et disparition des effets de la stimulation des fibres préganglionnaires de la chaîne sympathique cervicale sur la membrane nictitante et la pupille de l’œil de chat.
Action sur la circulation
La D-tubocurarine à forte dose est hypotensive par libération d’histamine à partir du foie, de la peau, du tissu conjonctif.
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree


