10. Anticoagulants et antiagrégants plaquettaires
– la première étape est l’hémostase primaire qui est immédiatement mise en jeu, et permet l’arrêt du saignement grâce à la formation d’un clou plaquettaire (thrombus plaquettaire). Les principaux acteurs de l’hémostase primaire sont la paroi vasculaire, les plaquettes, le facteur Willebrand (vWF) et le fibrinogène (voir figure 10.2) ;
– la deuxième étape est la coagulation : le clou plaquettaire étant fragile, il doit être consolidé par la formation d’un caillot de fibrine à partir du fibrinogène. Ce mécanisme fait intervenir de nombreux facteurs de coagulation plasmatiques et participe à la cascade de coagulation (voir figure 10.1, tableau 10.1) ;
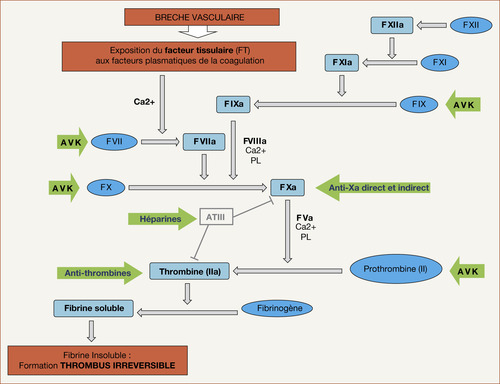 |
| Fig. 10.1 Schéma général de la coagulation. TxA2 : thromboxane A2 ; PL : phospholipides ; ATIII : antithrombine III ; AVK : antivitamine K. |
| Facteurs | Particularité | Demi-vie (h) | Taux physiologique 1 | |
|---|---|---|---|---|
| I | Fibrinogène | 120 | 0,5-1g/L | |
| II | Prothrombine (lia : thrombine) | Vit. K-dépendant | 80 | 40 % |
| V | Proaccélérine | 24 | 10-15 % | |
| VII | Proconvertine | Vit. K-dépendant | 6 | 5-10 % |
| VIII | Antihémophilique A | 12 | 30-50 % | |
| IX | Antihémophilique B | Vit. K-dépendant | 24 | 30-50 % |
| X | Facteur Stuart | Vit. K-dépendant | 48 | 10-20 % |
| XI | PTA (Plasma Thrombo plastin Antecedent) | 60 | 30 % | |
| XII | Facteur Hageman | 60 | – | |
| XIII | Facteur stabilisant de la fibrine | 240 | 2 % |
– la troisième étape est la fibrinolyse. Elle empêche l’installation et l’extension du thrombus formé par la coagulation.
Les processus à l’origine de la formation d’une thrombose artérielle ou veineuse sont différents. Une thrombose veineuse expose principalement au risque d’embolie pulmonaire. Côté artériel, la thrombose peut être à l’origine soit d’une occlusion artérielle avec une ischémie suivie d’une nécrose du lit d’aval, soit d’une migration embolique avec ischémie lorsque l’embole occlut une artère à distance.
Les médicaments qui interviennent dans le processus de l’hémostase sont des anticoagulants. Ils visent à traiter ou prévenir la formation de thrombose intra-artérielle ou intraveineuse.
On distingue deux types d’anticoagulants :
– les anticoagulants qui inhibent directement ou indirectement l’activité des facteurs lia et Xa (héparines et antithrombines) ;
– les anticoagulants qui modifient la synthèse des facteurs de coagulation (antivitamines K).
Les antiagrégants plaquettaires ne modifient pas l’activité ou la synthèse des facteurs de coagulation mais agissent sur l’hémostase primaire.
Héparines et antithrombines
Héparines
Les héparines sont des molécules mucopolysaccharidiques d’origine naturelle. L’activité anticoagulante des héparines dépend de la longueur de la chaîne pentasaccharidique. On distingue les héparines non fractionnées (HNF) ou héparine standard, l’héparine de bas poids moléculaire (HBPM) et les héparinoïdes. Les HNF et HBPM diffèrent de par leurs mécanismes d’action, leurs posologies et leurs modalités de surveillance. Les héparinoïdes, dont le seul représentant est le danaparoïde, sont utilisés en cas de contre-indication majeure ou d’intolérance à l’héparine.
Pour rappel, les principaux facteurs de coagulation ainsi que leur place dans le processus de coagulation sont représentés figure 10.1.
Héparines Non Fractionnées
Structure et mécanisme d’action (figure 10.1, tableau 10.2)
Les héparines non fractionnées potentialisent les effets de l’antithrombine III (AT III) d’un facteur 1 000. Elles forment avec l’AT III un complexe qui inactive très rapidement, principalement, les facteurs de la coagulation IIa et Xa. En cas de déficit en antithrombine III, l’effet de l’héparine est réduit.
Pharmacocinétique et conséquences pratiques
L’héparine n’est pas absorbée par voie digestive. Elle est administrée soit par voie intraveineuse soit par voie sous-cutanée. Après injection intraveineuse, la demi-vie varie de 30 à 90 minutes et s’allonge lorsque la dose administrée augmente. L’héparine se fixe sur de nombreuses protéines et cette fixation non spécifique est à l’origine d’une variation de l’effet anticoagulant. C’est pourquoi les posologies d’héparine non fractionnée nécessitent d’être ajustées à l’aide de tests biologiques. L’héparine ne traverse pas la barrière fœtoplacentaire chez la femme enceinte.
Modes d’administration (tableau 10.3)
Héparines De Bas Poids Moléculaire
Structure et mécanisme d’action (figure 10.1, tableau 10.2)
Les héparines de bas poids moléculaire forment avec l’AT III un complexe qui inactive très rapidement le facteur de la coagulation Xa.
Pharmacocinétique et conséquences pratiques
Compte tenu de la demi-vie plus longue des HBPM (environ 4 heures), elles peuvent être administrées en une seule injection sous-cutanée par 24 heures (au lieu de 2 ou 3 avec l’HNF). L’élimination des HBPM est rénale, ce qui pourrait être à l’origine d’un surdosage en cas d’insuffisance rénale.
DanaparoïDe
Le danaparoïde est un mélange de glycosaminoglycanes sulfatés extraits de la muqueuse intestinale de porc. Ce mélange ne contient pas d’héparine mais agit comme une HBPM avec une forte activité anti-Xa. Il est indiqué principalement dans le traitement prophylactique et curatif de maladies throm- boemboliques veineuses (MTEV) chez les patients atteints de thrombopénie induite par héparine (TIH) ou ayant des antécédents de TIH (Voir « Effets indésirables des héparines «).
Antithrombines
Les antithrombines, appelées aussi les hirudines, sont des inhibiteurs de la thrombine (facteur lia) empêchant ainsi la transformation du fibrinogène en fibrine. Les principales caractéristiques des antithrombines sont représentées dans les tableaux 10.2 et 10.3.
| Classe | DCI | Nom commercial | Mécanisme d’action 1 |
|---|---|---|---|
| Héparines et groupe de l’héparine | |||
| HNF | Héparine calcique Héparine sodique | Calciparine (SC) Héparine sodique (IV) | Activation de l’antithrombine et inhibition des facteurs lia et Xa |
| HBPM | Énoxaparine Daltéparine Nadroparine Tinzaparine | Lovenox (SC) Fragmine (SC) Fraxiparine (SC) Innohep (SC) | Activation de l’antithrombine et inhibition du facteur Xa (essentiellement) et du facteur lia (partiellement) |
| Héparinoïdes | Danaparoïde | Orgaran (SC) | Activation de l’antithrombine et inhibition du facteur Xa (essentiellement) et du facteur lia (partiellement) |
| Pentasaccharides | Fondaparinux | Arixtra (SC) | Activation de l’antithrombine et inhibition sélective du facteur Xa |
| Antithrombines | Bivalirudine Désirudine Lépirudine Dabigatran | Angiox (IV) Revasc (SC) Refludan (IV) Pradaxa (PO) | Inhibition du facteur lia |
| Inhibiteur facteur Xa | Rivaroxaban | Xarelto (PO) | Inhibition sélective du facteur Xa |
| MTEV : maladie thromboembolique veineuse ; TIH : thrombopénie induite par l’héparine ; PTH : prothèse totale de hanche ; PTG : prothèse totale de genou. | |||||
| Molécules | Traitement préventif des MTEV | Traitement curatif | |||
|---|---|---|---|---|---|
| Risque modéré | Risque élevé | ||||
| Posologie | Indication – Durée | Posologie | Indication – Durée | ||
| Héparine calcique | 150 Ul/kg/j en 2 à 3 inj. SC | Patients alités avec pathologie aiguë pendant 7 à 10j avec relais AVK entre 1er et 3e j | |||
| Héparine sodique | Phase aiguë de l’infarctus du myocarde et l’angor instable Bolus de 20 Ui/kg en ivd puis 20 ui/ kg/h en IV pendant 7 à 10 j avec relais AVK entre 1er et 3e j Objectif INR 1,5 à 3 fois le témoin | ||||
| Énoxaparine Lovenox | 2 000 Ul/j (SC) | Chirurgie générale < 10 j | 4 000 Ul/j (SC) | PTH-PTG : 4 à 5 semaines après l’intervention Patients alités : 6 à 14 j | mtev : 100 UI/kg x 2/j pendant 10 j, délai d’équilibration par AVK inclus Thrombose artérielle : 100 UI/kg x 2/j pendant 2 à 8 j |
| Daltéparine Fragmine | 2 500 Ul/j (SC) | Chirurgie générale < 10 j | 5 000 Ul/j (SC) | PTH-PTG : 35 j après l’intervention Patients alités : 12 à 14 j | mtev : 100 UI/kg x 2/j pendant 10 j, délai d’équilibration par AVK inclus Thrombose artérielle : 120 UI/kg x 2/j pendant 6 j |
| Nadroparine Fraxiparine | 2 850 Ul/j (SC) | Chirurgie générale < 10 j | MTEV : 85 UI/kg X 2/j pendant 10 j, délai d’équilibration par AVK inclus Thrombose artérielle : 85 UI/kg x 2/j pendant 6 j | ||
| Tinzaparine Innohep | 2 500 Ul/j (SC) | Chirurgie générale < 10 j | 3 500–4 500 Ul/j (SC) | Chirurgie cancérologique ou PTH-PTG | MTEV : 175 UI/kg/j pendant 10 j, délai d’équilibration par AVK inclus |
| Fondaparinux Arixtra | 2,5mg/j (SC) | PTG-PTH : 5 à 9 j après l’intervention Patients alités : 6 à 14 j | MTEV et embolie pulmonaire aiguë : 7,5mg/j pendant 5 j, relais AVK dès le 1er jour Thrombose artérielle : 2,5mg en 1 inj./j/kg pendant 8 j | ||
| Danaparoïde Orgaran | 750 Ul 3 fois/j pendant 7 j (SC) | Traitement prophylactique chez les patients avec des antécédents de TIH ou en cas de survenue de TIH | Manifestations thromboemboliques chez les patients atteints de TIH : bolus IVD de 2 500 UI puis perfusion continue 150–200 UI/h pendant 7 j Relais AVK dès que possible | ||
| Bivalirudine Angiox | Intervention coronaire percutanée : bolus de 0,75mg/kg en IVD puis 1,75mg/kg/h durant la durée de l’intervention | ||||
| Désirudine Revasc | 15mg 2 fois/j (lV) 5 à 15min avant l’intervention puis 2 inj./j pendant 9 à 12j | PTH-PTG : 1re inj. | |||
| Lépirudine Refl udan | TIH après confi rmation du diagnostic, 0,4mg/kg en bolus IVD, puis 0,15mg/kg en IV pendant 2 à 10 j | ||||
| Dabigatran Pradaxa | 220mg/j en 1 prise après l’intervention puis pendant 10 j en cas de PTG ou 28-35 j en cas de PTH (PO) | Prévention MTEV en cas de PTH-PTG | |||
| Rivaroxaban Xarelto | 10mg/j en une prise. La dose initiale : 6 à 10h après l’intervention puis pendant 28-35 j en cas de PTH ou 15 j en cas de PTG (PO) | Prévention MTEV en cas de PTH-PTG | |||
Dans cette classe médicamenteuse, le dabigatran étexilate (Pradaxa) a des propriétés pharmacocinétiques particulières. Il s’agit d’un précurseur thérapeutique qui, après administration par voie orale, est converti en sa substance active, le dabigatran. Le dabigatran est un inhibiteur direct, compétitif et réversible de la thrombine. Le dabigatran étexilate est un traitement de première intention indiqué en prévention primaire chez les patients pour lesquels l’administration d’un anticoagulant oral est prolongée au-delà de la sortie de l’hôpital (après notamment pose d’une prothèse de hanche). Il représente une alternative à la prescription d’un anticoagulant oral tel que les antivitamines K. Le dabigatran est faiblement lié aux protéines plasmatiques et n’est pas métabolisé par le cytochrome P450. Par conséquent, il n’est pas concerné par les interactions médicamenteuses liées à ce système enzymatique.
En revanche, le dabigatran est le substrat des protéines de transport « glycoprotéine P « ou P-gp et à ce titre des interactions médicamenteuses peuvent survenir avec les inhibiteurs et les inducteurs de la P-gp (tableau 10.4).
| HNF : héparine non fractionnée ; HBPM : héparines de bas poids moléculaire ; AVK : antivitamine K ; AINS : anti-inflammatoire non stéroïdien ; P-gp : glycoprotéine P. | |||
| Anticoagulants | Médicaments associés | Effets | Mécanisme |
|---|---|---|---|
| HNF HBPM Danaparoïde Fondaparinux Lépirudine Désirudine | Sels de potassium Diurétiques hyperkaliémants Inhibiteurs de l’enzyme de conversion | Hyperkaliémie | Potentialisation de l’effet hyperkaliémiant des héparines |
| Médicaments agissant sur l’hémostase (AVK, antithrombines, antiagrégants plaquettaires, etc.) | Augmentation du risque hémorragique | Potentialisation de l’effet anticoagulant des héparines | |
| Bivalirudine | Bivalirudine Médicaments agissant sur l’hémostase (AVK, antithrombines, antiagrégants plaquettaires, etc.) | Augmentation du risque hémorragique | Potentialisation de l’effet anticoagulant de la bivalirudine |
| Rivaroxaban | Inducteurs du CYP3A4 (rifampicine, phénytoïne, carbamazépine, etc.) | Diminution de l’effet anticoagulant (diminution de la concentration plasmatique du rivaroxaban) | Augmentation du métabolisme hépatique du rivaroxaban |
| Inhibiteur du CYP3A4 et de la P-gp (antifongiques azolés) | Augmentation du risque hémorragique par surdosage (augmentation concentration plasmatique du rivaroxaban) | Diminution du métabolisme hépatique du rivaroxaban | |
| HBPM | Augmentation du risque hémorragique | Effet cumulatif sur l’activité anti-Xa | |
| Dabigatran | Inducteur de la P-gp (rifampicine, millepertuis) | Diminution de l’effet anticoagulant | Diminution de l’exposition au dabigatran |
| Inhibiteurs de la P-gp (vérapamil, amidarone, clarithromycine, etc.) | Augmentation l’exposition au dabigatran | ||
| AVK | AINS | Augmentation du risque hémorragique | Potentialisation de l’effet AVK par augmentation de la fraction libre |
| Héparines, antiagrégants plaquettaires | Augmentation du risque hémorragique | Augmentation de l’hypocoagulabilité | |
| Inhibiteurs enzymatiques : antifongiques azolés, macrolides, cimétidine, etc. | Potentialisation de l’effet des AVK Risque accru d’hémorragie | Diminution du métabolisme hépatique | |
| Inducteurs enzymatiques : rifampicine, phénobarbital, carbamazépine, etc. | Diminution de l’effet des AVK Risque d’inefficacité thérapeutique des AVK | Augmentation du métabolisme hépatique | |
| Clopidogrel | Inhibiteurs de la pompe à protons (oméprazole, ésoméprazole), fluoxétine, antifongiques azolés, cimétidine, carbamazépine | Diminution de l’effet du clopidogrel | Inhibition CYP2C19. Diminution du taux du métabolite actif du clopidogrel |
Inhibiteur spécifique du facteur Xa
Après administration orale, il se lie à 95 % aux protéines plasmatiques. Il est métabolisé essentiellement par les cytochromes CYP3A4 et CYP2J2. De plus, le rivaroxaban est un substrat de la P-gp. Ces particularités pharmacocinétiques font que le rivaroxaban peut présenter de nombreuses interactions médicamenteuses (tableau 10.4).
Remarque
La place du dabigatran et du rivaroxaban dans la prévention primaire de la maladie thromboembolique reste à déterminer compte tenu de leur efficacité et de leur tolérance modeste par rapport au traitement de référence (enoxaparine). De ce fait, leur prescription est encore marginale. Cependant, plusieurs études de phase II et III sont en cours pour examiner l’effet antithrombotique de ces médicaments en prévention secondaire et en élargir le spectre des indications notamment en remplacement des antivitamines K.
Effets indésirables
Accidents Hémorragiques
Les accidents hémorragiques liés à l’héparinothérapie surviennent dans 5 % des cas. Ils sont favorisés par les surdosages, l’âge avancé, les actes invasifs.
En cas d’incident hémorragique modéré, il suffit de suspendre transitoirement le traitement et de le reprendre à dose plus faible.
En cas d’incident hémorragique grave, le sulfate de protamine par voie intraveineuse lente permet de neutraliser instantanément le traitement.
Thrombopénies Induites Par Héparine (Tih)
Il s’agit d’une complication rare (0,5 à 1 %) mais grave.
On distingue deux types de TIH :
– TIH type I : elle apparaît entre le 2e et le 5e jour de traitement avec une thrombopénie bénigne autour de 100 000G/L ;
– TIH type II : il s’agit d’une baisse des plaquettes de 50 % de la valeur de base ou d’une thrombopénie < 100 000G/L. Cette thrombopénie apparaît plus tardivement (9-10e jour de traitement) et peut survenir même au cours des traitements à dose préventive.
Il s’agit d’une aggravation de la maladie thromboembolique ou d’accidents d’ischémie artérielle aiguë. La TIH impose l’arrêt immédiat de l’héparine et l’utilisation d’autres moyens thérapeutiques : danaparoïde ou lépirudine.
Dans 95 % des cas, cette thrombopénie résulte d’une immunisation contre la membrane des plaquettes. Il est obligatoire de surveiller la numération des plaquettes au minimum 2 fois par semaine pendant 21 jours.
Le diagnostic de TIH peut être aidé en réalisant un test d’agrégation plaquettaire en présence d’héparine. Le test est dit positif lorsque les plaquettes d’un sujet témoin agrègent en présence du plasma du patient et d’héparine. Ces tests ne sont pas réalisés en urgence. Le meilleur moyen diagnostique de thrombopénie à l’héparine est de constater la remontée du chiffre des plaquettes dans les 5 jours suivant l’arrêt du traitement.
Surveillance biologique
Voir Fiche pharmacologie « Héparines et antithrombines», page 127.
Contre-indications – Précautions d’emploi
Voir Fiche pharmacologie « Héparines et antithrombines », page 127.
Antivitamines K
Les antivitamines K sont des médicaments anticoagulants oraux largement prescrits et utilisés parfois à vie. On distingue deux groupes en fonction de leur structure chimique (tableau 10.5) :
| Classe | DCI | Nom commercial | Mécanisme d’action |
|---|---|---|---|
| Antivitamines K de demi-vie courte | Acénocoumarol | Simtrom Minisintrom | Analogues structuraux de la vitamine K Inhibition de la synthèse des facteurs II, VII, IX et X |
| Antivitamines K de demi-vie longue | Warfarine Fluindione | Coumadine Préviscan |
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree


