7. Antibiotiques
Notions générales
Leur mécanisme d’action diffère selon la famille :
– les pénicillines, céphalosporines et glycopeptides altèrent la membrane bactérienne ;
– les aminosides, macrolides, tétracyclines et phénicolés inhibent la synthèse des protéines bactériennes ;
– la rifampicine, les fluoroquinolones et les sulfamides altèrent le bon fonctionnement du génome bactérien.
Une antibiothérapie bien conduite et justifiée exige une réflexion préalable intégrant des paramètres microbiologiques, pharmacologiques et cliniques afin de définir les modalités pratiques de sa mise en œuvre (monothérapie ou association, posologie et modalités d’administration, durée de traitement).
Sensibilité et résistance des germes aux antibiotiques
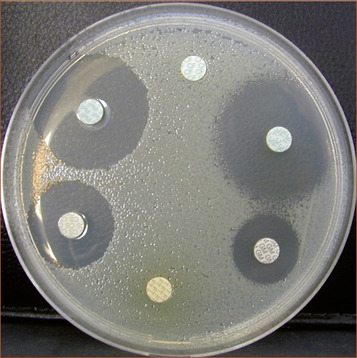
L’antibiogramme (figure 7.1) permet d’apprécier la sensibilité de la bactérie à l’antibiotique en mesurant l’inhibition que produit l’antibiotique sur une souche bactérienne. Deux méthodes sont possibles :
– la méthode turbidimétrique consiste à mesurer l’opacité d’une solution contenant le germe et l’antibiotique à tester. Plus l’activité de l’antibiotique sur le germe est importante, plus le trouble va diminuer ;
– la méthode de diffusion : sur un ensemencement de germes en boite de Pétri, sont disposés des disques renfermant chacun un antibiotique. L’antibiotique diffuse autour du disque avec un gradient de concentration et son activité sur le germe est évaluée par mesure du diamètre d’inhibition de croissance bactérienne autour du disque.
La CMI ou Concentration minimale inhibitrice est la plus faible concentration d’antibiotique capable d’inhiber la croissance du germe. Elle est parfois exprimée en CMI50, soit la concentration minimale capable d’inhiber 50 % de la croissance du germe étudié.
Ces deux paramètres permettent d’établir le spectre d’activité et de résistance d’un antibiotique.
Ainsi, pour tout antibiotique ou classe d’antibiotique, on déterminera les germes sensibles (S), inconstamment sensibles (IS), modérément sensibles (MS), résistants (R).
– efflux de la molécule hors de la bactérie ;
– destruction par une enzyme bactérienne (β-lactamases des staphylocoques ou des entérobactéries) ;
– modification de la cible d’action de l’antibiotique.
L’apparition de résistances acquises est généralement associée à une utilisation importante de l’antibiotique. Le caractère résistant peut se transmettre d’une bactérie à l’autre. Cette résistance des germes aux antibiotiques explique l’importance de l’antibiogramme qui permet de choisir le médicament le plus efficace pour un germe déterminé.
Modalités d’utilisation
ANTIBIOTHÉRAPIE CURATIVE (PROBABILISTE OU DOCUMENTÉE) OU ANTIBIOPROPHYLAXIE
L’antibiothérapie curative s’adresse à un patient déjà infecté.
L’antibiothérapie probabiliste (ou empirique) consiste à traiter d’emblée (après avoir effectué des prélèvements bactériologiques) un patient par un antibiotique choisi selon l’analyse de critères cliniques, qui tendent à démontrer que l’infection implique plus probablement une certaine espèce bactérienne, et qu’elle est sensible à cet antibiotique. Le deuxième critère de choix est pharmacologique en prenant en compte la capacité de l’antibiotique à diffuser dans les tissus infectés. Cette démarche est parfois suffisante. Elle est surtout utilisée dans les infections graves en attendant le résultat de la bactériologie.
Le prélèvement (ECBU [examen cytobactériologique des urines], hémoculture, ponction pleurale, par exemple) et la détermination des germes responsables de l’infection, ainsi que la détermination de leur sensibilité aux antibiotiques (par réalisation d’un antibiogramme) permettent ensuite de mettre en place une antibiothérapie curative documentée (mise en place après l’antibiothérapie probabiliste).
L’antibioprophylaxie consiste à administrer un antibiotique à un patient avant un geste chirurgical ou médical qui présente un haut risque d’infection locale ou générale. Elle précède ce geste et doit être de courte durée. Elle tient compte de la nature des germes susceptibles d’engendrer l’infection et du spectre d’action de l’antibiotique.
Gestion des ATB à coût élevé
Une IDE découvre une boite entièred’antibiotiques IV à coût élevé(Tazocilline 4g) qui était destiné exclusivement à un patient.
Le double de l’ordonnance nominative le confirme. Malheureusement, le patient, M. R. est décédé il y a 3 jours.Que doit-elle faire de ce stock d’antibiotiques ?
Si l’antibiotique a été délivré par la pharmacie sur ordonnance nominative, c’est que le service ne possède pas de dotation pour cet antibiotique, et donc que son utilisation est peu fréquente. Dans ce cas, l’IDE doit renvoyer à la pharmacie les unités restantes, en accompagnant son renvoi d’une fiche de retour, indiquant le nom du médicament, le dosage et le nombre d’unités retournées.
CHOIX DE LA VOIE D’ADMINISTRATION
– de la disponibilité des formes pharmaceutiques ;
– de la pharmacocinétique du médicament : certains médicaments ne sont pas résorbés par le tube digestif et devront donc forcément être administrés par voie parentérale (aminoside) ;
– de l’urgence (IV, IM [intramusculaire]) ;
– de la nature du site infectieux et de la gravité de l’infection (voie IV pour les infections de l’os, des méninges ou cardiovasculaires ; les infections cutanées, oculaires, vaginales se prêtent plus particulièrement à l’utilisation de forme d’administration locale : collyre, crème, pommade, etc.) ;
– de l’état du réseau veineux du patient ;
– de la possibilité d’emploi de la voie orale (difficile en cas de vomissements, de troubles de la conscience, etc.) ;
– des traitements associés (les antivitamines K [AVK] contre-indiquent la voie IM).
Administration d’ATB
Une IDE doit mettre en œuvre une prescription devancomycine 2gen IV continu pour un patient sédaté en service d’hématologie SI. Faire le calcul de dose, et de débit, définir les modalités d’administration, la durée de l’injection, les critères de surveillance.
Les spécialités de vancomycine disponibles se présentent sous forme de poudre pour solutions de perfusion en flacons de 1g, 500mg, 250mg, ou 125mg. Elles peuvent être reconstituées dans du sérum physiologique ou du sérum glucosé 5 %.
L’infirmière doit administrer 2g sur 24h. L’administration se fera au pousse-seringue électrique.
Elle reconstitue 2 flacons de 1g avec chacun 10mL de sérum physiologique, soit 20mL qui seront complétés dans la seringue avec 28mL de sérum physiologique. Le débit sera fixé à 48mL/24h = 2mL/h.
La perfusion se fera en fonction des voies déjà en place, soit en voie veineuse centrale (sur une voie dédiée à la vancomycine), soit en voie veineuse périphérique.
La perfusion de vancomycine est fréquemment douloureuse (au point d’injection), et peut entraîner des réactions d’hypersensibilité se manifestant soit par des signes cutanés (rougeurs) au point d’injection, soit plus rarement par des réactions allergiques générales (bouffées vasomotrices, choc).
De plus, la vancomycine présente de nombreuses incompatibilités physico-chimiques entraînant un risque de précipitation du médicament dans la voie d’injection.
De ce fait, l’infirmière doit surveiller :
– si l’administration se fait en voie veineuse centrale : la perméabilité du cathéter et les réactions générales du patient ;
– si l’administration se fait en voie veineuse périphérique : le point d’injection et l’état général du patient. En cas de réactions allergiques, elle doit immédiatement arrêter la perfusion et prévenir le médecin.
POSOLOGIE ET DURÉE DE TRAITEMENT
Certains antibiotiques dits « concentration-dépendants » (exemple : aminosides ou β-lactamines sur les germes G(+)) ont une efficacité dépendante de leurs concentrations plasmatiques). On recherche des pics de concentrations efficaces souvent obtenus par administration de doses fortes si la tolérance le permet et fractionnées dans la journée. La durée de traitement est généralement courte.
L’effet post-antibiotique correspond à une efficacité antibactérienne conservée après la disparition de l’antibiotique du sang (exemple : aminosides). Cette propriété permet de diminuer le nombre d’administrations de l’antibiotique dans une journée (jusqu’à 1 administration par jour).
D’autres antibiotiques, à action plus lente, ne nécessitent pas de concentration plasmatique élevée. Leur efficacité est dépendante de la durée de contact avec le germe : ils sont dits « temps-dépendants » (exemple : glycopeptides, macrolides ou tétracyclines). Dans ce dernier cas, l’efficacité est obtenue par maintien sur longue durée d’une concentration plasmatique efficace.
MONOTHÉRAPIE OU ASSOCIATION
La monothérapie possède de nombreuses indications (exemple : infections bronchopulmonaires acquises en ville, infections urinaires basses non compliquées, infections gonococciques non compliquées) en pratique de ville et à l’hôpital.
Lorsque l’infection possède un caractère de gravité, il est souvent utile d’avoir recours à une association. Elle permet d’élargir le spectre antibactérien (infection sévère, polymicrobienne), permet un effet synergique pour renforcer la bactéricidie (terrain fragile, germe résistant, site difficile d’accès), accélère la guérison, réduit la durée de traitement et prévient l’émergence de mutants résistants. Par exemple, l’administration d’une céphalosporine et d’un aminoside est une association très fréquente à l’hôpital pour le traitement des infections graves à bacille Gram négatif.
Mais ces associations sont susceptibles d’augmenter le coût et les effets secondaires, et peuvent aboutir à un échec par antagonisme d’action. Ainsi, il ne faut jamais associer une pénicilline et une tétracycline, car une pénicilline agit sur les germes en période de multiplication alors qu’une tétracycline ralentit cette multiplication.
Effets indésirables
La plupart des effets indésirables imputables aux antibiotiques sont rapidement réversibles à l’arrêt du traitement, sauf dans certains cas de toxicité irréversible, tels que l’ototoxicité avec les aminosides, ou les toxidermies bulleuses (syndromes de Stevens-Johnson et de Lyell) avec les sulfamides.
Les effets indésirables communs à une classe sont moins nombreux que ceux présentés spécifiquement par une molécule à l’intérieur d’une classe. Par exemple, le risque de rupture du tendon avec les fluoroquinolones est important pour la ciprofloxacine (Ciflox), alors qu’il est très faible pour la moxifloxacine.
De même, une réaction allergique urticarienne sous une β-lactamine impose la prescription d’une autre classe d’antibiotique, alors que le risque réel de réaction allergique avec une autre pénicilline ou céphalosporine n’est que de 10 %.
Les principaux effets indésirables des antibiotiques seront abordés dans la suite du chapitre, classe par classe.
Contre-indications sur des terrains particuliers
| Antibiotiques | Contre-indications absolues | Contre-indications relatives |
|---|---|---|
| β-lactamines | Hypersensibilité | Selon le cas : infections par les herpès virus (MNI : mononucléose infectieuse) |
| Aminosides | Hypersensibilité Myasthénie | Grossesse |
| Fluoroquinolones | Antécédents de tendinopathie (sportif, sujet âgé) Hypersensibilité Épilepsie Déficit en G6PD | Enfant jusqu’à la période de croissance (toxicité articulaire) Grossesse |
| Macrolides | Hypersensibilité | Allongement de l’espace QT Insuffisance hépatique sévère |
| Tétracyclines | Hypersensibilité Grossesse (6 derniers mois) : anomalies du bourgeon dentaire et dyschromie dentaire Enfants < 8 ans | Ulcérations de l’œsophage |
| Phénicolés | Hypersensibilité Antécédents d’insuffisance médullaire Insuffisance rénale sévère (clairance de la créatinine < 30mL/min) Nourrisson < 6 mois Nouveau-né < 1 mois Grossesse | |
| Sulfamides | Allaitement Déficit en G6PD Hypersensibilité Insuffisance hépatique sévère Nouveau-né < 1 mois Grossesse |
Surveillance d’une antibiothérapie
La surveillance d’un traitement antibiotique vise à vérifier son efficacité et sa tolérance.
L’efficacité doit être évaluée 48 à 72 heures après le début du traitement. D’un point de vue clinique, elle se juge par la disparition des symptômes initiaux et la baisse de la fièvre, et d’un point de vue biologique, par la normalisation des paramètres inflammatoires (C Reactive Protein [CRP] et vitesse de sédimentation [VS]) et infectieux (polynucléaires neutrophiles). Enfin, le succès bactériologique peut être évalué par la négativation des cultures sur des prélèvements réalisés au cours du traitement (efficacité) ou à distance de celui-ci (absence de rechute).
L’emploi des antibiotiques nécessite la surveillance de la survenue d’éventuels effets indésirables, tels que :
– les accidents immunologiques dont le plus grave est le choc anaphylactique avec les pénicillines. Un accident de ce type entraîne la contre-indication à l’utilisation de tous les antibiotiques de la famille ;
– les accidents rénaux avec les aminosides et tétracyclines. Le traitement pourra être accompagné d’une surveillance de la fonction rénale ;
– les désordres hématologiques avec les phénicolés. L’hémogramme sera surveillé ;
– la détérioration de l’audiogramme avec les aminosides (à surveiller) ;
Le suivi thérapeutique par dosage sanguin de certains antibiotiques potentiellement toxiques et dont l’efficacité et/ou la toxicité sont associées à leurs concentrations plasmatiques (aminosides, glycopeptides) aide à l’optimisation posologique du traitement.
Les grandes familles d’antibiotiques
Aminosides
GÉNÉRALITÉS
Les aminosides (tableau 7.2) inhibent la synthèse protéique des bactéries sensibles. Ils sont bactéricides sur de nombreux germes G(-) et certains G(+). Leur action est concentration-dépendante et leur index thérapeutique (écart entre les concentrations sanguines efficaces et les concentrations toxiques) étroit. Leur utilisation nécessite donc une surveillance des concentrations plasmatiques. Ils ne sont pas résorbés par le tube digestif et donc uniquement administrés par voie parentérale, sauf la néomycine qui est utilisée localement dans le traitement d’infections cutanées ou par voie orale pour stériliser les intestins avant une intervention chirurgicale. Ils sont éliminés par le rein.
| DCI | Nom de spécialités |
|---|---|
| Streptomycine | Streptomycine |
| Gentamicine | Gentamicine, Gentalline |
| Amikacine | Amiklin |
| Dibékacine | Débékacyl |
| Nétilmicine | Nétromicine |
| Isépamicine | Isépalline |
| Tobramycine | Nebcine |
| Spectinomycine | Trobicine |
PRINCIPALES INDICATIONS
La streptomycine est active sur Mycobacterium tuberculosis, mais du fait de sa forte toxicité, elle a été remplacée par la rifampicine dans le traitement de la tuberculose (voir « Antituberculeux »). Elle n’est utilisée qu’en dernière intention en cas de résistance aux associations d’antituberculeux classiques.
La gentamycine et l’amikacine sont utilisées dans le traitement empirique des infections hospitalières graves à germes G(-) (Pseudomonas aeruginosa), jusqu’à obtention de l’antibiogramme de l’infection. Leur action est synergique avec celle des β-lactamines et de la vancomycine, et les associations « aminoside+β-lactamine » ou « aminoside+vancomycine » élargissent le spectre d’action antibactérien et sont indiquées dans le traitement des infections sévères à germes G(-) ou certains G(+), par exemple pour le traitement empirique des méningites bactériennes chez l’adulte.
EFFETS INDÉSIRABLES
– néphrotoxicité (réversible à l’arrêt du traitement) : les aminosides ne doivent pas être associés à d’autres médicaments néphrotoxiques. Leur posologie doit être adaptée à la clairance de la créatinine, permettant d’évaluer la fonction rénale ;
– toxicité cochléovestibulaire : elle est cumulative et irréversible, et peut être responsable de troubles de l’équilibre et d’une diminution de l’audition irréversible ;
– accidents allergiques.
β-lactamines
GÉNÉRALITÉS
Cette famille englobe les pénicillines (tableau 7.3) et les céphalosporines (tableau 7.4). Elles possèdent en commun un même noyau β-lactame dont l’intégrité est essentielle à leur activité antibactérienne. Elles sont bactéricides et exercent leur activité en empêchant la synthèse de la paroi bactérienne.
| DCI | Nom de spécialités |
|---|---|
| Pénicilline G | |
| Benzylpenicilline | Extencilline |
| Pénicilline V | |
| Phénoxybenzylpénicilline | Oracilline |
| Pénicilline M | |
| Cloxacilline | Oracilline, Orbénine |
| Oxacilline | Bristopen |
| Pénicilline A | |
| Amoxicilline | Clamoxyl, Amodex |
| Amoxicilline + acide clavulanique | Augmentin |
| Ampicilline + sulbactam | Unacim |
| Carboxypénicillines | |
| Ticarcilline | Ticarpen |
| Ticarcilline + acide clavulanique | Claventin |
| Uréidopénicillines | |
| Pipéracilline + tazobactam | Tazocilline |
| DCI | Nom de spécialités |
|---|---|
| Céphalosporines lregénération | |
| Céfaclor | Alfatil |
| Céfadroxil | Oracéfal |
| Céfalexine | Kéforal |
| Céfradine | Zeefra |
| Céphalosporines 2egénération | |
| Céfuroxime | Cépazine, Zinnat |
| Céphalosporines de 3egénération (injectables) | |
| Céfépime | Axépim |
| Céfotaxime | Claforan |
| Cefpirome | Cefrom |
| Ceftazidime | Fortum |
| Ceftriaxone | Rocéphine |
| Céphalosporines de 3egénération (orales) | |
| Céfixime | Oroken |
| Céfotiam | Taketiam |
| Cefpodoxime | Orelox |
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree