12. Antalgiques
Un antalgique est un médicament qui a pour rôle de diminuer la douleur, alors que la définition d’un analgésique est la suppression de la sensibilité à la douleur. Derrière cette différence subtile, le terme antalgique est plus souvent réservé au paracétamol et à l’aspirine, alors que les analgésiques évoquent les morphiniques. Toutefois, cette différence est souvent négligée en pratique courante.
La douleur aiguë est un symptôme, qui a un rôle de « signal d’alarme » pour l’organisme ainsi informé d’une lésion tissulaire. Certaines douleurs qualifiées de chroniques, sont persistantes et ne jouent plus un rôle d’alarme pour l’organisme. Elles ont un fort retentissement psychologique et social pour le patient et sont souvent rebelles aux traitements antalgiques conventionnels.
Sur le plan physiopathologique on distingue trois types de douleurs :
– les douleurs par excès de nociception, souvent aiguës, conséquence d’une lésion tissulaire ;
– les douleurs neuropathiques (ou neurogènes), aiguës ou chroniques, et dues à une dysfonction ou à une lésion nerveuse, au niveau périphérique ou central ;
– les douleurs psychogènes, qui pourraient être dues à un abaissement du seuil de perception de la douleur ou à des troubles psychoaffectifs.
Mécanismes de la douleur
La transmission du message douloureux fait intervenir de très nombreux médiateurs, aux niveaux périphérique et central (corne postérieure de la moelle épinière notamment). Schématiquement, trois étapes se succèdent (figure 12.1) :
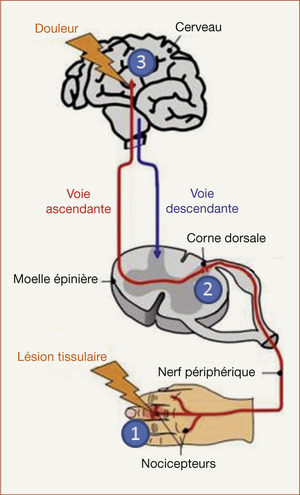 |
| Fig. 12.1 |
– l’infl ux nociceptif est élaboré au niveau de terminaisons nerveuses présentes dans la peau et les viscères, appelées nocicepteurs, avant d’être transmis par les fibres nerveuses périphériques. Il existe plusieurs types de nocicepteurs :
• les mécanorécepteurs, sensibles à la pression et à l’étirement. Ils sont prolongés par des fibres Aδ myélinisées et permettent une conduction rapide et précise du signal,
• les récepteurs polymodaux, sensibles à la chaleur ainsi qu’à des stimuli mécaniques ou chimiques. Ils sont prolongés par des fibres C non myélinisées, dont la conduction est lente et peu précise (douleur diffuse) ;
– l’influx est ensuite modulé au niveau de la corne dorsale de la moelle épinière ;
– enfin le message est intégré au niveau du cerveau pour devenir conscient.
Les antalgiques vont agir à différents niveaux de la transmission du message nociceptif.
Classification des antalgiques
Il existe plusieurs classifications des antalgiques. La plus répandue est la classification de l’OMS. La distinction des antalgiques selon leur site d’action (périphérique ou central), bien que peu appropriée, est toujours utilisée (tableau 12.1).
| *À la suite de la procédure européenne de réévaluation du rapport bénéfice/risque de tous les médicaments contenant du dextropropoxyphène, la Commission européenne a demandé en juin 2010 le retrait dans l’Union européenne des autorisations de mise sur le marché de toutes les spécialités contenant du dextropropoxyphène dans un délai maximum de 15 mois. | |||
| Palier | I | II | III |
|---|---|---|---|
| Douleur | Faible à modérée | Modérée/sévère | Sévère |
| Antalgiques centraux | Paracétamol Néfopam (Acupan) | Agonistes partiels Codéine Tramadol Dextropropoxyphène* | Agonistes entiers Morphine Fentanyl Sufentanil, alfentanil, rémifentanil Agonistes partiels Hydromorphone Oxycodone Agonistes/antagonistes Buprénorphine Nalbuphine |
| Antalgiques périphériques | Aspirine AINS | ||
Classification de l’OMS
Cette classification repose sur l’intensité de la douleur à traiter, et distingue trois paliers :
– les antalgiques de palier I sont indiqués pour les douleurs d’intensité faible à modérée, et sont des antalgiques non opioïdes ;
– les antalgiques de palier II sont les traitements des douleurs d’intensité modérée à sévère. Ils appartiennent aux opioïdes faibles, utilisés seuls ou en association à des antalgiques de palier I (paracétamol notamment) ;
– enfin les antalgiques de palier III sont les opioïdes forts, indiqués dans les douleurs très sévères. On retrouve dans ce groupe la morphine, principal alcaloïde extrait d’une espèce de pavot, Papaver somniferum. La morphine sert de base à l’élaboration des autres analgésiques opioïdes qui ont des structures très proches.
REMARQUE
On qualifie d’opioïdes les molécules qui se fixent aux récepteurs aux opioïdes ; ce terme englobe donc les substances produites par l’organisme (= substances endogènes) qui agissent sur ces récepteurs. Les termes « opiacé » (qui vient d’opium) ou « morphinique » font quant à eux référence aux molécules synthétisées à partir de la morphine, et non aux molécules endogènes.
Coantalgiques (ou coanalgésiques)
On retrouve notamment des antidépresseurs (amitriptyline, clomipramine, duloxétine, imipramine) et certains antiépileptiques (carbamazépine, gabapentine, prégabaline, clonazépam).
Antalgiques centraux et périphériques
Cette classification historique est toujours utilisée dans le langage courant, bien qu’elle semble aujourd’hui peu appropriée. En effet certains antalgiques que l’on croyait agir au niveau périphérique agissent plutôt au niveau central (c’est le cas du paracétamol, dont le mode d’action reste encore mal connu), alors que les opiacés, classiquement qualifiés d’« analgésiques centraux » ont également un effet périphérique, lié à la présence de récepteurs aux opioïdes au niveau périphérique.
Mécanisme d’action et effets pharmacologiques
Analgésiques opioïdes
MÉCANISME D’ACTION
Pour atténuer le message douloureux, l’organisme synthétise différents peptides : les endorphines, les enképhalines et les dynorphines. Ces peptides se fixent sur des récepteurs couplés à la protéine G appelés récepteurs aux opioïdes.
Ces récepteurs sont présents au niveau périphérique et central, et on les retrouve en forte concentration au niveau de la corne dorsale de la moelle épinière.
Il existe trois grands sous-types de récepteurs aux opioïdes : les récepteurs μ (mu), les récepteurs δ (delta) et les récepteurs К (kappa). Ils diffèrent par la nature de leurs agonistes endogènes et sont à l’origine d’effets biologiques différents.
Les analgésiques opioïdes vont jouer le rôle d’agonistes pour ces récepteurs, ce qui va entraîner une modification de la transmission et de l’influx nociceptif, à l’origine de l’effet antalgique.
EFFETS PHARMACOLOGIQUES
– analgésie : c’est le principal effet des morphiniques en thérapeutique ; il est dû en grande partie à leur effet agoniste sur les récepteurs mu ;
– dépression respiratoire : également due à l’effet agoniste sur les récepteurs mu, c’est un effet indésirable redouté des morphiniques ; cet effet secondaire n’a pas de conséquence clinique aux doses thérapeutiques ;
– tolérance : lors d’administrations répétées, on observe une diminution de l’efficacité, qui nécessite d’augmenter les doses pour obtenir un effet comparable à l’effet initial ;
– dépendance : elle se définit par l’apparition d’un syndrome de sevrage à l’arrêt du traitement ou en présence d’un antagoniste ; cet effet secondaire n’a pas de conséquence clinique aux doses thérapeutiques ;
– sédation ;
– euphorie, dysphorie, hallucinations ;
– effets digestifs :
• constipation, due à une diminution de la motilité intestinale liée à la présence de récepteurs aux opioïdes en concentration importante au niveau intestinal. Les opiacés ne sont plus employés dans cette indication mais un analogue structural, le lopéramide (Imodium) est un antidiarrhéique couramment utilisé,
• nausées et vomissements ;
– effet antitussif : particulièrement marqué pour la codéine. Toutefois son usage est de moins en moins fréquent dans cette indication à cause d’un risque de détournement à des fins illicites.
MÉDICAMENTS ET INDICATIONS
La grande majorité des opioïdes sont utilisés comme antalgiques.
Les liaisons des opiacés aux différents types de récepteurs expliquent leurs indications. La morphine est un puissant agoniste des récepteurs μ, elle a donc un effet analgésique fort (palier III) mais va également induire une dépression respiratoire ainsi que des phénomènes de tolérance et dépendance. Le fentanyl, très utilisé en thérapeutique, ainsi que ses dérivés, ont des propriétés semblables mais diffèrent par leur puissance antalgique. Le fentanyl est environ 100 fois, et le sufentanil 500 fois plus puissant que la morphine.
La buprénorphine est un agoniste partiel des récepteurs μ et antagoniste des récepteurs К. Pour cette raison, on la qualifie parfois d’agoniste/antagoniste. Elle est utilisée comme antalgique (Temgésic) mais aussi dans le traitement de substitution aux opiacés (Subutex).
La nalbuphine est un autre agoniste/antagoniste, mais agoniste pour les récepteurs К et antagoniste pour les récepteurs μ. Ce profil permet théoriquement d’obtenir un effet analgésique sans effet dépresseur respiratoire. Toutefois, même s’il est moins fréquent qu’avec la morphine, l’effet dépresseur respiratoire de la nalbuphine est réel, notamment à forte dose.
D’autres indications existent :
– anesthésie essentiellement pour le sufentanil et le rémifentanil. L’alfentanil est réservé à l’anesthésie ;
– toux pour la codéine ;
– traitement de substitution aux opiacés pour la méthadone et la buprénorphine.
Paracétamol
MÉCANISME D’ACTION
Bien que le paracétamol soit un médicament ancien et très couramment utilisé, son mode d’action n’est toujours pas parfaitement connu. L’effet du paracétamol est historiquement attribué à la seule inhibition des cycloxygénases, ce qui est aujourd’hui controversé. Les autres hypothèses sont une action sérotoninergique centrale, possiblement liée à l’activation par le paracétamol de récepteurs aux endocannabinoïdes.
EFFETS PHARMACOLOGIQUES
Le paracétamol a deux effets :
– un effet antalgique ;
– un effet antipyrétique.
MEDICAMENTS ET INDICATIONS
Notons enfin que le paracétamol est fréquemment associé aux antalgiques de palier II (voir tableau 12.3).
Aspirine et anti-inflammatoires non stéroïdiens
L’aspirine et certains AINS tels que l’ibuprofène sont couramment utilisés comme antalgiques de palier I. Outre leurs propriétés antalgiques, ces médicaments sont antipyrétiques et anti-inflammatoires à dose plus élevée. Voir chapitre 12 «Anti-inflammatoires ».
Néfopam
Le néfopam (Acupan) est un antalgique non opioïde d’action centrale, réservé au traitement des douleurs aiguës. Il est administré par voie IV ou IM (l’administration per os sur un sucre est hors AMM). Ses principaux effets indésirables sont des effets anticholinergiques (bouche sèche, tachycardie, rétention urinaire).
Prise en charge de la douleur
La douleur est un motif de consultation médicale très fréquent. La législation rend obligatoire la prise en charge de la douleur, qui a deux objectifs :
– le premier est de diminuer l’intensité de la douleur à un niveau supportable pour améliorer la qualité de vie du patient, réduire les répercussions psychologiques et favoriser la réinsertion ;
– le second objectif est de prévenir le passage à la chronicité.
La prise en charge dépend étroitement du type de douleur. Ainsi les douleurs par excès de nociception seront traitées en premier lieu par des antalgiques, alors que les douleurs neuropathiques seront traitées par certains antiépileptiques ou antidépresseurs. Enfin la psychothérapie est l’axe de traitement principal des douleurs psychogènes.
Lorsque la cause de la douleur est identifiée, un traitement étiologique doit accompagner le traitement symptomatique quand c’est possible.
Le personnel infirmier est habilité à entreprendre et adapter les traitements antalgiques dans le cadre de protocoles définis, après prescription médicale de ces protocoles. L’infirmier doit donc pouvoir évaluer l’efficacité et la toxicité des traitements.
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree


