7. Anesthésiques Généraux
A dose normale, ils ne touchent pas le fonctionnement du diaphragme. Ils provoquent une insensibilisation générale et une paralysie réversible ainsi que la perte de conscience. Ils induisent le « sommeil anesthésique ». On les considère comme des anesthésiques centraux, agissant sur le système nerveux central, par opposition aux anesthésiques locaux, actifs à la périphérie. Les anesthésiques généraux sont des gaz, des liquides volatils administrés par voie pulmonaire ou des solutions injectées par voie intraveineuse.
Qualités d’un bon anesthésique général
L’anesthésique général doit présenter 1) un coefficient thérapeutique élevé; 2) une induction rapide de l’anesthésie, sans excitation; 3) un réveil rapide, avec un effet analgésique prolongé; 4) une insensibilisation et un relâchement musculaire complets; 5) l’absence d’effets secondaires immédiats (accidents cardio-vasculaires et respiratoires), postanesthésiques (vomissements, nausées), tardifs (lésions hépatiques, rénales, cardiaques). Les anesthésiques volatils ou gazeux doivent être ininflammables, non explosifs, actifs à concentration faible pour éviter l’hypoxie, non décomposables par la chaux sodée. Les anesthésiques par voie intraveineuse ne doivent pas être irritants pour l’endothélium vasculaire.
Stades de l’anesthésie
L’anesthésie s’installe en plusieurs stades plus ou moins distincts: un stade d’analgésie, un stade d’excitation par inhibition des centres corticaux avec perte de la conscience, un stade chirurgical, caractérisé par une résolution musculaire et la perte des réflexes oculo-palpébral d’abord et pupillaire ensuite. Au-delà du stade chirurgical la poursuite de l’administration de l’anesthésique amène à un stade toxique: le bulbe est atteint, le patient est en apnée, il se cyanose, le pouls devient filant.
Retour à l’état de veille
Dès que cesse l’administration de l’anesthésique, les fonctions réapparaissent dans l’ordre inverse de leur disparition: réflexe pupillaire, réflexe oculopalpébral, tonus musculaire, abdominal, réflexe peaucier, etc.
Accidents et incidents de l’anesthésie
Les accidents et incidents sont immédiats ou retardés et portent sur les fonctions respiratoire, cardiaque, vasculaire, digestive. Les accidents respiratoires comprennent l’apnée, les spasmes laryngés ou pharyngés, l’hypersécrétion bronchique et l’atélectasie (collapsus des alvéoles).
Les accidents cardiaques peuvent être dus:
– à une stimulation des fosses nasales (nerf trijumeau), du larynx (nerf laryngé supérieur, branche du nerf pneumogastrique) qui entraîne une inhibition du centre bulbaire: c’est la syncope laryngoréflexe;
– à une fibrillation ventriculaire, observée avec les anesthésiques volatils halogénés: elle est dite syncope adrénalino-chloroformique.
De plus des arythmies, des extrasystoles, des rythmes nodaux et de la tachycardie peuvent être observés.
Les incidents vasculaires consistent en hypotension (barbituriques), hypertension (par excès de gaz carbonique), choc, avec fuite plasmatique, hémoconcentration, hypotension.
Les incidents digestifs, rares, procèdent de vomissements qui peuvent obstruer les voies respiratoires. Après l’anesthésie, le patient peut présenter des atteintes des bronches, des ictères, de l’albuminurie, des incidents cardiaques. Avec les progrès de la réanimation ces incidents sont rares.
Pharmacocinétique des anesthésiques généraux
Les anesthésiques gazeux ou volatils pénètrent dans les poumons, puis le sang pour atteindre le cerveau. La pénétration dans les poumons est fonction de la concentration dans l’air inspiré et de la ventilation pulmonaire. Le passage à partir des poumons vers le sang dépend de la concentration sanguine, de la perméabilité de la paroi alvéolaire, du débit circulatoire, de la solubilité de l’anesthésique dans le sang. On définit une concentration alvéolaire minimale (CAM), anesthésique chez 50% des patients, variable selon l’âge. Les anesthésiques injectés par voie intraveineuse comme les anesthésiques administrés par voie pulmonaire traversent la barrière hématoencéphalique, diffusent rapidement dans les cellules nerveuses Leur pénétration dépend de leur coefficient de partage cerveau/sang: halothane-2,6; méthoxyflurane-2,3; éther-1,1.
Les anesthésiques gazeux sont éliminés par les poumons après arrêt de l’anesthésie et hyperventilation. Les anesthésiques volatils peuvent s’accumuler transitoirement dans les graisses puis être éliminés soit par voie pulmonaire, soit par voie urinaire après transformation métabolique par les enzymes qui les rendent hydrophiles. Les anesthésiques par voie intraveineuse sont éliminés par le rein et subissent l’action des enzymes de dégradation. Par répétition des doses d’anesthésique on prolonge l’effet anesthésique et on maîtrise moins bien le processus d’élimination. La figure 7.1 montre l’évolution pharmacocinétique d’un anesthésique gazeux.
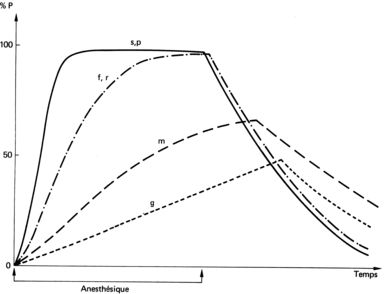 |
| Fig. 7.1 Pharmacocinétique d’un anesthésique gazeux comme le protoxyde d’azote.s, p : sang, poumons ; f, r : foie, reins ; m : muscles ; g : graisses ; P : pression partielle maximale d’anesthésique. |
Théories de l’action anesthésique
Plusieurs théories ont été proposées. Aucune n’est entièrement satisfaisante. Chacune semble présenter une part de vérité. On peut distinguer les théories physiques, biochimiques, neurophysiologiques. Parmi les théories physiques, citons la vieille théorie de Meyer et Overton (1899) selon laquelle il y aurait une relation entre la liposolubilité et l’action narcotique. Selon Traube (1904) l’action narcotique est reliée à la tensioactivité des anesthésiques qui ont tendance à se placer à l’interface eau-lipides entraînant une modification des constantes diélectriques. Cette théorie a été reprise récemment car sur des membranes artificielles de phospholipides on a observé une modification de la résonance paramagnétique électronique (RPE) sous l’influence des anesthésiques gazeux ou volatils. Les théories biochimiques font intervenir une modification des processus d’oxydoréduction cellulaire, ce qui est vrai, et de découplage de la phosphorylation oxydative. Les théories neurophysiologiques attribuent l’action anesthésique à une rupture de la conduction de l’influx nerveux de la périphérie vers la formation réticulée du mésencéphale.
Sont inhibés les récepteurs des acides aminés activateurs, glutamate et aspartate. On distingue les récepteurs canaux-ioniques NMDA (N méthyl-Daspartate), AMPA (aminométhylisoxalone propionate), kaïnate et les récepteurs métabotropiques Glu1 à Glu5 couplés à des protéines G.
L’inhibition des canaux ioniques membranaires entraîne la sédation par hyperpolarisation de la membrane neuronale.
On constate une facilitation de la transmission gaba-ergique par les barbituriques et le propofol.
ANESTHÉSIE PAR INHALATION
Protoxyde d’azote N2O
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree


