Luxations et subluxations des prothèses totales de hanche
Dislocation and subluxation after total hip replacement
Généralités
Anatomie de la hanche prothésée
• les muscles périarticulaires, peu utilisés en attendant l’intervention et souvent affaiblis chez les sujets âgés, peuvent être fragilisés par certaines pathologies (arthrite rhumatoïde), et par d’éventuelles interventions antérieures ;
• les abords qui détachent et/ou traversent les muscles périarticulaires supposent qu’ils cicatrisent et récupèrent leur force pour assurer la stabilité. Ceux qui détachent tout ou partie du grand trochanter nécessitent une consolidation osseuse. Tous fragilisent la capsule articulaire ;
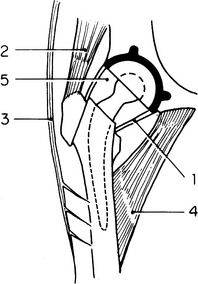
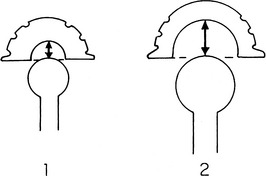
• il existe autour de la tête prothétique un espace mort plus ou moins grand. Il a la forme d’un tronc de cône à sommet fémoral et à base cotyloïdienne, et c’est autour de la tête que les parties molles sont le plus à distance de la pièce fémorale et le moins à même de la contenir dans la cupule. Cet espace est d’autant plus grand que le diamètre de la cupule est plus grand et celui de la tête plus petit (figure 1).
Fréquence
Il est difficile d’apprécier la fréquence des luxations qui varie de 0,16 % [88] à 9,5 % [140] dans les séries de prothèses de première intention. La dispersion est moins grande si l’on considère les plus grandes séries : 0,6 % pour 14 672 prothèses à Wrightington [22], 3,2 % pour 10 500 prothèses à la Mayo Clinic [147], 1,7 % pour 4833 prothèses à Cochin [6], 3,8 % pour 4300 prothèses dans la série de Picault [118].
Dans plusieurs méta-analyses, ce taux avoisine 2 % : 1,9 % pour 60 séries (115 008 prothèses) [81], 1,97 % pour 19 séries (15 381 prothèses) [44], 2 % pour 52 séries (105 171 prothèses) [75], 2,25 % pour 16 séries (3894 prothèses) [103].
Il est plus élevé (3,9 %) dans une enquête nationale américaine récente sur la fréquence de trois complications de 58 521 arthroplasties totales de hanche au cours des 6 premiers mois [120].
Il est probablement sous-estimé dans bien des séries pour plusieurs raisons :
• le devenir de tous les patients n’est pas connu et il existe des luxations parmi les perdus de vue [81] ;
• le taux de luxation augmente avec le recul et celui de nombreuses séries est insuffisant. Plusieurs séries ont ainsi rapporté une proportion importante de luxations secondaires et tardives : 22 % au-delà de 1 an pour Hedlundh et al. [71], 26 % pour Callaghan et al. au-delà de 2 ans [16] et 32 % de luxations au-delà de 5 ans pour Von Knoch et al. [143] ;
• les subluxations ne sont pas incluses, fautes d’être signalées ou reconnues, car elles ne se traduisent que par un ressaut ou un claquement qui n’est pas toujours rapporté à son origine. Leur fréquence serait de 5,5 % pour Ritter [121] et 2 % pour Eftekahr [44].
Diagnostic
Luxations
Il est possible qu’une luxation très précoce passe inaperçue quelque temps [47,138], surtout chez un malade qui n’a pas encore repris l’appui, mais cette éventualité est rare. Le plus souvent, le diagnostic de luxation ne fait aucun doute pour le patient et son entourage. Il s’agit en effet d’un accident aigu. L’inégalité de longueur et l’attitude vicieuse (rotation interne et/ou flexion dans les luxations postérieures, rotation externe dans les luxations antérieures) ne sont pas constantes.
Il faut faire préciser la position du membre inférieur immédiatement avant la luxation : mouvement de flexion évocateur d’une luxation postérieure ou au contraire mouvement d’extension et/ou rotation externe évocateur d’une luxation antérieure. À ces mouvements peut s’associer une adduction. Le mouvement luxant, cependant, ne peut pas toujours être précisé (jusque dans 26 % des cas pour Courtois et al. [31]).
Ailleurs, on retrouve un traumatisme vrai, surtout dans les luxations secondaires chez des patients ayant repris leurs activités, jusque-là indemnes de toute luxation [77,99].
Il faut mettre à part les luxations postopératoires immédiates qui surviennent en salle d’opération, chez des patients encore sous anesthésie, lors de changements de position non contrôlés [31,77]. On peut en rapprocher certaines luxations survenues au cours d’anesthésies pratiquées pour d’autres interventions [147].
La radiographie ne fait donc que confirmer le diagnostic de luxation dans la grande majorité des cas. Un profil, qui fait malheureusement défaut dans bien des cas, est indispensable pour préciser la position postérieure ou antérieure de la tête prothétique. Cependant, la direction de la luxation ne peut pas toujours être précisée et certains [147] individualisent ainsi des luxations supérieures qu’il est tentant d’expliquer par un mouvement d’adduction. En fait, on ne peut affirmer que la tête a quitté la cupule à sa partie haute. Elle peut s’être luxée en arrière ou en avant et ensuite déplacée en haut [44]. Le terme de luxation supérieure recouvre ainsi des luxations dont la direction n’a pu être précisée. Dans cette éventualité, l’examen sous anesthésie est essentiel. Une fois la luxation réduite, l’opérateur la reproduira ou plutôt l’ébauchera prudemment, de manière à préciser le mouvement luxant et en même temps, la direction de l’instabilité. La direction de l’instabilité est ainsi ignorée près d’une fois sur cinq : 18 % pour Woo et Morrey [147], 23 % pour Amstutz et Kody [4].
On parle de luxation récidivante à partir du deuxième épisode.
Subluxations
La tête se subluxe sur le rebord de la cupule mais se réduit rapidement, ce que le patient perçoit comme un ressaut parfois audible. La réduction peut être plus tardive, avec une sensation de blocage qui cède brusquement lors de la réduction. Ces épisodes sont souvent suivis d’une douleur pendant plusieurs jours. On ne peut pas être certain du diagnostic et faute d’attention, un certain nombre de subluxations sont méconnues par les patients et leurs chirurgiens. Il est donc difficile d’apprécier leur fréquence, qui va de 2 % [44] à 5,5 % [121].
Il est logique de penser que des subluxations répétées déforment progressivement la cupule, autorisant tôt ou tard une luxation et certains ont effectivement retrouvé des antécédents de subluxations chez des patients présentant des luxations tardives [143]. Néanmoins, il est difficile de savoir combien évoluent vers des luxations vraies. Des subluxations méconnues permettent sans doute d’expliquer certains éculements arrondis du rebord de la cavité de la cupule constatés lors de reprises pour descellement.
Direction
La plupart des luxations sont postérieures, ce qui s’explique par l’utilisation prédominante de la hanche en flexion, adduction et rotation interne : 61 % [147], 78 % [33], jusqu’à 100 % [93].
La direction de l’instabilité dépend également de la voie d’abord. La tête se luxe plus facilement du côté où les parties molles ont été fragilisées. Woo et Morrey [147] ont ainsi observé après abord postérieur 77 % de luxations postérieures, 3 % de luxations antérieures et 20 % de luxations supérieures alors qu’après abord antérieur, ces taux étaient respectivement de 46 %, 46 % et 8 %. Dans les séries où la voie postérieure a été utilisée exclusivement ou presque, les luxations postérieures sont largement prédominantes et avoisinent parfois 100 % [47, 93, 137].
Dans certaines séries cependant, la direction des luxations est paradoxale, ce qui s’explique probablement par des malpositions. Dans la série de Fontes et al. [50], où la voie postérieure a été la plus utilisée, le taux de luxation antérieure, attribuée à un excès d’antéversion de la cupule, était de 25 %. Dans celle de Dorr et al. [40], les abords postérieurs se sont compliqués de luxations antérieures et les abords antérolatéraux de luxations postérieures. Les opérateurs, craignant des luxations du côté de l’abord, ont trop orienté les pièces vers le côté opposé.
La voie transtrochantérienne respecte les muscles antérieurs et postérieurs. Dans la série de Woo et Morrey [147], les taux de luxation postérieure et antérieure des abords transtrochantériens étaient intermédiaires à ceux des abords postérieur et antérieur : 54 % et 19 % respectivement, avec 27 % de luxations supérieures. En revanche, dans la série de Cochin [6], où la voie transtrochantérienne a été la plus utilisée, les luxations étaient « le plus souvent postérieures » et dans celle d’Eftekahr, où cet abord a été exclusif, la quasi-totalité des luxations étaient postérieures [44]. Ceci pourrait s’expliquer par un défaut d’antéversion de la cupule.
Les luxations multidirectionnelles sont rares. Elles ont été décrites chez les patients ayant un long passé d’instabilité prothétique et/ou présentant d’importantes altérations des parties molles et de l’appareil d’abduction [5, 90].
Date de la première luxation
Les luxations précoces sont les plus fréquentes : 53 % pour André et al. [4], 59 % pour Woo et Morrey [147], 70 % pour Amstutz et Kody [4], 76 % pour Courtois et al. [31], 66 % pour Khan et al. [77], 70 % pour Williams et al. [145]. Elles peuvent s’expliquer par un défaut de cicatrisation des parties molles, l’hypotonie musculaire, la perte de la proprioceptivité [154], et éventuellement la présence d’un hématome profond [121], ce qui laisse espérer une guérison sans réintervention. Elles surviennent avant 1 ou 3 mois selon les auteurs. Ce délai devrait logiquement être celui de la cicatrisation des parties molles et de la consolidation d’une trochantérotomie, et correspondre à la date de reprise des activités courantes. Il est de l’ordre de 2 mois. Tous ne partagent pas cet avis, notamment Amstutz et Kody [4] qui considèrent que la cicatrisation des parties molles se poursuit jusqu’à la fin de la 1re année.
Les luxations secondaires surviennent alors que le patient a repris ses activités. Des mouvements de plus grande amplitude, autorisés par la récupération de la mobilité [6], voire de véritables traumatismes [77, 97] sont nécessaires. Elles sont souvent accessibles au traitement conservateur. Leur fréquence a été moins étudiée. Pour André et al. [6], il existe après le premier pic des luxations précoces un deuxième pic de fréquence au 6e mois, expliqué par la récupération de la mobilité à cette date. La série de Woo et Morrey [147] comporte également un taux de luxation secondaire élevé (18 % de 3 mois à 1 an et 17 % de 1 à 5 ans). Plus récemment, Hedlundh et al. [71] ont rapporté 22 % de luxations au-delà de 1 an et Callaghan et al. plus de 26 % au-delà de 2 ans [16].
Les luxations tardives constituent une entité particulière individualisée par Coventry chez des patients qui avaient présenté une première luxation (d’une prothèse de Charnley) au-delà de 5 ans [33]. Elles s’expliquent avant tout par une usure du polyéthylène (PE), ce qui explique ce délai. Elles ne sont guère accessibles qu’à un traitement chirurgical. Elles semblaient très rares dans les anciennes séries où elles avaient été peu étudiées (0,4 % pour Coventry et al. [33], 1,1 % pour Courtois et al. [31], 6 % pour Woo et Morrey [147]). Leur fréquence atteint 32 % dans la récente série de Von Knoch et al. [143]. Les luxations tardives étant souvent le fait d’une usure de la cupule, on peut expliquer cette augmentation par la plus grande activité des opérés et le vieillissement de la population.
Conséquences des luxations
Parties molles
C’est dans la période postopératoire précoce que ces lésions sont les plus graves. Une luxation sous anticoagulants expose à l’hématome, éventuellement compressif. Les sutures récentes des parties molles sont menacées de rupture. Une luxation postérieure peut compromettre la réparation capsulomusculaire d’une voie postéroexterne et peut au pire léser le nerf sciatique [47]. Elle favorise la formation d’une poche de décollement des parties molles en arrière du cotyle, point d’appel de nouvelles luxations. Une luxation antérieure peut compromettre la réparation capsulomusculaire d’une voie transglutéale. Les réinterventions précoces pour irréductibilité offrent la possibilité de réparer ces lésions, ce qui explique peut-être un plus faible taux de récidive qu’après réduction orthopédique [31,47]. Au fur et à mesure que les luxations se répètent, la capsule périprothétique se distend [51] et les espaces de décollement périprothétiques s’organisent.
Ces lésions des parties molles sont une cause d’instabilité qui s’ajoute à celles qui ont engendré la première luxation ; elles augmentent donc le risque de récidive (élevé après un abord postérieur où le plan capsulomusculaire fragilisé est très sollicité). Elles expliquent probablement les moins bonnes performances (vitesse de marche, durée de l’appui monopode) ou au moins la récupération plus lente des patients ayant présenté plusieurs luxations [19]. Elles se compliquent parfois d’ossifications [8, 47], qui peuvent avoir un effet bénéfique sur la stabilité prothétique mais peuvent aussi favoriser de nouvelles luxations par le biais d’un effet came.
Pièces prothétiques
La répétition des subluxations ou luxations entraîne un éculement du rebord de la cavité de la cupule, qui facilite de nouvelles échappées de la tête fémorale [153]. Cette déformation, que l’on constate au cours de reprises pour instabilité, n’a pu être reproduite expérimentalement par Nicholas [109] qui n’a observé, après 18 luxations, que des modifications minimes du rebord de la cupule et aucune modification du moment de forces nécessaire pour luxer la prothèse.
Les pièces prothétiques peuvent encore être altérées par le biais de certaines complications particulières : interposition de fragments de ciment [6,138], de vis ou cerclages rompus, avec usure à trois composants, dissociation tête-col ou insert-cupule de prothèses modulaires, qui oblige à une réintervention [9, 78,116,148], voire mobilisation d’une pièce fémorale sans ciment [52].
Mécanisme
Effets cames
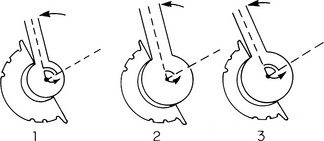
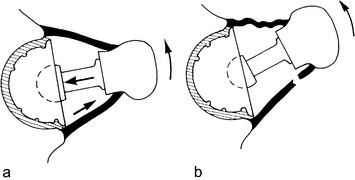
Le contact col-cupule est la principale cause de luxation par effet came. La mobilité prothétique est limitée par le contact entre le col fémoral et le rebord cotyloïdien, et la poursuite du mouvement au-delà de ce contact expose à la luxation (figures 2 et 3).
• le dessin prothétique qui détermine l’amplitude du débattement prothétique, c’est-à-dire l’évasement du cône de mobilité prothétique ;
• l’orientation des pièces prothétiques et la position du pelvis qui déterminent la position du cône de mobilité prothétique dans l’espace.
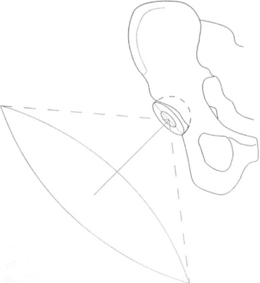
Les contacts col-cupule surviennent chaque fois que le conoïde de mobilité de la hanche déborde le cône de mobilité prothétique. Ces contacts risquent d’autant plus d’entraîner une luxation que la tête est plus petite, que la capsule est plus à distance de la tête prothétique et que le plan capsulomusculaire situé du côté opposé au contact est fragilisé, car il ne peut s’opposer à la poursuite du mouvement luxant (figures 4 et 5).
Il est donc logique de penser que la récupération d’une importante mobilité, notamment en flexion et rotation interne, favorise l’instabilité prothétique [6, 33, 34, 63, 103, 147], et ce d’autant plus que cette récupération est rapide, car les parties molles n’ont pas encore cicatrisé.
D’autres contacts peuvent entraîner une luxation par effet came :
• entre le col et des ostéophytes ou fragments de ciment qui débordent la cupule ;
• entre le col et des parties molles antérieures hypertrophiques ou ossifiées en rotation interne ;
• entre la métaphyse fémorale et le bassin, lorsqu’une médialisation du fémur la rapproche trop de la branche iliopubienne en rotation interne, ou de l’ischion en rotation externe. L’effet came peut être dû soit à un contact osseux, soit à la compression des parties molles entre la métaphyse fémorale et le pelvis (défaut de clairance entre le fémur et le bassin). Un déplacement antérieur d’un grand trochanter détaché par ostéotomie, une hypertrophie ou des ossifications de la partie antérieure du grand trochanter peuvent avoir le même effet en rotation interne entre les parties molles des deux cuisses en adduction.
Décoaptation
La fragilisation de la capsule, l’épanchement intra-articulaire, l’hypotonie voire la détente musculaire (en cas d’accourcissement ou de médialisation fémorale) favorisent la décoaptation des pièces prothétiques (figures 6 et 7).
Figure 7 Décoaptation sous l’effet de la pesanteur (hanche paralytique).
(Reproduite d’après D. Huten, Conférences d’enseignement 1996, Cahiers d’enseignement de la SOFCOT n° 55. Paris : Expansion Scientifique Française ; 1996. p. 24).
Elle se manifeste en position verticale par une subluxation inférieure de la tête prothétique sous l’effet de la pesanteur. Celle-ci peut expliquer un déclic lors de la phase oscillante du pas, surtout en terrain pentu ou dans les escaliers [112, 154], ou un ressaut de subluxation postérieure en position assise [49].
Une telle subluxation de la tête prothétique peut être suivie de luxation si un mouvement de rotation et/ou de flexion-extension se produit avant qu’elle n’ait regagné sa place dans le cotyle [154]. Ces mouvements se produisent surtout lors des changements de position ou de direction.
Les causes de faiblesse et de détente musculaire sont nombreuses. La faiblesse peut être due au vieillissement, à la non-utilisation pendant la période préopératoire [40, 47, 49], à l’étiologie (arthrite rhumatoïde) et au traumatisme opératoire [50, 154], surtout s’il est répété. La détente musculaire est le fait d’un défaut de reconstruction articulaire. La médialisation et l’ascension du grand trochanter dues à une résection fémorale excessive ou à une pseudarthrose trochantérienne lâche sont une cause évidente.
Il en est de moins connues qui détendent les muscles stabilisateurs :
• l’ascension du cotyle : souvent associée à une médialisation, elle entraîne une ascension et une médialisation du grand trochanter et détend donc les fessiers si elle n’est pas compensée par un allongement du col fémoral [61,125,139]. Elle rapproche également le fémur du bassin, avec un risque de contacts osseux [125]. Charnley considérait qu’il s’agissait d’une des principales causes d’instabilité prothétique [22] ;
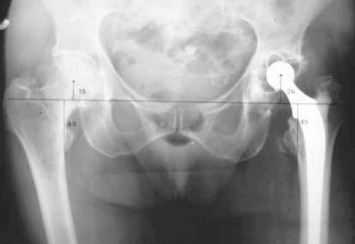
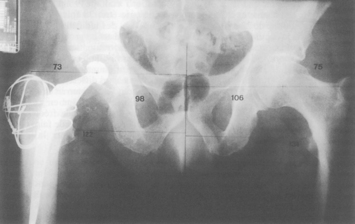
• la médialisation fémorale, sur laquelle de nombreux auteurs ont attiré l’attention [20,47,95]. Elle est souvent due à l’utilisation de prothèses à angle cervicocéphalique plus important que celui du fémur opéré, plus rarement à une implantation en valgus de la pièce fémorale [47]. Les patients présentant une coxa vara et un col long sont les plus menacés. La médialisation acétabulaire a le même effet : l’ablation d’importants ostéophytes de l’arrière-fond permet de couvrir la cupule et de médialiser le centre de rotation de la hanche, donc de diminuer le bras de levier du poids du corps, mais elle médialise d’autant le fémur. On peut ainsi mesurer deux paramètres lors de la planification préopératoire : le déport fémoral (distance entre le centre de la tête et l’axe diaphysaire) et le déport acétabulaire (distance entre le U radiologique et le centre de la cupule confondu avec celui de la tête). La somme des deux ou déport total [74] représente la médialisation du fémur sur lequel s’insèrent les muscles stabilisateurs de la hanche et notamment les fessiers. Une médialisation de plus de 1 cm entraînerait une détente musculaire importante [112]. En fait, il n’existe pas de données précises à ce sujet et il est possible que toutes les voies d’abord n’autorisent pas la même médialisation. Un col prothétique long retend les fessiers détendus par une médialisation, mais au prix d’un allongement du membre inférieur. L’ostéotomie trochantérienne avec abaissement et surtout latéralisation du grand trochanter permet de retendre les fessiers proportionnellement à cette médialisation. L’utilisation de prothèses latéralisantes est une autre solution, mais elles augmentent le bras de levier des forces varisantes transmises à la pièce fémorale et à sa fixation (figures 8 et 9).
Luxations tardives
Définies par leur survenue au-delà de 5 ans, il s’agit d’une entité particulière [33]. Si l’on exclut quelques luxations traumatiques, plusieurs mécanismes, parfois associés, peuvent être invoqués :
• la faiblesse musculaire qui augmente avec l’âge ;
• la distension de la capsule chez les patients ayant récupéré une grande mobilité et sa fragilisation par la réaction macrophagique réactionnelle aux particules d’usure [33, 34, 147] ;
• un épanchement intra-articulaire réactionnel à ces particules ;
• une déformation progressive du rebord de la cupule par des subluxations répétées [154] ;
• l’usure de la cupule surtout : la tête fémorale creuse dans la cupule un cylindre plus ou moins vertical selon l’inclinaison de la cupule [152], ce qui limite le débattement prothétique, en raison d’un contact très précoce du col avec le rebord de la cupule. Le débattement sera d’autant plus limité que le cylindre d’usure est profond et éloigné de la verticale : une usure de 5 mm à 45° d’obliquité diminue le débattement prothétique de 25°. Ce contact col-cupule peut entraîner une luxation du côté opposé au contact par effet came [153]. Il peut aussi, par sa répétition, entraîner une déformation du rebord de la cavité qui autorise l’issue de la tête en dehors de la cupule lors d’un contact col-cupule du côté opposé à cette déformation. Enfin, les impacts répétés du col sur la cupule peuvent la desceller et la mobiliser, avec un risque de luxation qui augmente au fur et à mesure que l’axe de la cupule s’éloigne de l’axe du conoïde de mobilité de la hanche [44, 154]. L’usure, facteur d’ostéolyse, et les impacts répétés du col sur la cupule rendent compte de la fréquence des descellements cotyloïdiens associés à ces luxations tardives [33].
Leur fréquence semble augmenter ou avoir été sous-estimée jusqu’à maintenant. Dans une série récente de la Mayo Clinic comportant 19 680 prothèses dont 2,6 % compliquées de luxation, les luxations tardives représentaient 32 % de la totalité des luxations [143]. Elles sont survenues en moyenne à 11,3 ans (5 à 24,9), avec une plus grande fréquence que les autres luxations chez les femmes et chez des patients plus jeunes lors de l’arthroplastie. Certains facteurs favorisants, dont certains seront étudiés plus loin, ont été individualisés : des antécédents de subluxation, un traumatisme important, l’apparition de troubles cognitifs ou neurologiques. Sur les radiographies ont été fréquemment notées : une usure de plus de 2 mm de la cupule, un descellement avec migration ou changement de position prothétique et une malposition initiale (rétroversion ou antéversion de plus de 30° ou inclinaison de plus de 55°). Leur pronostic était défavorable (55 % de récidives et 33 % de reprises), ce qui s’explique par les altérations de la cupule et de sa fixation.
Facteurs favorisants
Terrain
Âge
Plusieurs séries ont permis d’apprécier la fréquence de l’instabilité prothétique chez les patients de plus de 80 ans. Celle de Newington et al. [108] (112 prothèses) ne comporte que des étiologies dégénératives et inflammatoires et le taux de luxation y est de 15 %, sans différence entre les voies d’abord utilisées. Dans celle de Jolles et al. (2023 prothèses), il existait une différence significative entre le taux de luxation moyen (1,48 %) et celui des octogénaires (19 % de l’effectif), qui était de 2,91 % [74].
Le grand âge est un facteur reconnu de l’instabilité prothétique [103], sans doute explicable par la diminution de la force musculaire, les pathologies associées et le non-respect des précautions d’usage. Le risque de luxation est ainsi dix fois plus élevé chez les patients ayant un score ASA (American Society of Anesthesia) supérieur ou égal à 3 [74].
Sexe
Pour Woo et Morrey [147], le taux de luxation est significativement plus élevé chez la femme (3,8 % contre 2,5 %), de même que pour Turner (5,5 % contre 2,8 %) [137]. Cette différence peut être attribuée à une plus grande faiblesse musculaire [147] et une plus grande mobilité. La prédominance féminine est encore plus nette dans les luxations tardives [33, 143], ce qu’expliquent ces mêmes facteurs et une longévité plus importante.
Pathologies associées
Pathologie neuromusculaire
De nombreux auteurs ont mis en évidence le rôle néfaste des syndromes neurologiques (hémiplégie, spasticité, maladie de Parkinson, épilepsie, paralysies radiculaires) et des troubles psychiques (démence sénile, encéphalopathie éthylique) [4, 31, 47, 77, 114, 145]. Il faut en rapprocher les troubles du comportement d’origine éthylique dont la présence était fortement corrélée au taux de luxation des reprises dans une étude récente [115]. Dans une étude sur les luxations au cours des 3 premiers mois, les troubles cognitifs et/ou l’alcoolisme étaient les facteurs de risque les mieux individualisés [149]. L’usage de cupules particulières (tripolaires), une contention post-opératoire lorsqu’elle est possible [15, 145] sont indiqués chez de tels patients. Ces pathologies peuvent également survenir après l’intervention. Le risque de luxation est d’autant plus élevé qu’elles surviennent précocement (désorientation postopératoire avec agitation notamment), mais elles sont également incriminées dans les luxations tardives [143].
Autres atteintes articulaires
Fackler et Poss [47] ont attiré l’attention sur le rôle néfaste d’une désaxation en varus ou valgus de plus de 15° du genou sous-jacent qui expose aux malpositions fémorales. Turner [137] a surtout incriminé les importants genu valgum, où l’adduction de la hanche expose à l’instabilité. Le genu recurvatum entraîne une hyperextension de hanche qui favorise l’instabilité antérieure.
Obésité, taille
L’obésité expose aux effets cames par contact des parties molles internes en adduction [154] et aux malpositions dues aux difficultés d’installation et d’exposition [47]. Ces patients se mobilisent avec difficulté et ont du mal à éviter les mouvements luxants. À l’inverse, ils ont rarement une grande mobilité, ce qui les protège contre les contacts col-cupule. Une grande taille agirait par le biais d’un moment de force plus important lors des impacts col-cupule [115, 149].
Étiologie
Le taux de luxation est plus élevé dans toutes les séries de fractures transcervicales récentes traitées par arthroplastie totale (entre 8 et 18 %, avec une moyenne de 10 % dans sept séries publiées [63]). Il s’explique par une grande mobilité [63] mais aussi par le grand âge, la prédominance féminine et la fréquence des pathologies associées qui élèvent le score ASA [74].
Les nécroses ont également été incriminées [50, 75, 81]. L’étiologie éthylique peut expliquer des luxations précoces dues à des mouvements déconseillés. Certains ont invoqué la récupération d’une importante mobilité (souvent normale avant l’intervention) et une importante activité due au jeune âge [75, 81].
Plusieurs auteurs ont rapporté un taux de luxation plus important dans la maladie luxante de la hanche : 7,5 % [147] et 8 % [31]. Amstutz et Kody [4] l’attribuent aux difficultés de positionnement de la cupule, trop souvent verticale et antéversée. On peut aussi incriminer une capsulectomie complète et une trochantérotomie difficile à fixer. La tension des parties molles due à l’abaissement est au contraire un facteur de stabilité [75].
Ce sont surtout les antécédents chirurgicaux locaux qui exposent aux luxations : 4,8 % [147], 5,5 % [47]. Dans les séquelles de fracture opérée à plusieurs reprises, ce taux est particulièrement élevé [4], jusqu’à 22,2 % pour Woo et al. [147].
En fait, c’est surtout dans les reprises de prothèse que le taux de luxation s’élève : 8 % pour Amstutz et Kody [4], 13 % pour Woo et Morrey [147], 20,8 % pour Fackler et Poss [47], 28 % pour Lewinnek et al. [89]. L’importante série du symposium de la SOFCOT 1999 (1398 reprises) comportait 4,8 % de luxations au cours des premières semaines et 4,7 % à distance, soit 7,9 % au total [12]. Dans une série comparable de la Mayo Clinic (1548 reprises), ce taux était de 7,4 % [3] et dans l’enquête américaine de Phillips et al. (12956 reprises), il s’élevait à 14,4 %. Une cause de reprise expose particulièrement au risque de luxation : l’instabilité (24 % pour Wroblewski [154], 25,7 % pour Woo et Morrey [147]) et il faut avoir ces taux d’échec présents à l’esprit lorsque l’on traite une instabilité prothétique.
• désinsertion, voire excision de la néocapsule à des fins d’exposition [3] ;
• fragilisation des muscles par les interventions successives (muscles moyen et petit fessiers fibreux et atrophiques, disparition ou atrophie du plan postérieur) ;
• fibrose et ossifications antérieures (effet came en rotation interne) ;
• infiltration des parties molles et hématome profond [122, 154] ;
• difficultés de consolidation du grand trochanter ;
• utilisation de cupules cotyloïdiennes de grande taille, ménageant un espace mort important autour de la tête fémorale [47] ou de certaines prothèses fémorales de reprise à col long et valgisé (tels les premiers modèles de la prothèse de Wagner) qui réduit le bras de levier des forces varisantes mais médialise le fémur [154] ;
• prothèses fémorales massives sur lesquelles les parties molles périprothétiques, et notamment les muscles abducteurs, ne peuvent se réinsérer.
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree