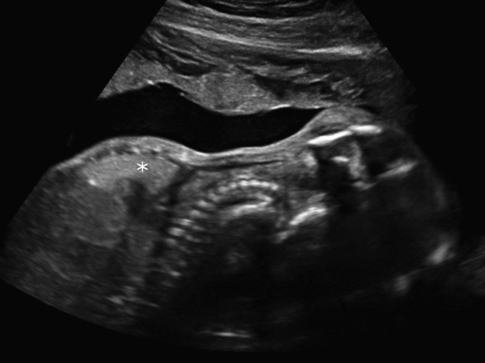
La période idéale pour l’étude morphologique du fœtus se situe vers 22 SA, entre 20 et 23 SA (voir chap. 1, Indications et dates des examens échographiques). Une étude précoce est maintenant préconisée entre 11 et 13 SA et 6 jours, en même temps que la datation de la grossesse. Cet examen permet avant tout la recherche d’un facteur de risque d’anomalie chromosomique (mesure de la clarté nucale dont l’augmentation n’est souvent que transitoire) et également le dépistage de grosses anomalies morphologiques (ce qui permet une décision plus précoce d’interruption de grossesse). Avec l’expérience, on peut modestement proposer les règles suivantes : Il ne s’agit pas d’un exercice solitaire. Il faut savoir s’entourer : Annoncer et expliquer une anomalie ne relève pas directement de la technique échographique. Il n’y a pas de règles car il n’y a pas LA bonne façon d’annoncer une mauvaise nouvelle : un peu d’expérience, beaucoup de bon sens et de sympathie, en tenant compte de la psychologie et de la sensibilité très particulière de la femme enceinte. S’il faut tout dire, il n’est pas nécessaire de le faire immédiatement. Il est parfois préférable d’exprimer un doute et de confirmer lors d’un deuxième examen, ce délai permettant de réfléchir et de programmer la suite des événements (consultations spécialisées, prélèvements). La notion de temps est importante car elle permet une « maturation », psychologique et médicale, tant pour la patiente que pour l’équipe médicale. Mais prendre son temps ne signifie pas abandon et un contact étroit doit être maintenu : rester disponible pour toute question présente ou à venir. L’étude échographique du fœtus et des organes fœtaux s’organise autour de trois plans de référence (fig. 6.1) : La « présentation » est le terme obstétrical pour désigner la partie du fœtus en rapport avec le détroit supérieur du bassin maternel et chaque présentation possède son repère (occiput pour la présentation céphalique normale, menton pour la face, sacrum pour le siège…). La « variété de position » indique l’orientation de la présentation (de son repère) : antérieure, postérieure, droite ou gauche. La présentation fœtale est habituellement figée à partir de 7 mois et demi, souvent plus tôt, mais parfois plus tard chez la multipare ou en cas d’excès de liquide. Habituellement, le dos du fœtus s’oriente du côté opposé au placenta. La clinique est théoriquement suffisante pour déterminer la présentation mais les exceptions sont très fréquentes (obésité, hydramnios, gémellaire…). Au 2e trimestre, le fœtus est très mobile, la présentation peut être notée mais cela n’a pas un intérêt majeur. Le type de présentations (fig. 6.2) sera précisé ou confirmé lors de l’examen du 3e trimestre (32–34 SA). Les présentations dystociques ou potentiellement dystociques (siège et transverse essentiellement) seront contrôlées vers 35–36 SA pour programmer une éventuelle correction (version par manœuvre externe) ou la conduite de l’accouchement. Pendant le travail, l’échographie en salle de naissance peut encore être très précieuse pour guider la conduite obstétricale (accouchement gémellaire en particulier) et l’étude de la variété de positions est parfois utilisée avant une application de forceps. Le fœtus est en position longitudinale et le siège se présente au détroit supérieur. On parle aussi de présentation « podalique ». On distingue (fig. 6.2) : L’échographie doit évaluer les éléments pronostiques de l’accouchement du siège : Il est possible de transformer une présentation du siège en une présentation céphalique en manipulant le fœtus à travers la paroi abdominale. C’est la « version » par manœuvre externe que nous détaillons dans l’encadré 6.1. Lorsque ni la tête ni le siège ne se présentent au détroit supérieur, on parlera de présentation transverse (ou oblique) (voir fig 6.2). Si elle persiste, c’est une présentation totalement dystocique qui implique a priori une césarienne avant ou en début de travail, exceptionnellement une manœuvre de « grande extraction » par voie basse en fin de travail (saisie des pieds et traction vers le bas). L’échographie précisera si la tête est à gauche ou à droite et si le dos s’oriente vers le haut ou vers le bas. L’ébauche d’un contour osseux (pariétal) permet l’identification et la mesure d’un diamètre céphalique transverse dès 8 SA (voir fig. 4.6). En fin de 1er trimestre, le crâne forme sur la coupe transversale une image ovoïde : le « gros bout » de l’œuf est occipital, le « petit bout » de l’œuf est frontal (voir fig. 4.30) et va s’aplatir légèrement au 2e trimestre avec le développement des bosses frontales. En coupe frontale, la voûte crânienne présente un contour remarquablement circulaire, reposant sur la base du crâne. Les pièces osseuses sont séparées par les sutures et les fontanelles (voir fig. 6.4), mieux visibles quand le faisceau ultrasonore est tangentiel à la voûte ou en utilisant l’artifice du mode 3D (en VCI-C) : la suture sagittale présente la grande fontanelle antérieure (ou bregma), qu’on doit utiliser en priorité pour explorer le cerveau dans les plans frontaux et sagittaux, et la petite fontanelle postérieure (ou lambda) beaucoup moins large et utile. Latéralement et un peu en avant, à l’union des écailles frontale, pariétale et temporale, on trouve la fontanelle du ptérion très utile pour étudier l’artère cérébrale moyenne (voir fig. 6.29) ou le ventricule cérébral proximal. Il existe en arrière une autre fontanelle avec l’os occipital, l’astérion, utilisée pour aborder le sinus transverse et la tente du cervelet. Le revêtement cutané s’individualise, en haute fréquence, dès la fin de la période embryonnaire (voir fig. 4.30). Son épaisseur (peau + tissu sous-cutané) atteint 2 à 3 mm à terme et ne doit pas dépasser 6 mm, en particulier au 2e trimestre où on doit l’évaluer au niveau de l’écaille occipitale, sur une coupe transversale oblique passant par le cavum du septum pellucidum, les pédoncules cérébraux et le cervelet : c’est un marqueur de trisomie 21 (voir chap. 7, Tissu sous-cutané, fig. 7.28 et voir chap. 16, Anomalies chromosomiques). Les cheveux sont souvent bien visibles en fin de grossesse, au niveau occipital, formant un double contour irrégulier ou des images « en flammèches » (voir fig. 6.4c). Les variations de la forme générale du crâne sont le plus souvent physiologiques, réalisant soit la brachycéphalie avec un crâne large et court dans le sens antéropostérieur, soit la dolichocéphalie avec un crâne allongé et étroit (voir fig. 8.16). Ces variations peuvent amener à nuancer l’interprétation du diamètre bipariétal et peuvent s’objectiver par le calcul de l’index céphalique (voir chap 7, Biométrie et voir chap. 8, Anomalies cranio-encéphaliques). Ces variations peuvent être : L’étude de la face peut être détaillée à partir de 3 mois et demi. Elle s’effectue selon les trois plans habituels mais se trouve souvent limitée, surtout en fin de grossesse, par l’orientation de la tête, l’interposition des avant-bras et des mains, l’insuffisance de liquide amniotique. Quand on en dispose, le mode 3D-4D « surface » permet un gain de temps évident sur un fœtus coopérant (fig. 6.5a, b, d et e) car il fournit une « synthèse » immédiate de l’étude de la face. Mais les circonstances ne sont pas toujours favorables (fig. 6.5c) et il faudra alors un peu « ramer » en mode 2D. La coupe sagittale médiane (fig. 6.6a), si elle est la plus spectaculaire, n’est sans doute pas la plus informative. Attention, une coupe parfaitement médiane peut passer à côté d’une fente labiale unilatérale. Le mode volumique triplan peut aider à obtenir une coupe de profil strict. Cette coupe montre le profil fœtal (front, ensellure nasale, nez, lèvres, menton) avec étude possible de la cavité buccale (langue, palais, voile et oropharynx) lors des mouvements d’ouverture (bâillements) et de déglutition. La mesure des os propres du nez s’effectue dans ce plan, avec un abord le plus orthogonal possible, en agrandissant ou en faisant un « zoom » sur le nez. Le profil « moyen » présente les quelques caractéristiques suivantes, dont on souligne encore le caractère subjectif :
Fœtus normal : étude morphologique et dépistage
Principes généraux
Dates des examens
En pratique
 être ordonné et suivre un plan, toujours le même et toujours y revenir quand on a dévié du chemin. Ce plan peut être un schéma mental ou reposer sur la check-list du compte rendu d’examen :
être ordonné et suivre un plan, toujours le même et toujours y revenir quand on a dévié du chemin. Ce plan peut être un schéma mental ou reposer sur la check-list du compte rendu d’examen :
 tour d’horizon rapide contrôlant l’activité cardiaque, la présentation, la quantité de liquide et la position du placenta ; fabrication de l’image mentale du fœtus en 3D, cette image guidant la sonde pour la suite de l’examen ;
tour d’horizon rapide contrôlant l’activité cardiaque, la présentation, la quantité de liquide et la position du placenta ; fabrication de l’image mentale du fœtus en 3D, cette image guidant la sonde pour la suite de l’examen ;
 biométrie (BIP, périmètre crânien, circonférence abdominale, fémur) qui permet un premier balayage morphologique ;
biométrie (BIP, périmètre crânien, circonférence abdominale, fémur) qui permet un premier balayage morphologique ;
 étude morphologique de haut en bas (tête et rachis, thorax puis abdomen, membres et extrémités), en recherchant à chaque étage les repères anatomiques et en « latéralisant » le fœtus (il faut s’imaginer à la place du fœtus pour bien identifier côté droit–côté gauche) ;
étude morphologique de haut en bas (tête et rachis, thorax puis abdomen, membres et extrémités), en recherchant à chaque étage les repères anatomiques et en « latéralisant » le fœtus (il faut s’imaginer à la place du fœtus pour bien identifier côté droit–côté gauche) ;
 mesures complémentaires et Doppler selon les constatations précédentes ;
mesures complémentaires et Doppler selon les constatations précédentes ;
 être « anticipatif ». Il faut imaginer la structure avant qu’elle se dévoile lors du déplacement de la sonde. C’est alors la discordance entre ce qu’on avait anticipé et ce qu’on voit qui attire l’attention ;
être « anticipatif ». Il faut imaginer la structure avant qu’elle se dévoile lors du déplacement de la sonde. C’est alors la discordance entre ce qu’on avait anticipé et ce qu’on voit qui attire l’attention ;
 être opportuniste. Les mouvements fœtaux peuvent exposer puis dissimuler certains repères critiques : lorsque le fœtus tourne le thorax ou le dos vers la sonde, il faut saisir immédiatement cette occasion d’une bonne étude des quatre cavités ou du rachis lombo-sacré (et des reins) car elle peut ne plus se représenter dans la suite de l’examen ;
être opportuniste. Les mouvements fœtaux peuvent exposer puis dissimuler certains repères critiques : lorsque le fœtus tourne le thorax ou le dos vers la sonde, il faut saisir immédiatement cette occasion d’une bonne étude des quatre cavités ou du rachis lombo-sacré (et des reins) car elle peut ne plus se représenter dans la suite de l’examen ;
 être concentré, ne pas se laisser distraire. L’exercice est difficile, la responsabilité est lourde, les fautes d’inattention sont impardonnables. Il faut faire comprendre à la patiente, et à son entourage, que l’on commence par un acte médical et que l’on reportera le commentaire, les explications, le « spectacle » en fin d’examen ;
être concentré, ne pas se laisser distraire. L’exercice est difficile, la responsabilité est lourde, les fautes d’inattention sont impardonnables. Il faut faire comprendre à la patiente, et à son entourage, que l’on commence par un acte médical et que l’on reportera le commentaire, les explications, le « spectacle » en fin d’examen ;
 toute anomalie doit faire rechercher une autre anomalie, et donc reprendre une étude morphologique approfondie.
toute anomalie doit faire rechercher une autre anomalie, et donc reprendre une étude morphologique approfondie.
Interprétation d’une image anormale
 parfois d’un deuxième avis indépendant, indispensable si un diagnostic de malformation peut conduire à accepter une interruption de grossesse si elle est demandée ;
parfois d’un deuxième avis indépendant, indispensable si un diagnostic de malformation peut conduire à accepter une interruption de grossesse si elle est demandée ;
 d’une discussion collégiale au sein de l’équipe obstétrico-pédiatrique ;
d’une discussion collégiale au sein de l’équipe obstétrico-pédiatrique ;
 de correspondants spécialistes, en particulier cardiopédiatre, neuropédiatre, chirurgien infantile et neurochirurgien, nécessaires pour discuter et programmer la prise en charge post-natale ; ou – mieux encore – une liaison bien établie avec le centre pluridisciplinaire de diagnostic prénatal du réseau périnatal ;
de correspondants spécialistes, en particulier cardiopédiatre, neuropédiatre, chirurgien infantile et neurochirurgien, nécessaires pour discuter et programmer la prise en charge post-natale ; ou – mieux encore – une liaison bien établie avec le centre pluridisciplinaire de diagnostic prénatal du réseau périnatal ;
 de la télétransmission des images, les téléconférences, les banques de données qui peuvent enrichir la compétence individuelle et éviter des déplacements inutiles et des forums de discussion sur Internet, parfois très réactifs et efficaces.
de la télétransmission des images, les téléconférences, les banques de données qui peuvent enrichir la compétence individuelle et éviter des déplacements inutiles et des forums de discussion sur Internet, parfois très réactifs et efficaces.
Attitude face à une anomalie
Définition des plans de coupe échographique
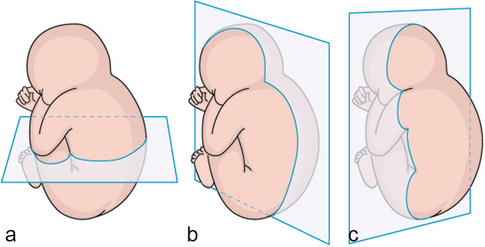
 le plan transversal ou axial, perpendiculaire au grand axe du tronc fœtal (par exemple, les coupes du BIP ou du diamètre abdominal transverse) ;
le plan transversal ou axial, perpendiculaire au grand axe du tronc fœtal (par exemple, les coupes du BIP ou du diamètre abdominal transverse) ;
 le plan sagittal, dans l’axe longitudinal et dans le sens antéropostérieur (par exemple, le profil au niveau de la face) ;
le plan sagittal, dans l’axe longitudinal et dans le sens antéropostérieur (par exemple, le profil au niveau de la face) ;
 le plan frontal (coronal), perpendiculaire au précédent (par exemple, le plan de coupe de la bifurcation aortique).
le plan frontal (coronal), perpendiculaire au précédent (par exemple, le plan de coupe de la bifurcation aortique).
Présentations du fœtus
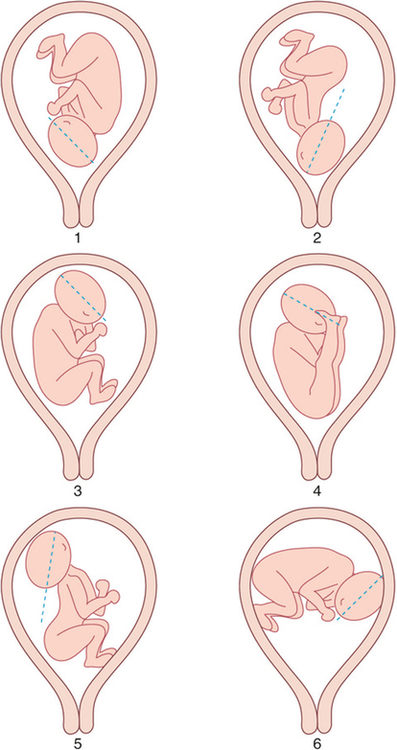
1 : céphalique fléchie ; 2 : céphalique défléchie ; 3 : siège complet ; 4 : siège décomplété ; 5 : siège avec déflexion de la tête ; 6 : transverse.
Présentation céphalique
 Normale : présentation dite du sommet avec fœtus en position longitudinale, tête basse en regard du détroit supérieur, en posture indifférente (le diamètre occipito-frontal est dans un plan transversal) ou fléchie en cas d’engagement (menton sur la poitrine, tête mal visible derrière la symphyse).
Normale : présentation dite du sommet avec fœtus en position longitudinale, tête basse en regard du détroit supérieur, en posture indifférente (le diamètre occipito-frontal est dans un plan transversal) ou fléchie en cas d’engagement (menton sur la poitrine, tête mal visible derrière la symphyse).
 Anormale : la déflexion de la tête fœtale (menton relevé et face vers le bas), lorsqu’elle est permanente, se transformera en cours de travail en une présentation de la face ou du front. Échographiquement, on notera :
Anormale : la déflexion de la tête fœtale (menton relevé et face vers le bas), lorsqu’elle est permanente, se transformera en cours de travail en une présentation de la face ou du front. Échographiquement, on notera :
 la difficulté évidente du repérage de la face ;
la difficulté évidente du repérage de la face ;
 le plan du bipariétal (et l’axe occipito-frontal) qui se prolonge dans le plan du rachis dorsal ;
le plan du bipariétal (et l’axe occipito-frontal) qui se prolonge dans le plan du rachis dorsal ;
 l’incurvation prononcée vers l’avant du rachis cervical (fig. 6.2 et 6.3).
l’incurvation prononcée vers l’avant du rachis cervical (fig. 6.2 et 6.3).
Présentation du siège
 la présentation du siège complet avec les membres inférieurs fléchis (fœtus « assis en tailleur ») ;
la présentation du siège complet avec les membres inférieurs fléchis (fœtus « assis en tailleur ») ;
 la présentation du siège décomplété, membres inférieurs étendus en attelle devant le tronc (semi-décomplété si un seul membre est étendu).
la présentation du siège décomplété, membres inférieurs étendus en attelle devant le tronc (semi-décomplété si un seul membre est étendu).
 dimensions fœtales, estimation du poids, céphalométrie à confronter aux résultats de la mesure du bassin (pelvimétrie par scanner ou pelviscan) ;
dimensions fœtales, estimation du poids, céphalométrie à confronter aux résultats de la mesure du bassin (pelvimétrie par scanner ou pelviscan) ;
 quantité de liquide amniotique, l’oligoamnios étant un facteur défavorable ;
quantité de liquide amniotique, l’oligoamnios étant un facteur défavorable ;
 éventuel circulaire du cordon surtout s’il est double ou triple ;
éventuel circulaire du cordon surtout s’il est double ou triple ;
 la très rare déflexion primitive de la tête qui contre-indique la voie basse.
la très rare déflexion primitive de la tête qui contre-indique la voie basse.
Présentation transverse
Crâne
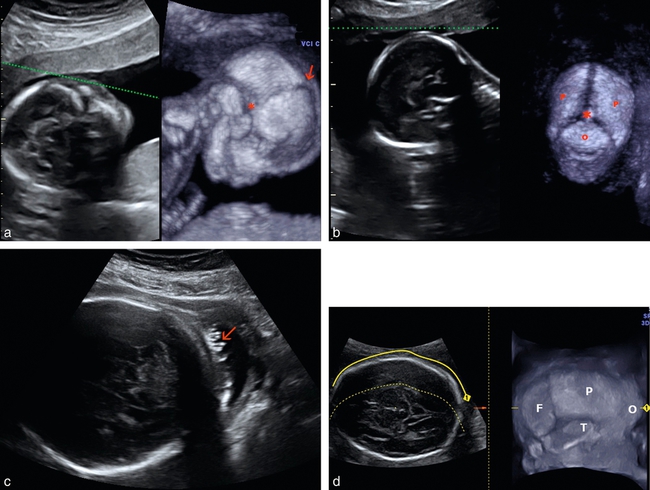
a. Mode VCI-C (coupe épaisse et mode osseux), à 4 mois, sur le côté du crâne : les sutures sont bien visibles avec le bregma (→) au sommet et le ptérion (*) latéralement. On ne voit ni le lambda, ni l’astérion car la tête est légèrement tournée vers l’observateur.
b. Mode VCI-C à 4 mois sur l’occiput : le lambda (*), repère essentiel pour les accoucheurs, entre l’écaille occipitale (O) et les pariétaux (P).
c. Surface occipitale, 33 SA. Image des cheveux formant des flammèches flottantes (→) dans le liquide amniotique.
d. À 25 SA, étude en reconstruction omniview mode osseux. F : os frontal ; P : os pariétal ; T : os temporal ; O : os occipital.
 constitutionnelles, par variation interindividuelle ou facteur génétique ;
constitutionnelles, par variation interindividuelle ou facteur génétique ;
 acquises, par modelage du crâne, en particulier en cas de présentation du siège ou d’oligoamnios important qui provoquent souvent une dolichocéphalie.
acquises, par modelage du crâne, en particulier en cas de présentation du siège ou d’oligoamnios important qui provoquent souvent une dolichocéphalie.
Face
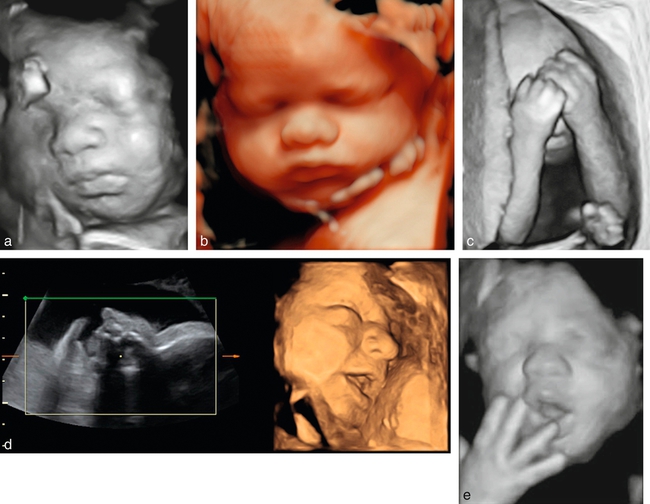
a. 33 SA. Évidence immédiate = nez et bouche normaux.
b. Grâce à un logiciel dédié, les traits de ce fœtus sont ici parfaitement dessinés.
c. 23 SA. Évidence immédiate = mauvaise volonté ou gros chagrin !
d. Visage (33 SA). Reconstruction en 4D surface d’un côté du visage parfaitement dessiné.
e. 29 SA, mode volumique. Fœtus bien élevé dissimulant un bâillement ! Mais l’observateur a saisi l’essentiel : intégrité de la bouche et des mains.
En coupe sagittale médiane
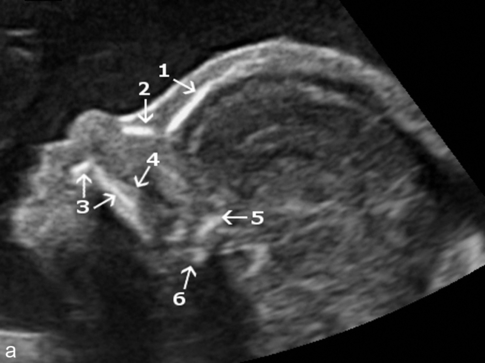
a. 24 SA. Sur cette vue de profil du fœtus on individualise : 1. os frontal ; 2. os propre du nez ; 3. maxillaire et son processus palatin ; 4. vomer ; 5. sphénoïde ; 6. os occipital (partie basilaire).
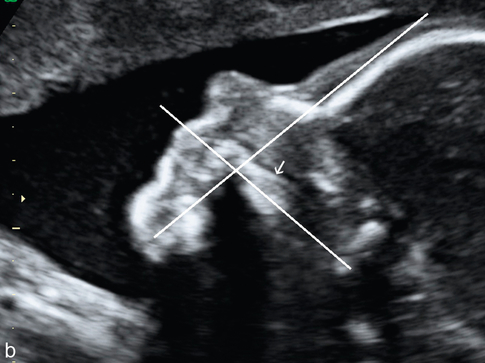
b. Mesure de l’angle fronto-maxillaire (24 SA). Coupe de profil. L’angle est délimité par un axe tangent à l’os frontal et par un axe tangent au palais. Attention à ne pas confondre le palais et le vomer (→).
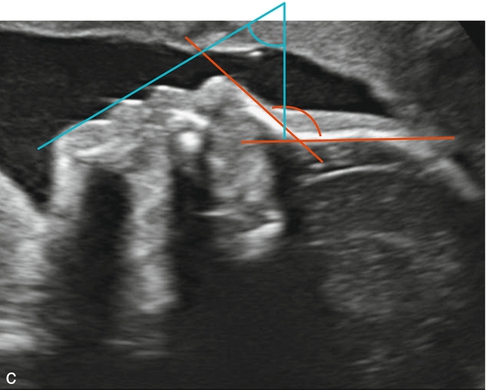
c. Angle facial supérieur : normal environ 131° (en rouge). Angle facial inférieur : normal environ 64–68° (en bleu).![]()
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree


6: Fœtus normal : étude morphologique et dépistage