Chapitre 5
Annexes du fœtus : liquide amniotique et membranes, placenta et cordon ombilical
Le développement initial du sac trophoblastique, de l’amnios et du cordon a été décrit au chapitre 4 et nous étudierons ici les annexes fœtales aux 2e et 3e trimestres :
 le liquide amniotique (LA) est un élément essentiel du bien-être fœtal ;
le liquide amniotique (LA) est un élément essentiel du bien-être fœtal ;
 les membranes ovulaires ne sont normalement pas visibles ;
les membranes ovulaires ne sont normalement pas visibles ;
 la structure échographique du placenta apporte peu d’informations sur son fonctionnement (qui sera surtout évalué par le Doppler ombilical et utérin) mais l’échographie est déterminante pour le dépistage des insertions basses ;
la structure échographique du placenta apporte peu d’informations sur son fonctionnement (qui sera surtout évalué par le Doppler ombilical et utérin) mais l’échographie est déterminante pour le dépistage des insertions basses ;
 l’étude de la totalité du cordon est impossible en examen de routine mais les anomalies dangereuses du cordon sont beaucoup plus rares que les simples variations anatomiques.
l’étude de la totalité du cordon est impossible en examen de routine mais les anomalies dangereuses du cordon sont beaucoup plus rares que les simples variations anatomiques.
Liquide amniotique
Le liquide amniotique est un élément essentiel du bien-être fœtal. Il participe également au bien-être de l’échographiste puisque ses variations de volume peuvent faciliter ou gêner considérablement l’exploration. La physiologie nous montre que le liquide amniotique est le reflet direct de la perfusion rénale du fœtus, donc de son état circulatoire et de l’état des relations fœtomaternelles : en évaluant le liquide amniotique, nous nous plaçons au bout d’une chaîne physiologique, ce qui permet de détecter les défaillances sur les maillons précédents.
Rappel physiologique
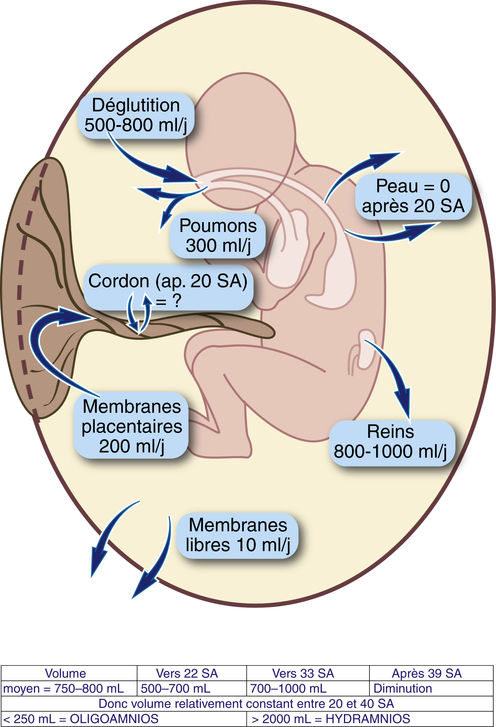
Les connaissances souffrent encore de beaucoup d’incertitudes, en particulier dans les mécanismes de régulation du volume et de la composition du liquide. La figure 5.1 résume les principales données sur la production et la résorption du liquide amniotique.
Il y a quatre voies principales pour la circulation du liquide :
 deux voies d’entrée qui sont la diurèse fœtale (800–1000 mL/j à terme) et la sécrétion pulmonaire (200–300 mL/j dont la moitié est reprise par la déglutition) ;
deux voies d’entrée qui sont la diurèse fœtale (800–1000 mL/j à terme) et la sécrétion pulmonaire (200–300 mL/j dont la moitié est reprise par la déglutition) ;
 deux voies de sortie qui sont la déglutition fœtale (500–800 mL/j à terme et toujours inférieure à la diurèse) et l’absorption à travers les membranes de la surface placentaire (voie dite « intramembranaire » qui est de l’ordre de 200 à 500 mL/j et qui compense le déséquilibre entre déglutition et diurèse).
deux voies de sortie qui sont la déglutition fœtale (500–800 mL/j à terme et toujours inférieure à la diurèse) et l’absorption à travers les membranes de la surface placentaire (voie dite « intramembranaire » qui est de l’ordre de 200 à 500 mL/j et qui compense le déséquilibre entre déglutition et diurèse).
Il y a des voies (probablement) accessoires :
 entrée au travers de la peau fœtale, surtout avant 20 SA car au-delà la kératinisation bloque la sortie d’eau ;
entrée au travers de la peau fœtale, surtout avant 20 SA car au-delà la kératinisation bloque la sortie d’eau ;
 production probable de liquide par les membranes elles-mêmes : cette hypothèse est souvent évoquée à partir d’études histologiques des membranes mais la preuve de ce phénomène, son importance et sa régulation sont encore inconnues ;
production probable de liquide par les membranes elles-mêmes : cette hypothèse est souvent évoquée à partir d’études histologiques des membranes mais la preuve de ce phénomène, son importance et sa régulation sont encore inconnues ;
 sortie par résorption à la surface du cordon : probablement minime et seulement après 20 SA ;
sortie par résorption à la surface du cordon : probablement minime et seulement après 20 SA ;
 sortie au travers des membranes libres extraplacentaires (voie « transmembranaire ») via l’accolement aux caduques utérines : la surface est très importante mais les publications ne font état que d’un flux très minime de l’ordre de 10 mL/j sans précision sur les preuves ou les méthodes de mesure.
sortie au travers des membranes libres extraplacentaires (voie « transmembranaire ») via l’accolement aux caduques utérines : la surface est très importante mais les publications ne font état que d’un flux très minime de l’ordre de 10 mL/j sans précision sur les preuves ou les méthodes de mesure.
Le liquide amniotique a un rôle majeur dans le développement fœtal :
Aspect échographique du liquide amniotique
Échographiquement, le liquide amniotique est presque anéchogène en première moitié de grossesse, identique au contenu vésical maternel. En deuxième partie de grossesse, il contient de fins échos mobiles, en abondance très variable et d’autant plus marqués que l’on utilise une haute fréquence (fig. 5.2). L’aspect peut être franchement floconneux en fin de grossesse et même tellement échogène que les vaisseaux du cordon semblent y découper des trous anéchogènes (fig. 5.2 et 5.3).
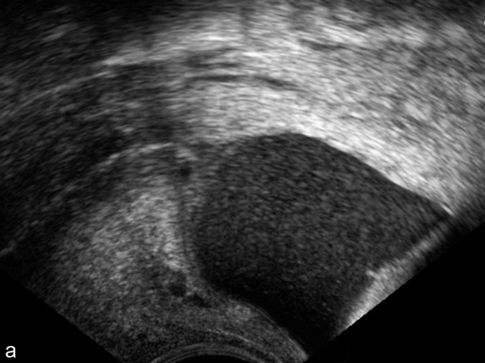
a. Voie vaginale et haute fréquence, aspect très finement échogène.
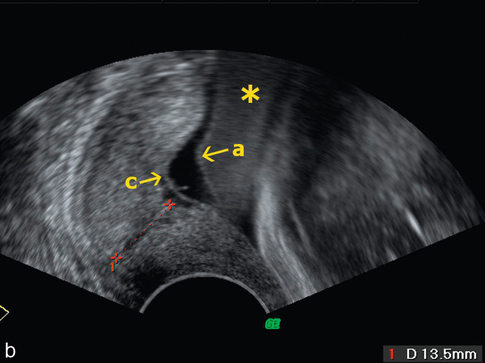
b. Voie vaginale, fin de grossesse, mesure du col : liquide échogène (*) soulignant le clivage entre amnios et chorion en regard du col. Les membranes sont intactes et le liquide très échogène ne doit pas être confondu avec un bord placentaire. On observe ici une poche amniochoriale avec un peu de liquide qui a filtré entre l’amnios (a) et le chorion (c).
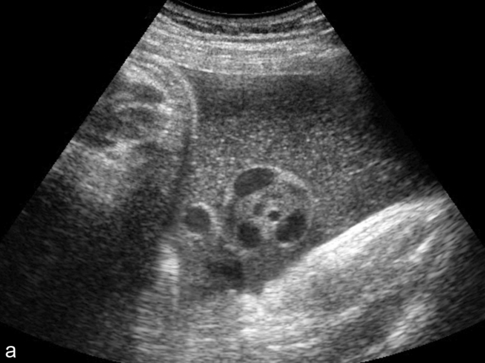
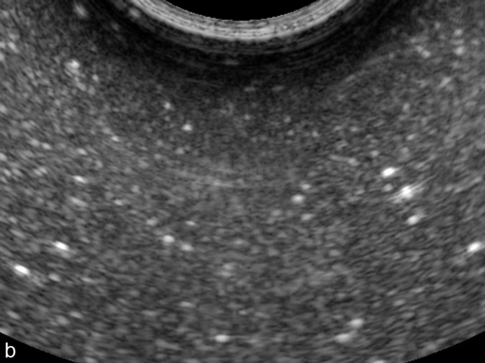
a. Aspect floconneux, très échogène, où le cordon dessine des « trous » anéchogènes.
b. Après accouchement normal : échographie d’un échantillon de LA contenant beaucoup de flocons de vernix et dont l’aspect macroscopique est presque « laiteux ».
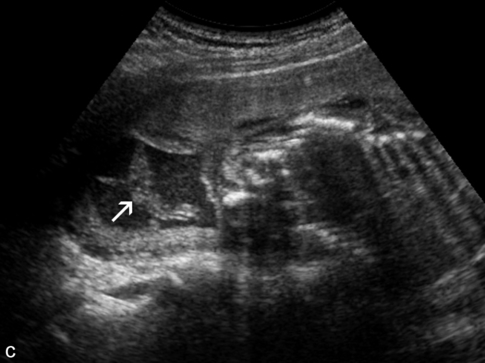
c. Sang et caillots flottant (→) dans le liquide (hématome décidual qui a diffusé au travers des membranes).
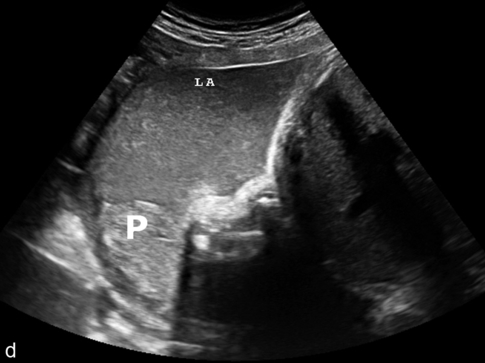
d. Liquide hyperéchogène (LA) à 40 SA, aussi échogène que le placenta (P) : cet aspect est inhabituel mais normal.
Ces échos amniotiques correspondent normalement à la desquamation de cellules cutanées et à des flocons de vernix. Le vernix est une production sébacée qui forme un enduit blanc, gras et pâteux, sur la peau du fœtus en deuxième partie de grossesse : plus on approche du terme, plus le vernix se détache de la peau pour former des particules en suspension pouvant donner un aspect presque laiteux au liquide. La présence ou l’absence des flocons, leur abondance ou la date d’apparition sont extrêmement variables d’un fœtus à l’autre.
Mais, ces mêmes échos peuvent être produits par la présence de sang ou de méconium et il est a priori impossible en échographie d’identifier la nature des flocons (particules trop petites par rapport à la longueur d’onde). Les échos se regroupent parfois pour former des structures flottantes (fig. 5.3c) et ceci est quand même très évocateur de caillots sanguins (après une ponction ou en cas d’hématome décidual qui diffuse à travers les membranes). Il n’y a donc pas d’information pronostique – sur la vitalité ou la maturité fœtale – à retirer de l’aspect échographique du liquide.
Évaluation quantitative du liquide amniotique
Le volume de liquide amniotique est relativement constant entre 20 et 40 semaines, alors que le poids fœtal passe de 400 à plus de 3000 g. Le volume maximal de liquide est atteint entre 7 mois et 7 mois et demi (environ 800 à 1000 mL), mais, comparativement au volume fœtal, l’abondance est plus grande vers 5–6 mois (« hydramnios physiologique »). Au voisinage du terme, on observe une décroissance absolue et relative du liquide (« oligoamnios physiologique »).
Évaluation quantitative « à l’estime »
Cette méthode subjective est le plus souvent suffisante pour reconnaître un liquide normal ou abondant. L’échographiste entraîné est habitué à « voir son liquide » sur l’écran (fig. 5.2, 5.3 et 5.4) : belles poches de liquide, membres libres et bien mobiles, cordon bien visible. Cela contraste avec le malaise et les difficultés techniques rencontrées en cas d’insuffisance, avec parfois des aspects de compression fœtale (fig. 5.5). Quant à l’hydramnios, il distend de manière évidente l’utérus et écarte exagérément la sonde et la paroi des structures fœtales (fig. 5.4b).
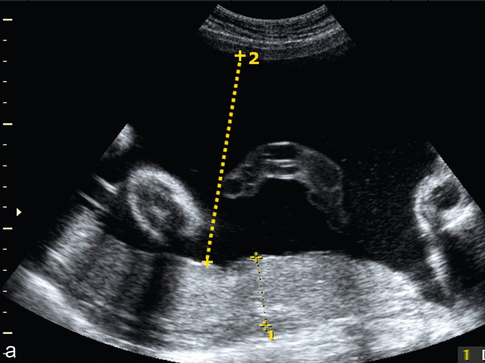
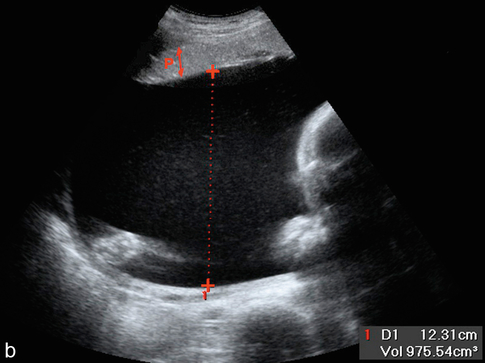
a. Hydramnios modéré (ou excès de liquide) à 7 mois : plus grande citerne = 95 mm (2) ; épaisseur du placenta (1) = 25 mm.
b. Hydramnios majeur par sténose duodénale à 30 SA : plus grande citerne = 123 mm ; IA supérieur à 35, placenta (P) un peu aminci (épaisseur = 20 mm).
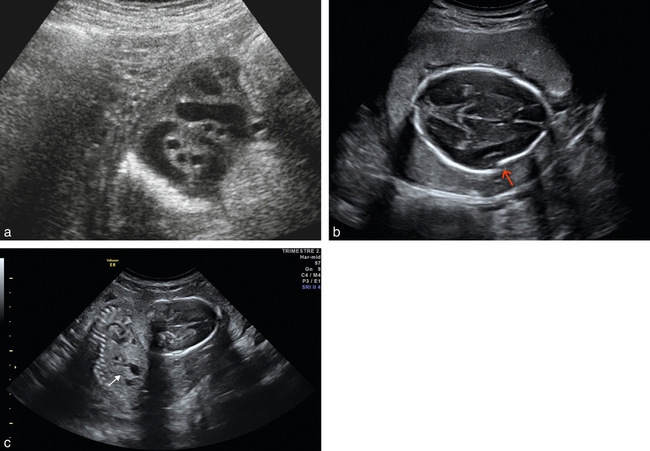
a. Terme dépassé (41 SA et 2 jours) : une seule citerne retrouvée mais elle ne contient que du cordon. C’est un oligoamnios franc qui invite à une surveillance accrue et à envisager un déclenchement du travail.
b. Oligoamnios à 5 mois par rupture très prématurée des membranes. Chevauchement des os du crâne (→).
c. Oligoanamnios à 18 SA. Rein unique dysplasique (→). Fœtus recroquevillé sur lui-même.
Évaluation biométrique « objective »
Tableau 5.1
Index amniotique (IA) : répartition des valeurs.
| IA (mm) | 1er p | 5e p | 50e p | 95e p | 99e p |
| Mesure moyenne | 62 mm | 76 mm | 129 mm | 219 mm | 269 mm |
| 16–36 SA | 73 mm | 88 mm | 142 mm | 229 mm | 277 mm |
| 37–41 SA | 55 mm | 68 mm | 115 mm | 196 mm | 241 mm |
| > 41 SA | 56 mm | 67 mm | 108 mm | 174 mm | 209 mm |
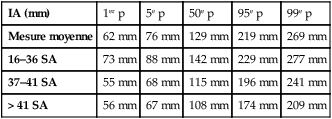
D’après Moore TR. The amniotic fluid index in normal human pregnancy. Am J Obstet Gynecol 1990 ; 162(5) : 1168–73.
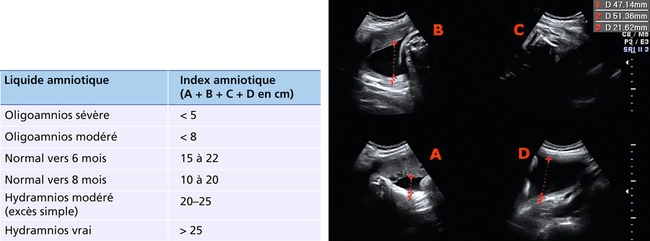
Index normal à 11–12 cm. L’une des mesures (quadrant D) n’est pas dans un axe strictement vertical (sans conséquence) et le quadrant C ne contient pas de liquide.
« Règle du 1 cm » de Chamberlain et Manning
Méthode des « quatre quadrants » de Phelan et Rutherford (voir fig. 5.6 et tableau 5.1)
La face antérieure de l’utérus est divisée en quatre quadrants (centrés par l’ombilic, donc seulement deux quadrants avant 20 SA). Dans chaque quadrant, on recherche la plus grande citerne dont on mesure la profondeur dans un axe vertical (par rapport au plan de la table d’examen) et l’on fait la somme des quatre valeurs (dont une ou deux peuvent être nulles) qui définit l’index amniotique (IA) : le tableau 5.1 propose les valeurs limites en pratique courante.
Certains perfectionnent (ou compliquent) encore l’évaluation de l’index amniotique en utilisant une courbe en percentiles prenant en compte l’âge gestationnel et la diminution physiologique de la quantité de liquide amniotique en fin de grossesse. Dans cette étude (voir tableau 5.1), la variation de mesure intra-observateur est de 5 mm et la variation inter-observateur de 9,5 mm (ce qui remarquablement et étonnamment faible !).
Excès de liquide amniotique et hydramnios
L’hydramnios – ou polyhydramnios des Anglo-Saxons – est classiquement défini par un volume de liquide supérieur à 2 L à terme (normalement de l’ordre de 800 mL). Entre 1 et 2 L pour les hydramnios modérés, on parlera plutôt de liquide abondant ou d’excès de liquide, termes plus rassurants pour tout le monde. Il s’agit ici de valeurs théoriques car il n’y a jamais, en pratique, de mesure directe du liquide qu’il s’agisse d’une pesée lors de l’accouchement ou d’un calcul du volume de dilution d’un marqueur injecté (non réalisable en pratique quotidienne). On reste le plus souvent au niveau de l’impression et de l’approximation : beaucoup de liquide, pas beaucoup ou pas du tout…
L’échographie (fig. 5.4) permet toujours un diagnostic aisé de l’hydramnios vrai, les mesures des citernes permettant de suivre l’évolution (mais pas beaucoup mieux que la hauteur utérine ou le périmètre ombilical maternel).
Hydramnios chronique
L’hydramnios chronique (fig. 5.4) est modéré (inférieur à 5 L le plus souvent), d’évolution progressive sans gêne fonctionnelle pour la mère et, surtout, l’utérus reste souple sous la sonde. L’enquête étiologique repose sur l’examen échographique et s’organise en deux parties : insuffisance de résorption du liquide amniotique et excès de production.
Insuffisance de résorption digestive du liquide
 par malformation digestive : atrésie de l’œsophage et sténose duodénale surtout (obstruction haute, voir fig. 5.4b) ;
par malformation digestive : atrésie de l’œsophage et sténose duodénale surtout (obstruction haute, voir fig. 5.4b) ;
 par compression digestive : tumeur du cou (lymphangiome, goitre) et du thorax, hernie diaphragmatique ;
par compression digestive : tumeur du cou (lymphangiome, goitre) et du thorax, hernie diaphragmatique ;
 par trouble de la déglutition : fente labiopalatine, macroglossie, syndrome de Pierre Robin, malformations du système nerveux central, immobilisme fœtal par pathologies neuromusculaires (maladie de Steinert, syndrome de Pena-Shokeir avec RCIU et arthrogrypose) ;
par trouble de la déglutition : fente labiopalatine, macroglossie, syndrome de Pierre Robin, malformations du système nerveux central, immobilisme fœtal par pathologies neuromusculaires (maladie de Steinert, syndrome de Pena-Shokeir avec RCIU et arthrogrypose) ;
 par anomalies chromosomiques et/ou syndromes polymalformatifs (nanisme à thorax étroit).
par anomalies chromosomiques et/ou syndromes polymalformatifs (nanisme à thorax étroit).
Excès du production du liquide
 par gêne circulatoire en amont d’une insuffisance cardiaque (malformation, trouble du rythme à type de tachycardie supraventriculaire, myocardite, shunt artérioveineux), souvent associée secondairement à une ascite ou une anasarque fœtoplacentaire ;
par gêne circulatoire en amont d’une insuffisance cardiaque (malformation, trouble du rythme à type de tachycardie supraventriculaire, myocardite, shunt artérioveineux), souvent associée secondairement à une ascite ou une anasarque fœtoplacentaire ;
 par anémie fœtale sévère qui agit à la fois par l’insuffisance cardiaque et par modification de l’osmolarité plasmatique, également fréquemment associée à une ascite ou anasarque fœtale (hémolyse par allo-immunisation érythrocytaire type Rhésus, parvovirus B19, hémorragie fœtomaternelle, alpha-thalassémie homozygote…) ;
par anémie fœtale sévère qui agit à la fois par l’insuffisance cardiaque et par modification de l’osmolarité plasmatique, également fréquemment associée à une ascite ou anasarque fœtale (hémolyse par allo-immunisation érythrocytaire type Rhésus, parvovirus B19, hémorragie fœtomaternelle, alpha-thalassémie homozygote…) ;
 par anencéphalie et méningocèle avec transfert de liquide à travers les méninges découvertes ;
par anencéphalie et méningocèle avec transfert de liquide à travers les méninges découvertes ;
 par grossesse gémellaire monochoriale avec forme mineure du syndrome transfuseur–transfusé (STT) ;
par grossesse gémellaire monochoriale avec forme mineure du syndrome transfuseur–transfusé (STT) ;
 par augmentation de la diurèse fœtale dans la macrosomie diabétique, plus exceptionnellement l’hyperaldostéronisme comme dans le syndrome de Bartter.
par augmentation de la diurèse fœtale dans la macrosomie diabétique, plus exceptionnellement l’hyperaldostéronisme comme dans le syndrome de Bartter.
Enquête étiologique négative
L’indication du caryotype fœtal ne fait pas l’unanimité mais on peut proposer l’attitude suivante :
 systématique en cas de malformation fœtale associée (soit pour documenter une malformation létale, soit pour guider la prise en charge d’une malformation non létale) et en cas de RCIU inexpliqué associé ;
systématique en cas de malformation fœtale associée (soit pour documenter une malformation létale, soit pour guider la prise en charge d’une malformation non létale) et en cas de RCIU inexpliqué associé ;
 peu utile dans les hydramnios fonctionnels de l’insuffisance cardiaque, de l’anémie, du STT ou du diabète ;
peu utile dans les hydramnios fonctionnels de l’insuffisance cardiaque, de l’anémie, du STT ou du diabète ;
 conseillée dans l’hydramnios isolé mais important où des ponctions évacuatrices sont nécessaires ;
conseillée dans l’hydramnios isolé mais important où des ponctions évacuatrices sont nécessaires ;
Hydramnios aigu
L’hydramnios aigu est considérable (10 L et plus), souvent précoce (fin du 2e trimestre) et il évolue sur quelques jours. Il entraîne un retentissement fonctionnel évident : gêne respiratoire, douleurs, vomissements, œdèmes… L’utérus est énorme et constamment dur sous la sonde.
L’échographie retrouve parfois une malformation (anencéphalie, tératome sacro-coccygien), mais l’étiologie essentielle est la grossesse gémellaire monochoriale diamniotique avec déséquilibre des circulations fœtoplacentaires (syndrome transfuseur–transfusé ou STT). Le fœtus transfusé flotte dans une immense « piscine », alors que l’autre fœtus, le transfuseur (hypotrophique), est parfois difficile à retrouver, plaqué en périphérie dans son sac amniotique sans liquide (jumeau « coincé » ou stuck-twin). Le pronostic est dans tous les cas très réservé, la prise en charge reposant sur les ponctions évacuatrices répétées et la coagulation par laser des anastomoses placentaires (voir chap. 18, Grossesses gémellaires).
Oligoamnios (fig. 5.5 et 5.7)
Selon les sources, sa fréquence varie dans une large fourchette, 0,4 et 4 % des grossesses. En théorie, on parlera d’oligoamnios (ou oligohydramnios ou oligoanamnios) quand la quantité de liquide est inférieure à 250 mL à terme. En pratique, la définition et le diagnostic sont exclusivement échographiques car la clinique est extrêmement pauvre : l’oligoamnios est franc ou sévère quand la plus grande citerne visible est inférieure à 2 cm ou l’index amniotique inférieur à 5.
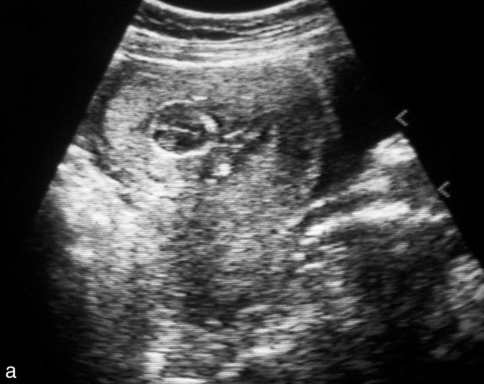
a. Anamnios précoce (2 mois et demi), seul le crâne est bien identifiable.
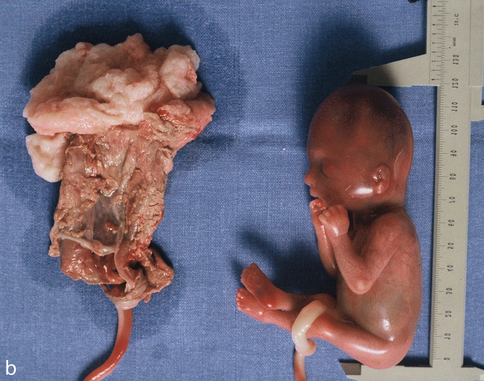
b. Le placenta est extrachorial (les membranes s’insèrent en dedans de la surface placentaire), le sac est petit et le cordon en sort par un orifice beaucoup plus petit que le fœtus. Noter l’absence de spiralisation du cordon par immobilisme fœtal précoce.
L’absence totale de liquide amniotique définit l’anamnios où les seules lacunes liquidiennes autour du fœtus correspondent à des coupes du cordon (fig. 5.5). La définition classique exclut la perte de liquide par rupture des membranes mais il s’agit d’une subtilité nosologique sans utilité pratique : le terme d’oligoamnios est avant tout descriptif et la fuite de liquide est la première étiologie recherchée.
L’enquête étiologique recherchera donc :
 avant tout, l’hypoplasie pulmonaire qui compromet le pronostic vital ;
avant tout, l’hypoplasie pulmonaire qui compromet le pronostic vital ;
 le syndrome d’immobilité fœtale par compression (déformations du squelette avec pied bot et dolichocéphalie, raideurs articulaires, hypotrophie musculaire) dont le pronostic est bon ;
le syndrome d’immobilité fœtale par compression (déformations du squelette avec pied bot et dolichocéphalie, raideurs articulaires, hypotrophie musculaire) dont le pronostic est bon ;
 l’infection ovulaire qui peut être la cause ou la conséquence de la rupture des membranes ;
l’infection ovulaire qui peut être la cause ou la conséquence de la rupture des membranes ;
 la prématurité soit spontanée, soit provoquée ;
la prématurité soit spontanée, soit provoquée ;
 les dystocies diverses lors de l’accouchement (dynamique ou mécanique), et la souffrance fœtale par compression du cordon.
les dystocies diverses lors de l’accouchement (dynamique ou mécanique), et la souffrance fœtale par compression du cordon.
Oligoamnios par fuite de liquide amniotique
La fuite de liquide amniotique, par rupture prématurée des membranes (RPM), est souvent évidente à l’interrogatoire et à l’examen au spéculum montrant l’écoulement en provenance du col ou une quantité anormale de liquide dans le vagin. En cas de doute, divers tests vaginaux sont proposés, plus ou moins spécifiques du liquide amniotique : mesure du pH, test de cristallisation, recherche de cellules fœtales, dosage de la diamine-oxydase, de l’α-fœtoprotéine, de l’IGFBP1.
La grossesse extramembraneuse (fig. 5.7) est un cas particulier et rare. Lorsque la rupture des membranes se produit très tôt, au 1er trimestre et avant l’accolement des caduques, et si l’avortement ne se produit pas rapidement (comme c’est le plus souvent le cas), on peut assister au développement d’une grossesse extramembraneuse. Le liquide amniotique s’évacue, la cavité amniotique cesse de grandir, le fœtus quitte la poche amniochoriale qui se rétracte progressivement sur le placenta formant une corolle avec un petit orifice d’où sort le cordon. Le fœtus se développe alors en dehors de l’amnios, dans la cavité utérine tapissée par la caduque pariétale.
 l’anamnios n’est pas spécifique mais il est total car l’œuf est ouvert en permanence (fig. 5.7a) ;
l’anamnios n’est pas spécifique mais il est total car l’œuf est ouvert en permanence (fig. 5.7a) ;
 le fœtus est immobile (également non spécifique) ;
le fœtus est immobile (également non spécifique) ;
 le placenta est hyperéchogène, épais et « tassé » par la rétraction utérine.
le placenta est hyperéchogène, épais et « tassé » par la rétraction utérine.
Le diagnostic de grossesse extramembraneuse est surtout rétrospectif à l’examen du placenta ou du produit d’expulsion (fig. 5.7b) : le placenta est largement extrachorial avec un sac inséré près de l’émergence du cordon, le sac membraneux est petit et le cordon en sort par un orifice beaucoup plus petit que le fœtus.
En dehors de ce cas très particulier, le pronostic de la rupture prématurée des membranes est toujours difficile à établir avec précision. C’est avant tout le risque d’hypoplasie pulmonaire que l’on cherche à évaluer :
 la date de la rupture constitue le premier facteur pronostique, unanimement admis par tous les auteurs :
la date de la rupture constitue le premier facteur pronostique, unanimement admis par tous les auteurs :
 avant 17 SA (fig. 5.5c), les chances de survie sans séquelles sont très faibles et l’interruption de grossesse est une option raisonnable,
avant 17 SA (fig. 5.5c), les chances de survie sans séquelles sont très faibles et l’interruption de grossesse est une option raisonnable,
 entre 17 et 26 SA, le risque d’hypoplasie va décroissant avec un taux de 50 % vers 20 SA, l’expectative sans traitement est le plus souvent proposée,
entre 17 et 26 SA, le risque d’hypoplasie va décroissant avec un taux de 50 % vers 20 SA, l’expectative sans traitement est le plus souvent proposée,
 après 26 SA, l’hypoplasie est plus rare et une attitude plus active est recommandée (prévention de la prématurité, de la maladie des membranes hyalines et de l’infection) d’autant que l’on entre dans la période de viabilité médicale ;
après 26 SA, l’hypoplasie est plus rare et une attitude plus active est recommandée (prévention de la prématurité, de la maladie des membranes hyalines et de l’infection) d’autant que l’on entre dans la période de viabilité médicale ;
 la sévérité de l’oligoamnios : la récupération intermittente ou permanente d’un volume de liquide normal améliore nettement le pronostic ;
la sévérité de l’oligoamnios : la récupération intermittente ou permanente d’un volume de liquide normal améliore nettement le pronostic ;
 la durée de la rupture (c’est-à-dire la durée d’exposition du fœtus à l’oligoamnios) n’apparaît pas, isolément, comme un facteur déterminant car elle est largement dépendante de la date de la rupture ;
la durée de la rupture (c’est-à-dire la durée d’exposition du fœtus à l’oligoamnios) n’apparaît pas, isolément, comme un facteur déterminant car elle est largement dépendante de la date de la rupture ;
 l’étude échographique des poumons fœtaux est pour le moment assez décevante :
l’étude échographique des poumons fœtaux est pour le moment assez décevante :
 les mouvements respiratoires ne sont pas corrélés avec la présence ou l’absence d’hypoplasie,
les mouvements respiratoires ne sont pas corrélés avec la présence ou l’absence d’hypoplasie,
 l’échogénicité pulmonaire (en comparaison avec le foie) n’apporte pas d’information fiable,
l’échogénicité pulmonaire (en comparaison avec le foie) n’apporte pas d’information fiable,
 le volume pulmonaire peut être évalué par le calcul de la surface pulmonaire sur une coupe transversale du thorax (ou en reconstruction 3D) mais la mesure est d’autant plus difficile que l’oligoamnios est sévère et que la grossesse est avancée,
le volume pulmonaire peut être évalué par le calcul de la surface pulmonaire sur une coupe transversale du thorax (ou en reconstruction 3D) mais la mesure est d’autant plus difficile que l’oligoamnios est sévère et que la grossesse est avancée,
 le Doppler des artères pulmonaires a été proposé dans cette indication car l’hypoplasie entraîne une élévation des résistances.
le Doppler des artères pulmonaires a été proposé dans cette indication car l’hypoplasie entraîne une élévation des résistances.
 l’IRM serait plus performante pour le calcul du volume pulmonaire mais également plus gênée par les mouvements fœtaux (et par les restrictions pour l’usage du galodinium).
l’IRM serait plus performante pour le calcul du volume pulmonaire mais également plus gênée par les mouvements fœtaux (et par les restrictions pour l’usage du galodinium).
Oligoamnios par insuffisance de production
 les uronéphropathies : il s’agit soit d’atteintes rénales bilatérales sévères (agénésies rénales, dysplasies multikystiques ou polykystoses rénales), soit d’uropathies obstructives bilatérales ou basses (valves de l’urètre postérieur, mégavessie, obstructions pyélo-urétérales bilatérales). On peut considérer que toutes les uronéphropathies qui s’accompagnent d’un oligoamnios ont un pronostic catastrophique (voir chap. 14) ;
les uronéphropathies : il s’agit soit d’atteintes rénales bilatérales sévères (agénésies rénales, dysplasies multikystiques ou polykystoses rénales), soit d’uropathies obstructives bilatérales ou basses (valves de l’urètre postérieur, mégavessie, obstructions pyélo-urétérales bilatérales). On peut considérer que toutes les uronéphropathies qui s’accompagnent d’un oligoamnios ont un pronostic catastrophique (voir chap. 14) ;
 l’insuffisance rénale fonctionnelle accompagne la plupart des retards de croissance intra-utérins (RCIU). L’oligoamnios est un indice de gravité très important. Il est secondaire à une redistribution vasculaire qui privilégie les organes nobles (cerveau et cœur) au détriment des autres, en particuliers les reins d’où un effondrement de la fonction rénale fœtale et une chute de la diurèse. Le problème devient celui de l’étiologie du RCIU (voir chap. 7) : ou bien il existe une insuffisance vasculaire utéroplacentaire, ou bien il faut rechercher une fœtopathie (malformation, anomalie chromosomique, infection). Une atteinte rénale directe, et souvent réversible, peut se rencontrer dans certaines infections virales (CMV, parvovirus B19 : voir chapitre 17) ou de traitements maternels (anti-inflammatoires non stéroïdiens, anti-hypertenseurs type IEC) ;
l’insuffisance rénale fonctionnelle accompagne la plupart des retards de croissance intra-utérins (RCIU). L’oligoamnios est un indice de gravité très important. Il est secondaire à une redistribution vasculaire qui privilégie les organes nobles (cerveau et cœur) au détriment des autres, en particuliers les reins d’où un effondrement de la fonction rénale fœtale et une chute de la diurèse. Le problème devient celui de l’étiologie du RCIU (voir chap. 7) : ou bien il existe une insuffisance vasculaire utéroplacentaire, ou bien il faut rechercher une fœtopathie (malformation, anomalie chromosomique, infection). Une atteinte rénale directe, et souvent réversible, peut se rencontrer dans certaines infections virales (CMV, parvovirus B19 : voir chapitre 17) ou de traitements maternels (anti-inflammatoires non stéroïdiens, anti-hypertenseurs type IEC) ;
 les anomalies chromosomiques sont rarement en cause et, a priori, l’oligoamnios isolé n’est pas une indication de caryotype fœtal. En cas de RCIU, le risque d’anomalie chromosomique serait même plus faible en présence d’un oligoamnios.
les anomalies chromosomiques sont rarement en cause et, a priori, l’oligoamnios isolé n’est pas une indication de caryotype fœtal. En cas de RCIU, le risque d’anomalie chromosomique serait même plus faible en présence d’un oligoamnios.
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree