Chapitre 2 Imagerie digestive
Techniques d’imagerie
Modalités d’imagerie disponibles
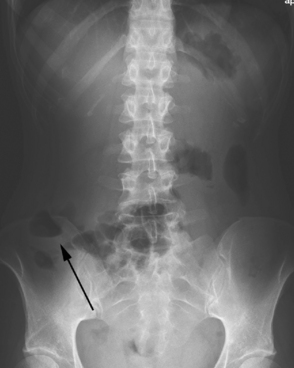
Pendant des décennies, le cliché d’abdomen sans préparation a constitué l’examen de débrouillage en pathologie digestive (fig. 2.1). On pouvait réaliser jusqu’à six clichés : un cliché centré sur les coupoles en position debout, un grand cliché d’ensemble en décubitus dorsal puis en position debout, deux clichés en décubitus latéral droit et gauche et un cliché sur le pelvis. Il existait d’autres clichés plus spécifiques, centrés sur le pancréas et la vésicule. Aujourd’hui, il n’existe quasiment plus aucune indication à réaliser un cliché d’abdomen sans préparation. On peut s’en servir pour chercher un pneumopéritoine en cas de douleurs abdominales aiguës et de contracture, mais on sait que les pneumopéritoines de petite abondance ne sont pas détectés sur l’abdomen sans préparation et que l’examen tomodensitométrique est beaucoup plus fiable.
L’abdomen sans préparation peut également, et c’est probablement l’indication la plus raisonnable, servir au cours des syndromes occlusifs. Il apporte une aide au diagnostic positif en montrant une dilatation des anses intestinales lorsque l’examen clinique est difficile. Il peut surtout être utilisé lors de la surveillance du syndrome occlusif lorsqu’un traitement médical avec aspiration digestive a été institué. Cependant, dans la majorité des cas, il n’est pas utile si un examen tomodensitométrique est réalisé.
Les opacifications digestives – transit œso-gastro-duodénal, transit du grêle, lavement baryté – ont elles aussi perdu quasiment toutes leurs indications. Il n’est plus question de chercher une pathologie tumorale ou ulcéreuse gastrique par une opacification, ni de dépister un polype ou un cancer du côlon ou du rectum par un lavement baryté.
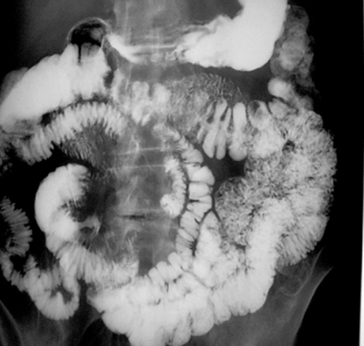
Le transit du grêle a résisté un peu plus longtemps compte tenu de la difficulté de l’exploration endoscopique à ce niveau (fig. 2.2). Il a lui aussi aujourd’hui disparu au profit de méthodes endoscopiques avancées ou de l’imagerie par résonance magnétique. En centre spécialisé, il arrive encore que certaines anastomoses soient opacifiées par des produits hydrosolubles avant rétablissement de la continuité lors de chirurgie abdominale complexe, afin de vérifier l’absence de fuite anastomotique. Il est donc important que l’on tende à contribuer à la diminution de ces examens d’opacification en discutant chaque indication et en les réservant à des indications très sélectionnées.
En raison de sa simplicité et de sa diffusion, l’échographie abdominale constitue fréquemment l’examen de première intention pour l’étude de la pathologie digestive. Performante pour analyser les organes pleins de la cavité abdominale – foie, rate, pancréas – elle a été également utilisée par certains, avec moins de succès, pour la pathologie colique, voire grêle.
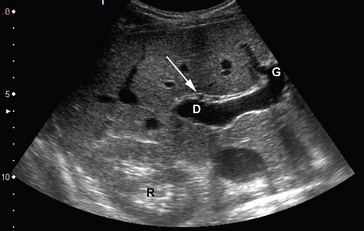
L’échographie Doppler permet l’analyse des vaisseaux abdominaux, artériels et veineux. Incontournable dans les années 1980, elle est maintenant à la fois concurrente et complémentaire du scanner et de l’IRM. L’avantage de l’échographie tient en sa simplicité et sa diffusion. Elle souffre considérablement de son caractère opérateur-dépendant et des performances extraordinaires qu’obtiennent aujourd’hui la tomodensitométrie et surtout l’imagerie par résonance magnétique pour l’exploration de l’abdomen. On peut considérer que l’échographie reste l’examen de première intention pour la pathologie hépatovésiculaire et qu’elle peut être utilisée pour le dépistage d’une lésion pancréatique ou splénique (fig. 2.3).
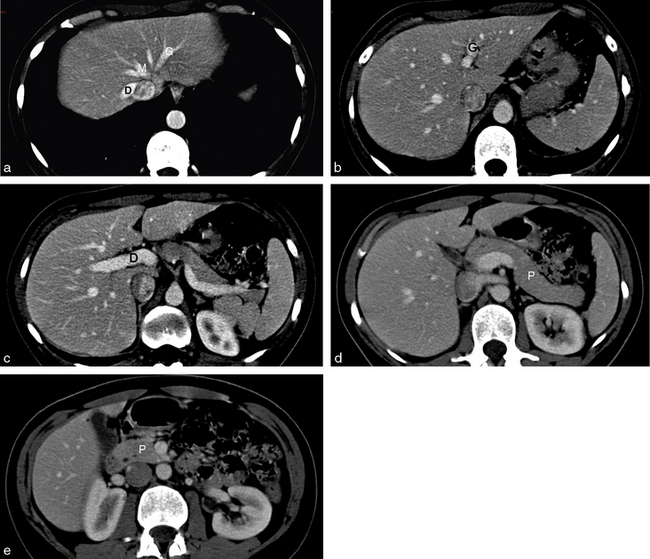
L’examen tomodensitométrique était au début relativement peu adapté à l’analyse de la cavité abdominale. À l’heure actuelle, les appareils modernes multidétecteurs permettent l’exploration de la cavité abdominale avant injection, lors d’un temps artériel puis lors d’un temps portal en quelques secondes (fig. 2.4). L’examen tomodensitométrique peut être utilisé en pathologie hépatique, pancréatique, splénique, et pour l’analyse du tube digestif. Dans l’ensemble des indications, il est largement concurrencé par l’imagerie par résonance magnétique, caractérisée par un contraste spontané de grande qualité.
L’imagerie par résonance magnétique est devenue l’examen de référence absolument indispensable et strictement indiscutable pour la pathologie neurologique. L’histoire de l’évolution de l’imagerie montre bien que l’exploration des différents appareils en imagerie médicale a toujours suivi l’exemple de l’imagerie neurologique. C’est en imagerie de l’encéphale que le scanner a été utilisé en premier, il en a été de même pour l’IRM. On pourrait multiplier les exemples avec les différentes techniques utilisées en tomodensitométrie ou en imagerie par résonance magnétique, qui ont toujours été introduites initialement par l’imagerie de l’encéphale. Ainsi, il n’est pas très difficile de prédire qu’à court terme, c’est l’imagerie par résonance magnétique qui sera l’examen de référence pour l’analyse de l’ensemble des pathologies digestives. C’est en fait déjà largement le cas pour l’exploration des pathologies hépatique, pancréatique, splénique et du tube digestif (fig. 2.5).
En matière de pathologie hépatique, c’est le contraste spontané de très haute qualité, bien supérieur à celui obtenu en scanner, qui permet fréquemment de répondre aux questions sans qu’il soit besoin d’injecter de produit de contraste. En pathologie vésiculaire, biliaire et pancréatique, les techniques qui permettent l’analyse canalaire, cholangiopancréatographie et wirsungographie par résonance magnétique, fournissent des renseignements anatomiques de très haute qualité et sont devenues indispensables à l’analyse de la pathologie kystique.
En matière de pathologie de l’intestin grêle, entéro- IRM et entéroscanner sont à la fois concurrents et complémentaires, mais il est certain que l’entéro-IRM, année après année, gagne du terrain. Elle a pour principal avantage d’être une technique non irradiante, indispensable chez les patients atteints de maladie inflammatoire, qui sont des maladies chroniques intéressant des sujets jeunes. Finalement, ce n’est que dans les situations d’urgence que l’imagerie par résonance magnétique laisse encore le champ libre au scanner. Il s’agit en fait principalement de commodité par plus grande disponibilité du scanner, car il faut bien dire que la majorité des situations d’urgence pourrait être explorée en IRM, mais il est vrai que la disponibilité et la rapidité d’acquisition en scanner ne rendent pas urgente cette substitution.
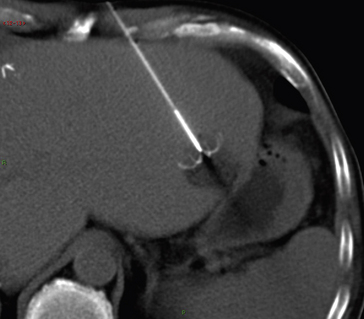
L’imagerie d’intervention ou radiologie interventionnelle a pris une place très importante en matière de thérapeutique digestive. En pathologie hépatique, la ponction-biopsie hépatique d’une tumeur hépatique sous contrôle échographique ou tomodensitométrique est devenue la modalité de référence pour l’obtention d’un prélèvement histologique. En pathologie tumorale, il existe un large éventail de modalités d’intervention – destruction locale d’une tumeur par radiofréquence, chimio-embolisation de carcinome hépatocellulaire multi focal par injection directement dans l’artère hépatique de l’agent de chimiothérapie et d’un produit d’embolisation, embolisation artérielle d’une tumeur hépatique compliquée d’hémorragie active (fig. 2.6). En pathologie vésiculaire et biliaire, les drainages biliaires externes, la mise en place par voie percutanée de prothèses endobiliaires et le drainage de cholécystite alithiasique sont des interventions très couramment réalisées. Plus généralement, le drainage des abcès abdominaux est désormais un acte de pratique courante ; utilisé initialement pour les abcès simples, cette méthode s’est étendue aux abcès complexes, mal limités, à contenu épais, avec des débris, multiloculés, voire même avec des fistules intestinales. Parallèlement, les embolisations d’hémostase peuvent concerner l’ensemble du secteur artériel à l’origine d’une hémorragie active.
Place de l’imagerie
Pour l’analyse de la pathologie du tube digestif, les examens d’endoscopie sont généralement effectués de première intention pour l’œsophage, l’estomac, le duodénum et le cadre colique. L’imagerie est utilisée dans le cadre du bilan d’extension des tumeurs du tube digestif. Pour la pathologie du grêle, entéroscanner et entéro-IRM sont à la fois concurrents et complémentaires.
C’est évidemment le cas des douleurs abdominales extraordinairement fréquentes et plus généralement des troubles fonctionnels digestifs, qu’il s’agisse de la sphère haute (dyspepsie) ou de la sphère basse (troubles fonctionnels intestinaux) (Encadré 2.1). Dans ce cadre pathologique, il est évidemment indispensable de ne pas passer à côté d’une affection organique, et il est donc souvent licite de réaliser une endoscopie haute ou une endoscopie basse, voire une échographie. Mais il importe de ne pas multiplier ou répéter les examens d’imagerie qui n’ont pas d’intérêt diagnostique.
Encadré 2.1 Troubles fonctionnels digestifs
Le terme très vague de dyspepsie, qui correspond à ce que les patients expriment souvent sous le terme de digestion difficile, traduit un dysfonctionnement du tube digestif supérieur. Il peut s’agir de phénomène douloureux, de crampes, de brûlures, d’une tendance nauséeuse, parfois de vomissements. L’état général est parfaitement conservé, l’examen clinique est tout à fait normal. On n’a jamais mis en évidence de support organique crédible à ces manifestations cliniques. L’objectif est évidemment, chez ces patients, de ne pas multiplier les investigations complémentaires. S’ils consultent un gastro-entérologue, une fibroscopie œso-gastro-duodénale est généralement réalisée et une échographie est fréquemment prescrite. Il s’agit de limiter les explorations complémentaires à ces examens simples, de ne pas demander d’autres examens – scanner, IRM – et de ne pas les répéter.
 Il n’existe quasiment plus aucune indication à réaliser un cliché d’abdomen sans préparation.
Il n’existe quasiment plus aucune indication à réaliser un cliché d’abdomen sans préparation.
 Les opacifications digestives (transit œso-gastro-duodénal, transit du grêle, lavement baryté) ont elle aussi perdu presque toutes leurs indications.
Les opacifications digestives (transit œso-gastro-duodénal, transit du grêle, lavement baryté) ont elle aussi perdu presque toutes leurs indications.
 L’échographie abdominale constitue l’examen de première intention pour analyser les organes pleins de la cavité abdominale et la pathologie biliaire.
L’échographie abdominale constitue l’examen de première intention pour analyser les organes pleins de la cavité abdominale et la pathologie biliaire.
 L’examen tomodensitométrique peut être utilisé en pathologie hépatique, pancréatique, splénique et pour l’analyse du tube digestif.
L’examen tomodensitométrique peut être utilisé en pathologie hépatique, pancréatique, splénique et pour l’analyse du tube digestif.
 Le scanner reste l’examen de référence dans toutes les situations d’urgences : douleur abdominale aiguë, occlusion intestinale, traumatisme abdominal.
Le scanner reste l’examen de référence dans toutes les situations d’urgences : douleur abdominale aiguë, occlusion intestinale, traumatisme abdominal.
 L’imagerie par résonance magnétique devient l’examen de référence dans de nombreux domaines de la pathologie digestive, notamment en matière de pathologies hépatique, biliaire, pancréatique, du grêle et rectale.
L’imagerie par résonance magnétique devient l’examen de référence dans de nombreux domaines de la pathologie digestive, notamment en matière de pathologies hépatique, biliaire, pancréatique, du grêle et rectale.
 L’imagerie d’intervention ou radiologie interventionnelle a pris une place thérapeutique très importante, notamment en pathologie tumorale.
L’imagerie d’intervention ou radiologie interventionnelle a pris une place thérapeutique très importante, notamment en pathologie tumorale.
Pathologie hépatique
Cirrhose
La cirrhose hépatique est définie par l’association de trois lésions : une destruction des hépatocytes, ou nécrose hépatocytaire, le développement d’une fibrose hépatique, conséquence de cette destruction hépatocytaire, et la réorganisation des hépatocytes sous la forme de nodules de régénération. En fonction de la taille des nodules de régénération, on distingue les cirrhoses micronodulaires (les nodules de régénération ont moins de 3 mm de diamètre) des cirrhoses macronodulaires (les nodules de régénération ont plus de 3 mm de diamètre).
L’hypertension portale se traduit le plus souvent par la survenue d’hémorragies digestives.
Le score de MELD (pour Model for End-stage Liver Disease), initialement utilisé pour sélectionner les candidats à la transplantation hépatique, est également fréquemment utilisé pour évaluer la sévérité d’une cirrhose (Encadré 2.2). Ce score prend en compte les valeurs de la bilirubinémie, de l’INR (taux de prothrombine normalisé) et de la créatininémie.
Encadré 2.2 Transplantation hépatique
Les complications de la transplantation hépatique sont dominées par le rejet qui peut se faire sous une forme aiguë ou chronique et par des complications qui peuvent intéresser l’anastomose artérielle, l’anastomose portoporte ou l’anastomose biliaire.
Imagerie
L’échographie est réalisée de première intention en casde suspicion de cirrhose. En fonction du stade évolutif, le volume hépatique peut être normal, augmenté ou diminué. On cherche des anomalies du foie qui peut être plus échogène et d’échostructure plus grossière que celle d’un foie normal, ainsi que des anomalies des contours. Les contours du foie sont normalement lisses, alors qu’ils deviennent bosselés en cas de cirrhose, traduisant l’existence de nodules de régénération (fig. 2.7).
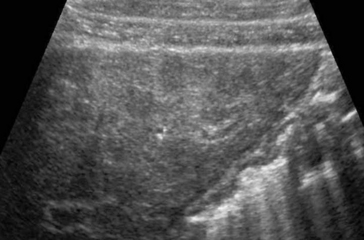
Fig. 2.7 Cirrhose hépatique : échographie.
Noter l’échostructure du parenchyme hépatique grossière et irrégulière.
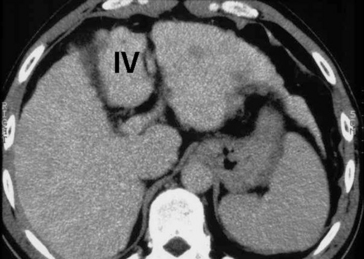
On cherche également une dysmorphie hépatique (Encadré 2.3) associant l’atrophie du foie droit et du segment IV, à une hypertrophie du lobe gauche et du lobe caudé (segment I) (fig. 2.9 et 2.10).
Encadré 2.3 Segmentation hépatique
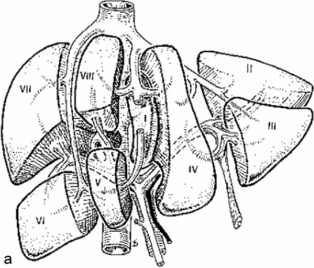
C’est un chirurgien français, Claude Couinaud, qui a proposé de diviser le foie en huit segments. Cette classification est actuellement universellement utilisée (fig. 2.8 a,b).
• Le segment I correspond au lobe caudé, ou lobe de Spiegel. Il est compris entre la face antérieure de la veine cave et la face postérieure de la veine porte.
• Le lobe gauche du foie est divisé en deux segments : le segment II en haut (et en arrière), le segment III en bas (et en avant). On parle également pour la réunion de ces segments II et III du secteur latéral gauche.
• Le segment IV correspond au segment interposé entre le lobe gauche et le foie droit. Il correspond au lobe carré. On parle également parfois de secteur paramédian gauche.
• Le foie droit est divisé en deux secteurs :
Les trois méthodes d’imagerie – échographie, tomodensitométrie et imagerie par résonance magnétique – sont très sensibles pour la détection d’une ascite, même d’abondance minime (fig. 2.11).
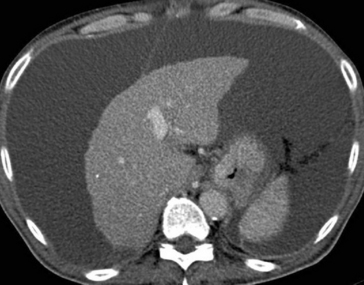
Fig. 2.11 Ascite : examen tomodensitométrique.
On note une atrophie hépatique marquée et un très important épanchement intrapéritonéal libre.
L’échographie, la tomodensitométrie et l’imagerie par résonance magnétique permettent de poser le diagnostic d’hypertension portale par la mise en évidence d’une splénomégalie (signe sensible mais peu spécifique) et surtout de dérivations portocaves qui, du fait de l’augmentation de la pression dans le système porte, font communiquer le système porte et le système cave (Encadré 2.4).
Encadré 2.4 Hypertension portale
Les blocs intrahépatiques sont dus le plus souvent à une cirrhose.
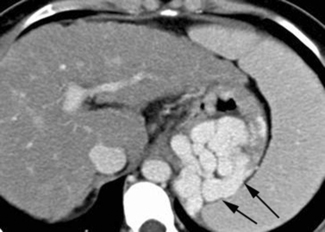
L’augmentation de la pression portale se traduit par une splénomégalie, une dilatation des veines mésentériques et portales et le développement d’anastomoses portocaves (fig. 2.12). Ces dérivations portocaves sont au nombre de cinq :
• dérivations portocaves supérieures entre la veine gastrique gauche (système porte) et les veines gastriques et œsophagiennes (système azygos tributaire du système cave) qui vont former les varices gastriques ou œsophagiennes susceptibles de saigner ;
• dérivations portocaves postérieures entre la veine splénique et la veine rénale, soit de façon directe – on parle de dérivations splénorénales directes –, soit par l’intermédiaire des vaisseaux courts de l’estomac – on parle de dérivations spléno-gastro-rénales ou splénorénales indirectes. Dans ce deuxième cas, des varices gastriques aptes à saigner peuvent également se développer ;
• dérivations portocaves antérieures, par la reperméation de la veine para-ombilicale qui fait communiquer la branche portale gauche et des veines de la paroi abdominale antérieure, tributaires du système cave ;
• dérivations portocaves inférieures entre la veine mésentérique inférieure (système porte) et les veines hémorroïdaires (système cave) ;
• il existe également des anastomoses portocaves intrahépatiques et de multiples dérivations portocaves atypiques qui peuvent se faire à travers le rétropéritoine, par l’intermédiaire des vaisseaux de l’intestin grêle ou du côlon ou à travers des adhérences secondaires à une intervention chirurgicale.
Le dépistage classique du carcinome hépatocellulaire sur cirrhose était réalisé par l’association du dosage (sérique) du taux d’alpha-fœtoprotéine tous les 6 mois, alterné avec la réalisation semestrielle également d’une échographie. On tend à l’heure actuelle à abandonner le dosage du taux de l’alpha-fœtoprotéine qui est le plus fréquemment normal en cas de petit carcinome hépatocellulaire. Il est donc logique de réaliser une échographie semestrielle de dépistage. Il est important qu’elle soit réalisée par un radiologue échographiste rompu à la pathologie hépatique et que le même médecin effectue ce dépistage année après année.
 L’imagerie participe au diagnostic de cirrhose et a une place majeure pour le diagnostic de ses complications.
L’imagerie participe au diagnostic de cirrhose et a une place majeure pour le diagnostic de ses complications.
 L’échographie constitue l’examen de première intention.
L’échographie constitue l’examen de première intention.
 Elle peut être complétée par un examen tomodensitométrique, mais surtout par une imagerie par résonance magnétique.
Elle peut être complétée par un examen tomodensitométrique, mais surtout par une imagerie par résonance magnétique.
 Quelle que soit la technique utilisée, les signes de cirrhose associent des anomalies des bords du foie, une dysmorphie hépatique et la présence d’un épanchement intrapéritonéal libre et de signes d’hypertension portale.
Quelle que soit la technique utilisée, les signes de cirrhose associent des anomalies des bords du foie, une dysmorphie hépatique et la présence d’un épanchement intrapéritonéal libre et de signes d’hypertension portale.
 Le dépistage du carcinome hépatocellulaire sur cirrhose est réalisé par une échographie tous les 6 mois.
Le dépistage du carcinome hépatocellulaire sur cirrhose est réalisé par une échographie tous les 6 mois.
Tumeurs du foie
Tumeurs malignes du foie
Carcinome hépatocellulaire
Le carcinome hépatocellulaire est une lésion tumorale qui se développe dans la majorité des cas sur un foie de cirrhose. C’est la tumeur maligne hépatique primitive la plus fréquente. Le carcinome hépatocellulaire peut compliquer une cirrhose alcoolique, mais il est encore plus fréquent chez les patients atteints de cirrhose post-hépatitique B et surtout de cirrhose post-hépatitique C. Le carcinome hépatocellulaire peut être diagnostiqué lors de symptômes propres à la tumeur – douleurs, altération de l’état général –, lors de la décompensation d’une cirrhose jusque-là compensée ou, très fréquemment à l’heure actuelle, lors de la surveillance régulière de patients atteints de cirrhose. C’est donc l’échographie qui, réalisée régulièrement chez un malade atteint de cirrhose, décèle l’existence d’une lésion arrondie, souvent hypo-échogène, parfois hétérogène (« Sur le vif » 2.1). Certains complètent cette échographie par une échographie avec injection de produit de contraste ultrasonore qui démontre le caractère hypervasculaire du carcinome hépatocellulaire au temps artériel et le lavage de la lésion au temps portal.
Sur le vif 2.1 Carcinome hépatocellulaire sur cirrhose
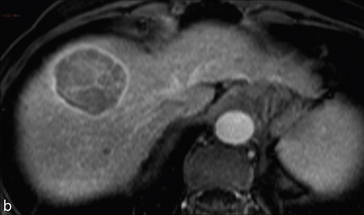
Le diagnostic le plus probable est celui de carcinome hépatocellulaire sur cirrhose. On décide de réaliser un examen par résonance magnétique. Cet examen montre un nodule de 4 cm bien limité, très hétérogène, à l’origine d’un hypersignal sur la séquence pondérée en T2 avec un liséré périphérique (fig. 2.13).
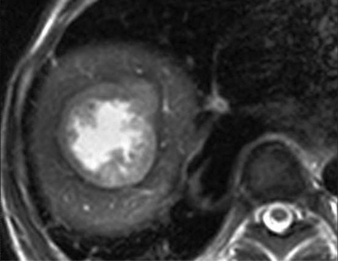
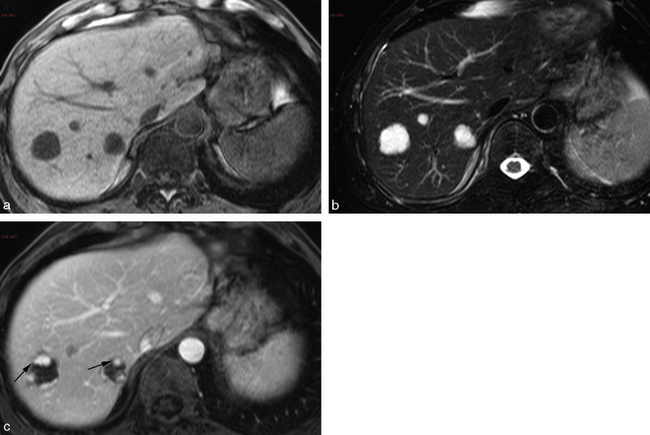
Fig. 2.13 Carcinome hépatocellulaire sur cirrhose.
Il existe une lésion arrondie, hétérogène, bien limitée, développée au sein d’un foie cirrhotique.
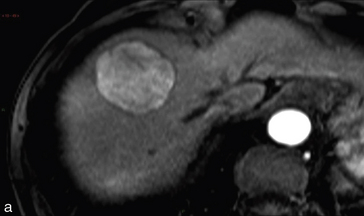
Comme en échographie, la tomodensitométrie et l’imagerie par résonance magnétique sont aptes à montrer le caractère hypervascularisé de la lésion au temps artériel avec lavage au temps portal. C’est-à-dire que la lésion est rehaussée plus que le reste du foie au temps artériel et au contraire moins que le reste du foie sur les temps portal et tardif (fig. 2.14). On cherche de plus une hétérogénéité de la lésion et un éventuel liséré péritumoral correspondant à une capsule ou à une pseudo-capsule. Il est important de mesurer le plus grand diamètre de la lésion, de chercher d’autres localisations et une extension aux structures de voisinage. L’extension la plus fréquente se fait vers les branches de la veine porte qui sont obstruées par une extension de la tumeur. L’ensemble de ces données participe au choix de la meilleure option thérapeutique. Il est important de souligner qu’il est maintenant possible de porter définitivement le diagnostic de carcinome hépatocellulaire sur les seuls critères de l’imagerie à la condition qu’on visualise, sur un foie de cirrhose, une lésion plus rehaussée que le reste du foie au temps artériel – c’est ce que les Anglais appellent le wash-in – et moins rehaussée que le reste du foie au temps portal – c’est ce que les Anglais appellent le wash-out. On parle à ce propos de critères de Barcelone.
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree