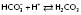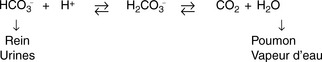15 Régulation de l’équilibre acide-base
Définitions
Le pH
Le pH exprime l’acidité ou l’alcalinité d’un milieu, il est lié à la concentration en ions H+.
Seules de faibles variations (6,90–7,70) sont compatibles avec la vie.
Régulation
• les systèmes tampons (moyens de lutte quasi instantanés, automatiques mais vite débordés car limités par les concentrations de leurs divers composants) ;
• les poumons puis les reins (moyens de lutte plus longs à se mettre en œuvre mais d’une plus grande efficacité et permettant en conditions physiologiques une restauration complète du pH).
Systèmes tampons
Si l’organisme est soumis à un acide fort, la partie basique du système tampon va réagir : l’ion bicarbonate (HCO3−) s’associe avec l’ion H+ en excès pour former de l’acide carbonique qui se dissocie en dioxyde de carbone (CO2) et en eau (H2O), éliminés par les poumons sous forme de CO2 et de vapeur d’eau (figure 16).
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree