Chapitre 1
Imagerie post-thérapeutique des gliomes de haut grade
J.-P. Cottier, M. Ribeiro, S. Chapet, C. Destrieux, X. Cazals, M.-A. Lauvin, Y. Pointreau and A. Raimbault
L’incidence des gliomes est estimée en France à 6/100 000 habitants par an et cette incidence est en augmentation progressive et régulière depuis 1950 [1]. Ils représentent actuellement en France 42 % des tumeurs cérébrales primitives, et chez l’adulte 80 % de ces gliomes sont malins (10 % de grade IV et 70 % de grade III) [2]. Avec des médianes de survie de 14 mois, leur pronostic est redoutable [3].
Place de la thérapeutique oncologique médicale et radiothérapique
Indications de la chimio et radiothérapie
Radiothérapie
La radiothérapie est la thérapeutique la plus généralement proposée en postopératoire ou après biopsie lorsque la résection optimale n’est pas envisageable. Dans une méta-analyse canadienne, Laperriere et al. [4] ont analysé 758 observations issues de 6 essais randomisés comparant la radiothérapie postopératoire à l’absence de traitement complémentaire. Ils retrouvaient un bénéfice significatif (p < 0,00001) en termes de survie en cas de radiothérapie par rapport aux soins de confort seuls.
Chimiothérapie
Les nitroso-urées étaient les chimiothérapies le plus souvent utilisées après traitement radiochirurgical. Dans une méta-analyse regroupant 12 essais randomisés de chimiothérapie adjuvante, l’apport des nitroso-urées représentait un gain de survie absolue de 6 % à 1 an et une réduction relative de 15 % du risque de décès [5].
Chimioradiothérapie concomitante
Une des voies de recherche pour améliorer les résultats des traitements adjuvants des gliomes de haut grade a été la radiosensibilisation de ces tumeurs hypoxiques effectuée soit par l’inhalation d’oxygène associé à du dioxyde de carbone, soit par l’utilisation d’un dérivé imidazolé. Les résultats n’ont pas été concluants alors que la synergie entre un agent alkylant : le témolozomide (TMZ : Temodal) et les radiations ionisantes s’est révélée plus efficace. Initialement utilisé dans les récidives de gliomes de haut grade aux doses de 150 à 200 mg/m2, per os, 5 jours/mois le TMZ a été testé à la dose de 75 mg/m2, 7 jours/7, délivré de manière concomitante à une irradiation focalisée à la dose de 60 Gy (grays) en 30 fractions suivi par 6 cycles de chimiothérapie mensuelle. Cette étude de phase II avait inclus 64 patients. La tolérance hématologique était bonne avec une probabilité de survie à 2 ans de 31 % [6]. Ces résultats prometteurs ont été le point de départ d’un large essai randomisé multicentrique de phase III, mené sous l’égide de l’Organisation européenne de recherche et traitement du cancer (EORTC) et du National Cancer Institute (NCI) canadien [3].
Chez les sujets en bon état général de moins de 70 ans
Cet essai rapporté par Stupp et al. en 2005 [3] a inclus 573 patients d’âge compris entre 18 et 70 ans porteurs d’un glioblastome (grade 4) opéré depuis moins de 6 semaines, avec bilan biologique normal. Il comparait la radiothérapie standard de 60 Gy en 30 séances et 6 semaines au traitement expérimental rapporté dans la phase II. Dans chacun des deux bras de traitement, 40 % des patients avaient eu une chirurgie macroscopiquement complète et 45 % une résection partielle, 15 % n’avaient eu qu’une biopsie. La tolérance hématologique était bonne avec 7 % de neutropénie et/ou thrombopénie importante. L’analyse de la survie à 2 ans montrait un bénéfice significatif (p < 0,001) en faveur de la chimiothérapie concomitante avec une augmentation des probabilités de survie de 10 à 27 %. La réduction du risque relatif de décès était de 37 % pour les patients recevant le TMZ en concomitant puis en adjuvant. La méthylation du gène codant pour une enzyme de réparation des lésions induites par la chimiothérapie, la O-6-méthylguanine-DNA-méthyltransférase (MGMT), était associée à une meilleure sensibilité à la chimiothérapie. Parmi les 206 patients testés, le statut méthylé de l’enzyme était un facteur pronostic-indépendant. La médiane de survie des patients porteurs de cette méthylation était de 22 mois versus 15 mois dans le cas contraire. Ce protocole de chimioradiothérapie concomitante puis adjuvante avec le TMZ est devenu le protocole de référence des patients de moins de 70 ans en bon état général (OMS [Organisation mondiale de la santé] de grade 0-1) après résection optimale du glioblastome. Pour les tumeurs de grade 3, (astrocytome et/ou oligodendrogliome anaplasique), le traitement standard reste la chirurgie, suivie d’une radiothérapie. La chimiothérapie par TMZ est débutée en cas de récidive tumorale.
Chez les sujets en bon état général de plus de 70 ans
L’incidence croissante des gliomes de haut grade chez les sujets âgés et le mauvais pronostic de ces tumeurs ont incité la communauté médicale à entreprendre plusieurs essais randomisés pour définir la prise en charge la mieux adaptée chez ces patients fragiles. L’essai randomisé français de l’Association des neuro-oncologues d’expression française (ANOCEF), rapporté par Keime-Guibert et al. en 2007 [7], a inclus 85 patients de plus de 70 ans avec un indice de Karnofsky supérieur à 70 %. Il comparait les soins de confort associés ou non à une irradiation focale à la dose de 50 Gy en fractions de 1,8 Gy, 5 fractions/semaine. La médiane de survie était significativement améliorée de 17 à 29 semaines chez les patients qui recevaient une radiothérapie. L’étude de la qualité de vie et l’évaluation des fonctions neurocognitives ne retrouvaient pas de différence significative entre les deux groupes.
L’essai randomisé allemand NOA-08 publié en 2012 a comparé chez des patients de plus de 65 ans avec un index de Karnofsky supérieur à 60 le TMZ à 100 mg/m2/jour une semaine sur 2 à une radiothérapie normofractionnée à la dose de 60 Gy. Les résultats globaux en termes de survie étaient comparables. La survie sans maladie était significativement améliorée chez les patients porteurs de la méthylation du gène MGMT quand ils recevaient du TMZ. Les auteurs concluaient à la non-infériorité du TMZ seul par rapport à la radiothérapie standard chez les patients âgés, le statut de la méthylation du gène MGMT pouvant constituer un élément décisionnel dans le choix du traitement en pratique courante [8].
Pronostic
L’actualisation des résultats à 5 ans de l’essai de l’EORTC a été publiée en 2009 [9]. Les probabilités de survie étaient pour l’ensemble du groupe respectivement de 16, 12 et 10 % à 3, 4 et 5 ans. L’association d’une chimiothérapie par TMZ améliorait la survie dans tous les sous-groupes de patients. Ceux porteurs de la méthylation du gène MGMT en tiraient le bénéfice le plus significatif. Chez les sujets âgés, la médiane de survie était de 5 à 6 mois, le performans status restant le facteur pronostique le plus important.
Chimiothérapie de rattrapage
Les patients inclus dans le bras standard de l’essai de l’EORTC avaient pour la plupart reçu du TMZ en traitement de rattrapage lors de la reprise évolutive de leur gliome [3]. Une étude de phase II a évalué après échappement au TMZ l’efficacité d’une chimiothérapie de rattrapage par irinotécan (Campto) associée à un antiangiogénique : le bévacizumab (Avastin) [10]. Ce protocole habituellement utilisé en cancérologie digestive a retrouvé un taux de réponse de 57 % parmi les 35 patients inclus avec une médiane de survie de 42 semaines. Malgré une augmentation du risque thromboembolique, la toxicité a été jugée acceptable. Dans la pratique clinique, ce protocole est régulièrement utilisé en seconde ligne de traitement, permettant dans certains cas des stabilisations prolongées du glioblastome.
Dose et fractionnement de la radiothérapie
Limites de doses dans les organes à risque
Il convient de respecter les contraintes de doses selon le guide des bonnes pratiques de radiothérapie externe (tableau 1.1) [11]. Les valeurs présentées ne sont valables qu’en cas de normo-fractionnement.
Tableau 1.1
Contraintes des zones à risque [11]
| Encéphale sain | Dose maximale de 45 Gy sur l’encéphale total, 60 Gy dans 30 % de l’encéphale |
| Tronc cérébral | Dose maximale de 50 Gy Sur un volume très limité, la dose pourra atteindre 55 Gy |
| Nerf optique, chiasma, hypophyse | Dose maximale de 54 Gy |
| Moelle épinière | Dose maximale de 45 Gy en fractionnement habituel |
| Œil | Dose moyenne < 35 Gy. |
| Cristallin | Dose la plus basse possible, si possible dose moyenne < 5–10 Gy |
| Méat acoustique externe, oreilles moyenne et interne | Dose maximale de 50–55 Gy |
| Cochlée | Dose maximale < 40 Gy |
| Lobes temporaux | Dose aussi faible que possible |
Volume et balistique
La majorité des récidives locales survenant dans le volume d’irradiation, l’irradiation panencéphalique n’est plus recommandée au profit d’une irradiation focalisée avec des marges de 2 cm au pourtour du volume tumoral initial, réadapté aux barrières anatomiques [4]. Le volume tumoral macroscopique ou Gross Tumor Volume (GTV) est déterminé par le rehaussement après injection de produit de contraste sur la séquence pondérée en T1 après injection d’un chélate de gadolinium. L’extension microscopique tumorale, ou Clinical Target Volume (CTV), correspond en général à la zone d’œdème péritumoral visible sur la séquence pondérée en T2. Une marge supplémentaire de 5 mm au pourtour du CTV est souvent ajoutée pour tenir compte des incertitudes de positionnement sous la machine de traitement définissant ainsi le Planning Target Volume (PTV). Les problématiques liées à ces volumes sont complexes et les pratiques encore non uniformes [12]. Ces volumes sont adaptés en fonction des limites de dose tolérables aux organes à risques (fig. 1.1).
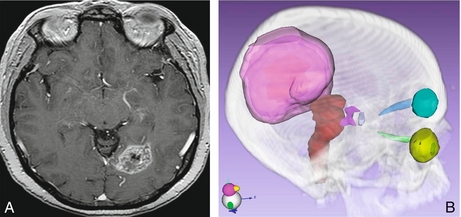
Fig. 1.1 Planification de la radiothérapie d’un glioblastome.
A. Coupe pondérée en T1 après injection d’un chélate de gadolinium. Glioblastome occipital gauche.
B. Reconstruction 3D des volumes cibles à irradier (Gross Tumor Volume [GTV] en rose foncé, Clinical Target Volume [CTV] en rose clair, Planning Tumor Volume [PTV] en violet) et des organes à risques (globes oculaires, cristallins, nerfs optiques, chiasma, hypophyse, tronc cérébral).
Évaluation de la réponse précoce et tardive au traitement
Méthodes d’imagerie
Protocole IRM pour la surveillance des gliomes malins
Cet examen IRM obéit à un protocole rigoureux et reproductible. Les séquences doivent être effectuées au cours de la surveillance avec les mêmes types de paramètres d’acquisition, la même orientation des coupes (CA-CP [commissure antérieure – commissure postérieure] étant la plus usitée) et si possible sur le même appareil (au moins la même puissance de champ). Les séquences fondamentales sont représentées par les séquences pondérées en T1 avant et après injection d’un chélate de gadolinium (coupes 2D en écho de spin axiales et coronales ou acquisition 3D en écho de gradient ; l’acquisition étant réalisée au moins 5 min après l’injection du chélate de gadolinium) et les coupes pondérées en T2 Flair (Fluid Attenuated Inversion Recovery) (2D ou 3D). Les coupes axiales en T2 écho de gradient ou en imagerie de susceptibilité magnétique sont utiles pour la mise en évidence des phénomènes hémorragiques (saignement per ou postopératoire, remaniements hémorragiques des tumeurs et des lésions radiques). Les techniques fonctionnelles (diffusion à la recherche d’arguments pour une hypercellularité, perfusion pour l’évaluation de la néoangiogenèse) apportent des renseignements complémentaires très utiles et devraient être systématiquement associées. De même, l’imagerie métabolique (spectroscopie monovoxel et au mieux multivoxel) aide dans les cas difficiles à la caractérisation tissulaire. Le volume d’acquisition spectroscopique est positionné de façon plus pertinente sur les séries après injection du chélate de gadolinium qui ne modifie pas la qualité des spectres. Dans certains centres, il est désormais possible d’identifier en spectroscopie proton (2-hydroxy-glutarate) les lésions porteuses de la mutation IDH1, dont l’impact pronostique est évoqué plus loin [13]. En pratique, on peut intercaler les séquences pondérées en T2 et l’imagerie fonctionnelle entre les séquences pondérées en T1 (avant et après injection du chélate de gadolinium) pour permettre la meilleure imprégnation possible de la tumeur par l’agent de contraste. Un protocole d’évaluation des gliomes est proposé dans l’encadré 1-1.
Méthodes scintigraphiques
L’importante activité métabolique corticale physiologique explique que la scintigraphie au 18F-FDG soit peu indiquée dans la détection du tissu tumoral résiduel après traitement. Dans les semaines suivant les traitements, un accroissement transitoire de la captation du 18F-FDG peut être noté au niveau du site lésionnel en raison de son infiltration par les macrophages consommateurs de glucose. Les sensibilités et spécificités du 18F-FDG dans l’identification d’une récidive tumorale ou des modifications induites par les traitements sont améliorées par la coregistration avec les images IRM et par l’acquisition d’images tardives 3 à 8 heures après injection. En effet, en augmentant le contraste entre les lésions spécifiques hypermétaboliques et la substance grise, les acquisitions tardives améliorent la visualisation du processus tumoral.
Les acides aminés (méthionine, tyrosine, choline) et les nucléosides (fluorothymidine) marqués peuvent aussi être utilisés en TEP avec une meilleure spécificité de fixation cellulaire [14]. La 11C-méthionine évalue la consommation tissulaire en acides aminés. En raison de son implication dans la synthèse protéique, ce radiotraceur est considéré comme un indicateur plus sensible que le 18F-FDG pour le dénombrement des cellules en phase de prolifération (délimitation et extension du tissu tumoral). Il présente cependant un métabolisme non protéique avec une fraction significative incorporée dans la composition de phospholipides qui rend difficile la quantification précise du métabolisme protéique. Sa liaison avec le carbone-11 qui possède une demi-vie de 20 minutes en limite l’utilisation à quelques centres TEP qui sont à proximité d’un cyclotron et des laboratoires de radiochimie et de radiopharmacie nécessaires à sa production.
La 18F-fluoroéthyl-tyrosine (18F-FET) est un radiotraceur de plus en plus utilisé en raison de sa cinétique plus adaptée à la modélisation de la synthèse des protéines (et avec une demi-vie de 110 minutes lorsqu’il est utilisé avec le fluor-18). La 18F-FET est captée par un système de transport spécifique (le L-système) qui permet de discriminer la multiplication cellulaire accrue de l’augmentation du métabolisme glucidique [15]. La 18F-fluorothymidine (18F-FLT) permet une évaluation directe de la prolifération cellulaire car elle entre directement dans la voie de synthèse de l’ADN et demeure piégée dans la cellule après phosphorylation par la thymidine-kinase.
Quelques équipes ont également proposé l’utilisation de la choline marquée au carbone-11 pour différencier les pathologies bénignes et malignes, la choline étant un précurseur de la biosynthèse de la phosphotidylcholine et d’autres phospholipides, principaux composants de la membrane cellulaire. De plus, la choline a récemment pu être marquée au fluor-18, ce qui facilite grandement son utilisation [14].
Évaluation postopératoire précoce
Les buts de cette imagerie sont : déterminer l’existence et l’importance d’un reliquat tumoral, détecter des complications chirurgicales et servir de référence pour la surveillance ultérieure après radio et/ou chimiothérapie complémentaires. Vidiri et al. [16] ont montré qu’il existait une corrélation très significative entre la survie et la qualité de l’exérèse (avec respectivement une survie médiane de 16, 13 et 7 mois en cas d’exérèse totale, subtotale et partielle).
L’IRM est la méthode de choix pour l’imagerie postopératoire précoce. De nombreux auteurs ont montré sa supériorité pour détecter du tissu tumoral résiduel par rapport au scanner (meilleure résolution en contraste de l’IRM en termes de prise de contraste et de caractérisation tissulaire, moins de faux négatifs) et la scintigraphie. Elle est également beaucoup plus fiable que les constatations peropératoires du chirurgien qui méconnaît près de la moitié des reliquats [17].
Le processus de cicatrisation débute dès la fin de l’intervention et se poursuit pendant plus de 6 semaines. Durant la phase initiale (3 premiers jours), anomalies vasculaires (vasoconstriction puis vasodilatation) et rupture de la BHE (barrière hématoencéphalique) sont responsables d’une fine prise de contraste linéaire de la tranche de section. Ce rehaussement est quasi constant (90 %) au bout de 24 heures [17]. Lors de la phase subaiguë (du 3e au 30e jour), s’installe un œdème vasogénique qui atteint son maximum vers J10-J14 et disparaît lors de la 4e semaine. Durant cette phase, la cicatrisation s’effectue par l’intermédiaire de bourgeons granulomateux avec néovascularisation. En imagerie, on observe, outre l’hypersignal T2 Flair péricavitaire, des rehaussements irréguliers, en motte, au niveau de la tranche de section et dans les zones d’œdème adjacentes. Le rehaussement bénin cicatriciel dure en général entre 1 et 3 mois (mais des prises de contraste liées au geste chirurgical ont été décrites jusqu’à 6 mois).
Il est donc essentiel que la recherche d’un reliquat tumoral post-chirurgical soit effectuée dans les 72 heures qui suivent l’intervention et si possible dans les premières 24 heures. La mise en évidence d’un fin épaississement linéaire est alors très probablement bénin, secondaire à la chirurgie (fig. 1.2). En revanche, la découverte d’une prise de contraste linéaire épaisse et/ou nodulaire est alors associée à une récidive tumorale (sensibilité = 0,91, spécificité = 1) [17].
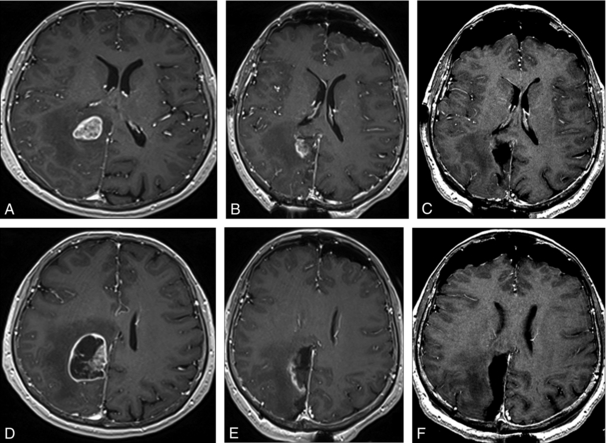
Fig. 1.2 Imagerie postopératoire précoce après exérèse d’un glioblastome touchant les gyri pariétal et cingulaire droit : coupes pondérées en T1 après injection.
A, D. IRM préopératoire.
B, E. IRM réalisée à J1 de l’exérèse : prises de contrastes nodulaire cingulaire (B) et linéaire épaisse pariétale (E) suspectes de reliquats tumoraux. Reprise chirurgicale avec exérèse de bourgeons tumoraux résiduels.
C, F. IRM à J1 de la nouvelle intervention : absence de reliquat tumoral décelable.
Stay updated, free articles. Join our Telegram channel

Full access? Get Clinical Tree








